Патент на изобретение №2240304
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ ГИПЕРФОРИНА, ИХ ИСПОЛЬЗОВАНИЕ И ПРЕПАРАТЫ, СОДЕРЖАЩИЕ ЭТИ ПРОИЗВОДНЫЕ
(57) Реферат:
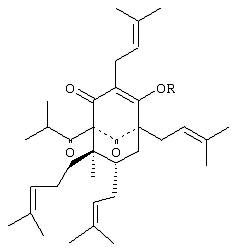
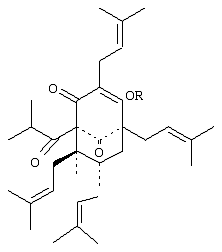
Изобретение относится к новому соединению формулы I в которых R представляет собой ароматический ацильный фрагмент, который необязательно имеет один или несколько заместителей, которые могут быть одинаковыми или различными и которые выбирают из гидрокси, метокси и аминогруппы. Соединения I проявляют антидепрессантную активность и могут быть использованы в фармацевтической композиции. 2 с. и 2 з.п. ф-лы, 1 табл.
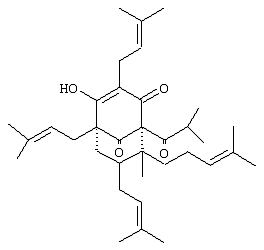
Настоящее изобретение относится к новым производным гиперфорина, их применению для лечения депрессии и состояния тревоги, а также к препаратам, содержащим эти производные. Надземная масса цветущего Hypericum perforatum содержит вещества, относящиеся к нескольким классам веществ с различной структурой, которые оказывают прямое или косвенное воздействие на центральную нервную систему. Более конкретно указанные соединения включают в себя гиперицин, гиперфорин и димерные флавоны, которые оказывают антидепрессивное и транквилизирующее действие на животных и человека. Механизмы воздействия этих соединений различны: действие в качестве ингибитора моноаминоксидазы, влияние на высвобождение серотонина и действие, подобное действию бензодиазепина. Гиперфорин формулы который является одним из основных компонентов липофильной фракции в надземной массе цветущего Hypericum perforatum, в последнее время стал объектом многочисленных исследований, которые позволили установить его важную роль в качестве антидепрессанта; исследования, проведенные заявителем, подтвердили, что эта молекула обладает действием, аналогичным действию серотонина. Гиперфорин не очень стабилен в условиях обычного экстрагирования и консервации; как описано в заявке WO 97/13489 (на имя Шваба), содержание гиперфорина в водно-спиртовом экстракте зверобоя падает почти до нуля уже через несколько недель. И снова, как сказано в заявке WO 97/13489, чтобы получить стабильные экстракты с постоянным содержанием гиперфорина, экстрагирование, очистку и консервацию, необходимо производить в присутствии антиоксидантов, таких как витамин С и его сложные эфиры, серосодержащие аминокислоты и т.п. Высокая нестабильность гиперфорина существенно затрудняет изготовление лекарственных препаратов из него. Благодаря настоящему изобретению открыты производные гиперфорина, которые являются более стабильными и проявили более высокую активность в качестве антидепрессантов в специфических фармакологических тестах. Этими производными по настоящему изобретению являются соединения формулы I: в которых R представляет собой – насыщенную или ненасыщенную, с прямой или разветвленной цепью, C1 -C22 ацильную группу, необязательно имеющую один или несколько заместителей, которые могут быть одинаковыми или различными и которые выбирают из группы, в которую входят атомы галогенов, нитро, амино, C1-C6 алкиламино, ди-C 1-C6 алкиламино, C1-C6 ациламиногруппы; -циклоалифатический или ароматический ацильный остаток, в котором ароматический фрагмент необязательно имеет один или несколько заместителей, которые могут быть одинаковыми или различными и которые выбирают из группы, включающей в себя атомы галогенов, гидрокси, метоксиаминогруппы; -глицидный остаток, в котором одна или несколько гидроксильных групп необязательно являются алкилированными или ацилированными. Термин “ароматический ацильный остаток” обозначает предпочтительно бензоильный или циннамильный остаток, имеющий одну или несколько амино- или алкоксигрупп. Термин “глицидный остаток” обозначает остаток из одного сахара, связанного посредством эфирной связи с гидроксильной группой в 1 положении пиранозильного или фуранозильного кольца, причем другие гидроксильные группы этого сахара необязательно являются метилированными или ацетилированными. Предпочтительными R-группами являются ацетил, монохлороацетил, бутирил, Производные гиперфорина по настоящему изобретению можно получить обычными способами ацилирования или гликозилирования гидроксильных групп. Например, по существу чистый гиперфорин или экстракт, обогащенный гиперфорином, можно подвергнуть взаимодействию с хлоридами кислот или ангидридами кислот RCOOH (R имеет вышеуказанные значения) в подходящих растворителях, например, в пиридине. С другой стороны, гликозилирование можно провести, используя реакционноспособные производные нужного сахара (ROH) с подходящими защитными группами, например, В соответствии с наиболее удобным способом по настоящему изобретению соединения I получают путем экстрагирования надземной массы цветущего Hypericum perforatum двуокисью углерода в сверхкритических условиях, с последующим разделением между растворителями и получением производных гиперфорина в полученном экстракте. Листья и стебли цветущего зверобоя отдельно или в смеси, в основном в виде природной смеси, экстрагируют двуокисью углерода в сверхкритических условиях под давлением от 180 до 260 бар, предпочтительно 240 бар, и при температуре в диапазоне от 35 до 50°С, предпочтительно 40°С. Получают липофильный экстракт, содержащий около 50% гиперфорина. Экстракт содержит значительные количества ксантонов, восков, жирных кислот и триглицеридов. Процентное содержание гиперфорина можно затем повысить, если, в соответствии с настоящим изобретением, солюбилизировать полученный экстракт в метаноле или в частично водном растворе ацетонитрила, а затем экстрагировать полученный раствор н-гексаном или алифатическими углеводородами. Углеводородная фаза содержит нежелательные вещества, которые удаляют; гидрофильную фазу разбавляют приблизительно равным объемом воды и алифатическими углеводородами. Для получения производных, как описано выше, можно использовать экстракт зверобоя. Производные по настоящему изобретению могут не проявлять активности in vitro на рецепторы, а в то же время они особенно активны in vivo, оказывая сильное антидепрессивное действие, зависящее от дозы. В тестах in vivo на мышах и крысах соединения по настоящему изобретению показали более высокую активность, чем гиперфорин и этанольные или метанольные экстракты Hypericum. В качестве испытаний in vivo для проверки антидепрессивного эффекта были использованы тест на развитие недостаточной активности при попытках избежать воздействия и тест на подавление потребления этанола сардинскими крысами с алкогольной зависимостью; тесты проводили способами, описанными в литературе. В тесте на развитие недостаточной активности при попытках избежать воздействия, соединения по настоящему изобретению показали более высокую активность, чем известные экстракты, и эта активность была сопоставима с активностью известных медикаментов, таких как имипрамин. В этом тесте крыс закрепляли и подвергали слабым кратковременным неизбежным электрошоковым воздействиям в течение 50 мин. (предварительное испытание). Через двадцать четыре часа по хвостам животных определяли их способность избегать таких же стимулов в ситуации, когда избежать воздействий невозможно. Крыса в среднем совершает 26 попыток избежать воздействия на 30 воздействий (контрольные экземпляры, не подвергавшиеся воздействиям), в то время как животные, которых подвергали предварительному испытанию, совершали только 1-3 попытки избежать воздействия (контрольные экземпляры, не проходившие лечения). Гипореактивность, вызванную предварительным испытанием, не наблюдали у животных, которых за 1-3 недели до испытаний лечили антидепрессантами, такими как имипрамин или флуоксетин. Соединения по настоящему изобретению, введенные крысам за один час до того, как подвергнуть их неизбежному стрессу, вызывали повышение реактивности в тесте на попытки избежать воздействия, причем это повышение было еще более сильным, когда животных подвергали предварительному лечению за 1-2 недели до испытания. Например, результаты лечения крыс соединением I, в котором R представляет собой ацетил, показаны в приведенной ниже таблице. В таблице показан антидепрессивный эффект гиперфоринацетата у крыс в ходе проведения теста на развитие недостаточной активности при попытках избежать воздействия, где крыс подвергали предварительному испытанию в течение 2 недель. Статистический анализ: Крускал-Уоллиса, непараметрический, ANOVA KW=13,462 р + 0,0012. Спиртовый экстракт Hypericum и гексановый экстракт против контроля, не подвергавшегося воздействию, р<0,01. Гиперфоринацетат, 25 мг, против контроля, не подвергавшегося воздействию – не оговорено. Контроль, не подвергавшийся воздействию, против AND – р<0,01. В тесте на снижение потребления алкоголя у сардинских крыс (что является показателем депрессии и тревожного состояния) в соответствии с протоколами тестов, описанными в литературе, вещества по настоящему изобретению, после двухдневного введения, вызывали 60-70% снижение потребления алкоголя, которому крысы предпочитали воду (в сравнении с контролем). Используя соединения формулы I, можно изготовить лекарственные препараты в мягких желатиновых капсулах, твердых желатиновых капсулах, в таблетках, в виде свечей; предпочтительно изготавливать из соединений по настоящему изобретению лекарственные препараты в мягких желатиновых капсулах или в формах с постепенным высвобождением активного ингредиента. Дозировки соединений по настоящему изобретению в таких лекарственных препаратах варьируются от 5 до 50 мг на дозу в обычных лекарственных формах и до 200 мг на дозу в лекарственных формах, обеспечивающих постепенное высвобождение; в этом случае предпочтительной дозой является 200 мг для ежедневной дозы. Приведенные ниже примеры более подробно иллюстрируют настоящее изобретение. Пример 1 – Получение экстракта, обогащенного гиперфорином. 10 кг биомассы Hypericum perforatum экстрагируют в соответствии со способом, описанным ниже, в экстракторе на 25 л для газа под сверхкритическим давлением; экстрактор оснащен двумя сепараторами. 10 кг надземной массы цветущего Hypericum perforatum механически высушивают после сбора, при температуре не выше 60°С, подвергают экструзии, чтобы разрушить клетки, и экстрагируют при помощи СO2 в условиях сверхкритического давления: – температура: 45°С в экстракторе, 30°С в первом сепараторе и 20°С во втором сепараторе; – давление: 240 бар в экстракторе, 100 бар в первом сепараторе и 50 бар во втором сепараторе. Поток СO2 пропускали со скоростью 10 л в минуту в течение 45 минут. Экстракт концентрировали во втором сепараторе, в то время как большую часть воды, присутствующей в растительной матрице, концентрировали во втором сепараторе. Экстракт, присутствующий во втором сепараторе, солюбилизировали в 3,2 л метанола, и этот раствор экстрагировали 3×1,5 л н-гексана. Гексановую фазу промыли потоком 98 метанола, используя гиперфорин в качестве маркера, который должен оставаться в метанольной фазе. Гексановую фазу удаляют, а комбинированные метанольные разбавляют 0,6 л воды и повторно экстрагируют 2×0,6 л н-гексана. Комбинированные фазы гексана обесцвечивают 0,3% углем, высушивают под Na2SO4, затем концентрируют под вакуумом при температуре не выше 40°С до получения масла. Получают 0,22 кг воскообразного экстракта, в котором содержание гиперфорина составляет около 70%. Пример 2 – Синтез гиперфоринацетата. В раствор 12 г растительного экстракта, полученного в примере 1, в 48 мл пиридина добавили Ас2O (9,8 мл) и перемешивали при комнатной температуре. Ход реакции контролировали при помощи тонкослойной хроматографии (гексан: ЕtОАс 95:5; гиперфорин Rf: 0,24; ацетат Rf: 0,49) (Rf – скорость движения вещества по хроматографической бумаге). Через 24 часа реакционную смесь разбавляли водой и экстрагировали смесью гексана с эфиром (3:1). Органическую фазу промывали разбавленной НСl, насыщенным NаНСО3 и соляным раствором. После высушивания (Na2SO4) и выпаривания остаток очищали хроматографией на колонне с силикагелем (около 30 г), элюировали сначала петролейным эфиром, чтобы удалить жиры, затем использовали смесь гексан: ЕtOАс 95:5, как только искомое соединение начинало элюироваться; получали 3,34 г (0,28) гиперфоринацетата в виде бесцветной пасты. С37Н54O 5, MW 578 CI-MS: 579 (М+Н)+ ИК (жидкая пленка): 1779, 1732, 1660, 1634, 1447, 1377, 1339, 1146 см-1 . 1H ЯМР (200 МГц, CDCl3): 5,03 (br s, 2Н), 5.00 (br s, 2H), 3.05 (dd, J=15, 7Hz, 1H), 2.87 (dd, J=15, 7Hz, 1H), 2.22 (s, OAc), 1.66-1.53 (br s, 8×3H), 1.08 (d, J=6.5 Hz, 3H), 0.98 (s, 3H), 0.85 (d, J=6.5 Hz, 3H). Пример 3 – Синтез гиперфорин-3,4,5-триметоксибензоата В раствор растительного экстракта из примера 1 (1,0 г) в пиридине (4 мл) добавили 3, 4, 5-триметоксибензоилхлорид (323 мг), и раствор перемешивали при комнатной температуре в течение 24 часов. За ходом реакции не могли следить при помощи тонкослойной хроматографии, поскольку перемешиваемый материал и продукт имеют очень близкий показатель Rf (скорость движения вещества по хроматографической бумаге) в различных растворителях. Реакционную смесь разбавляли водой и экстрагировали смесью эфира и гексана (3:1). Органическую фазу промывали разбавленной НСl, насыщенным NаНСО3 (промывка соляным раствором вызывает образование эмульсии). После высушивания Na2SO4 и выпаривания остаток очищали хроматографией на колонне с силикагелем (около 5 г), элюировали сначала петролейным эфиром, чтобы удалить жиры, затем использовали смесь гексан: ЕtOАс 95:5 до получения гиперфоринтриметоксибензоата (317 мг) в виде бесцветного масла. С45Н 62O8, MW 730 CI-MS: 731 (М+Н)+ ИК (жидкая пленка): 1732, 1660, 1634, 1589, 1465, 1331, 1153, 1130, 914 см-1. 1Н ЯМР (200 МГц, CDCl 3): 7.27 (s, 2H), 5.04 (br s, 2H), 5.02 (br s, 2H), 3.86 (s, OMe), 3.82 (s, 2 × ОМе), 3.10 (dd, J=15, 7Hz, 1H), 2.92 (dd, J=15, 7Hz, 1H), 1.66-1.53 (br s, 8 x 3H), 1.13 (d, J=6.5 Hz, 3H), 1.04 (s, 3H), 0.99 (d, J=6.5 Hz, 3H). Пример 4 – Таблетки в оболочке, содержащие продукт по примеру 2, мг: Гиперфоринацетат 100 Соевые полисахариды 18,25 Поперечносшитая натрий-карбоксиметилцеллюлоза 13,50 Кремнезем 6,50 Поливинилпирролидон 5,00 Стеарат магния 0,50 Оболочка: Гидроксипропилметилцеллюлоза 3,75 Тальк 2,75 Диоксид титана 1,25 Триацетин 0,75 Полисорбат 80 0,25 Красная окись железа 1,00
Формула изобретения
1. Соединение формулы I в которой R представляет собой ароматический ацильный фрагмент, который необязательно имеет один или несколько заместителей, которые могут быть одинаковыми или различными и которые выбирают из гидрокси, метокси и аминогруппы. 2. Соединения по п.1, в которых R выбирают из п-аминобензоила или триметоксибензоила. 3. Соединение по п.2, где R представляет собой триметоксибензоил. 4. Антидепрессантная фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по пп.1-3 в смеси с подходящим носителем.
|
||||||||||||||||||||||||||

 -аминобутирил, п-аминобензил, триметоксибензил, триметоксициннамил,
-аминобутирил, п-аминобензил, триметоксибензил, триметоксициннамил,  -глюкозил и
-глюкозил и  -D-глюкопиранозил-бромид-тетраацетат.
-D-глюкопиранозил-бромид-тетраацетат.