Патент на изобретение №2237055
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ АЦЕТОФЕНОНА (МЕТИЛФЕНИЛКЕТОНА)
(57) Реферат:
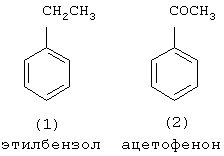
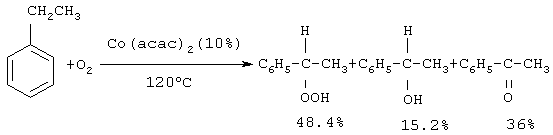
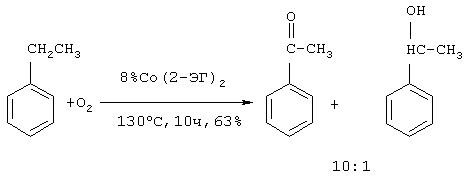
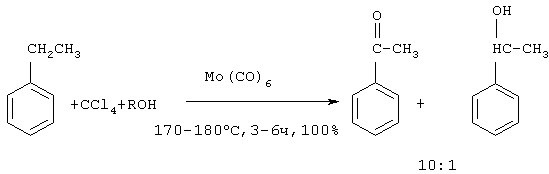
Изобретение относится к усовершенствованному способу получения ацетофенона, который используют в парфюмерии. Способ заключается в окислении этилбензола алкилгипохлоритом, генерированного in situ из четыреххлористого углерода и спирта под действием катализатора Mo(СО)6, при температуре 170-180 Предлагаемое изобретение относится к области органической химии, в частности к способу получения ацетофенона (метилфенилкетона). Ацетофенон и его производные являются душистыми веществами и используются в парфюмерии [Хим. энциклопедия. – М.: Советская энциклопедия, 1988, т. 1, с.442 /1/]. Один из известных способов получения ацетофенона основан на реакции ацилирования (Фриделя-Крафтса) из бензола с ацетилхлоридом или уксусным ангидридом в присутствии АlСl3, либо FеСl3 [А.Н. Несмеянов, Н.А. Несмеянов. Начала органической химии, кн. 2, М., 1970, с.148-159 /2/]. Хлористый алюминий в этой реакции приходится брать в эквивалентном хлорангидриду (или ангидриду) количестве, так как он полностью связывается в комплекс и продолжает быть связанным с кетоном после его образования. К очевидным недостаткам данного метода следует отнести 1. Большой расход катализатора (АlСl3 используется в эквимолярном количестве по отношению к ангидриду). 2. Для выделения ацетофенона после окончания процесса в реактор добавляется большое количество воды для промывки органического слоя до нейтральной реакции, что приводит к образованию значительного количества сточных вод, которые необходимо утилизировать с полным удалением соединений алюминия. 3. Процесс является нетехнологичным и дорогим (большой расход АlСl3 или FeCl3, образование токсичных отходов, добавление целой технологической стадии по разложению реакционной массы, невозможность повторного использования АlСl3 или FeCl3, которые гидролизуются с образованием Аl(ОН)3 и Fе(ОН)3). Жидкофазное окисление кислородом воздуха этилбензола, инициированное солями металлов, приводит к образованию на I стадии гидроперекиси этилбензола, которая разлагается с выделением ацетофенона (цепная реакция) При окислении этилбензола в присутствии окислов металлов реакция протекает неоднозначно. При этом селективность образования кислородсодержащих продуктов, представленных гидроперекисью этилбензола, Недостатки метода 1. Повышенная взрывоопасность из-за использования в качестве окислителя кислорода и образования гидроперекиси. 2. Низкий выход целевого продукта. 3. Значительные трудности при выделении целевого продукта, связанные с образованием побочных продуктов (метилфенилкарбинол). При облучении раствора полиоксометаллата в уксусной кислоте с этилбензолом образуется ацетофенон с выходом 6 молей (2) на моль полиоксометаллата (РМО11VO4-40, PW12O3-40). Этилбензол окисляется кислородом воздуха, растворенным в уксусной кислоте, а полиоксометаллат играет роль катализатора [Г.Б. Шульпин, М.М. Кац. Журн. общ. химии, Т.59, в. 12, 2738-2742 (1989) /4/]. Фотохимический метод получения ацетофенона в присутствии фосфоровольфрамат и фосфоромолибдат ионов имеет ряд существенных недостатков: 1. Фотохимические реакции проходят исключительно в прозрачном стеклянном или кварцевом оборудовании, объем которого строго ограничен. По этой причине данный способ не может быть масштабирован и характеризуется низкой производительностью и является нетехнологичным. 2. Большой расход катализатора, который способен проводить всего 6 каталитических циклов. 3. Значительные трудности при выделении целевого продукта, связанные с удалением солей полиоксометаллата. 4. Образование большого количества отходов. При окислении этилбензола кислородом воздуха в присутствии ацетилацетонатов меди и кобальта образуется до 31-36% ацетофенона, при этом основным продуктом реакции является (49-57%) фенилэтилгидропероксид [В.Ф. Назимок, В.И. Овчинников, В.М. Потехин. Жидкофазное окисление алкилароматических углеводородов. – М.: Химия, 1987. 240С./5/]: Увеличить скорость и селективность реакции окисления этилбензола можно добавлением к солям металлов переменной валентности солей некоторых щелочноземельных металлов, например, к Со(асас)2 добавляют Mg(нафтенат)2 в мольном соотношении 100:1 /5/: Недостатки этого способа 1. Пожаро- и взрывоопасность процесса. 2. Низкий выход целевого продукта. 3. Трудности при выделении целевого продукта из-за образования побочных продуктов (метилфенилкарбинол). 4. Низкая селективность процесса. В присутствии Rh-содержащих катализаторов [(Рh3Р)3RhСl, Rh(асас)3, Рh(2-этилгексаноат)2] окисление этилбензола молекулярным кислородом при 130 На основании сходства по трем признакам (идентичные исходные реагенты – этилбензол, использование катализатора, образование в результате реакции ацетофенона) за прототип взят метод окисления этилбензола молекулярным кислородом в присутствии кобальтового катализатора /6/: Прототип имеет следующие недостатки 1. Взрыво- и пожароопасность процесса из-за его проведения с участием молекулярного кислорода при повышенной температуре. 2. Низкий выход целевого продукта. 3. Значительная продолжительность реакции. Авторами предлагается способ получения ацетофенона, не имеющий указанных недостатков. Сущность способа заключается в окислении этилбензола из химически инертных мономеров ССl4 и метанола (или этанола) под действием гексакарбонила молибдена Мо(СО)6 при мольном соотношении [Мо(СО)6]:[ЭБ]:[ССl4]:[МеОН или ЕtOН]=1:100-500:500-1500:500-1500. Окислителем в данном случае является метилгипохлорит МеОСl (или этилгипохлорит EtOCl), генерированные in situ из ССl4 и МеОН (EtOH), под действием Мо(СО)6, играющего роль катализатора. При этом катализатор является ответственным как за образование алкилгипохлорита, так и за последующие окислительные реакции с его участием. Образование алкилгипохлоритов доказано йодометрическим титрованием. Четыреххлористый углерод используется в реакции в 2-3-кратном избытке, т.к. он играет роль растворителя и окислителя одновременно. При оптимальных условиях выход ацетофенона по предлагаемому методу достигает 85-92%. Существенные отличия предлагаемого способа от прототипа 1. Высокий выход целевого продукта. 2. Доступность и дешевизна компонентов катализатора. 3. Низкий расход молибденового катализатора. 4. Образование небольшого количества отходов. 5. Непрореагировавшие четыреххлористый углерод и спирты без дополнительной очистки могут быть возвращены в реакцию. 6. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат, экологическая безопасность процесса. 7. Новый способ окисления этилбензола с использованием CCl4 решает проблему квалифицированной утилизации четыреххлористого углерода, что предусмотрено Монреальской конвенцией, участником которой является наша страна. Предлагаемый способ поясняется примерами ПРИМЕР 1. В стальной микроавтоклав из нержавеющей стали (V=17 мл) помещали 0.1 ммоль Мо(СО)6, 10 ммоль этилбензола, 30 ммоль ССl4, 30 ммоль метанола, автоклав герметично закрывали, реакцию проводили при 170 Ик-спектр, Спектр ЯМР 13С ( Масс-спектр, m/z (jотн. (%)): 120.14 [М]+ (37), 32(58), 39(9), 43(28), 51(44), 77(100), 105(86). Найдено (%): С, 80.00; Н, 6.25. C8H8O. Вычислено: С, 79.97; Н, 6.71. ПРИМЕР 2. В стальной микроавтоклав из нержавеющей стали (V=17 мл) или в стеклянную ампулу (V=20 мл) (результаты параллельных опытов практически одинаковы) помещали 0.1 ммоль Мо(СО)6, 20 ммоль этилбензола, 50 ммоль ССl4, 50 ммоль этанола, автоклав герметично закрывали (ампулу запаивали). Реакцию проводили при 180 Формула изобретения
Способ получения ацетофенона (метилфенилкетона) окислением этилбензола, отличающийся тем, что в качестве окислителя используют алкилгипохлорит, генерированный in situ из четыреххлористого углерода и спирта под действием катализатора М0(СО)6 при температуре 170-180 MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 07.11.2004
Извещение опубликовано: 10.12.2006 БИ: 34/2006
|
||||||||||||||||||||||||||

 С, в течение 3-6 ч при мольном соотношении [Mo]:[ЭБ]:[CCl4]:[ROH]=1:100-500:500-1500:500-1500. Способ обеспечивает получение целевого продукта с выходом 72-92%. 1 табл.
С, в течение 3-6 ч при мольном соотношении [Mo]:[ЭБ]:[CCl4]:[ROH]=1:100-500:500-1500:500-1500. Способ обеспечивает получение целевого продукта с выходом 72-92%. 1 табл.
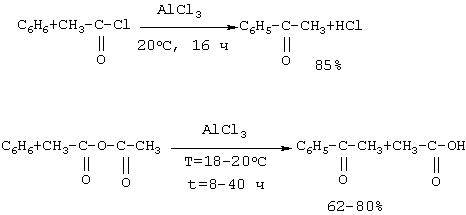
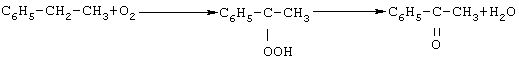
 -фенилэтанолом и ацетофеноном, зависит от природы катализатора. Наиболее высокой избирательностью по гидроперекиси среди гетерогенных катализаторов обладает оксид свинца, а по ацетофенону – оксид никеля [И.В. Бачерикова, Я.Б. Гороховатский, Н.П. Евмененко. Кинетика и катализ, т. 15, в. 2, 440-445 (1974) /3/1.
-фенилэтанолом и ацетофеноном, зависит от природы катализатора. Наиболее высокой избирательностью по гидроперекиси среди гетерогенных катализаторов обладает оксид свинца, а по ацетофенону – оксид никеля [И.В. Бачерикова, Я.Б. Гороховатский, Н.П. Евмененко. Кинетика и катализ, т. 15, в. 2, 440-445 (1974) /3/1.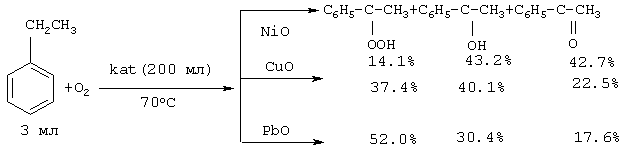
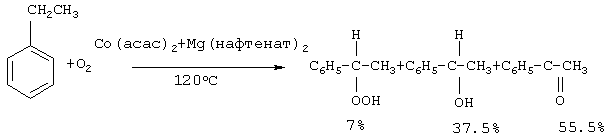
 /см-1: 1750 (С=O).
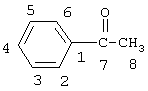
/см-1: 1750 (С=O). , м.д., ТМS): 136.93 (С-1), 128.45 (С-2, С-6), 128.26 (С-3, С-5), 131.79 (С-4), 196.30 (С-7), 24.88 (С-8).
, м.д., ТМS): 136.93 (С-1), 128.45 (С-2, С-6), 128.26 (С-3, С-5), 131.79 (С-4), 196.30 (С-7), 24.88 (С-8).