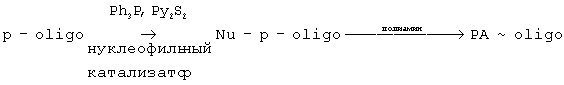Патент на изобретение №2236467
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ДНК-ЧИПОВ
(57) Реферат:
Изобретение относится к области молекулярной биологии и биоорганической химии и может быть использовано для изготовления ДНК-чипов. Для изготовления чипа предварительно проводят синтез конъюгата полиамин-олигонуклеотид (PA-oligo) по стандартной методике. Для этого олигонуклеотид, содержащий 5’- или 3’-концевую фосфатную группу, активируют парой трифенилфосфин-дипиридилдисульфид в присутствии нуклеофильного катализатора в абсолютном органическом растворителе, после чего образующееся активное производное инкубируют с полиамином в подходящем растворителе (диметилсульфоксид, диметилформамид или вода). В качестве нуклеофильного катализатора используют преимущественно метилимидазол, диметиламинопиридин или N-окись диметиламинопиридина. В качестве полиамина используют различные полиамины, содержащие от 3 до 1000 аминогрупп в молекуле. Полученный раствор конъюгата PA-oligo разбавляют до необходимой концентрации, равной 1
Изобретение относится к области молекулярной биологии и биоорганической химии и может быть использовано для изготовления ДНК-чипов. Создание микрочипов с иммобилизованными наборами олигонуклеотидов (ДНК-чипов) требует разработки эффективных способов иммобилизации олигонуклеотидов на твердые носители. Такие ДНК-чипы, представляющие собой твердые подложки с большим числом иммобилизованных олигонуклеотидов, могут использоваться для решения широкого спектра задач в молекулярной биологии, медицине, биотехнологии для анализа экспрессии генов, анализа мутаций, диагностики генетических, инфекционных и онкологических заболеваний. Известны способы получения ДНК-чипов, включающие предварительную обработку стеклянной поверхности (твердой подложки) путем формирования на ней агарозной пленки [V.Afanassiev, V.Hanemann, S.Wolfl, Nucl.Acids Res., 2000, V.28, e66 (i-v)] или пленки из полилизина [R.Jenison, S.Yang, A.Haeberli, B.Polisky, Nature Biotechnology, 2001, V.19, 62-65] или полиэтиленимина [P.H.Lee, S.P.Sawan, Z.Modurson, L.J.Amold, M.A.Reynolds, Bioconjugate Chemistry, 2002, v.13, 97-103]. Агарозную пленку затем модифицируют с целью образования на поверхности альдегидных групп, наносят олигонуклеотид, содержащий аминолинкер и после образования ковалентных связей с поверхностью в виде оснований Шиффа их восстанавливают боргидридом натрия. В случае стеклянных слайдов, покрытых полилизином или полиэтиленимином, для образования ковалентной связи между подложкой и олигонуклеотидом, содержащим аминолинкер, используют бифункциональные сшивающие агенты. Недостатками известных способов являются необходимость длительной предварительной подготовки твердой поверхности, использование дополнительных химических обработок для активирования поверхности, а также использование дополнительных реагентов, обеспечивающих образование ковалентной связи олигонуклеотида при соприкосновении с подложкой. При этом химическая реакция, приводящая к присоединению олигонуклеотида к поверхности, проходит с недостаточно высокой эффективностью, поскольку протекает на твердой фазе. Наиболее близким к заявляемому способу – прототипом является способ получения ДНК-чипов [C.Consolandi, B.Castiglioni, R.Bordoni, E.Busti, C.Battaglia, L.R.Bernardi, G.De Bellis. Nucleosides, Nucleotides, Nucleic Acids, 2002, v.21, 561-580], заключающийся в том, что стеклянные слайды обрабатывают 3-глицидоксипропилтриметоксисиланом для введения эпоксигрупп на поверхность стекла, после чего стекла обрабатывают раствором полилизина в течение 1 часа, промывают и сушат. Затем аминогруппы полилизина активируют, погружая слайды в раствор 1,4-фенилендиизоцианата на 2 часа. После промывания и высушивания слайды хранят в темноте под вакуумом до использования. Полученные слайды используют для приготовления ДНК-чипов, для чего раствор олигонуклеотида, содержащего аминолинкер, наносят в виде рядов точек на поверхность слайда, слайды помещают на ночь в камеру с повышенной влажностью. Затем слайды обрабатывают в течение 15 мин буфером, содержащим этаноламин, для блокирования непрореагировавших изотиоцианатных групп, отмывают буфером и водой. После этого готовые ДНК-чипы пригодны для использования в последующих реакциях, основанных на методе молекулярной гибридизации. Недостатком способа является необходимость длительной предварительной подготовки твердой подложки, а также использование дополнительных реагентов, обеспечивающих образование ковалентной связи олигонуклеотида при соприкосновении с подложкой. Реакция присоединения олигонуклеотида к поверхности протекает на твердой фазе, что приводит к низкой эффективности иммобилизации. Способ не позволяет варьировать поверхностную емкость иммобилизованных олигонуклеотидов на ДНК-чипах, а также предусматривает использование только стеклянных слайдов в качестве твердой подложки. Технической задачей изобретения является упрощение известного способа и повышение его функциональных возможностей. Поставленная техническая задача достигается предлагаемым способом, заключающимся в следующем. Предварительно проводят синтез конъюгата олигонуклеотида с соответствующим линкером по стандартной методике [Годовикова Т.С., Зарытова В.Ф., Халимская Л.М. Биоорганическая химия, 1986, т.12, 475-481]. В качестве линкера используют различные полиамины. Олигонуклеотид, содержащий 5’- или 3’-концевую фосфатную группу, активируют парой трифенилфосфин-дипиридилдисульфид в присутствии нуклеофильного катализатора в абсолютном органическом растворителе (диметилсульфоксид или диметилформамид), после чего образующееся активное производное инкубируют с полиамином в подходящем растворителе (диметилсульфоксид, диметилформамид или вода), что приводит к образованию конъюгата пoлиaмин-oлигoнyклeoтид (PA-oligo) В качестве нуклеофильного катализатора преимущественно используют метилимидазол, диметиламинопиридин или N-окись диметиламинопиридина. В качестве полиамина могут использоваться различные полиамины, содержащие от 3 до 1000 аминогрупп в молекуле, в частности спермин, спермидин, полилизин, поли (лизин-фенилаланин), полиэтиленимин (фиг.1). К одной молекуле полиамина могут присоединиться несколько молекул олигонуклеотида. Соотношение PA/oligo можно варьировать, меняя исходное количество взятых в реакцию компонентов (полиамина и олигонуклеотида). Полученный раствор конъюгата PA-oligo разбавляют диметилсульфоксидом или водой до необходимой концентрации, равной от 1 Способ обеспечивает прочное связывание конъюгата PA-oligo с подложкой: промывание ДНК-чипов калий-фосфатным буфером (рН 7.0) и водой (~90°С) приводит к потере 10-20% иммобилизованного олигонуклеотида по сравнению со слайдами; промытыми буфером и водой при комнатной температуре; даже после отмывки детергентом олигонуклеотид все еще остается связанным с поверхностью (50%). Количество связавшегося с поверхностью иммобилизованного конъюгата PA-oligo и соответственно его поверхностная емкость линейно зависит от его концентрации в исходном растворе в широком диапазоне концентраций – от 1 Иммобилизованные конъюгаты PA-oligo проявляют с помощью раствора феназиний бромида (фиг.4) [Зарытова В.Ф., Кутявин И.В., Левина А.С., Мамаев С.В., Подыминогин М.А. Докл. АН СССР, 1988, т.302, 102-104] или с помощью конъюгата стрептавидин-щелочная фосфатаза и хромогенных субстратов в случае, если олигонуклеотид содержит биотиновую метку (фиг.5) [Кабилов М.Р., Пышный Д.В., Дымшиц Г.М., Гашникова Н.М., Покровский А.Г., Зарытова В.Ф., Иванова Е.М. Мол. биология, 2002, т.36, 424-431]. Для демонстрации возможности использования полученных предлагаемым способом ДНК-чипов в гибридизационном анализе проводили следующие эксперименты. Стеклянные слайды с иммобилизованным конъюгатом PA-oligo обрабатывали буфером, содержащим 400-звенный фрагмент ДНК, содержащий биотиновую метку и имеющий в своей структуре участок, комплементарный иммобилизованному олигонуклеотиду. В контрольном эксперименте использовали аналогичный фрагмент ДНК, не имеющий комплементарного участка. После проведения реакции с фрагментами ДНК слайды отмывали буфером, и присоединившиеся фрагменты ДНК проявляли по биотиновой метке с помощью конъюгата стрептавидин-щелочная фосфатаза и хромогенных субстратов. Из фиг.6 видно, что при исходной концентрации иммобилизованного олигонуклеотида 4 Определяющими отличиями предлагаемого способа от прототипа являются следующие. 1. Проводят предварительный синтез конъюгата полиамин-олигонуклеотид (PA-oligo), что позволяет: – практически количественно присоединять олигонуклеотид к твердой подложке; реакция, приводящая к образованию ковалентной связи между олигонуклеотидом и линкером, впоследствии иммобилизованным на поверхность, происходит с максимальной эффективностью; – присоединять конъюгат к любой твердой поверхности и таким образом расширить функциональные возможности способа, т.е. использовать получаемые конъюгаты как универсальные производные олигонуклеотидов для приготовления ДНК-чипов различного формата (ДНК-чипы на плоских слайдах и пленках, на пластиковых планшетах, на гранулированных носителях); – избежать использования кросс-сшивающих или активирующих реагентов в процессе иммобилизации олигонуклеотидных конъюгатов на твердую поверхность; – присоединять несколько молекул олигонуклеотида к полиамину, что повышает эффективность иммобилизации. – присоединять олигонуклеотид, содержащий полиаминовый линкер, к немодифицированной поверхности, что позволяет значительно упростить и ускорить процесс приготовления ДНК-чипов. 2. Нанесение раствора, содержащего конъюгат полиамин-олигонуклеотид, на твердую подложку осуществляют в концентрации 1 Пример 1. Предварительно осуществляют синтез конъюгата олигонуклеотида с полилизином (PA-oligo). К раствору олигонуклеотида pGCATCAAG (1 Пример 2. Эксперимент проводят, как в примере 1, но перед нанесением на подложку к раствору конъюгата добавляют NaOH до концентрации 0.001 М. Пример 3. Эксперимент проводят, как в примере 1, но в качестве полиамина используют спермидин. В качестве олигонуклеотида используют pGGCA-bio (bio – остаток биотина, присоединенный к 3’-концевому фосфату через пропилендиаминовый линкер). Раствор конъюгата наносят на стеклянную подложку микропипеткой по 2 мкл (диаметр образующихся пятен ~2 mm2). Визуализацию иммобилизованного конъюгата PA-oligo проводят по биотиновой метке с помощью конъюгата стрептавидин-щелочная фосфатаза и хромогенных субстратов (фиг.5). Пример 4. Эксперимент проводят, как в примере 1, но в качестве растворителя на стадии реакции с полиамином используют диметилсульфоксид (DMSO). Для этого активированный олигонуклеотид после взаимодействия с парой Рh3Р-Py2S2 в присутствии DMAP осаждают эфиром и переосаждают два раза эфиром из DMSO. Затем осадок растворяют в 96 мкл DMSO и добавляют 4 мкл 0.1 М раствора полилизина в DMSO. Пример 5. Эксперимент проводят, как в примере 1, но в качестве твердой подложки используют нитроцеллюлозу, нейлон и полихлорвинил (фиг.6 а, б и с соответственно). Проявление пятен проводят с использованием конъюгата стрептавидин-щелочная фосфатаза и хромогенных субстратов. Пример 6. Синтез PA-oligo проводят, как в примере 1. В качестве олигонуклеотида используют 15-мер GATTATTTGGAAAAGp. Реакционную смесь после синтеза конъюгата PA-oligo разбавляют водой до необходимой концентрации (2 Предлагаемый способ получения ДНК-чипов обладает следующими преимуществами перед известным способом: – иммобилизацию олигонуклеотидов на поверхность твердой подложки осуществляют более простой, воспроизводимой и эффективной процедурой; – иммобилизация конъюгатов PA-oligo на твердую поверхность протекает практически количественно; – поверхностную емкость иммобилизованных олигонуклеотидов варьируют путем изменения исходной концентрации конъюгата PA-oligo; – для получения олигонуклеотидных конъюгатов используют полиамины с числом аминогрупп в молекуле от 3 до 1000; – способ обеспечивает получение стабильных коньюгатов, которые могут храниться в растворе в течение, по крайней мере, нескольких месяцев перед использованием; – конъюгаты олигонуклеотидов с полиаминами могут присоединяться к любой твердой поверхности, что делает их универсальными производными для получения ДНК-чипов любого формата. Кроме того, предлагаемый способ обеспечивает “трехмерную” иммобилизацию олигонуклеотидов на твердую поверхность, что позволяет имитировать “растворный” (более эффективный, чем твердофазный) вариант проведения последующих реакций с биополимерами. Иммобилизованные олигонуклеотиды находятся на оптимальном расстоянии от поверхности твердой подложки, что позволяет избежать стерических затруднений при последующих взаимодействиях с биомолекулами, находящимися в растворе. Формула изобретения
1. Способ получения ДНК-чипов, включающий синтез конъюгата олигонуклеотида с соответствующим линкером, нанесение раствора полученного коньюгата на поверхность твердой подложки в виде рядов точек с последующим высушиванием и отмывкой от неприсоединившихся компонентов, отличающийся тем, что в качестве линкера используют полиамин, а нанесение конъюгата полиамин-олигонуклеотид на твердую подложку осуществляют в концентрации 1 2. Способ по п.1, отличающийся тем, что в качестве линкера используют полиамины, содержащие от 3 до 1000 аминогрупп в молекуле, преимущественно спермин, спермидин, полилизин, поли(лизин-фенилаланин), полиэтиленимин. 3. Способ по п.1, отличающийся тем, что в качестве твердой подложки используют стекло, кремний, капрон, нитроцеллюлозу, бумагу, пластиковые планшеты, металл, керамику, полимерные материалы. РИСУНКИ
|
||||||||||||||||||||||||||

 10-7-1
10-7-1