Патент на изобретение №2236414
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЁННЫХ ЭТИЛ-(2-ДИАЛКОКСИФОСФОРИЛ-4ЦИАНО)-БУТАНИМИДАТОВ
(57) Реферат:
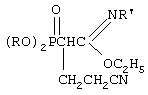
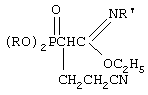
Изобретение относится к химии фосфорорганических соединений, а именно к новому способу получения N-замещенных фосфорилированных имидатов, имеющих в структуре цианэтильную группу. Описывается способ получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов заключающийся во взаимодействии N-замещенных этил-(2-диалкоксифосфорил)этанимидатов с акрилонитрилом в присутствии катализатора этилата натрия в среде диоксана при мольном соотношении N-замещенный этил-(2-диалкоксифосфорил)этанимидат : акрилонитрил : этилат натрия (1:1,05-1,15:0,1-0,15) соответственно и температуре 40-60°С. Технический результат – получение новых химических соединений перспективных для получения биологически активных соединений для нужд медицины и сельского хозяйства. Изобретение относится к химии фосфорорганических соединений, а именно к новому способу получения N-замещенных фосфорилированных имидатов, имеющих в структуре цианэтильную группу, общей формулы где R=С3-С4 – алкил или изоалкил; R’=С(O)СН3, С(O)С6Н5, Si(CH3)3; которые являются новыми по структуре фосфорорганическими соединениями и могут служить исходными в получении биологически активных соединений для нужд медицины и сельского хозяйства. Осуществление предложенного способа оказалось возможным благодаря наличию в исходных N-замещенных этил-(2-диалкоксифосфорил) этанимидатах высоких С-Н-кислотных свойств активированной метиленовой группы. Известно присоединение нитрила диалкоксифосфорилуксусной кислоты к эфирам непредельных карбоновых кислот с получением бифункциональных соединений сложной структуры, содержащих нитрильную и сложноэфирную группировки. Реакции проводились в присутствии алкоголятов щелочных металлов в безводных спиртах при нагревании реакционных смесей до 4 часов на кипящей водяной бане (А.Н. Пудовик, Н.М. Лебедева. ЖОХ, 1955, т.25, с.1920-1924. А.Н. Пудовик, Н.М. Лебедева. ЖОХ, 1955, т.25, с.2235-2240). Недостатками данного метода являются невысокие выходы (менее 17-71%) продуктов присоединения. А также в результате получают соединения иной структуры, чем в предлагаемом изобретении. Известен метод присоединения эфира диалкоксифосфорилуксусной кислоты к акрилонитрилу в присутствии в качестве катализатора этилата натрия с получением С-цианэтилированных эфиров диалкоксифосфорилуксусной кислоты. Процессы проводились в растворе этилового спирта, общий выход нитрилов составил 50% от теоретического (Присоединение фосфонуксусного эфира и его гомологов к непредельным электрофильным реагентам. А.Н. Пудовик, Н.М. Лебедева. ЖОХ, т.22, № 12, 1952, с.228-2132). Недостатком данного метода является невысокий выход нитрилов. Вышеописанным методом получают соединения совершенно иной структуры по сравнению с предлагаемым изобретением. Задачей предлагаемого изобретения является разработка нового технологичного малостадийного метода синтеза N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов. Техническим результатом является расширение арсенала химических соединений, получение новых N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов с высоким выходом (более 75%) перспективных для получения биологически активных соединений для нужд медицины и сельского хозяйства. Указанный технический результат достигается разработкой нового способа получения N-замещенных этил-(2-диалкокси-фосфорил-4-циано)бутанимидатов формулы где R=С3-С4-алкил или изоалкил; R’=С(O)СН3, С(O)С6Н5, Si(СН3)3; заключающийся во взаимодействии N-замещенных этил-(2-диалкоксифосфорил) этанимидатов с акрилонитрилом в присутствии катализатора этилата натрия в среде диоксана при мольном соотношении N-замещенный этил-(2-диалкоксифосфорил)этанимидат : акрилонитрил : этилат натрия (1:1,05-1,15:0.1-0,15) соответственно и температуре 40-60 Химическая схема предложенного способа получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов: где R=C3-C4 – алкил или изоалкил; R’=C(O)CH3,C(O)C6H5, Si(CH3)3; Нуклеофильное присоединение N-замещенных алкил(диалкоксифосфорил) этанимидатов к акрилонитрилу происходит по Вначале реакции образуется амбидентный анион из этанимидата под действием алкокси-аниона Затем образовавшийся анион нуклеофильно атакует молекулу акрилонитрила с образованием мезомерного аниона. Этот мезомерный анион является сильным основанием и способен отрывать протон от молекулы этилового спирта. Не исключено, что в качестве донора протона выступает метиленовая группа N-замещенного алкил(диалкоксифосфорил)этанимидата. При выборе растворителя для проведения реакций присоединения к акрилонитрилу нами были учтены следующие требования к растворителю: создание гомогенной реакционной массы, поддержание необходимого температурного режима и инертность по отношению к реагирующим компонентам. Всем этим требованиям отвечает диоксан, в нем растворяется этилат натрия и другие реагенты, есть возможность повышения температуры до 60 В начальный момент взаимодействия нет необходимости в дополнительном нагреве, так как реакция начинается самопроизвольно даже при комнатной температуре. Затем для повышения степени превращения исходных реагентов и ускорения реакции проводили дополнительное нагревание реакционной массы до 40-60 Использование в данном процессе 5-15% избытка акрилонитрила по сравнению со стехиометрическим количеством необходимо из-за взаимодействия его со следами этилового спирта, вносимого в реакционную массу с катализатором. Предложенный метод получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов характеризуется простотой эксперимента, осуществляется в достаточно мягких условиях и обеспечивает высокий (более 75%) выход целевых соединений. Способ осуществляется следующим образом. Для синтеза N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов к смеси, состоящей из N-замещенного этил-(2-диалкоксифосфорил)этанимидата и акрилонитрила, взятых в мольных количествах 1:1,05-1,15 соответственно и растворенных в осушенном диоксане, при комнатной температуре и перемешивании прибавляли небольшими порциями катализатор – этилат натрия. Количество катализатора составляло 10-15 мол.% от количества N-замещенного имидата. Процесс протекает с небольшим разогревом реакционной массы, и для завершения его рекомендуется нагревание реакционной смеси при 50-60 Пример 1. Этил-N-ацетил-(2-диизопропоксифосфорил-4-циано)бутанимидат, К смеси 4,0 г (0,0136 моль) этил-N-ацетил-(2-диизопропокси-фосфорил)этанимидата, 0,8 г (0,0150 моль, 10% изб. мольн.) акрилонитрила и 16 мл сухого диоксана при температуре 20-25 ИК-спектр, Пример 2. Этил-N-триметилсилил-(2-дибутоксифосфорил-4-циано)бутанимидат, К смеси 5,0 г (0,0142 моль) этил-N-триметилсилил-(2-дибутоксифосфорил)этанимидата, 0,85 г (0,0156 моль, 10% изб. мольн.) акрилонитрила и 18 мл сухого диоксана при температуре 20-25 ПК-спектр, Пример 3. Этил-N-ацетил-(2-дибутоксифосфорил-4-циано)бутанимидат, К смеси 4,5 г (0.0140 моль) этил-N-ацетил-(2-дибутокси-фосфорил)этанимидата, 0,9 г (0.0161 моль, 15% изб. мольн.) акрилонитрила и 16 мл сухого диоксана при температуре 20-25 ИК-спектр, Пример 4. Этил-N-бензоил-(2-диизопропоксифосфорил-4-циано)бутанимидат, К смеси 6,0 г (0,0169 моль) этил-N-бензоил-(2-диизопро-поксифосфорил)этанимидата, 0,96 г (0,0177 моль, 5% изб. мольн.) акрилонитрила и 20 мл сухого диоксана при температуре 20-25 ИК-спектр, Предложенный метод позволяет осуществлять синтез N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов из соответствующих этанимидатов, что оказалось возможным вследствие высоких С-Н-кислотных свойств активированной метиленовой группы последних. Метод заключается во взаимодействии N-замещенных этил-(2-диалкоксифосфорил)этанимидатов с акрилонитрилом в присутствии этилата натрия в качестве катализатора с образованием N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов. Достоинством разработанного метода является простота технологии и универсальность, так как он позволяет из соответствующих исходных этанимидатов получать С-цианэтилированные их гомологи. Формула изобретения
Способ получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов где R-C3-C4-алкил или изоалкил; R’-C(O)CH3, C(O)C6H5, Si(CH3)3, заключающийся во взаимодействии N-замещенных этил-(2-диалкоксифосфорил)этанимидатов с акрилонитрилом в присутствии катализатора-этилата натрия в среде диоксана при мольном соотношении N-замещенный этил-(2-диалкоксифосфорил)этанимидат:акрилонитрил:этилат натрия (1:1,05-1,15:0,1-0,15) соответственно и температуре 40-60°С. MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 30.04.2005
Извещение опубликовано: 10.12.2006 БИ: 34/2006
|
||||||||||||||||||||||||||

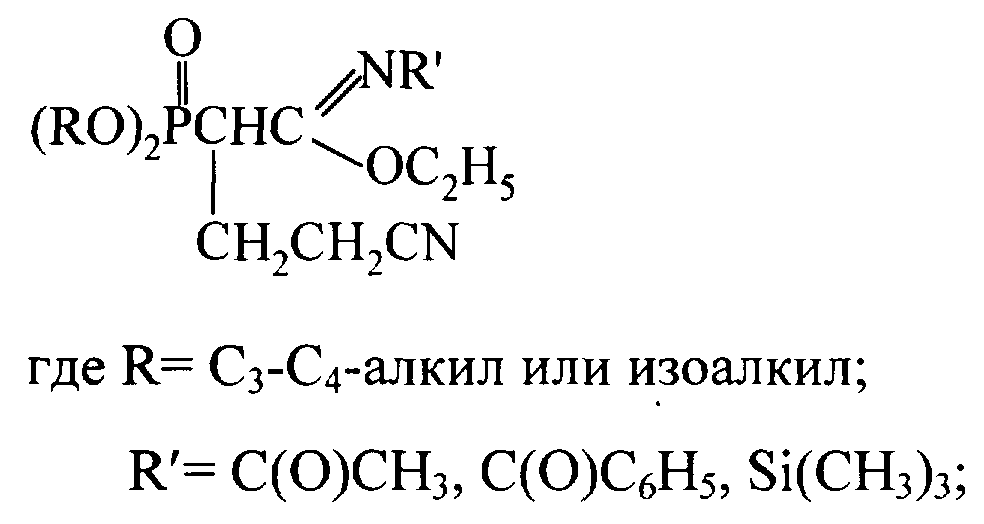
 С.
С.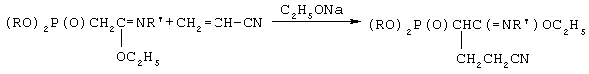
 -углеродному атому. На основании изучения литературных данных механизм взаимодействия N-замещенного этил(диалкоксифосфорил)этанимидата с акрилонитрилом можно представить следующим образом:
-углеродному атому. На основании изучения литературных данных механизм взаимодействия N-замещенного этил(диалкоксифосфорил)этанимидата с акрилонитрилом можно представить следующим образом: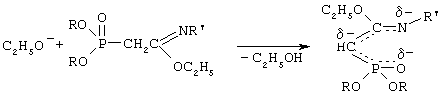
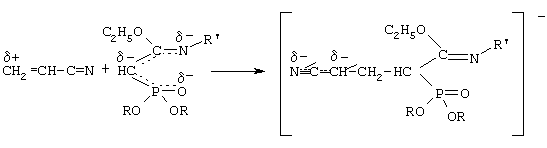
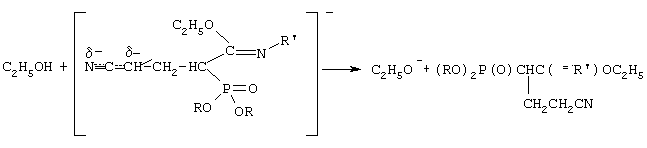
 LC 5/40. Идентификация синтезированных соединений проводилась по данным элементного анализа, молекулярной рефракции, определения молекулярной массы, ИК-спектроскопии. Для лучшего понимания сущности предложенного технического решения приводятся конкретные примеры синтезов.
LC 5/40. Идентификация синтезированных соединений проводилась по данным элементного анализа, молекулярной рефракции, определения молекулярной массы, ИК-спектроскопии. Для лучшего понимания сущности предложенного технического решения приводятся конкретные примеры синтезов.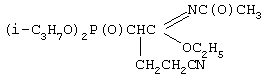
 , см-1: 775, 980-1020 (РОС); 1124 (СОС); 1248 (Р=O); 1660 (C=N); 1720 (NC=O); 2240 (C
, см-1: 775, 980-1020 (РОС); 1124 (СОС); 1248 (Р=O); 1660 (C=N); 1720 (NC=O); 2240 (C N).
N).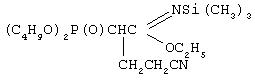
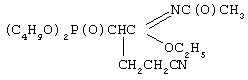
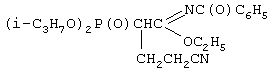
 Car); 1676 (C=N); 1736 (NC=O); 2250 (C
Car); 1676 (C=N); 1736 (NC=O); 2250 (C