Патент на изобретение №2236411
|
||||||||||||||||||||||||||
(54) МЕТАЛЛОКОМПЛЕКСЫ КАРБОРАНИЛПОРФИРИНОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ
(57) Реферат:
Изобретение относится к новым соединениям, металлкомплексам карборанилпорфиринов общей формулы I, обладающим противоопухолевой активностью и низкой токсичностью, которые могут быть использованы в борнейтронзахватной терапии рака. 3 ил. Изобретение относится к новым соединениям общей формулы I; которые могут быть использованы в борнейтронзахватной терапии рака (БНЗТ), Известно по аналогичной структуре соединение (S. В. Kahl and M.S. Коо./ Synthesis of Tetrakis-carborane-carboxylate Esters of 2,4-Bis-( Соединение было получено при взаимодействии хлорангидрида 1-о-карборанкарбоновой кислоты с диметиловым эфиром бис-( Полученные соединения могут быть использованы для БНЗТ. Нами предлагается синтез металлокомплексов карборанилпорфиринов, расширяющих ассортимент препаратов, потенциально возможных в применении к методу БНЗТ. Использовались производные 5,10,15,20-тетрафенилпорфирина и природный гемин – железный комплекс протопорфирина IX, которые вводились в конденсации с различными карборанами. Мы синтезировали новые металлокомплексы карборанилпорфиринов на основе природных или синтетических порфиринов. В описании изобретения приведено несколько типов данных соединений. Пример №1 1,3,5,8-Тетраметил-2,4-дивинил-6,7-ди[2′-(м-карборан-9-ил)метоксикарбонилэтил]порфиринато железо (III) (1a). К раствору 100 мг (0,15 ммоля) протогемина в 8 мл хлористого метилена и 8 мл пиридина, охлажденному до 0 Электронный спектр (СНСl3), По данной методике получены также соединения 1б,1г, 1д, 1е. 1,3,5,8-Тетраметил-2,4-дивинил-6,7-ди[2′-N-(о-карборан-3-ил)кар-бамоилэтил]порфиринато железо (III) (1б). Выход: 86,7 мг (62%). Электронный спектр (СНСl3), Пример №2 1,3,5,8-Тетраметил-2,4-дивинил-6,7-ди[2′-(нидо-7,8-ди-карборан-3-ил)карбамоилэтил]порфиринато железо (III) тетрабутиламмоний (1в). К раствору 50 мг (0.05 ммоля) (1б) в 15 мл тетрагидрофурана прибавляют 39.2 мг (0.15 ммоля) тетрабутиламмония и кипятят 4 часа. Отогняют тетрагидрофуран, промывают остаток 15 мл воды, отфильтровывают, осадок сушат. Выход 47.5 мг (85%). Электронный спектр (СНСl3), По аналогичной методике получены также соединения 1ж, 1л, 1м, 1н. 1,3,5,8-Тетраметил-2,4-дивинил-6(7)-[2′-(клозо-монокарборан-1-ил)-метоксикарбонилэтил]-7(6)-(2′-карбоксиэтил)порфиринато железо (III) (1г). Выход 65.8мг (57%). Электронный спектр (СНСl3), 1,3,5,8-Тетраметил-2,4-дивинил-6(7)-[2′-фенил,2′-(клозо-монокарборан-1-ил)метоксикарбонилэтил]-7(6)-(2′-карбоксиэтил)порфиринато железо (III) (1д). Выход 74,9 мг (59%). Электронный спектр (СНСl3), 1,3,5,8-Тетраметил-2,4-дивинил-6(7)-[2′-(клозо-монокарборан-1-ил)-метоксикарбонилэтил]-7(6)-[2′-N-(о-карборан-3-ил)карбамоилэтил]порфиринато железо (III) (1е). Выход 37.4 мг (63%). Электронный спектр (СНСl3), Пример №3 [2-(1′-клозо-о-метилкарборанил)гидроксиметил-5,10,15, 20-тетрафенилпорфиринато] медь(II) (1ж). К раствору 70 мг (0.1 ммоль) медного комплекса 2-формил-5,10,15,20-тетрафенилпорфирина в 10 мл тетрагидрофурана прибавляют при 20 Реакционную массу выливают в 15 мл воды, экстрагируют хлористым метиленом (3*5) мл. Растворитель отгоняют в вакууме, остаток очищают на колонке с сили-кагелем. Выход 46 мг (53%). Электронный спектр (СНСl3), По аналогичной методике получены также соединения 1з, 1и, 1к. [2-(1′-клозо-м-изопропилкарборанил) гидроксиметил-5,10,15,20-тетрафенилпорфиринато] медь(II) (1з). Выход 51 мг (57%). Электронный спектр (СНСl3), [2-(1′-клозо-о-метилкарборанил)гидроксиметил-5,10,15,20-тетрафенилпорфиринато] кобальт(II) (1и). Выход 40 мг (46%). Электронный спектр (СНСl3), [2-(1′-клозо-м-изопропилкарборанил) гидроксиметил-5,10,15,20-тетрафенилпорфиринато] кобальт(II) (1к). Выход 48 мг (54%). Электронный спектр (СНСl3), [2-(1′-нидо-о-метилкарборанилтетрабутиламмоний) гидроксиметил-5,10,15, 20-тетрафенилпорфиринато] медь(II) (1л). Выход 36 мг (65%). Электронный спектр (СНСl3), [2-(1′-нидо-м-изопропилкарборанилетрабутиламмоний) гидроксиметил-5,10,15,20-тетрафенилпорфиринато] кобальт(II) (1м). Выход 38 мг (67%). Электронный спектр (СНСl3), Все металлокомплексы карборанилпорфиринов были выделены с помощью колоночной хроматографии в виде микрокристалллов темно-красного цвета, хорошо растворимых в хлороформе, хлористом метилене, ацетоне, диметилсульфоксиде, метаноле и плохо растворимые в воде. Ниже представлены результаты испытаний противоопухолевой активности основных представителей новых металлокомплексов карборанилпорфиринов. Исследована цитотоксическая активность основных представителей новых металлокомплексов карборанилпорфиринов для культивируемых линий опухолевых клеток человека А549 (аденокарцинома легких) и К562 (лейкоз). В параллельных экспериментах тестировали токсичность этих же соединений для неопухолевых клеток – культура первичных фибробластов кожи человека (ФКЧ). Вещества растворяли в диметилсульфоксиде до концентрации 10 мМ. Дальнейшие разведения проводили в водных средах; конечная концентрация диметилсульфоксида в культуре клеток не превышала 0,1% и не оказывала влияния на жизнеспособность клеток. Гибель клеток, определяемую по восстановлению клетками 1-(4,5-диметилтиазол-2-ил)-3,5-дифенилформазана (МТТ-тест) [Mossman, 1983], регистрировали через 72 ч инкубации клеток с металлокомплексами карборанилпорфиринов. На первом этапе тестирования представлялось необходимым подтвердить, что металлокомплексы порфиринов обладают не меньшей цитотоксичностью, чем исходный тетрафенилпорфирин. Действительно, введение Сu в координационную сферу тетрафенилпорфирина позволило получить несколько более активное соединение (фиг. 1). Этот эксперимент установил принципиальную возможность использования металлокомплексов порфиринов для индукции гибели опухолевых клеток. Далее испытаны соединения-представители основных групп заявляемых веществ. На фиг.2 представлены сравнения противоопухолевой активности 1,3,5,8-тетраметил-2,4-дивинил-6(7)-[2’клозо-монокарборан-1-ил)метилоксикарбонилэтил]-7(6)-(2-карбоксиэтил)порфирината железа (1г), а также -о-метил- (1л), м-изопропил-клозо- (1ж) и нидо- (1з) карборанилпроизводных медного комплекса тетрафенилпорфирина. Такой выбор соединений для биологических испытаний объясняется тем, что 1г представляет собой производное природного соединения – протогемина, а 1ж-л являются производными синтетического тетрафенилпорфирина. Оказалось, что наибольшей активностью обладало соединение 1з (концентрация, вызывающая гибель 50% клеток (ЛД50), составила около 13 мкМ) (фиг. 2). Вещества 1ж и 1л также вызывали гибель клеток А549 в низких микромолярных концентрациях(фиг. 2). Наконец, изучена токсичность наиболее активного производного – 1з – для опухолевых (К562) и неопухолевых (ФКЧ) клеток. Важно, что этот медьсодержащий карборанилпорфирин был нетоксичен для ФКЧ в концентрациях до 100 мкМ в течение 72 ч инкубации, тогда как это же вещество вызывало гибель клеток К562 в более низких дозах: ЛД50 порядка 10 мкМ (фиг. 3). Лишь в высоких концентрациях (около 100 мкМ), при которых карборанилпорфирины образовывали преципитаты в водной среде, медьсодержащее соединение 1з вызывало незначительное снижение выживание неопухолевых фибробластов. Таким образом, преимущественная активность новых карборанилпорфиринов для культивируемых злокачественных клеток в сравнении с неопухолевыми позволяет считать эти соединения перспективными для дальнейших исследований как противоопухолевых агентов. Подписи к чертежам Цитотоксичность новых металлокомплексов карборанилпорфиринов для клеточных линий А549 (фиг.1-2), К562 и ФКЧ (фиг.3). Фиг.1: возрастание токсичности при металлировании ТФП; фиг. 2: – сравнительная активность металлокомплекса карборанилпорфирина на основе гемина (1г) и медьсодержащих карборанилпорфиринов (1ж-л); фиг.3: – токсичность 1з для опухолевых (К562), но не для неопухолевых (ФКЧ) клеток. Цитотоксическую активность соединений определяли в МТТ-тесте (96-луночный формат). Формула изобретения
Металлокомплексы карборанилпорфиринов общей формулы где Iа: R=H; R1=R3=R5=R8= -CH3; R2=R4= -CH=CH2; R6=R7=м-C2B10H11-CH2-COO-(CH2)2-; M=Fe+ Iб: R=H; R1=R3=R5=R8= -CH3; R2=R4= -CH=CH2; R6=R7= o-C2B10H11-NH-CO-(CH2)2-; M=Fe+ Iв: R=H; R1=R3=R5=R8= -CH3; R2=R4= -CH=CH2; Iг: R=H; R1=R3=R5=R8= -CH3; R2=R4= -CH=CH2; R6(R7)= -(CH2)2-COO-CH2-CB11H–11 R6(R7)= -CH2CH2COOH; M=Fe+ Iд: R=H; R1=R3=R5=R8= -CH3; R2=R4= -CH=CH2; R6(R7)= -CH2CH2COOH; M=Fe+ Iе: R=H; R1=R3=R5=R8= -CH3; R2=R4= -CH=CH2; R6(R7)= o -C2B10H11-NH-CO-(CH2)2– R6(R7)= -(CH2)2-COO-CH2-CB11H–11; M=Fe+ Iж: R=C6H5; R2=R3=R4=R5=R6=R7=R8=H; M=Cu Iз: R=C6H5; R2=R3=R4=R5=R6=R7=R8=H; M=Cu Iи: R=C6H5; R2=R3=R4=R5=R6=R7=R8=H; M=Co Iк: R=C6H5; R2=R3=R4=R5=R6=R7=R8=H; M=Co Iл: R=C6H5; R2=R3=R4=R5=R6=R7=R8=H; M=Cu Iм: R=C6H5; R2=R3=R4=R5=R6=R7=R8=H; M=Co, обладающие противоопухолевой активностью. РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 07.06.2008
Извещение опубликовано: 20.06.2010 БИ: 17/2010
|
||||||||||||||||||||||||||

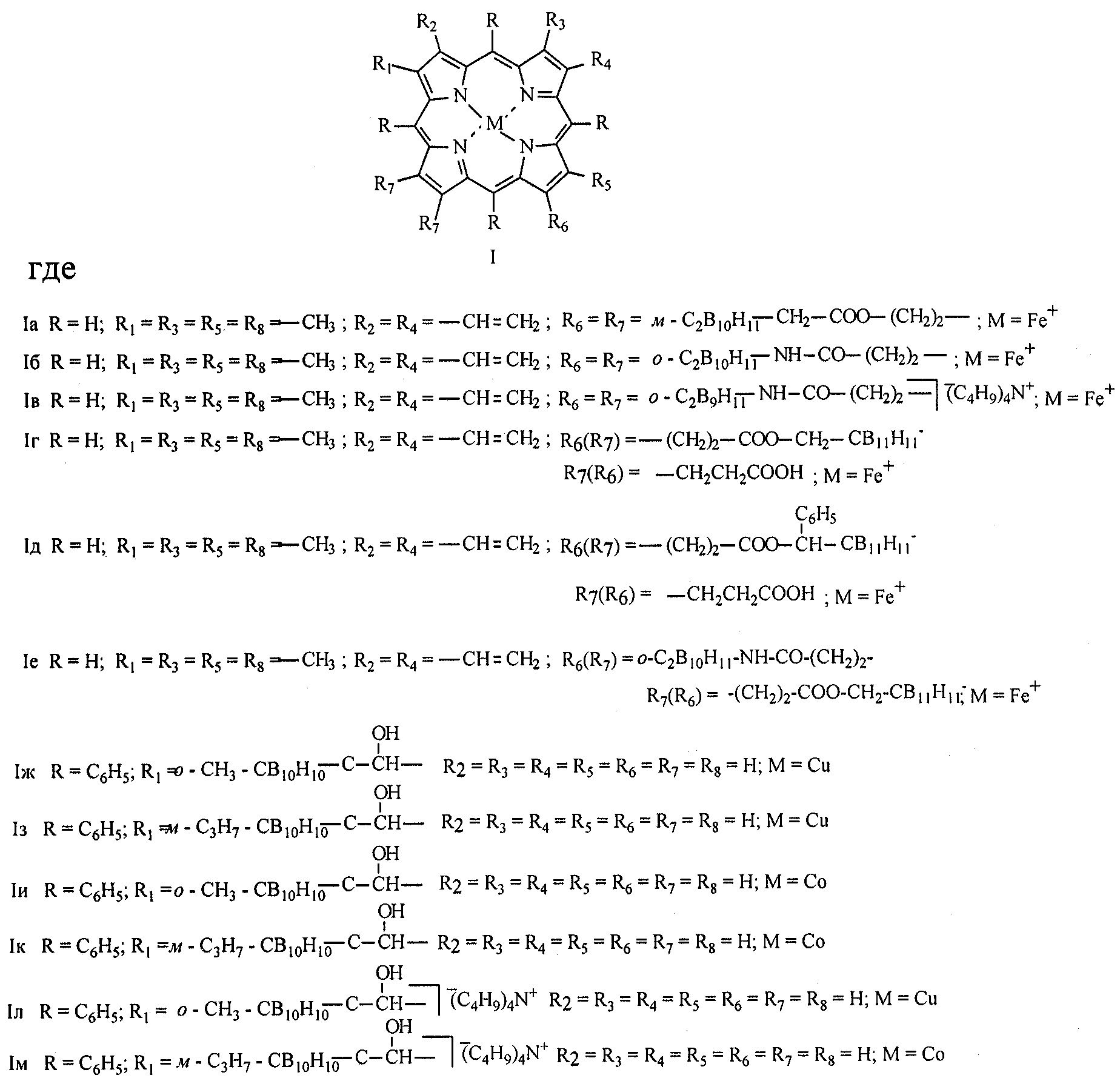
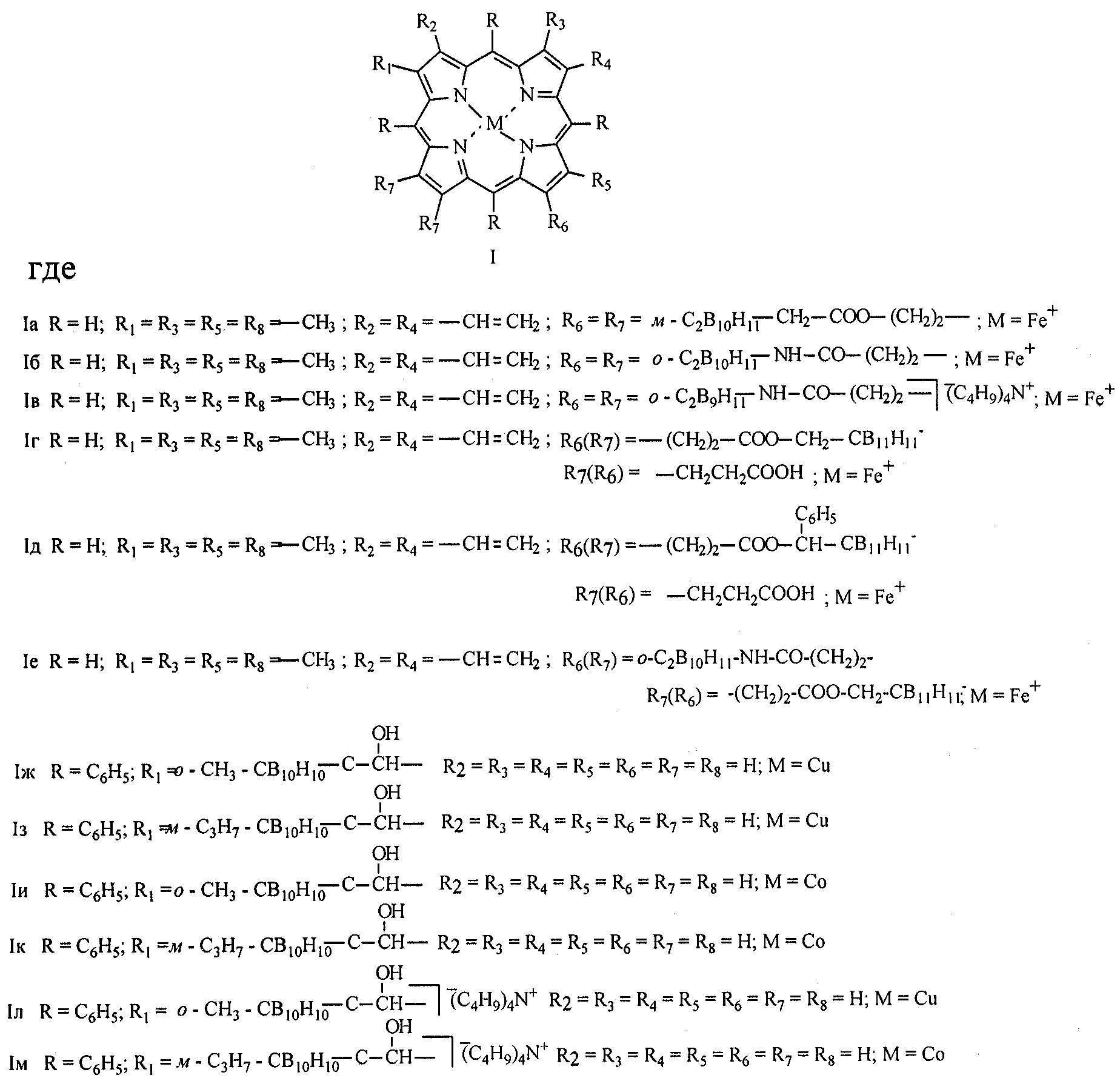
 ,
,
 С, прибавляют 100 мг (0.46 ммоля) дитретбутилпирокарбоната и перемешивают 10 мин. Затем прибавляют 9-гидроксиметил-м-карборан и еще через пять минут 10 мг 4-диметиламинопиридина. Реакционную массу перемешивают 4 ч. После отгонки растворителей в вакууме продукт выделяют с помощью колоночной хроматографии на силикагеле. Выход: 102,7 мг (71%).
С, прибавляют 100 мг (0.46 ммоля) дитретбутилпирокарбоната и перемешивают 10 мин. Затем прибавляют 9-гидроксиметил-м-карборан и еще через пять минут 10 мг 4-диметиламинопиридина. Реакционную массу перемешивают 4 ч. После отгонки растворителей в вакууме продукт выделяют с помощью колоночной хроматографии на силикагеле. Выход: 102,7 мг (71%). max, нм (
max, нм (
 10-3): 643 (5.22); 542 (10.78); 511.4 (11.19); 389.2 (99.00). ИК-спектр (KBr),
10-3): 643 (5.22); 542 (10.78); 511.4 (11.19); 389.2 (99.00). ИК-спектр (KBr),  , см-1: 2590 (ВН), 1713 (СО), 1602 (-СН=СН2). Масс-спектр, m/z: 964 [М+].
, см-1: 2590 (ВН), 1713 (СО), 1602 (-СН=СН2). Масс-спектр, m/z: 964 [М+].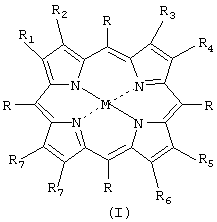
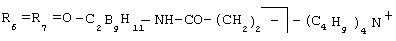 ; M=Fe+
; M=Fe+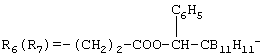
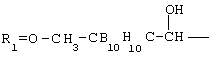 ;
;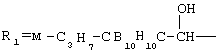 ;
;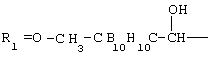 ;
;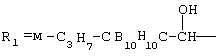 ;
;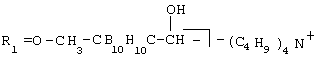 ;
;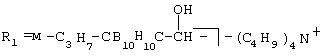 ;
;