Патент на изобретение №2236235
|
||||||||||||||||||||||||||
(54) АГОНИСТ МЕДИ, КОТОРЫЙ СВЯЗЫВАЕТСЯ С САЙТОМ СВЯЗЫВАНИЯ МЕДИ АМИЛОИДНОГО ПРОТЕИНА-ПРЕДШЕСТВЕННИКА (АРР) И/ИЛИ ОКАЗЫВАЕТ ИНГИБИРУЮЩЕЕ ДЕЙСТВИЕ НА ВЫСВОБОЖДЕНИЕ АМИЛОИД-А
(57) Реферат:
Изобретение относится к области медицины и касается агониста меди, который связывается с сайтом связывания меди амилоидного протеина-предшественника (АРР) и/или оказывает ингибирующее действие на высвобождение амилоид А
Настоящее изобретение относится к агонистам меди, которые связываются с сайтом связывания меди амилоидного протеина-предшественника (АРР) и/или оказывают ингибирующее действие на высвобождение амилоид-А При болезни Альцгеймера Несмотря на то, что физиологическая роль АРР выявлена еще неокончательно, АРР обладает некоторыми особенностями, сходными с молекулами клеточной адгезии и молекулами, участвующими в заживлении ран. К ним относятся, например, сайты связывания АРР с сульфатом гепарина, коллагеном, ламинином, протеазами, лектином и ионами металлов. Предпринимающиеся в настоящее время попытки лечения болезни Альцгеймера направлены на то, чтобы блокировать образование амилоид-А Таким образом, в основу настоящего изобретения была положена задача разработать средства, которые можно было бы использовать для предупреждения или лечения болезни Альцгеймера. Указанная задача решается с помощью отличительных признаков, представленных в формуле изобретения. Было установлено, что АРР специфично взаимодействуют с Zn (II) и Cu (II) в двух определенных сайтах. Связывание с Cu(II) вызывает окисление двух цистеинов АРР, что приводит к образованию дополнительного цистина. Один из двух высвободившихся в результате этого электронов восстанавливает связанную медь (II) до меди (I), судьба же второго электрона до настоящего времени не выяснена. Было установлено далее, что добавление меди (II) в клетки млекопитающих приводит к увеличению высвобождения АРР-продуктов Таким образом, один из объектов настоящего изобретения относится к агонисту меди, отличающемуся тем, что он связывается с сайтом связывания меди амилоидного протеина-предшественника (АРР) и/или уменьшает или ингибирует высвобождение амилоид-А В контексте настоящего изобретения понятие “агонист меди” относится к любой субстанции, например к неорганическому или органическому соединению, которое может связываться с сайтом связывания меди АРР и/или уменьшать либо ингибировать высвобождение амилоид-А Таким образом, действие в качестве агониста меди предпочтительно основано на том, что субстанция специфично и с более высокой аффинностью, чем ионы меди, связывается с сайтом связывания меди АРР или специфично связывается с той областью последовательности АРР, которая ответственна за связывание с медью, и, присутствуя в сайте (стерически), препятствует дальнейшему связыванию меди, соответственно вытесняет ионы меди. Агонисты меди представляют собой такие конкурентно (за сайты связывания меди) и неконкурентно связывающие лиганды, которые могут имитировать физиологическое действие меди. В контексте настоящего изобретения агонисты меди представляют собой и такие субстанции, которые не связываются с сайтами связывания меди, но, например, стабилизируют конформацию АРР, характерную для комплекса медь-АРР, т.е. могут имитировать физиологическое действие меди на другие сайты связывания (помимо непосредственного сайта связывания меди). В контексте настоящего описания понятие “уменьшать или ингибировать высвобождение амилоид-А Специалист может на основе обычных стандартных для данной области методов идентифицировать и получить соединения, обладающие описанным выше действием в качестве агонистов меди. В случае агонистов, которые не встречаются в естественных условиях (например, для небольших синтезированных методами органической химии веществ, которые представлены в виде так называемых библиотек), олигонуклеотидов, олигопептидов и нуклеотидных аналогов, синтез осуществляют согласно обычным методам, которые хорошо известны специалисту. Субстанции, которые могут служить в качестве потенциальных агонистов, можно выявлять с помощью аффинной хроматографии, например, с использованием метода “BIAcore-Technik”. При этом указанные выше соединения тестируют в отношении связывания с АРР, прежде всего с доменами АРР, которые содержат сайты связывания меди. Затем выявленные лиганды тестируют в отношении действия на АРР-процессирование в системе клеточной культуры, например, с помощью анализа конкурентного связывания с соответствующими антителами. На основе этого специалист также с помощью обычных методов, например, аналогичных методам, описанным в примерах 4 и 5, может определить, являются ли выявленные агонисты переносимыми для пациентов, и при необходимости установить зависимость действия от дозы. Таким образом, предлагаемый в изобретении способ выявления агонистов меди, которые связываются с сайтом связывания АРР и/или оказывают ингибирующее действие на высвобождение амилоид-А (а) АРР или один из его фрагментов, несущий сайт связывания меди, вводят в контакт с различными концентрациями соединения, которое может обладать указанным выше действием, и (б) выявляют уменьшение количества А В предпочтительном варианте осуществления этот способ отличается тем, что (а) АРР или один из его фрагментов, несущий сайт связывания меди, вводят в контакт с находящейся в растворе или иммобилизованной библиотекой субстанций, соответственно с низкомолекулярными субстанциями, выделенными из микроорганизмов и/или растений, (б) с использованием находящейся в растворе библиотеки субстанций или жидких низкомолекулярных субстанций проводят иммунопреципитацию комплекса сайт связывания меди/лиганды из раствора, содержащего антитела, которые являются специфичными для АРР или его фрагмента, или с использованием иммобилизованной библиотеки субстанций высвобождают лиганды из комплекса сайт связывания меди/лиганды путем добавления солей меди, (в) выявляют лиганды и (г) отбирают лиганды, которые в результате конкурентного или неконкурентного связывания с сайтами связывания меди АРР или другими сайтами АРР оказывают ингибирующее действие на высвобождение амилоид-А В контексте настоящего изобретения понятие “лиганд” означает любую субстанцию, которая при осуществлении указанных выше способов связывается с сайтами связывания меди или другими сайтами АРР. Указанные выше антитела представляют собой, например, моноклональные или поликлональные антисыворотки, которые распознают АРР и пригодны для иммунопреципитации. Они имеются в продаже, например производятся фирмой Boehringer Mannheim, фирмой Dianova, фирмой Sigma. Другие антитела, пригодные для выявления АРР, комплексов АРР и A В качестве библиотек субстанций используют банки органических химических соединений, которые в результате случайного синтеза образуются вокруг “лидерной” субстанции. Такие библиотеки могут быть получены на коммерческой основе (например, от фирмы Morphosys, Мюнхен; фирмы Analytikon, Берлин) или могут быть получены в результате сотрудничества с химическими лабораториями (например, новые химические соединения, получаемые с использованием комбинационной химии). Низкомолекулярные субстанции можно выделять из микроорганизмов и растений с помощью BIAcore-метода. Контактирование осуществляют либо с находящимися в растворе, либо с иммобилизованными АРР, соответственно фрагментами АРР. Образовавшиеся комплексы осаждают из раствора с помощью антител и затем выявляют с помощью флуоресценции, радиоактивности или аналитическими методами, такими как масс-спектроскопия, газовая хроматография и т.д. Для выявления соответствующего фрагмента АРР сначала определяют связывание тестируемых субстанций со всем АРР, а затем выявляют все более и более короткие фрагменты, которые обладают такими же способностями к связыванию, что и полноразмерная молекула. Еще одной возможностью осуществления стадии (б) является использование метода аффинной хроматографии, например BIAcore, при котором либо молекулу АРР, либо ее лиганды иммобилизуют на поверхности носителя. Затем на эту поверхность наносят путем инъекции соответствующую молекулу и, если происходит связывание, то вводят соль меди для того, чтобы снова разорвать связь. За этим процессом можно осуществлять непосредственное наблюдение с помощью биосенсорного метода. В предпочтительном варианте осуществления способ идентификации по изобретению включает стадию (г) инкубации клеток млекопитающего, стабильно трансфектированных человеческим АРР695, с полученными на стадиях (а)-(в) лигандами и выявление продуцирования амилоид-А В альтернативном варианте на стадии (г) полученный на стадиях (а)-(в) лиганд вводят трансгенной мыши, которая экспрессирует человеческий амилоид-А Кроме того, настоящее изобретение относится к лекарственным средствам, которые содержат агонисты меди по изобретению. При необходимости эти лекарственные средства дополнительно содержат фармацевтически приемлемый носитель. Специалистам известны пригодные носители и составы таких лекарственных средств. Пригодные носители включают, например, забуференные фосфатом растворы поваренной соли, воду, эмульсии, например эмульсии типа масло в воде, смачиватели, стерильные растворы и т.д. Вводить лекарственное средство можно перорально или парентерально. Методы парентерального введения включают местное, внутриартериальное, внутримышечное, подкожное, интрамедуллярное, интратекальное, интравентрикулярное, внутривенное, внутрибрюшинное или интраназальное введение. Соответствующая доза назначается лечащим врачом и зависит от различных факторов, например от возраста, пола, веса пациента, стадии болезни, методики и формы введения и т.д. Таким образом, настоящее изобретение относится к применению описанных выше агонистов меди для изготовления лекарственного средства, предназначенного для предупреждения или лечения болезни Альцгеймера. Ниже изобретение более подробно описано со ссылкой на прилагаемые чертежи. На фиг.1 представлено процессирование амилоидного протеина-предшественника (АРР770) с образованием А На чертеже используется однобуквенный код; белые буквы обозначают аминокислотную последовательность А На фиг.2 представлена иммунопреципитация меченного с помощью с-mус АРР695. С помощью поликлональных антител 18/47 к с-mус проводили иммунопреципитацию в лизате (mус-АРР695) и в кондиционированной среде (myc-sAPP695) с клетками дикого типа (фиг.2а, СНО-К1) и с устойчивыми к меди клетками СНО (фиг.2б, CHO-CUR3). Осажденные образцы после переноса на нитроцеллюлозную мембрану подвергали иммуноблоттингу с использованием моноклонального антитела 22С11 к АРР. Контроль: среда (“mock/s”) и лизат (“mock/c”) “mock”-трансфектированных клеток. На фиг.3 представлена иммунопреципитация Ноlо-АРР695 в лизате (фиг.3а), растворимого АРР695 (фиг.3б) и А Проявление sAPP695 в виде дуплета (фиг.3б) при высоких концентрациях меди обусловлено различным содержанием в нем сиалиновой кислоты. Фрагмент (фиг.3г), находящийся несколько выше полосы, соответствующей А Измеренные в этом эксперименте относительные количества сАРР (незаштрихованные треугольники), sAPP (незаштрихованные квадраты) и общего секретированного протеина (черные ромбы) количественно оценивали в виде процента радиоактивности при определенной концентрации меди в основной среде, указанной на фиг.3в; величины А На фиг.4 представлена иммунопреципитация Ноlо-АРР695 в лизате (фиг.4а), растворимого АРР695 (фиг.4б) и А Эндогенный уровень sAPP751/770 в К1-клетках выше, чем в CUR3-клетках (см. фиг.2), и зависит от концентрации меди, поэтому его оценивали количественно. Данные представляют собой средние значения по двум независимым экспериментам. Численные значения измеренных в этом опыте относительных количеств сАРР (незаштрихованные кружки), sAPP695 (незаштрихованные квадраты), sAPP751/770 (незаштрихованные треугольники) и общего секретированного протеина (черные ромбы) приведены на фиг.4в. На фиг.4д представлены данные такого же эксперимента, что и для фиг.4в, при этом А На фиг.5 представлена количественная оценка относительных уровней sAPP695, р3 и А Увеличение уровня sAPP695 (черные ромбы) достигало максимума в К1-клетках при 10 мкМ Cu(II) (фиг.5а), а в CUR3-клетках при 50 мкМ Cu(II) (фиг.5б); после чего его уровень опять снижался. Изменение уровня sAPP (незаштрихованные треугольники) начиналось позднее по сравнению с изменениями уровня протеина р3, максимальный уровень которого достигался при несколько меньших дозах Cu(II), что, по всей вероятности, обусловлено большим временем полужизни по сравнению с sAPP. В противоположность этому уровни А Ниже изобретение проиллюстрировано на примерах. Пример 1: Общие методы Клеточные линии и трансфекция Клетки СНО трансфектировали несущим с-mус-метку вектором АРР695 (Peraus и др., J. Neurosci., Введение метаболической метки и иммунопреципитация Стабильно трансфектированные СНО-клетки, находящиеся в чашке для выращивания культуры (60 мм), обрабатывали в течение 4 ч 2 мл минимальной поддерживающей среды (MEM), которая не содержала метионина (фирма Sigma, Мюнхен) и была дополнена [35S] метионином (220 мкКи) (фирма Amersham, Брауншвейг) и 5% N2. Кондиционированную среду (СМ) и клетки собирали и подвергали иммунопреципитации. Перед этим определяли концентрации протеина анализом протеина по методу фирмы “BioRad” (Bradford и др., Anal. Biochem., 72, с. 248-254 (1976)) или несущие радиоактивную метку протеины осаждали с помощью 10%-ной трихлоруксусной кислоты (ТХК) и измеряли уровни включенного [35S] метионина (прибор типа Beckman LS 6000IC). Клетки лизировали в буфере для экстракции, который содержал 50 мМ Трис-НСl (значение рН 7,5), 150 мМ NaCl, 2 мМ ЭДТК, 2% тритона Х-100, 2% NP40, 10 мкг/мл апротинина и 10 мкг/мл лейпептина. Для отделения клеточного дебриса лизат и среду центрифугировали в течение 10 мин при 13000 Антитела и электрофорез При выявлении АРР поликлональные кроличьи антитела к рекомбинантному Fd-APP770 (антисыворотка 22734/6 к аминокислотным остаткам 18-687 АРР770 или антисыворотка 23850/6 к аминокислотным остаткам 18-491 ААР (фиг.1)) для осаждения разбавляли в соотношении 1:500. Антисыворотки получали в лаборатории известными специалистам стандартными методами. А Обработка действующим веществом и анализ на основе LHD Во время фазы внесения метки к культуральной среде добавляли хлорид меди или хлорид цинка (концентрации: от 5 мкМ до 200 мкМ). D-(-)-пеницилламин (PEN; фирма Sigma), батокупроиндисульфонат (ВС; фирма Aldrich) и 1,10-фенантролин (PEN; фирма Sigma) добавляли в среду до получения конечной концентрации 100 мкМ (PEN и ВС), соответственно 200 мкМ (PEN). Жизнеспособность клеток оценивали по выходу лактатдегидрогеназы (LDH) (41). Выход LDH оценивали на основе измерений ферментативной активности (в ед./л) через 2 и 4 ч в среде, состоящей из 70% конфлюэнтных монослоев СНО-клеток, находящихся в модифицированной по методу Дульбекко среде Игла (среда DMEM). Пример 2: Экспрессия АРР в клетках, которые трансфектированы кДНК, кодирующей АРР695 Для исследования влияния меди на процессирование АРР при уменьшающихся концентрациях меди, соответственно увеличивающихся концентрациях меди (0-200 мкМ), использовали родительскую линию СНО-К1-клеток и устойчивых к меди CUR3-клеток. CUR3-клетки использовали для исследования влияния внутриклеточной меди на процессирование АРР. По сравнению с СНО-К1-клетками в CUR3-клетках присутствует более низкая концентрация внутриклеточной меди, что вызвано усиленным оттоком меди вследствие увеличенной в 70 раз концентрации откачивающего медь “АТФ-азного насоса типа Menkes P” (внутриклеточный насос меди/внутриклеточная система экспорта меди). После трансфекции СНО-К1-клеток и CUR3-клеток с помощью кДНК, кодирующей АРР695, содержащий N-концевой с-mус-эпитоп (фиг.1), оказывалось возможным легко выявить экспрессию АРР с помощью иммунопреципитации с использованием поликлональной антисыворотки к c-myc и последующего иммуноблоттинга с использованием моноклонального антитела 22С11 (фиг.2а, б). Поликлональное антитело к c-mус вызывало иммунопреципитацию меченного с помощью с-mус АРР695 с относительной молекулярной массой 105 кДа в клеточном лизате (сАРР695) и кондиционированной среде (sAPP695). Как и ожидалось, c-myc APP695 не был обнаружен ни в лизате, ни в среде клеток, которые были трансфектированы только pcDNA3. Пример 3: Уменьшение концентрации А Для исследования регуляции метаболизма АРР с помощью ионов меди СНО-клетки, стабильно трансфектированные с помощью APP695, маркировали в течение 4 ч меченным с помощью 35S метионином в присутствии различных концентраций меди и после иммунопреципитации с помощью поликлональных антител (730), которые распознают АРР (22734/6), соответственно А При инкубации CUR3-клеток с возрастающими концентрациями меди концентрация голопротеина АРР и растворимого АРР существенно возрастала. По сравнению с основной средой максимум sAPP, составлявший 265%, достигался при 50 мкМ Cu (II), после чего индуцировалось общее продуцирование секретируемых протеинов (фиг.3в; таблица 1). Секретирование р3, С-концевого фрагмента секреторного АРР, образующегося в результате расщепления с помощью Пример 4: Стимуляция продуцирования А Для проверки, можно ли осуществлять созданием дефицита меди модуляцию сАРР, sAPP и дальнейших продуктов разложения, проводили следующие эксперименты. Для исследования, необходима ли медь (II) для экспрессии и процессинга АРР, медь (II) удаляли с помощью образующего хелатный комплекс с медью (II) D-пеницилламина (PEN), а медь (I) – с помощью батокупроиндисульфоновой кислоты, образующей хелатный комплекс с медью (I), который не может проникать внутрь клетки. Было установлено, что это не влияет на продуцирование А Пример 5: Исследование АРР751/770-изоформ, содержащих эндогенно экспрессируемый KPI, в CHO-Kl-клетках Изоформы АРР751/770, содержащие эндогенно экспрессируемый KPI (ингибирующий протеазу домен типа Кунитца, который встраивают путем альтернативного сплайсинга в АРР751 и АРР770), исследовали в CHO-Kl-клетках путем иммунопреципитации протеинов, меченных с помощью [35S]метионина, в клеточном лизате и кондиционированных средах с использованием поликлональной антисыворотки 22734 к АРР (фиг.1; фиг.4а,б). Высвобождение КР1-АРР соответствовало высвобождению c-myc-APP695 (фиг.4). Две основные полосы, которые относятся к относительным молекулярным массам 130 кДа и 105 кДа, соответствуют sAPP751/770, соответственно sAPP695. Последняя изоформа может быть также осаждена с помощью антисыворотки к с-mус. При инкубации CHO-Kl-клеток с возрастающими концентрациями меди существенно возрастают уровни АРР и р3 (АРР: сАРР на 295%, sAPP695 на 475% и sAPP751/770 на 275% при концентрации меди 10 мкМ, а р3 на 154% при концентрации меди 10 мкМ; фиг.4а-д; таблица 1). Одновременно резко уменьшается продуцирование А Кроме того, проводили количественную оценку относительных уровней sAPP695, р3 и А Пример 6: Выявление агонистов меди для АРР, обладающих ингибирующим действием на высвобождение амилоид-А Связывающий медь пептид АРР и APLP2 (протеин, гомологичный АРР, который, также как АРР и APLP1, принадлежит к семейству АРР-генов), APPN262 (искусственно созданная укороченная на С-конце форма АРР, которая состоит из 262 N-концевых остатков АРР) и другие искусственно созданные АРР-формы, которые последовательно укорачивают на несколько доменов на С-конце варианты АРР и APLP2, несущие сайты связывания меди, а также их фрагменты вводили в контакт с различными концентрациями Zn(II). Используемые концентрации Zn2+ составляли 10 мкМ, 50 мкМ, 100 мкМ и 200 мкМ. Затем исследовали, при каких концентрациях Zn (II) может происходить ингибирование высвобождения А (1) СНО-клетки, стабильно трансфектированные человеческим АРР695, инкубировали в среде MEM с указанными выше концентрациями Zn (II) (от 10 до 200 мкМ в ЗФР). В качестве контролей также инкубировали СНО-клетки в присутствии ионов меди (от 10 до 50 мкМ в ЗФР) или без них. Продуцирование А Было обнаружено, что при концентрации Zn (II) от 50 мкМ и выше продуцирование А (2) Из трансгенных мышей, клетки которых экспрессируют А (3) Трансгенным мышам (см. (2)) вводили перорально, внутривенно, внутрибрюшинно, подкожно и внутрикожно Zn (II) в ЗФР в указанных выше концентрациях и определяли согласно методу, описанному выше в (1), продуцирование А Формула изобретения
1. Применение агониста меди, который связывается с сайтом связывания меди амилоидного протеина-предшественника (АРР) и/или уменьшает либо ингибирует высвобождение амилоид-А 2. Применение по п.1, где агонист меди выбирают из группы, включающей двухвалентные ионы металлов, олигопептиды, олигонуклеотиды, олигосахариды, нуклеотидные аналоги, библиотеки химических субстанций или низкомолекулярные природные субстанции, выделенные из микроорганизмов, соответственно из растений. 3. Способ выявления агониста меди, который связывается с сайтом связывания меди АРР и/или оказывает ингибирующее действие на высвобождение амилоид-А 4. Способ по п.3, где уменьшение уровня А 5. Способ выявления агониста меди, который связывается с сайтом связывания меди АРР и/или оказывает ингибирующее действие на высвобождение амилоид-А 6. Способ по п.5, где стадия (г) включает инкубацию клеток млекопитающих, стабильно трансфектированных человеческим АРР695, в присутствии полученных на стадиях (а)-(в) лигандов и выявление продуцирования амилоид-А 7. Способ по п.5, где стадия (г) включает введение полученных на стадиях (а)-(в) лигандов трансгенным млекопитающим, которые экспрессируют человеческий амилоид-А 8. Применение по п.2, где агонист меди идентифицируют с помощью способов согласно п.3 или 5. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 02.03.2005
Извещение опубликовано: 10.03.2006 БИ: 07/2006
NF4A Восстановление действия патента СССР или патента Российской Федерации на изобретение
Дата, с которой действие патента восстановлено: 20.05.2007
Извещение опубликовано: 20.05.2007 БИ: 14/2007
|
||||||||||||||||||||||||||

 -ПЕПТИДА
-ПЕПТИДА -секретазой большого интегрального связанного с мембраной амилоидного протеина-предшественника (АРР), основные изоформы которого содержат аминокислоты: 695 (АРР695), 751 (АРР751) или 770 (АРР770) (J. Hardy, Trends Neurosci.,
-секретазой большого интегрального связанного с мембраной амилоидного протеина-предшественника (АРР), основные изоформы которого содержат аминокислоты: 695 (АРР695), 751 (АРР751) или 770 (АРР770) (J. Hardy, Trends Neurosci., 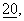 с. 154-159 (1997)). АРР-процессирование в А
с. 154-159 (1997)). АРР-процессирование в А -секретазы препятствует образованию амилоида и приводит к высвобождению пептида р3, который содержит остатки 17-40/42
-секретазы препятствует образованию амилоида и приводит к высвобождению пептида р3, который содержит остатки 17-40/42 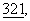 с. 265-279 (1997)). Однако ингибирование этих протеаз приводит к нежелательным побочным действиям, поскольку эти протеазы участвуют в процессировании различных трансмембранных протеинов. До настоящего времени основные усилия по лечению болезни Альцгеймера и других форм деменции концентрировались в основном на улучшении процессов обмена веществ в головном мозге и на замещении определенных дефицитных нейромедиаторов или на ингибировании воспалительных процессов, сопровождающих болезнь. Однако эти лекарственные средства не учитывают различий между различными формами деменции, а нацелены на наблюдающиеся при всех формах деменции вторичные сопутствующие проявления.
с. 265-279 (1997)). Однако ингибирование этих протеаз приводит к нежелательным побочным действиям, поскольку эти протеазы участвуют в процессировании различных трансмембранных протеинов. До настоящего времени основные усилия по лечению болезни Альцгеймера и других форм деменции концентрировались в основном на улучшении процессов обмена веществ в головном мозге и на замещении определенных дефицитных нейромедиаторов или на ингибировании воспалительных процессов, сопровождающих болезнь. Однако эти лекарственные средства не учитывают различий между различными формами деменции, а нацелены на наблюдающиеся при всех формах деменции вторичные сопутствующие проявления. – и
– и 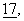 с. 7714-7724 (1997)) или экспрессионным вектором (pcDNA3) с помощью высокоэффективного метода трансфекции с использованием фосфата кальция (Chen и др., Biotechniques,
с. 7714-7724 (1997)) или экспрессионным вектором (pcDNA3) с помощью высокоэффективного метода трансфекции с использованием фосфата кальция (Chen и др., Biotechniques, 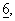 с. 632-638 (1988)). ДНК APP695-N-tag плазмиды pSP65 (фирма Invitrogen) клонировали в векторе pcDNA3 (фирма Invitrogen/ITC Biotechnology, Гейдельберг) с использованием сайтов клонирования Smal, соответственно EcoRV. Эффективность трансфекции проверяли с помощью иммунопреципитации АРР с использованием поликлонального кроличьего антитела к с-mус (18/47; созданного к аминокислотной последовательности EQKLISEEDL, т.е. последовательности с-mус; фирма Eurogentec, Серен, Бельгия) и иммуноблоттинга с использованием моноклонального мышиного антитела 22С11 (фирма Boehringer Mannheim) с помощью системы анализа “ECL” (фирма Amersham, Брауншвейг). Родительские СНО-К1-клетки, а также устойчивый к меди вариант клеток CUR3 выращивали при 37
с. 632-638 (1988)). ДНК APP695-N-tag плазмиды pSP65 (фирма Invitrogen) клонировали в векторе pcDNA3 (фирма Invitrogen/ITC Biotechnology, Гейдельберг) с использованием сайтов клонирования Smal, соответственно EcoRV. Эффективность трансфекции проверяли с помощью иммунопреципитации АРР с использованием поликлонального кроличьего антитела к с-mус (18/47; созданного к аминокислотной последовательности EQKLISEEDL, т.е. последовательности с-mус; фирма Eurogentec, Серен, Бельгия) и иммуноблоттинга с использованием моноклонального мышиного антитела 22С11 (фирма Boehringer Mannheim) с помощью системы анализа “ECL” (фирма Amersham, Брауншвейг). Родительские СНО-К1-клетки, а также устойчивый к меди вариант клеток CUR3 выращивали при 37 С в среде Игла (ВМЕ), дополненной 2 мМ L-глутамином, 0,1 мМ пролином, 20 мМ HEPES и 10% фетальной телячьей сыворотки (фирма Boehringer Mannheim). Основная концентрация меди составляла 0,8 мкМ. CUR3-клетки выращивали в среде, содержащей 200 мкМ меди.
С в среде Игла (ВМЕ), дополненной 2 мМ L-глутамином, 0,1 мМ пролином, 20 мМ HEPES и 10% фетальной телячьей сыворотки (фирма Boehringer Mannheim). Основная концентрация меди составляла 0,8 мкМ. CUR3-клетки выращивали в среде, содержащей 200 мкМ меди. g и состав среды регулировали таким образом, чтобы она содержала 25 мМ Трис-НСl (значение рН 8,5), 1 мМ фенилметилсульфонилфторид (ФМСФ), 10 мкг/мл апротинина, 10 мкг/мл лейпептина, 0,5% тритона Х-100 и 0,5% NP40. Солюбилизированные протеины разбавляли в 100 мМ Трис-НСl (значение рН 7,5), 300 мМ NaCl и 4 мМ ЭДТК в соотношении 1:2. Супернатант инкубировали в течение ночи при 4
g и состав среды регулировали таким образом, чтобы она содержала 25 мМ Трис-НСl (значение рН 8,5), 1 мМ фенилметилсульфонилфторид (ФМСФ), 10 мкг/мл апротинина, 10 мкг/мл лейпептина, 0,5% тритона Х-100 и 0,5% NP40. Солюбилизированные протеины разбавляли в 100 мМ Трис-НСl (значение рН 7,5), 300 мМ NaCl и 4 мМ ЭДТК в соотношении 1:2. Супернатант инкубировали в течение ночи при 4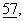 с. 115-126 (1989).
с. 115-126 (1989).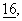 с. 899-908 (1996), и количественно оценивали с помощью системы “Fuji-Bas-Phosphorlmager”. Данные выражали в виде среднего значения
с. 899-908 (1996), и количественно оценивали с помощью системы “Fuji-Bas-Phosphorlmager”. Данные выражали в виде среднего значения стандартное отклонение и, если не указано иное, они представляли собой результаты по крайней мере по двум независимым опытам.
стандартное отклонение и, если не указано иное, они представляли собой результаты по крайней мере по двум независимым опытам.