Патент на изобретение №2234921
|
||||||||||||||||||||||||||
(54) СПОСОБ ЛЕЧЕНИЯ ГРИБОВИДНОГО МИКОЗА
(57) Реферат: Изобретение относится к медицине, а именно к дерматологии, и касается способа лечения грибовидного микоза. Для этого вводят индуктор эндогенного интерферона ридостин в виде внутримышечных инъекций препарата по 8 мг 2 раза в неделю, курсом в 6 инъекций. Одновременно с ридостином назначают преднизолон в дозе 0,5 мг/кг/сут. в течение 21 дня, затем снижают дозировку на 2,5 мг в 3 сут. Лечение приводит к достижению высокой клинической эффективности у больных со II и III стадией процесса при снижении риска осложнений. 3 табл. Изобретение относится к медицине, а именно к дерматологии, и может быть использовано для лечения злокачественной лимфомы кожи. 1. Установлено, что интерфероны (  , ,  и и  Обобщая результаты более 20 сообщений о клиническом применении препаратов ИФН в терапии Т-ЗЛК, G. Burg в своей монографии “Strategies for Immunointerventions in Dermatology” (Springer-Verlag Berlin Heidelberg. – 1997. – P.164, P.322, 324) делает заключение об эффективности этой группы иммуномодулирующих средств, в особенности ИФН-альфа, в виде монотерапии в среднем у 60% пациентов, причем у 50% больных с частичной ремиссией процесса, и только у 10% – с полной клинической ремиссией. Опыт применения препаратов ИФН в терапии больных с ГМ представлен также в немногочисленных работах отечественных исследователей и свидетельствует об умеренной клинической эффективности применяемых схем интерферонотерапии при лечении больных с ГМ на различных стадиях развития процесса (таблица 1).
Прототипом изобретения является способ лечения Т-ЗЛК (ГМ), заключающийся в проведении иммунотерапии интерфероном – альфа2 в дозе 3-5 млн ME 3 раза в неделю в течение 2-3 месяцев. Данным способом было пролечено 14 больных Т-ЗЛК: 4 с 2 стадией и 10 с 3 стадией развития патологического процесса. Терапия оказалась эффективной у 9 из 14 больных (64,3%), из числа которых полной клинической ремиссии не было достигнуто ни у одного больного, у 7 пациентов зафиксирована частичная ремиссия, у 2 больных – минимальное улучшение. У 5 из 14 больных монотерапия интерфероном приводила к прогрессированию заболевания (Ламоткин И.А. Поражения кожи при злокачественных лимфопролиферативных заболеваниях: Дис. докт. мед. наук. – Санкт-Петербург. – 2001, – 227 с.). В то же время в процессе терапии интерферонами больных с Т-ЗЛК были отмечены плохая переносимость лечения, формирование сопутствующих нежелательных явлений, таких как выраженный озноб, гипертермия, анорексия, тошнота, снижение веса, депрессия и др. (Фараджев З.Г. Лимфопролиферативные заболевания кожи и саркома Капоши (патогенез и методы терапии): Дис…докт. мед. наук, М., 1990. – 278 с.; Ламоткин И.А. Поражения кожи при злокачественных лимфопролиферативных заболеваниях: Дис…докт. мед. наук. – Санкт- Петербург, – 2001, – 227 с.).
Альтернативой введению экзогенного интерферона служат методы повышения синтеза собственных интерферонов активированными лимфоцитами. Известен препарат ридостин, обладающий полифункциональным иммуномодулирующим действием и относящийся к группе индукторов интерферона (ИФН).
Ридостин – новый отечественный индуктор интерферона “раннего типа”, основным действующим началом которого является двуспиральная рибонуклеиновая кислота (дс РНК) киллерных штаммов дрожжей Saccharomyces cerevisiae. Ридостин представляет собой смесь натриевых солей двуспиральной и одноцепочечной рибонуклеиновой кислоты (5 мг), натрий хлорида (3 мг) в виде лиофилизированной пористой массы белого цвета. Основной характеристикой препарата является интерферониндуцирующая активность (альфа-, бета- и гамма- интерфероны), доказанная в ходе клинических испытаний на добровольцах и в клинической практике, когда введение ридостина приводило к повышению титров
Обобщая результаты более 20 сообщений о клиническом применении препаратов ИФН в терапии Т-ЗЛК, G. Burg в своей монографии “Strategies for Immunointerventions in Dermatology” (Springer-Verlag Berlin Heidelberg. – 1997. – P.164, P.322, 324) делает заключение об эффективности этой группы иммуномодулирующих средств, в особенности ИФН-альфа, в виде монотерапии в среднем у 60% пациентов, причем у 50% больных с частичной ремиссией процесса, и только у 10% – с полной клинической ремиссией. Опыт применения препаратов ИФН в терапии больных с ГМ представлен также в немногочисленных работах отечественных исследователей и свидетельствует об умеренной клинической эффективности применяемых схем интерферонотерапии при лечении больных с ГМ на различных стадиях развития процесса (таблица 1).
Прототипом изобретения является способ лечения Т-ЗЛК (ГМ), заключающийся в проведении иммунотерапии интерфероном – альфа2 в дозе 3-5 млн ME 3 раза в неделю в течение 2-3 месяцев. Данным способом было пролечено 14 больных Т-ЗЛК: 4 с 2 стадией и 10 с 3 стадией развития патологического процесса. Терапия оказалась эффективной у 9 из 14 больных (64,3%), из числа которых полной клинической ремиссии не было достигнуто ни у одного больного, у 7 пациентов зафиксирована частичная ремиссия, у 2 больных – минимальное улучшение. У 5 из 14 больных монотерапия интерфероном приводила к прогрессированию заболевания (Ламоткин И.А. Поражения кожи при злокачественных лимфопролиферативных заболеваниях: Дис. докт. мед. наук. – Санкт-Петербург. – 2001, – 227 с.). В то же время в процессе терапии интерферонами больных с Т-ЗЛК были отмечены плохая переносимость лечения, формирование сопутствующих нежелательных явлений, таких как выраженный озноб, гипертермия, анорексия, тошнота, снижение веса, депрессия и др. (Фараджев З.Г. Лимфопролиферативные заболевания кожи и саркома Капоши (патогенез и методы терапии): Дис…докт. мед. наук, М., 1990. – 278 с.; Ламоткин И.А. Поражения кожи при злокачественных лимфопролиферативных заболеваниях: Дис…докт. мед. наук. – Санкт- Петербург, – 2001, – 227 с.).
Альтернативой введению экзогенного интерферона служат методы повышения синтеза собственных интерферонов активированными лимфоцитами. Известен препарат ридостин, обладающий полифункциональным иммуномодулирующим действием и относящийся к группе индукторов интерферона (ИФН).
Ридостин – новый отечественный индуктор интерферона “раннего типа”, основным действующим началом которого является двуспиральная рибонуклеиновая кислота (дс РНК) киллерных штаммов дрожжей Saccharomyces cerevisiae. Ридостин представляет собой смесь натриевых солей двуспиральной и одноцепочечной рибонуклеиновой кислоты (5 мг), натрий хлорида (3 мг) в виде лиофилизированной пористой массы белого цвета. Основной характеристикой препарата является интерферониндуцирующая активность (альфа-, бета- и гамма- интерфероны), доказанная в ходе клинических испытаний на добровольцах и в клинической практике, когда введение ридостина приводило к повышению титров  Установленные иммуномодулирующие свойства ридостина, в том числе с повышением противоопухолевых потенций организма, зафиксированы в Регистре лекарственных средств Российской Федерации (Редакция 1999-2002 гг.) и обосновывают возможность его применения в качестве адъювантного препарата в комплексной терапии заболеваний, в том числе пролиферативных, сопровождающихся нарушениями иммунного статуса.
Цель изобретения – повышение эффективности лечения Т-ЗЛК при снижении риска клинических осложнений от проводимой терапии.
Поставленная цель реализуется назначением больным Т-ЗЛК (ГМ) индуктора эндогенного интерферона ридостина и кортикостероидного гормона преднизолона в терапевтической дозе с постепенным ее снижением. Способ лечения применяется в условиях специализированного дерматологического отделения при полном госпитальном режиме (или в условиях стационара дневного пребывания).
Больным ЗЛК проводилась терапия ГКС гормонами в стартовой дозе 0,5 мг/кг/сут, в первые 2 недели инфузионно, затем перорально в дозе 0,5 мг/кг/сут, с последующим снижением дозы на 2,5 мг в 3 сут. На фоне ГКС-терапии осуществляли введение ридостина.
В соответствии с общими рекомендациями по применению ридостина препарат вводили в/м по 8 мг активного вещества, растворенного “ех tempore” в 2,0 мл воды для инъекций. Ридостин назначали с 1 недели общей терапии больных, вводили 2 раза в неделю с интервалом 2-3 дня, всего на курс по 4-6 инъекций препарата.
Длительность основного курса лечения составляла до 30 дней, после чего продолжалась пероральная терапия ГКС со снижением дозы.
Положительная клиническая динамика, как правило, начиналась в первые недели терапии и выражалась в уменьшении гиперемии и инфильтрации в очагах, снижении интенсивности зуда и жжения кожи. Во время введения ридостина и после завершения курса продолжался регресс симптоматики, и к 4-6 неделе лечения состояние эритродермии практически разрешалось, инфильтративно-бляшечные высыпания уплощались, пятнистые проявления исчезали, чаще оставляя при регрессе гиперпигментированные участки кожи.
Предложенный способ был применен в лечении 13 больных Т-ЗЛК, 9 из которых находились в состоянии эритродермии (по классификации TNM – III стадия развития процесса), 4 пациента с ГМ2 (IIA стадия) с явлениями частичной эритродермии в возрасте от 39 до 70 лет, в том числе 3 женщин и 10 мужчин. Давность заболевания составляла от 2,5 до 6 лет.
Диагнозы были гистологически верифицированы в клинике УрНИИД-ВиИ. Ранее больные лечились в основном с использованием системных и топических кортикостероидов, что позволяло достигать крайне непродолжительной клинической ремиссии (3-5 месяцев). Анамнестически и клинически пациенты данной группы отличались частыми обострениями процесса (от 3 до 6 эпизодов), быстрым развитием эритродермии, сопровождаемой возникновением пиогенных осложнений на коже, наличием сопутствующей патологии систем и органов воспалительного характера.
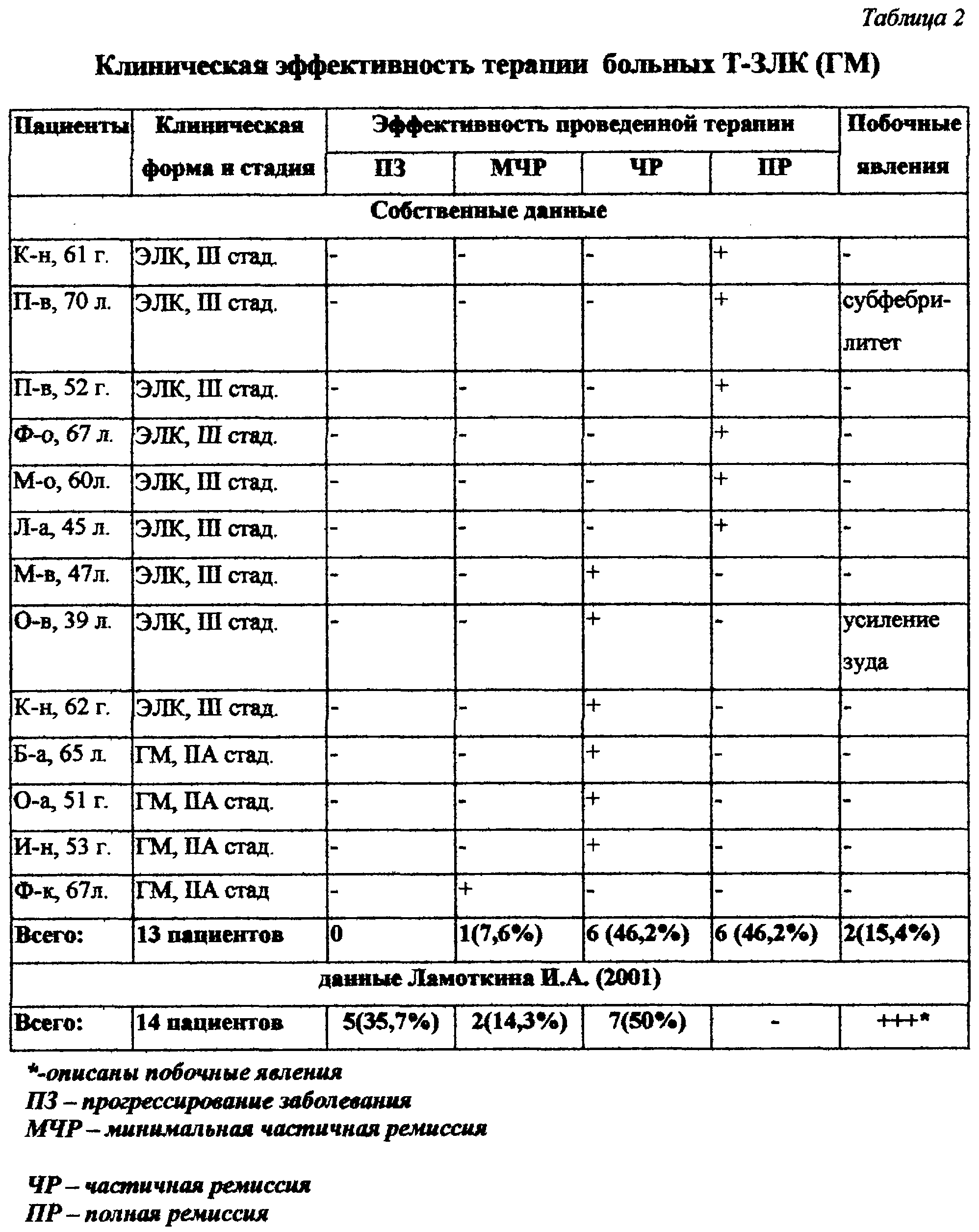
В таблице 2 приведены собственные данные клинической эффективности модифицированного способа лечения Т-ЗЛК ридостином в сравнении с данными Ламоткина И.А. (2001), применявшего интерферон – альфа 2.
Из данных таблицы 2 видно, что описываемый метод лечения не приводил к прогрессированию процесса ни у одного больного, в отличие от прототипа, где у 35,7% больных после интерферонотерапии процесс прогрессировал. У всех пациентов после окончания терапии с ридостином достигалось клиническое улучшение: у 1 больного минимальное, в равных пропорциях (по 6 больных – 46,2%) частичная и полная ремиссия. Метод сравнения был значительно менее эффективен: у 14,3% больных – минимальное улучшение, а у 50% – лишь частичная ремиссия заболевания. Кроме того, при лечении ридостином побочные явления были зафиксированы только у 2 больных (15,4%), они легко купировались, не требовали отмены препарата.
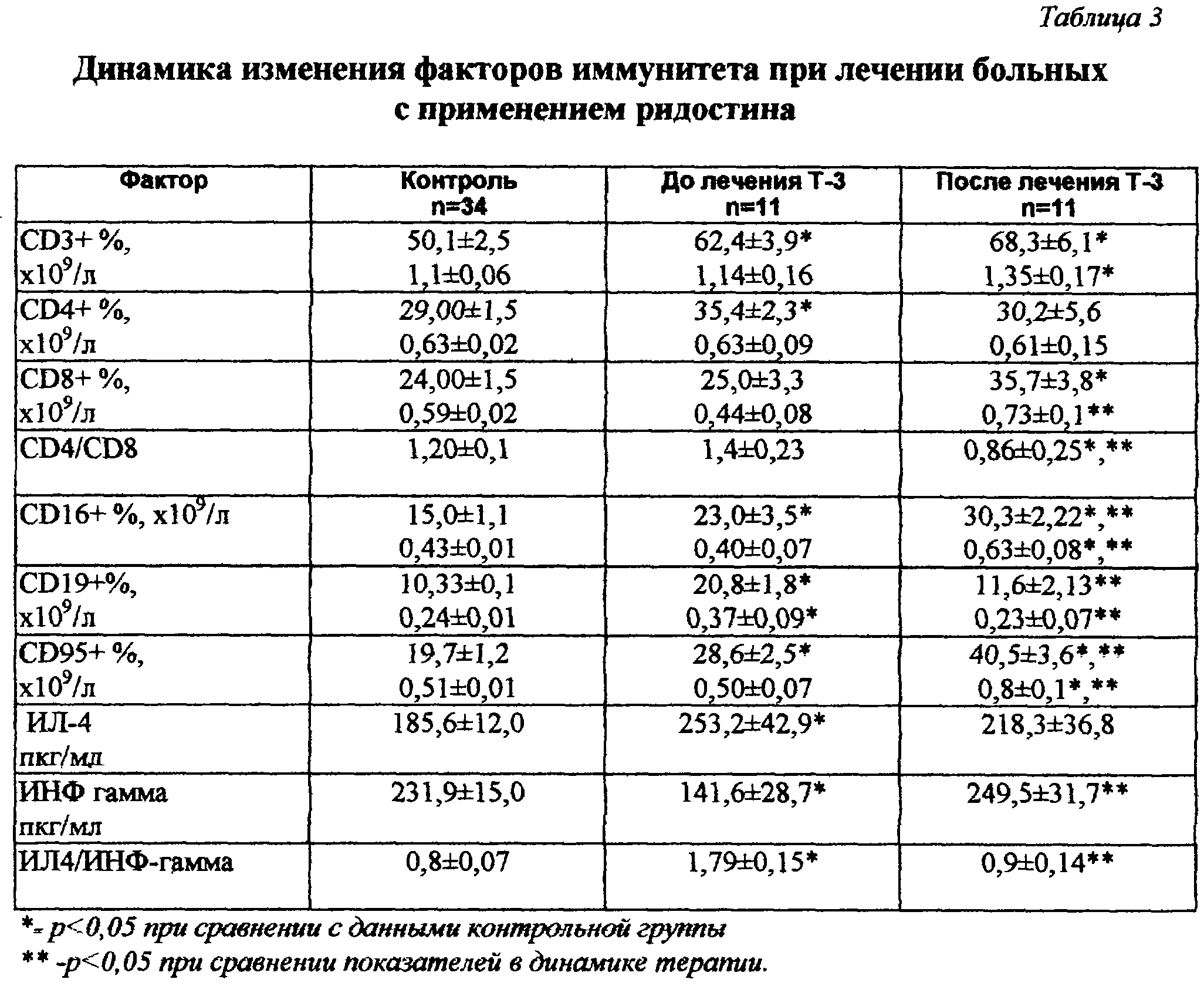
Клиническая эффективность терапии с применением ридостина сопровождалась значимыми изменениями в иммунном статусе пациентов с Т-ЗЛК (ГМ) после окончания лечения (таблица 3). Лечение ридостином определяло достоверное увеличение сниженного до начала терапии содержания интерферона – гамма в сыворотке крови и даже тенденцию к превышению нормативного показателя, что свидетельствовало о патогенетическом воздействии препарата. Достижение клинического эффекта после окончания терапии ридостином сопровождалось также однонаправленным увеличением популяций CD8+, CD16+ лимфоцитов и клеток, экспрессирующих апоптоз-ассоциированный рецептор, что свидетельствовало о достоверной активации факторов противоопухолевого иммунитета, определяющих возможность регресса лимфоидной неоплазии.
Использование предлагаемого способа терапии поясняется следующими примерами.
Пример 1. Больной П-в., 52 года. Поступил с жалобами на наличие высыпаний на коже туловища и конечностей, интенсивный постоянный кожный зуд. Болен данным заболеванием в течение 2 лет, отмечает непрерывно-рецидивирующее течение заболевания, несмотря на проводимую терапию (десенсибилизирующую, дезинтоксикационную, системную (преднизолон до 20 мг/сут, топические ГКС). Гистологическое исследование и иммунофенотипирование образца кожи в УрНИИДВиИ МЗ РФ позволили установить диагноз: Злокачественная Т-клеточная лимфома кожи. Грибовидный микоз, эритродермическая форма (III стадия).
При осмотре больного: кожные покровы в состоянии эритродермии, кожа красновато-синюшного оттенка, выраженная инфильтрация, мелкочешуйчатое шелушение, экскориации на коже туловища и верхних конечностей, гиперкератоз ладоней и подошв. Соматически: ИБС, атеросклеротический кардиосклероз, НК 0-I; хронический бронхит. Печень не увеличена в размерах, селезенка не пальпируется.
При клинико-лабораторном исследовании в стационаре УрНИИДВиИ были обнаружены отклонения от нормы в основных иммунологических показателях: дисиммуноглобулинемия, гипер-Е-иммуноглобулинемия, нарушение соотношения популяций Т-хелперы/Т-супрессоры, повышение уровня CD19 (В-клетки), сниженное в 1,7 раза содержание ИФН-гамма в сыворотке крови. В периферической крови – лейкоцитоз, лимфоцитопения, эозинофилия.
Было назначено лечение ридостином по традиционной схеме в форме в/м инъекций по 8 мг активного вещества, растворенного “ex tempore” в 2,0 мл воды для инъекций. Ридостин назначали с 1 недели общей терапии больных, вводили 2 раза в неделю с интервалом 2-3 дня, всего проведено 6 инъекций препарата. Одновременно назначался преднизолон per os 30 мг/сут в течение 21 дня, с последующим снижением на 2,5 мг в 3 сут, антигистаминные препараты, наружная мазевая терапия. Лечение проводилось под контролем гемограммы 1 раз в 5 дней.
В результате проводимой терапии после 2 инъекции препарата ридостин (1 неделя лечения) отмечалось значительное уменьшение интенсивности кожного зуда и жжения; после 4 инъекции (2 неделя лечения) – было зафиксировано снижение гиперемии и шелушения кожи, в этот же период значимо уменьшились инфильтрация кожи, ее шелушение. Разрешение эритродермических проявлений наступило на 4 неделе лечения. Побочных реакций и осложнений терапии не отмечалось.
В повторной иммунограмме после проведения курса терапии наблюдалось существенное снижение уровня IgE, приближение к нормальным величинам уровня IgG и соотношения популяций Т-хелперы/Т-супрессоры. В периферической крови – нормализация содержания ИФН-гамма, лимфоцитов и эозинофилов. Больной выписан в состоянии полной клинической ремиссии, продолжительность курса терапии составила 38 дней.
Пример 2. Больная Б-а, 65 лет, находилась под наблюдением в клинике УрНИИДВиИ с 1999 г., после неоднократных гистологических исследований в 2001 г. верифицирован диагноз: Т-клеточная злокачественная лимфома кожи. Грибовидный микоз, НА стадия. Больная неоднократно проходила стационарное лечение в клинике с использованием десенсибилизирующих, дезинтоксикационных препаратов, системной терапии (преднизолон 30 мг/сут до 14-20 дней) и наружной кортикостероидной терапии, выписывалась с улучшением на поддерживающей терапии глюкокортикосгероидами. Кожный процесс приобрел резистентность к проводимой терапии, частые обострения сочетались с непродолжительными периодами ремиссии (2-3 месяца).
При клинико-лабораторном исследовании в УрНИИДВиИ в иммунограмме была обнаружена дисиммуноглобулинемия, умеренное повышение IgE, высокое содержание IL-4. В периферической крови – умеренный лейкоцитоз, эозинофилия.
Было назначено лечение ридостином по традиционной схеме в форме в/м инъекций по 8 мг активного вещества, растворенного “ex tempore” в 2,0 мл воды для инъекций. Ридостин назначали с 1 недели общей терапии больной, вводили 2 раза в неделю с интервалом 2-3 дня, всего проведено 6 инъекций препарата. Одновременно назначались преднизолон per os 35 мг/сут в течение 21 дня, с последующим снижением на 5 мг в 5 дней, антигистаминные препараты, наружная мазевая терапия. Лечение проводилось под контролем гемограммы 1 раз в 5 дней.
В результате проводимой терапии после 4 инъекции препарата ридостин (2 неделя лечения) отмечались уменьшение активной гиперемии и инфильтрации в области бляшек, уменьшение зуда в местах высыпаний. После 6 инъекций препарата пятнистые высыпания практически регрессировали, а бляшки значительно уменьшились по высоте, полностью исчез зуд. В течение 3 недель после окончания введения ридостина доза преднизолона медленно снижалась до полной отмены. При выписке (общий срок пребывания в стационаре 43 дня) процесс регрессировал на 50%, что характеризует исход терапии как частичную ремиссию процесса. Побочных реакций и осложнений во время терапии не отмечалось.
Динамическое изучение иммунологического статуса выявило тенденцию к снижению IgE в периферической крови, снижение лейкоцитоза, эозинофилии.
Предложенным способом в УрНИИДВиИ пролечено 13 больных Т-ЗЛК в возрасте от 39 до 70 лет, в том числе 3 женщины и 10 мужчин. Давность заболевания составляла от 2 до 17 лет, диагнозы были гистологически верифицированы впервые в клинике УрНИИДВиИ. Ранее больные лечились с использованием системных и топических кортикостероидов, что не позволяло добиться полной клинической ремиссии. После проведенного курса терапии ридостином и преднизолоном состояние значительного клинического улучшения достигнуто у 12 из 13 больных (92,4%), у одного больного (7,6%) – минимальное улучшение процесса. Длительность ремиссии составила от 12 до 19 месяцев.
Таким образом, апробирован новый способ лечения Т-ЗЛК (грибовидного микоза), включающий назначение индуктора интерферона в сочетании со средне терапевтическими дозами преднизолона, что позволило существенно повысить эффективность терапии при снижении риска возникновения осложнений.
Установленные иммуномодулирующие свойства ридостина, в том числе с повышением противоопухолевых потенций организма, зафиксированы в Регистре лекарственных средств Российской Федерации (Редакция 1999-2002 гг.) и обосновывают возможность его применения в качестве адъювантного препарата в комплексной терапии заболеваний, в том числе пролиферативных, сопровождающихся нарушениями иммунного статуса.
Цель изобретения – повышение эффективности лечения Т-ЗЛК при снижении риска клинических осложнений от проводимой терапии.
Поставленная цель реализуется назначением больным Т-ЗЛК (ГМ) индуктора эндогенного интерферона ридостина и кортикостероидного гормона преднизолона в терапевтической дозе с постепенным ее снижением. Способ лечения применяется в условиях специализированного дерматологического отделения при полном госпитальном режиме (или в условиях стационара дневного пребывания).
Больным ЗЛК проводилась терапия ГКС гормонами в стартовой дозе 0,5 мг/кг/сут, в первые 2 недели инфузионно, затем перорально в дозе 0,5 мг/кг/сут, с последующим снижением дозы на 2,5 мг в 3 сут. На фоне ГКС-терапии осуществляли введение ридостина.
В соответствии с общими рекомендациями по применению ридостина препарат вводили в/м по 8 мг активного вещества, растворенного “ех tempore” в 2,0 мл воды для инъекций. Ридостин назначали с 1 недели общей терапии больных, вводили 2 раза в неделю с интервалом 2-3 дня, всего на курс по 4-6 инъекций препарата.
Длительность основного курса лечения составляла до 30 дней, после чего продолжалась пероральная терапия ГКС со снижением дозы.
Положительная клиническая динамика, как правило, начиналась в первые недели терапии и выражалась в уменьшении гиперемии и инфильтрации в очагах, снижении интенсивности зуда и жжения кожи. Во время введения ридостина и после завершения курса продолжался регресс симптоматики, и к 4-6 неделе лечения состояние эритродермии практически разрешалось, инфильтративно-бляшечные высыпания уплощались, пятнистые проявления исчезали, чаще оставляя при регрессе гиперпигментированные участки кожи.
Предложенный способ был применен в лечении 13 больных Т-ЗЛК, 9 из которых находились в состоянии эритродермии (по классификации TNM – III стадия развития процесса), 4 пациента с ГМ2 (IIA стадия) с явлениями частичной эритродермии в возрасте от 39 до 70 лет, в том числе 3 женщин и 10 мужчин. Давность заболевания составляла от 2,5 до 6 лет.
Диагнозы были гистологически верифицированы в клинике УрНИИД-ВиИ. Ранее больные лечились в основном с использованием системных и топических кортикостероидов, что позволяло достигать крайне непродолжительной клинической ремиссии (3-5 месяцев). Анамнестически и клинически пациенты данной группы отличались частыми обострениями процесса (от 3 до 6 эпизодов), быстрым развитием эритродермии, сопровождаемой возникновением пиогенных осложнений на коже, наличием сопутствующей патологии систем и органов воспалительного характера.
В таблице 2 приведены собственные данные клинической эффективности модифицированного способа лечения Т-ЗЛК ридостином в сравнении с данными Ламоткина И.А. (2001), применявшего интерферон – альфа 2.
Из данных таблицы 2 видно, что описываемый метод лечения не приводил к прогрессированию процесса ни у одного больного, в отличие от прототипа, где у 35,7% больных после интерферонотерапии процесс прогрессировал. У всех пациентов после окончания терапии с ридостином достигалось клиническое улучшение: у 1 больного минимальное, в равных пропорциях (по 6 больных – 46,2%) частичная и полная ремиссия. Метод сравнения был значительно менее эффективен: у 14,3% больных – минимальное улучшение, а у 50% – лишь частичная ремиссия заболевания. Кроме того, при лечении ридостином побочные явления были зафиксированы только у 2 больных (15,4%), они легко купировались, не требовали отмены препарата.
Клиническая эффективность терапии с применением ридостина сопровождалась значимыми изменениями в иммунном статусе пациентов с Т-ЗЛК (ГМ) после окончания лечения (таблица 3). Лечение ридостином определяло достоверное увеличение сниженного до начала терапии содержания интерферона – гамма в сыворотке крови и даже тенденцию к превышению нормативного показателя, что свидетельствовало о патогенетическом воздействии препарата. Достижение клинического эффекта после окончания терапии ридостином сопровождалось также однонаправленным увеличением популяций CD8+, CD16+ лимфоцитов и клеток, экспрессирующих апоптоз-ассоциированный рецептор, что свидетельствовало о достоверной активации факторов противоопухолевого иммунитета, определяющих возможность регресса лимфоидной неоплазии.
Использование предлагаемого способа терапии поясняется следующими примерами.
Пример 1. Больной П-в., 52 года. Поступил с жалобами на наличие высыпаний на коже туловища и конечностей, интенсивный постоянный кожный зуд. Болен данным заболеванием в течение 2 лет, отмечает непрерывно-рецидивирующее течение заболевания, несмотря на проводимую терапию (десенсибилизирующую, дезинтоксикационную, системную (преднизолон до 20 мг/сут, топические ГКС). Гистологическое исследование и иммунофенотипирование образца кожи в УрНИИДВиИ МЗ РФ позволили установить диагноз: Злокачественная Т-клеточная лимфома кожи. Грибовидный микоз, эритродермическая форма (III стадия).
При осмотре больного: кожные покровы в состоянии эритродермии, кожа красновато-синюшного оттенка, выраженная инфильтрация, мелкочешуйчатое шелушение, экскориации на коже туловища и верхних конечностей, гиперкератоз ладоней и подошв. Соматически: ИБС, атеросклеротический кардиосклероз, НК 0-I; хронический бронхит. Печень не увеличена в размерах, селезенка не пальпируется.
При клинико-лабораторном исследовании в стационаре УрНИИДВиИ были обнаружены отклонения от нормы в основных иммунологических показателях: дисиммуноглобулинемия, гипер-Е-иммуноглобулинемия, нарушение соотношения популяций Т-хелперы/Т-супрессоры, повышение уровня CD19 (В-клетки), сниженное в 1,7 раза содержание ИФН-гамма в сыворотке крови. В периферической крови – лейкоцитоз, лимфоцитопения, эозинофилия.
Было назначено лечение ридостином по традиционной схеме в форме в/м инъекций по 8 мг активного вещества, растворенного “ex tempore” в 2,0 мл воды для инъекций. Ридостин назначали с 1 недели общей терапии больных, вводили 2 раза в неделю с интервалом 2-3 дня, всего проведено 6 инъекций препарата. Одновременно назначался преднизолон per os 30 мг/сут в течение 21 дня, с последующим снижением на 2,5 мг в 3 сут, антигистаминные препараты, наружная мазевая терапия. Лечение проводилось под контролем гемограммы 1 раз в 5 дней.
В результате проводимой терапии после 2 инъекции препарата ридостин (1 неделя лечения) отмечалось значительное уменьшение интенсивности кожного зуда и жжения; после 4 инъекции (2 неделя лечения) – было зафиксировано снижение гиперемии и шелушения кожи, в этот же период значимо уменьшились инфильтрация кожи, ее шелушение. Разрешение эритродермических проявлений наступило на 4 неделе лечения. Побочных реакций и осложнений терапии не отмечалось.
В повторной иммунограмме после проведения курса терапии наблюдалось существенное снижение уровня IgE, приближение к нормальным величинам уровня IgG и соотношения популяций Т-хелперы/Т-супрессоры. В периферической крови – нормализация содержания ИФН-гамма, лимфоцитов и эозинофилов. Больной выписан в состоянии полной клинической ремиссии, продолжительность курса терапии составила 38 дней.
Пример 2. Больная Б-а, 65 лет, находилась под наблюдением в клинике УрНИИДВиИ с 1999 г., после неоднократных гистологических исследований в 2001 г. верифицирован диагноз: Т-клеточная злокачественная лимфома кожи. Грибовидный микоз, НА стадия. Больная неоднократно проходила стационарное лечение в клинике с использованием десенсибилизирующих, дезинтоксикационных препаратов, системной терапии (преднизолон 30 мг/сут до 14-20 дней) и наружной кортикостероидной терапии, выписывалась с улучшением на поддерживающей терапии глюкокортикосгероидами. Кожный процесс приобрел резистентность к проводимой терапии, частые обострения сочетались с непродолжительными периодами ремиссии (2-3 месяца).
При клинико-лабораторном исследовании в УрНИИДВиИ в иммунограмме была обнаружена дисиммуноглобулинемия, умеренное повышение IgE, высокое содержание IL-4. В периферической крови – умеренный лейкоцитоз, эозинофилия.
Было назначено лечение ридостином по традиционной схеме в форме в/м инъекций по 8 мг активного вещества, растворенного “ex tempore” в 2,0 мл воды для инъекций. Ридостин назначали с 1 недели общей терапии больной, вводили 2 раза в неделю с интервалом 2-3 дня, всего проведено 6 инъекций препарата. Одновременно назначались преднизолон per os 35 мг/сут в течение 21 дня, с последующим снижением на 5 мг в 5 дней, антигистаминные препараты, наружная мазевая терапия. Лечение проводилось под контролем гемограммы 1 раз в 5 дней.
В результате проводимой терапии после 4 инъекции препарата ридостин (2 неделя лечения) отмечались уменьшение активной гиперемии и инфильтрации в области бляшек, уменьшение зуда в местах высыпаний. После 6 инъекций препарата пятнистые высыпания практически регрессировали, а бляшки значительно уменьшились по высоте, полностью исчез зуд. В течение 3 недель после окончания введения ридостина доза преднизолона медленно снижалась до полной отмены. При выписке (общий срок пребывания в стационаре 43 дня) процесс регрессировал на 50%, что характеризует исход терапии как частичную ремиссию процесса. Побочных реакций и осложнений во время терапии не отмечалось.
Динамическое изучение иммунологического статуса выявило тенденцию к снижению IgE в периферической крови, снижение лейкоцитоза, эозинофилии.
Предложенным способом в УрНИИДВиИ пролечено 13 больных Т-ЗЛК в возрасте от 39 до 70 лет, в том числе 3 женщины и 10 мужчин. Давность заболевания составляла от 2 до 17 лет, диагнозы были гистологически верифицированы впервые в клинике УрНИИДВиИ. Ранее больные лечились с использованием системных и топических кортикостероидов, что не позволяло добиться полной клинической ремиссии. После проведенного курса терапии ридостином и преднизолоном состояние значительного клинического улучшения достигнуто у 12 из 13 больных (92,4%), у одного больного (7,6%) – минимальное улучшение процесса. Длительность ремиссии составила от 12 до 19 месяцев.
Таким образом, апробирован новый способ лечения Т-ЗЛК (грибовидного микоза), включающий назначение индуктора интерферона в сочетании со средне терапевтическими дозами преднизолона, что позволило существенно повысить эффективность терапии при снижении риска возникновения осложнений.

Формула изобретения Способ лечения грибовидного микоза, включающий применение иммунотерапии и преднизолона, отличающийся тем, что в качестве индуктора эндогенного интерферона применяют ридостин в виде внутримышечных инъекций по 8 мг 2 раза в неделю общим курсом 6 инъекций и одновременно с ридостином назначают преднизолон per os в дозе 0,5 мг/кг/сут, с последующим снижением дозы на 2,5 мг в 3 суток. MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 17.09.2005
Извещение опубликовано: 10.12.2006 БИ: 34/2006
|
||||||||||||||||||||||||||
