Патент на изобретение №2230454
|
||||||||||||||||||||||||||
(54) ХЛАДООГРАЖДАЮЩИЙ РАСТВОР ДЛЯ ЗАМОРАЖИВАНИЯ ТРОМБОЦИТОВ ПРИ УМЕРЕННО-НИЗКОЙ ТЕМПЕРАТУРЕ
(57) Реферат: Изобретение относится к медицине, а именно к криоконсервированию клеток крови. Хладоограждающий раствор для замораживания тромбоцитов имеет следующий состав, мас.%: гексаметиленбистетраоксиэтилмочевина – 10,0, фумарат натрия 1,5-2,3, лимонная кислота – 0,9-1,1, вода для инъекций – остальное. Раствор обеспечивает сохранение высокого процента физиологически полноценных тромбоцитов при криоконсервировании при умереннонизкой температуре. 3 табл. Изобретение относится к медицине, в частности к криоконсервированию клеток крови. В качестве прототипа нами использована работа Е.П.Сведенцова и соавт. “Водный раствор для криоконсервирования тромбоцитов” при -196  С (1).
Существенными недостатками прототипа являются: 1) отсутствие в составе криозащитного раствора антигипоксанта, способствующего быстрому восстановлению энергетических процессов в клетке после ее выхода из холодового анабиоза; 2) наличие в прототипе умеренно токсичного антиагреганта – ЭДТА Na2; 3) обязательное использование ультранизкой температуры (-196 С (1).
Существенными недостатками прототипа являются: 1) отсутствие в составе криозащитного раствора антигипоксанта, способствующего быстрому восстановлению энергетических процессов в клетке после ее выхода из холодового анабиоза; 2) наличие в прототипе умеренно токсичного антиагреганта – ЭДТА Na2; 3) обязательное использование ультранизкой температуры (-196 С) при замораживании биообъекта, что сопряжено с высокой дороговизной криогенного оборудования, большой затратностью применяемого жидкого азота и необходимостью обслуживания высококвалифицированным техническим персоналом.
Для устранения вышеуказанных недостатков в известный раствор вводят компонент – фумарат натрия с целью восстановления и усиления энергетического потенциала клетки после ее оттаивания, т.к. фумаровая кислота участвует в цикле Кребса, обеспечивающего жизнедеятельность клетки, из состава же раствора исключен компонент – ЭДТА Na2. Кроме того устранена высокозатратная жидкоазотная технология криоконсервирования, т.к. новый состав раствора позволяет применять доступный, экономичный метод замораживания тромбоцитов до -40 С) при замораживании биообъекта, что сопряжено с высокой дороговизной криогенного оборудования, большой затратностью применяемого жидкого азота и необходимостью обслуживания высококвалифицированным техническим персоналом.
Для устранения вышеуказанных недостатков в известный раствор вводят компонент – фумарат натрия с целью восстановления и усиления энергетического потенциала клетки после ее оттаивания, т.к. фумаровая кислота участвует в цикле Кребса, обеспечивающего жизнедеятельность клетки, из состава же раствора исключен компонент – ЭДТА Na2. Кроме того устранена высокозатратная жидкоазотная технология криоконсервирования, т.к. новый состав раствора позволяет применять доступный, экономичный метод замораживания тромбоцитов до -40 С по экспоненциальной программе в электроморозильниках.
Таким образом, предлагаемый хладоограждающий раствор содержит следующие ингредиенты, мас.%:
1) криопротектор – гексаметиленбистетраоксиэтилмочевину (ее аббревиатура – ГМБТОЭМ), имеющую наименьшую токсичность из всех эффективных криофилактиков: ее ЛД50 составляет 15,5 С по экспоненциальной программе в электроморозильниках.
Таким образом, предлагаемый хладоограждающий раствор содержит следующие ингредиенты, мас.%:
1) криопротектор – гексаметиленбистетраоксиэтилмочевину (ее аббревиатура – ГМБТОЭМ), имеющую наименьшую токсичность из всех эффективных криофилактиков: ее ЛД50 составляет 15,5 0,6 г/кг массы мыши (Сведенцов Е.П. и др. (2);
2) антигипоксант – фумарат натрия;
3) антикоагулянт – лимонную кислоту;
4) воду для инъекций.
Все ингредиенты, входящие в хладоограждающий раствор, производятся в РФ.
Пример использования средства: хладоограждающий раствор, содержащий ГМБТОЭМ в концентрации 10%, фумарат натрия 1,9%, лимонную кислоту 1%, воду для инъекций до 100 мл, имеющий рН 5,5-6,5, смешивают с тромбоцитным концентратом в полимерном контейнере “Компопласт”. Смесь выдерживают при комнатной температуре в течение 20 мин; замораживают по экспоненциальной программе в электрическом морозильнике в 4-литровой ванне с этиловым спиртом, охлажденном до -28 0,6 г/кг массы мыши (Сведенцов Е.П. и др. (2);
2) антигипоксант – фумарат натрия;
3) антикоагулянт – лимонную кислоту;
4) воду для инъекций.
Все ингредиенты, входящие в хладоограждающий раствор, производятся в РФ.
Пример использования средства: хладоограждающий раствор, содержащий ГМБТОЭМ в концентрации 10%, фумарат натрия 1,9%, лимонную кислоту 1%, воду для инъекций до 100 мл, имеющий рН 5,5-6,5, смешивают с тромбоцитным концентратом в полимерном контейнере “Компопласт”. Смесь выдерживают при комнатной температуре в течение 20 мин; замораживают по экспоненциальной программе в электрическом морозильнике в 4-литровой ванне с этиловым спиртом, охлажденном до -28 С, выдерживая в нем 15 мин. Затем контейнер с тромбоцитами переносят в электроморозильник для замораживания до -40 С, выдерживая в нем 15 мин. Затем контейнер с тромбоцитами переносят в электроморозильник для замораживания до -40 С и оставляют в нем для хранения. Термограмму записывают по датчику, установленному в аналогичном контейнере “Компопласт” с данным хладоограждающим раствором. Размораживание осуществляют в 20-литровой ванне при +38 С и оставляют в нем для хранения. Термограмму записывают по датчику, установленному в аналогичном контейнере “Компопласт” с данным хладоограждающим раствором. Размораживание осуществляют в 20-литровой ванне при +38 С в течение 35-45 с при покачивании контейнера 3-4 раза в секунду. Определяют морфологическую сохранность размороженных тромбоцитов (подсчет в камере Горяева), их функциональную активность (адгезию к стеклу, индуцированную агрегацию и реакцию на гипотонический шок). Расчет производится в процентах в сравнении с аналогичными показателями клеток до замораживания.
Экспериментальные исследования выполнены в лаборатории консервирования крови и тканей ГУ Кировского НИИ гематологии и переливания крови. Изучены три варианта хладоограждающих растворов для замораживания тромбоцитного концентрата, различающихся по процентному содержанию входящих в него ингредиентов. Состав растворов представлен в табл. 1. С в течение 35-45 с при покачивании контейнера 3-4 раза в секунду. Определяют морфологическую сохранность размороженных тромбоцитов (подсчет в камере Горяева), их функциональную активность (адгезию к стеклу, индуцированную агрегацию и реакцию на гипотонический шок). Расчет производится в процентах в сравнении с аналогичными показателями клеток до замораживания.
Экспериментальные исследования выполнены в лаборатории консервирования крови и тканей ГУ Кировского НИИ гематологии и переливания крови. Изучены три варианта хладоограждающих растворов для замораживания тромбоцитного концентрата, различающихся по процентному содержанию входящих в него ингредиентов. Состав растворов представлен в табл. 1.
 При смешивании с тромбоцитами донорской крови в соотношении 1:1 конечная концентрация веществ (табл. 2), входящих в состав растворов 1, 2, 3, уменьшалась в 2 раза по сравнению с исходной, рН среды оставалась в пределах 5,5-6,5, оптимальной для тромбоцитов.
При смешивании с тромбоцитами донорской крови в соотношении 1:1 конечная концентрация веществ (табл. 2), входящих в состав растворов 1, 2, 3, уменьшалась в 2 раза по сравнению с исходной, рН среды оставалась в пределах 5,5-6,5, оптимальной для тромбоцитов. Замораживание происходило по двухступенчатой экспоненциальной программе: на первом этапе погружали контейнер с подготовленной смесью хладоограждающего раствора с тромбоцитным концентратом в 4-литровую спиртовую ванну, охлажденную до -28
Замораживание происходило по двухступенчатой экспоненциальной программе: на первом этапе погружали контейнер с подготовленной смесью хладоограждающего раствора с тромбоцитным концентратом в 4-литровую спиртовую ванну, охлажденную до -28 С, через 15 мин контейнер с тромбоцитами вынимали из ванны и помещали в электроморозильник для замораживания при умеренно низкой температуре до -40 С, через 15 мин контейнер с тромбоцитами вынимали из ванны и помещали в электроморозильник для замораживания при умеренно низкой температуре до -40 С, на это затрачивалось 8 мин. Контроль за охлаждением проводили по термограмме, записываемой по датчику, введенному в контейнер с хладоограждающим раствором с конечной концентрацией его ингредиентов. С, на это затрачивалось 8 мин. Контроль за охлаждением проводили по термограмме, записываемой по датчику, введенному в контейнер с хладоограждающим раствором с конечной концентрацией его ингредиентов.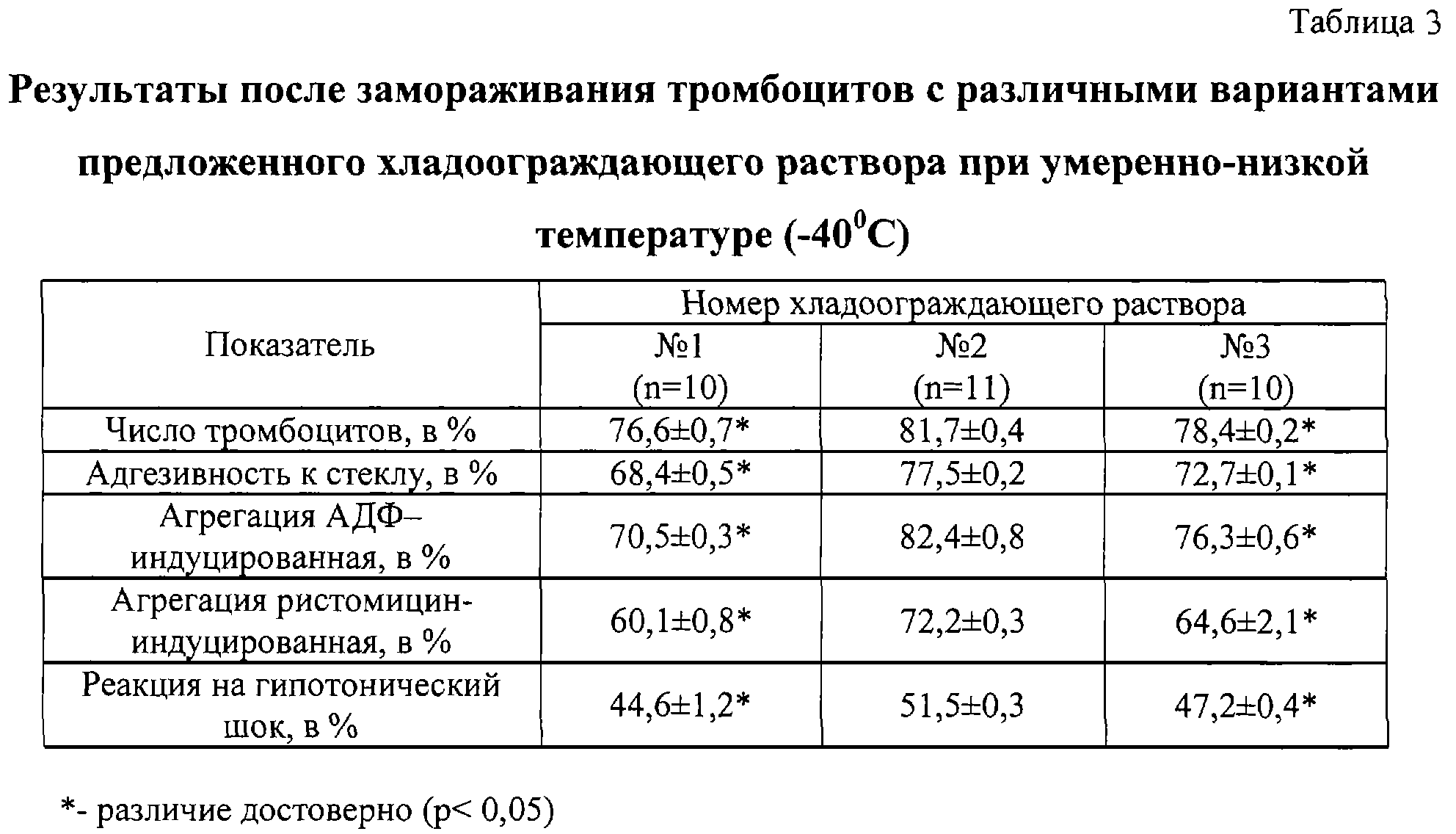 Размораживание производили через 1-28 суток в 20-литровой водяной ванне при +38
Размораживание производили через 1-28 суток в 20-литровой водяной ванне при +38 С в течение 35-40 с.
Отогревали до +2 С в течение 35-40 с.
Отогревали до +2 С. Выполняли исследования тромбоцитов на морфологическую сохранность и функциональную полноценность (табл.3); показатели даны в процентах к исходным (до замораживания).
Получены выраженные положительные результаты после замораживания и отогрева тромбоцитов с различными вариантами предложенного хладоограждающего раствора: сохранилось морфологически 76,6 С. Выполняли исследования тромбоцитов на морфологическую сохранность и функциональную полноценность (табл.3); показатели даны в процентах к исходным (до замораживания).
Получены выраженные положительные результаты после замораживания и отогрева тромбоцитов с различными вариантами предложенного хладоограждающего раствора: сохранилось морфологически 76,6 0,7% – 81,7 0,7% – 81,7 0,4% к исходному числу клеток (до замораживания), функциональная активность по разным тестам равнялась от 60,1 0,4% к исходному числу клеток (до замораживания), функциональная активность по разным тестам равнялась от 60,1 0,8% до 82,4 0,8% до 82,4 0,8%, а реакция на гипотонический шок (РГШ) составила от 44,6 0,8%, а реакция на гипотонический шок (РГШ) составила от 44,6 1,2% до 51,5 1,2% до 51,5 0,3% к исходным показателям. Надо отметить, что РГШ является наиболее важным тестом для тромбоцитов, т.к. прямо коррелирует с их состоянием после трансфузии тромбоцитного концентрата в сосудистое русло.
Разработанный нами хладоограждающий раствор прозрачен, со слабым желтоватым оттенком, без запаха, рН 5,5-6,5. Он хорошо смешивается с тромбоцитным концентратом, предотвращает агрегацию клеток, обеспечивает морфологическую и функциональную сохранность при положительной температуре и высокий процент физиологически полноценных тромбоцитов после замораживания-оттаивания. Это дает возможность применять его для консервирования замораживанием тромбоцитов при умеренно низкой температуре в лечебных учреждениях и учреждениях службы крови, которые имеют электроморозильники на -40 0,3% к исходным показателям. Надо отметить, что РГШ является наиболее важным тестом для тромбоцитов, т.к. прямо коррелирует с их состоянием после трансфузии тромбоцитного концентрата в сосудистое русло.
Разработанный нами хладоограждающий раствор прозрачен, со слабым желтоватым оттенком, без запаха, рН 5,5-6,5. Он хорошо смешивается с тромбоцитным концентратом, предотвращает агрегацию клеток, обеспечивает морфологическую и функциональную сохранность при положительной температуре и высокий процент физиологически полноценных тромбоцитов после замораживания-оттаивания. Это дает возможность применять его для консервирования замораживанием тромбоцитов при умеренно низкой температуре в лечебных учреждениях и учреждениях службы крови, которые имеют электроморозильники на -40 С и отделения длительного хранения крови.
Литература
1. Сведенцов Е.П., Селезнева О.М., Симкин Д.С., Новосадов В.М. Водный раствор для криоконсервирования тромбоцитов. Патент №1561227 (Роспатент). Регистр. 12.04.93.
2. Сведенцов Е.П., Селезнева О.М., Костяев А.А. О токсичности нового криоконсерванта для тромбоцитов. – В кн.: Вопросы трансфузиологии и клинической медицины. Киров, 1992 – С.7-8. С и отделения длительного хранения крови.
Литература
1. Сведенцов Е.П., Селезнева О.М., Симкин Д.С., Новосадов В.М. Водный раствор для криоконсервирования тромбоцитов. Патент №1561227 (Роспатент). Регистр. 12.04.93.
2. Сведенцов Е.П., Селезнева О.М., Костяев А.А. О токсичности нового криоконсерванта для тромбоцитов. – В кн.: Вопросы трансфузиологии и клинической медицины. Киров, 1992 – С.7-8.
Формула изобретения
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.05.2004
Извещение опубликовано: 10.06.2006 БИ: 16/2006
|
||||||||||||||||||||||||||
