Патент на изобретение №2228744
|
||||||||||||||||||||||||||
(54) АНТИОКСИДАНТНОЕ СРЕДСТВО
(57) Реферат: Изобретение относится к медицине, а именно к созданию новых лекарственных препаратов. Антиоксидантное средство содержит водный раствор парааминобензойной кислоты и аллантоина при следующем соотношении компонентов, мас.%: парааминобензойная кислота – 1,37  10-5 – 1,37, аллантоин – 1,58 10-5 – 1,37, аллантоин – 1,58 10-5 – 1,58, вода – остальное. Средство обладает выраженным антиоксидантным действием. 1 ил., 6 табл.
Изобретение относится к препаратам, содержащим органические активные ингредиенты, и может быть использовано в качестве лекарственного препарата, а также пищевой добавки, предупреждающих развитие свободнорадикальных процессов и нарушение антиоксидантной системы живых организмов при различных биологических процессах (старение, стресс) и заболеваниях, связанных с нарушениями свободно-радикальных процессов: воспалении, раке, бронхолегочных, сердечно-сосудистых и генетически обусловленных заболеваниях.
Жизнедеятельность биологических объектов возможна только благодаря существованию защитных систем, звеньями которых являются ферментативные и неферментативные антиоксиданты – вещества, обладающие способностью подавлять свободнорадикальное окисление. Их можно разделить на структурные, затрудняющие доступ компонентов окислительной реакции друг к другу или модифицирующие окисляемость субстрата (токоферол, холестерол, хелаторы металлов переменной валентности), и истинные антиоксиданты, способные, вступая в реакцию с активными формами кислорода, образовывать либо молекулярные продукты, либо радикалы с меньшей реакционной способностью (СОД, каталаза, глутатионпероксидаза).
В настоящее время известно большое число антиоксидантов, используемых в медицинской, фармацевтической, косметической и пищевой промышленности. При этом используются как природные так и синтетические антиоксиданты – ферменты антиоксидантной защиты, такие как супероксиддисмутаза (High effeciency skin protection formulation with sunscreen agents and antioxidants/патент US6015548, от 18.01.2000, МПК А 61 К 7/42, А 61 К 7/44, А 61 К 7/00, А 61 К 31/355, А 61 К 31/34) [1]. Глутатион – проявляет антиоксидантные свойства при ишемии.
Защитными агентами против окислительного стресса и хронических болезней являются некоторые витамины – витамин С – аскорбиновая кислота (Stabilized ascorbyl composition – WO 9823152 от 4.06.1998, МПК A 01 N 43/08, А 61 К 31/34 [2]; каротиноиды, токоферол (Preparation for enhancement of the antioxidant status of cells – WO 9918814 от 22.04.1999, МПК A 23 L 1/302, A 23 L 1/304, A 23 L 1/305, A 61 K 45/06 [3], витамин Е (Synergistic compositions for extending animal feed shelf life – US5498434 от 12.03.1996, МПК A 23 D 7/00 [4]), витамин A (High efficiency skin protection formulation with sunscreen agents and antioxidants – US 6015548 от 18.01.2000, A 61 K 7/42, A 61 K 7/44, A 61 K 7/00, A 61 K 31/355, A 61 K 31/34 [1]).
Недостатками используемых в качестве антиоксидантов веществ является их нестабильность (у ферментов), жирорастворимость (у токоферола, каротинов), высокий молекулярный вес, что затрудняет их проницаемость через клеточные мембраны.
Известно использование аллантоина в качестве антиоксиданта (патент RU 2176910 С1 7 А 61 К 31/00, 31/52, 35/00, 35/22 от 20.12.2001) [5], в котором показаны его антиоксидантные свойства, проявляющиеся в ингибировании интенсивности перекисного окисления липидов (ПОЛ) и нормализации и восстановлении оптимального соотношения активности антиоксидантных ферментов супероксиддисмутазы (СОД) и каталазы.
Недостатком аллантоина является пониженная активность каталазы в эритроцитах животных (на 40% по сравнению с контролем) при окислительном стрессе, индуцированном гипербарической оксигенацией (ГБО) (табл. 2, Б5 описания патента).
Показано защитное действие ПАБК для кожи от ультрафиолетового излучения (Sunscreen compositions US 5620682 от 15.04.1997, МПК А 61 К 7/42; А 61 К 7/44) [9]. ПАБК является стимулятором процессов раннего развития, в частности стимулирует развитие икры осетровых рыб (RU 93056336 А 6 А 01 К 61/00, от 17.12.93) [10]. Известно, что парааминобензойная кислота используется, как индуктор интерферона (RU 2132681 С1 6 А 61 К 31/195, от 21.10.98) [11], антикоагулянтное средство (RU 96113786 А 6 А 61 К 31/245, от 08. 07. 96) [12]. Обнаружены антиоксидантные свойства ПАБК на тканях головного мозга, печени, сыворотки крови в опытах in vivo, а также в опытах in vitro в концентрации 10 мг/кг веса животного (Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421 [13], а также заявка “Антиоксидант” RU 96113753, А 6 А 61 К 31/195, 31/245 от 08.07.1996 [14]).
Однако антиоксидантные свойства ПАБК не достаточны при ГБО-индуцированном окислительном стрессе для нормализации в печени и почках животных количества вторичного продукта ПОЛ – шиффовых оснований (ШО) (табл. 2, З5, К5). Применение ПАБК при ГБО не нормализует в тканях животных активность звеньев антиоксидантной системы – ферментов СОД и каталазы. На фоне применения ПАБК активность каталазы в эритроцитах и печени, остается на 39% и 49% ниже контрольных значений (табл.5, Б5, З5). При введениии ПАБК зарегистрирована неравномерная активация СОД в тканях животных: в легких – 309% относительно незащищенных животных и 93% относительно интактного контроля (табл.5, Д5), в почках и печени активность фермента остается ингибированной на 39% и 53% (табл.5, И5, Ж5).
Известны также антиоксидантные свойства ПАБК при окислительном стрессе, индуцированном облучением и гипоксией (Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421) [13]. Однако при облучении и гипоксии антиоксидантная активность ПАБК не достаточна для предотвращения накопления в тканях крыс продукта ПОЛ-малонового диальдегида (МДА), введение ПАБК приводит только к приближению уровня МДА к интактному контролю (табл. 1 и 2 в статье Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421) [13].
Техническим результатом изобретения является снижение уровня продуктов перекисного окисления липидов (шиффовых оснований и малонового диальдегида), нормализация и восстановление скоординированности действия антиоксидантных ферментов (супероксиддисмутазы и каталазы) при окислительном стрессе за счет оптимального соотношения исходных антиоксидантов аллантоина и ПАБК, обусловленные синергизмом действия составляющих. Технический результат достигается тем, что в антиоксидантное средство, содержащее водный раствор ПАБК, согласно изобретению, средство дополнительно содержит аллантоин при следующем соотношении компонентов, мас.%:
Парааминобензойная кислота 1,37 10-5 – 1,58, вода – остальное. Средство обладает выраженным антиоксидантным действием. 1 ил., 6 табл.
Изобретение относится к препаратам, содержащим органические активные ингредиенты, и может быть использовано в качестве лекарственного препарата, а также пищевой добавки, предупреждающих развитие свободнорадикальных процессов и нарушение антиоксидантной системы живых организмов при различных биологических процессах (старение, стресс) и заболеваниях, связанных с нарушениями свободно-радикальных процессов: воспалении, раке, бронхолегочных, сердечно-сосудистых и генетически обусловленных заболеваниях.
Жизнедеятельность биологических объектов возможна только благодаря существованию защитных систем, звеньями которых являются ферментативные и неферментативные антиоксиданты – вещества, обладающие способностью подавлять свободнорадикальное окисление. Их можно разделить на структурные, затрудняющие доступ компонентов окислительной реакции друг к другу или модифицирующие окисляемость субстрата (токоферол, холестерол, хелаторы металлов переменной валентности), и истинные антиоксиданты, способные, вступая в реакцию с активными формами кислорода, образовывать либо молекулярные продукты, либо радикалы с меньшей реакционной способностью (СОД, каталаза, глутатионпероксидаза).
В настоящее время известно большое число антиоксидантов, используемых в медицинской, фармацевтической, косметической и пищевой промышленности. При этом используются как природные так и синтетические антиоксиданты – ферменты антиоксидантной защиты, такие как супероксиддисмутаза (High effeciency skin protection formulation with sunscreen agents and antioxidants/патент US6015548, от 18.01.2000, МПК А 61 К 7/42, А 61 К 7/44, А 61 К 7/00, А 61 К 31/355, А 61 К 31/34) [1]. Глутатион – проявляет антиоксидантные свойства при ишемии.
Защитными агентами против окислительного стресса и хронических болезней являются некоторые витамины – витамин С – аскорбиновая кислота (Stabilized ascorbyl composition – WO 9823152 от 4.06.1998, МПК A 01 N 43/08, А 61 К 31/34 [2]; каротиноиды, токоферол (Preparation for enhancement of the antioxidant status of cells – WO 9918814 от 22.04.1999, МПК A 23 L 1/302, A 23 L 1/304, A 23 L 1/305, A 61 K 45/06 [3], витамин Е (Synergistic compositions for extending animal feed shelf life – US5498434 от 12.03.1996, МПК A 23 D 7/00 [4]), витамин A (High efficiency skin protection formulation with sunscreen agents and antioxidants – US 6015548 от 18.01.2000, A 61 K 7/42, A 61 K 7/44, A 61 K 7/00, A 61 K 31/355, A 61 K 31/34 [1]).
Недостатками используемых в качестве антиоксидантов веществ является их нестабильность (у ферментов), жирорастворимость (у токоферола, каротинов), высокий молекулярный вес, что затрудняет их проницаемость через клеточные мембраны.
Известно использование аллантоина в качестве антиоксиданта (патент RU 2176910 С1 7 А 61 К 31/00, 31/52, 35/00, 35/22 от 20.12.2001) [5], в котором показаны его антиоксидантные свойства, проявляющиеся в ингибировании интенсивности перекисного окисления липидов (ПОЛ) и нормализации и восстановлении оптимального соотношения активности антиоксидантных ферментов супероксиддисмутазы (СОД) и каталазы.
Недостатком аллантоина является пониженная активность каталазы в эритроцитах животных (на 40% по сравнению с контролем) при окислительном стрессе, индуцированном гипербарической оксигенацией (ГБО) (табл. 2, Б5 описания патента).
Показано защитное действие ПАБК для кожи от ультрафиолетового излучения (Sunscreen compositions US 5620682 от 15.04.1997, МПК А 61 К 7/42; А 61 К 7/44) [9]. ПАБК является стимулятором процессов раннего развития, в частности стимулирует развитие икры осетровых рыб (RU 93056336 А 6 А 01 К 61/00, от 17.12.93) [10]. Известно, что парааминобензойная кислота используется, как индуктор интерферона (RU 2132681 С1 6 А 61 К 31/195, от 21.10.98) [11], антикоагулянтное средство (RU 96113786 А 6 А 61 К 31/245, от 08. 07. 96) [12]. Обнаружены антиоксидантные свойства ПАБК на тканях головного мозга, печени, сыворотки крови в опытах in vivo, а также в опытах in vitro в концентрации 10 мг/кг веса животного (Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421 [13], а также заявка “Антиоксидант” RU 96113753, А 6 А 61 К 31/195, 31/245 от 08.07.1996 [14]).
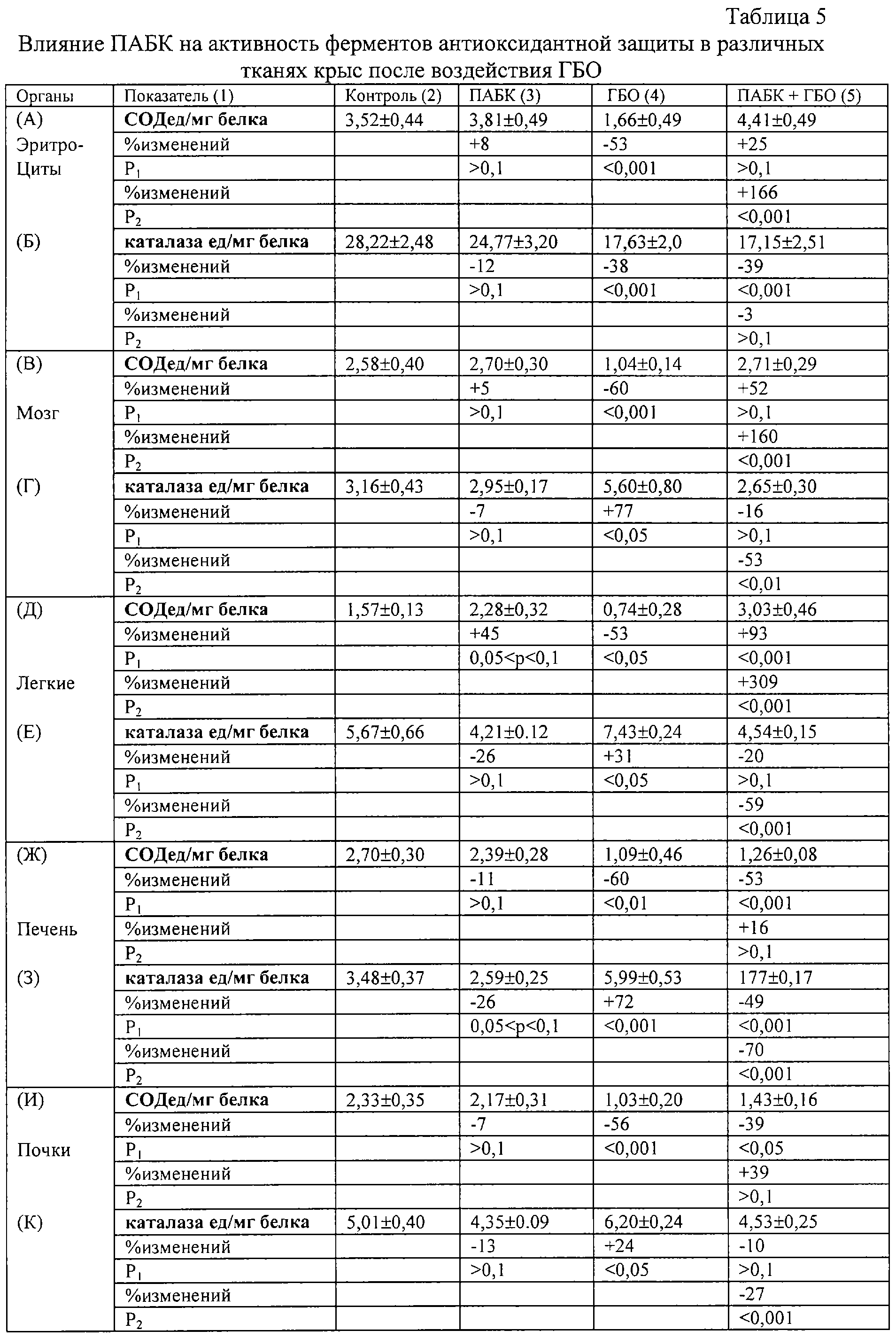
Однако антиоксидантные свойства ПАБК не достаточны при ГБО-индуцированном окислительном стрессе для нормализации в печени и почках животных количества вторичного продукта ПОЛ – шиффовых оснований (ШО) (табл. 2, З5, К5). Применение ПАБК при ГБО не нормализует в тканях животных активность звеньев антиоксидантной системы – ферментов СОД и каталазы. На фоне применения ПАБК активность каталазы в эритроцитах и печени, остается на 39% и 49% ниже контрольных значений (табл.5, Б5, З5). При введениии ПАБК зарегистрирована неравномерная активация СОД в тканях животных: в легких – 309% относительно незащищенных животных и 93% относительно интактного контроля (табл.5, Д5), в почках и печени активность фермента остается ингибированной на 39% и 53% (табл.5, И5, Ж5).
Известны также антиоксидантные свойства ПАБК при окислительном стрессе, индуцированном облучением и гипоксией (Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421) [13]. Однако при облучении и гипоксии антиоксидантная активность ПАБК не достаточна для предотвращения накопления в тканях крыс продукта ПОЛ-малонового диальдегида (МДА), введение ПАБК приводит только к приближению уровня МДА к интактному контролю (табл. 1 и 2 в статье Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421) [13].
Техническим результатом изобретения является снижение уровня продуктов перекисного окисления липидов (шиффовых оснований и малонового диальдегида), нормализация и восстановление скоординированности действия антиоксидантных ферментов (супероксиддисмутазы и каталазы) при окислительном стрессе за счет оптимального соотношения исходных антиоксидантов аллантоина и ПАБК, обусловленные синергизмом действия составляющих. Технический результат достигается тем, что в антиоксидантное средство, содержащее водный раствор ПАБК, согласно изобретению, средство дополнительно содержит аллантоин при следующем соотношении компонентов, мас.%:
Парааминобензойная кислота 1,37 10-5 – 1,37
Аллантоин 1,58 10-5 – 1,37
Аллантоин 1,58 10-5-1,58
Вода Остальное
Изобретение поясняется таблицами и графиком
В таблицах:
1. Влияние аллантоина на содержание продуктов перекисного окисления липидов в различных тканях крыс, обработанных повышенным давлением кислорода.
2. Влияние ПАБК на содержание продуктов перекисного окисления липидов в различных тканях крыс, обработанных повышенным давлением кислорода.
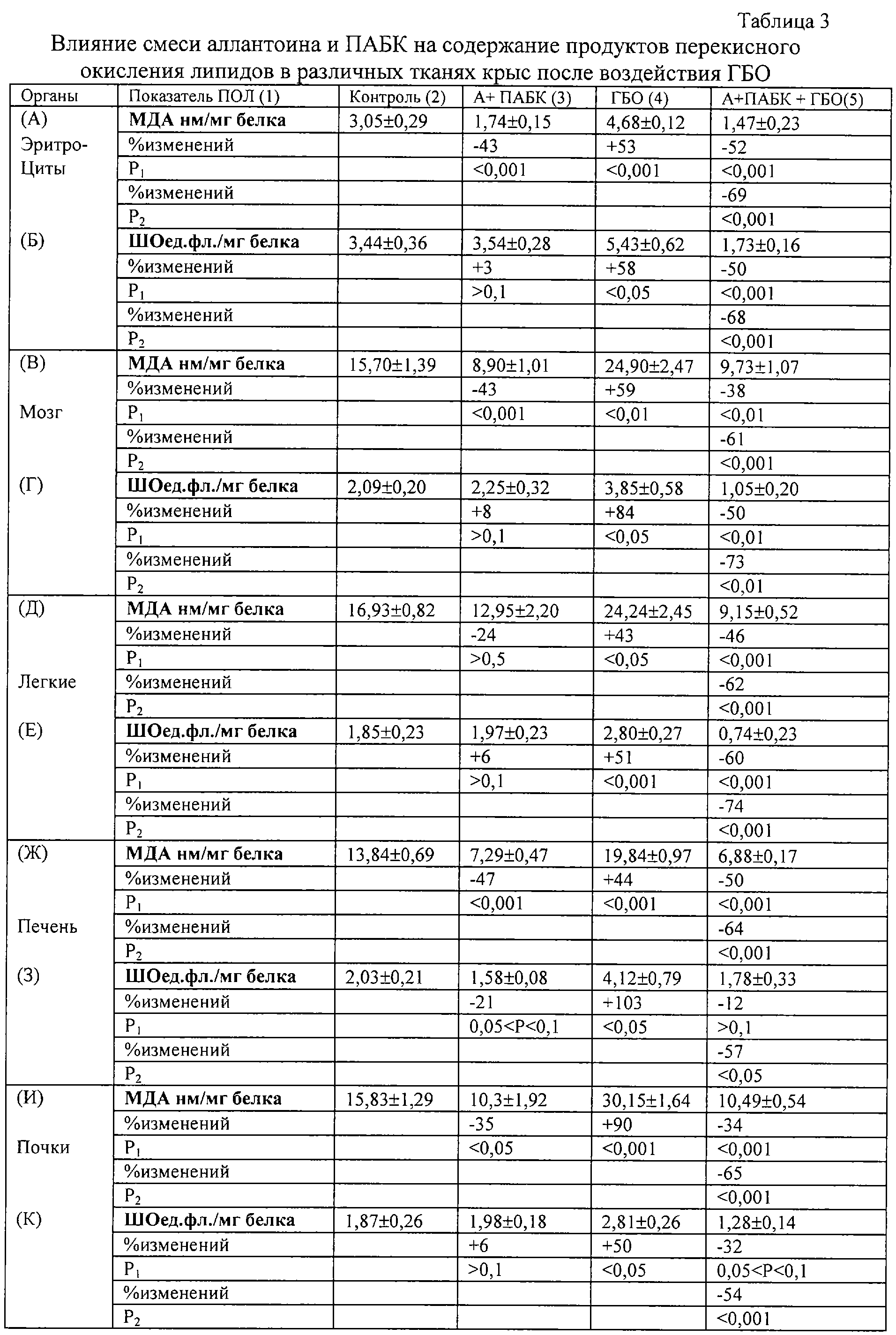
3. Влияние компаунда аллантоин и ПАБК на содержание продуктов перекисного окисления липидов в различных органах и тканях крыс, обработанных повышенным давлением кислорода.
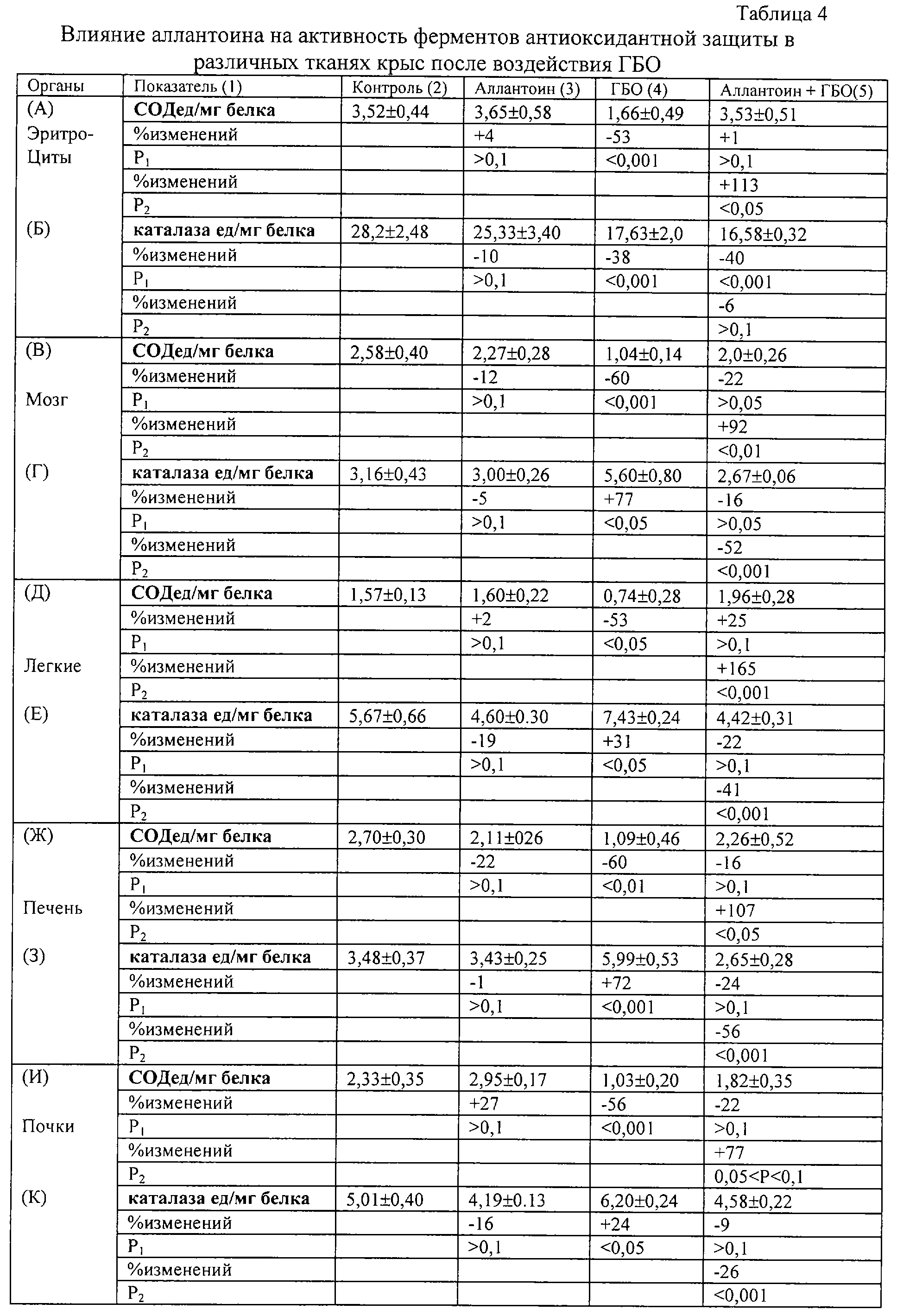
4. Влияние аллантоина на активность ферментов антиоксидантной защиты в различных тканях крыс, обработанных повышенным давлением кислорода.
5. Влияние ПАБК на активность ферментов антиоксидантной защиты в различных тканях крыс, обработанных повышенным давлением кислорода.
6. Влияние аллантоина и ПАБК на активность ферментов антиоксидантной защиты в различных тканях крыс, обработанных повышенным давлением кислорода.
На чертеже приведен график зависимости интенсивности Fe2+, индуцированной хемилюминесценции от концентрации смеси аллантоина и ПАБК (в импульсах за 500 с), где 1 – контроль, 2 – ПАБК-1,37 10-5-1,58
Вода Остальное
Изобретение поясняется таблицами и графиком
В таблицах:
1. Влияние аллантоина на содержание продуктов перекисного окисления липидов в различных тканях крыс, обработанных повышенным давлением кислорода.
2. Влияние ПАБК на содержание продуктов перекисного окисления липидов в различных тканях крыс, обработанных повышенным давлением кислорода.
3. Влияние компаунда аллантоин и ПАБК на содержание продуктов перекисного окисления липидов в различных органах и тканях крыс, обработанных повышенным давлением кислорода.
4. Влияние аллантоина на активность ферментов антиоксидантной защиты в различных тканях крыс, обработанных повышенным давлением кислорода.
5. Влияние ПАБК на активность ферментов антиоксидантной защиты в различных тканях крыс, обработанных повышенным давлением кислорода.
6. Влияние аллантоина и ПАБК на активность ферментов антиоксидантной защиты в различных тканях крыс, обработанных повышенным давлением кислорода.
На чертеже приведен график зависимости интенсивности Fe2+, индуцированной хемилюминесценции от концентрации смеси аллантоина и ПАБК (в импульсах за 500 с), где 1 – контроль, 2 – ПАБК-1,37 10-11%, аллантоин – 1,58 10-11%, аллантоин – 1,58 10-11%, 3 – ПАБК – 1,37 10-11%, 3 – ПАБК – 1,37 10-10%, аллантоин – 1,58 10-10%, аллантоин – 1,58 10-10%, 4 – ПАБК – 1,37 10-10%, 4 – ПАБК – 1,37 10-9%, аллантоин – 1,58 10-9%, аллантоин – 1,58 10-9%, 5 – ПАБК – 1,37 10-9%, 5 – ПАБК – 1,37 10-8%, аллантоин – 1,58 10-8%, аллантоин – 1,58 10-8%, 6 – ПАБК – 1,37 10-8%, 6 – ПАБК – 1,37 10-7%, аллантоин – 1,58 10-7%, аллантоин – 1,58 10-7%, 7 – ПАБК – 1,37 10-7%, 7 – ПАБК – 1,37 10-6%, аллантоин – 1,58 10-6%, аллантоин – 1,58 10-6%, 8 – ПАБК – 1,37 10-6%, 8 – ПАБК – 1,37 10-5%, аллантоин – 1,58 10-5%, аллантоин – 1,58 10-5%, 9 – ПАБК – 1,37 10-5%, 9 – ПАБК – 1,37 10-4%, аллантоин – 1,58 10-4%, аллантоин – 1,58 10-4%, 10 – ПАБК – 1,37 10-4%, 10 – ПАБК – 1,37 10-3%, аллантоин – 1,58 10-3%, аллантоин – 1,58 10-3%, 11 – ПАБК – 1,37 10-3%, 11 – ПАБК – 1,37 10-2%, аллантоин – 1,58 10-2%, аллантоин – 1,58 10-2%, 12 – ПАБК – 1,37 10-2%, 12 – ПАБК – 1,37 10-1%, аллантоин – 1,58 10-1%, аллантоин – 1,58 10-1%, 13 – ПАБК – 1,37%, аллантоин – 1,58%.
Антиоксидантные свойства различных концентраций смеси, включающей ПАБК (Ереванский завод химреактивов) и аллантоин (фирмы “Serva”) в диапазоне концентраций от 1,37% до 1,37 10-1%, 13 – ПАБК – 1,37%, аллантоин – 1,58%.
Антиоксидантные свойства различных концентраций смеси, включающей ПАБК (Ереванский завод химреактивов) и аллантоин (фирмы “Serva”) в диапазоне концентраций от 1,37% до 1,37 10-11% и от 1,58% до 1,58 10-11% и от 1,58% до 1,58 10-11% соответственно, оценивали по известной методике в модельном эксперименте по интенсивности Fe2+ хемилюминесценции (Шерстнев М.П., Атапаев Т.Б., Владимиров Ю.А. “Активированная родомином Ж хемилюминисценция плазмы крови в присутствии ионов двухвалентного железа”, Биофизика, 1989, т. XXXIV, в.4, стр.684-687) [15]. Модельная система состояла из 3 мл 0.2 М К-фосфатного буфера (рН 7,4), 0,1 мл 10% водной эмульсии липопротеидов яичного желтка, 50 мкл 1 мМ водного раствора родомина Ж в качестве активатора ХЛ реакции, 0,5 мл водного раствора FeSO4·7Н2O (3 мМ) в качестве индуктора процессов ПОЛ, 0,4 мл смеси аллантоина и ПАБК различной концентрации.
Интенсивность свободнорадикальных процессов оценивали по светосумме Fe-индуцируемой ХЛ, отражающей интенсивность процессов перекисного окисления липидов (ПОЛ) при окислительном стрессе (Владимиров Ю.А. “Свечение, сопровождающее биохимические реакции”, Соросовский образовательный журнал, №6, 1999, стр. 25-32) [16].
Хемилюминесцентный анализ проводили на установке для регистрации индуцированной ХЛ на основе сцинтилляционного спектрофотометра 22028 (RFT, ГДР), где детектором служил фотоэлектронный умножитель ФЭУ-37.
Как показано на чертеже 1, зарегистрировано дозазависимое влияние смеси аллантоина и ПАБК на уровень светосуммы. Смесь, содержащая ПАБК и аллантоин в диапазоне концентраций 1,37 10-11% соответственно, оценивали по известной методике в модельном эксперименте по интенсивности Fe2+ хемилюминесценции (Шерстнев М.П., Атапаев Т.Б., Владимиров Ю.А. “Активированная родомином Ж хемилюминисценция плазмы крови в присутствии ионов двухвалентного железа”, Биофизика, 1989, т. XXXIV, в.4, стр.684-687) [15]. Модельная система состояла из 3 мл 0.2 М К-фосфатного буфера (рН 7,4), 0,1 мл 10% водной эмульсии липопротеидов яичного желтка, 50 мкл 1 мМ водного раствора родомина Ж в качестве активатора ХЛ реакции, 0,5 мл водного раствора FeSO4·7Н2O (3 мМ) в качестве индуктора процессов ПОЛ, 0,4 мл смеси аллантоина и ПАБК различной концентрации.
Интенсивность свободнорадикальных процессов оценивали по светосумме Fe-индуцируемой ХЛ, отражающей интенсивность процессов перекисного окисления липидов (ПОЛ) при окислительном стрессе (Владимиров Ю.А. “Свечение, сопровождающее биохимические реакции”, Соросовский образовательный журнал, №6, 1999, стр. 25-32) [16].
Хемилюминесцентный анализ проводили на установке для регистрации индуцированной ХЛ на основе сцинтилляционного спектрофотометра 22028 (RFT, ГДР), где детектором служил фотоэлектронный умножитель ФЭУ-37.
Как показано на чертеже 1, зарегистрировано дозазависимое влияние смеси аллантоина и ПАБК на уровень светосуммы. Смесь, содержащая ПАБК и аллантоин в диапазоне концентраций 1,37 10-5 – 1,37% и 1,58 10-5 – 1,37% и 1,58 10-5 – 1,58% соответственно, эффективно снижает светосумму свечения. Это означает, что под влиянием смеси аллантоина и ПАБК интенсивность свободнорадикальных процессов снижается. Выход за пределы концентраций смеси приводит к возрастанию интенсивности процессов ПОЛ.
Кроме модельного эксперимента, повышенные антиоксидантные свойства смеси аллантоина и ПАБК в заявляемых концентрациях подтверждены в экспериментах на животных.
Пример.
Свежеприготовленный водный раствор, содержащий 1,58 10-5 – 1,58% соответственно, эффективно снижает светосумму свечения. Это означает, что под влиянием смеси аллантоина и ПАБК интенсивность свободнорадикальных процессов снижается. Выход за пределы концентраций смеси приводит к возрастанию интенсивности процессов ПОЛ.
Кроме модельного эксперимента, повышенные антиоксидантные свойства смеси аллантоина и ПАБК в заявляемых концентрациях подтверждены в экспериментах на животных.
Пример.
Свежеприготовленный водный раствор, содержащий 1,58 10-5% аллантоина и 1,37 10-5% аллантоина и 1,37 10-4% раствора ПАБК вводили животным внутрибрюшинно за 1 ч, 12 ч и 24 ч до обработки повышенным давлением кислорода (0,5 МПа 2 ч) из расчета 5 10-4% раствора ПАБК вводили животным внутрибрюшинно за 1 ч, 12 ч и 24 ч до обработки повышенным давлением кислорода (0,5 МПа 2 ч) из расчета 5 10-3 мл смеси на 1 г массы животного.
Испытания проводились на белых крысах-самцах весом 200 грамм. Антиоксидант вводили в концентрациях в пересчете на вес животного внутрибрюшинно за 1, 12 и 24 часа до обработки ГБО. Условия окислительного стресса моделировались повышенным давлением кислорода 0,5 МПа в течение 2 часов. Сразу после окончания действия повышенного давления кислорода животных декапитировали и готовили гомогенаты из тканей мозга, печени, легких и почек. Гепаринизированную кровь ценрифугировали в течение 10 минут при 3000 об/мин. Интенсивность перекисного окисления липидов (ПОЛ) оценивали по уровню шиффовых оснований (ШО) и малонового диальдегида (МДА). Антиоксидантный статус тканей оценивали по активности ферментов СОД и каталазы.
В условиях ГБО-индуцированного окислительного стресса наблюдается повышение интенсивности ПОЛ во всех тканях: уровень МДА повышается на 43-90% (табл. 1, А4, В4, Д4, Ж4, И4), содержание ШО возрастает на 50-103% (табл. 1, Б4, Г4, Е4, З4, К4). При этом наблюдалось нарушение скоординированности в работе сопряженных антиоксидантных ферментов – СОД и каталазы. В условиях ГБО наблюдается ингибирование активности СОД на 53-60% в различных тканях крыс (табл.4, В4, Д4, Ж4, И4), тогда как активность каталазы возрастает на 24-77% в тканях (табл. 4, Г4, Е4, 34, К4), а в эритроцитах снижается на 38% относительно интактного контроля (табл. 4, Б4).
Таким образом, ГБО-индуцированный окислительный стресс, использованный нами в качестве экспериментальной модели, сопровождается существенной интенсификацией ПОЛ, напряженностью и нарушением функционирования компонентов антиоксидантной ферментной системы в тканях крыс.
Анализ результатов проведенных исследований показал, что смесь аллантоина и ПАБК проявляет выраженные антиоксидантные свойства при ГБО-индуцированном окислительном стрессе, что выражается в существенном снижении интенсивности ПОЛ в эритроцитах, мозге, легких, печени и почках животных. При этом в тканях животных зарегистрировано снижение уровня вторичного молекулярного продукта ПОЛ – МДА на 35-47% по сравнению с интактным контролем (табл. 3, А5, В5, Д5, Ж5, И5). Снижение содержания ШО составляет 32-50% относительно интактного контроля и 54-74% относительно гипероксического контроля (табл. 3, Б5, Г5, Е5, З5, К5). Отсюда следует, что уровень ПОЛ при применении смеси аллантоина и ПАБК не просто нормализуется, а опускается ниже нормы. Это свидетельствует о высокой антиоксидантной емкости и мощности изучаемой смеси.
Применение смеси аллантоина и ПАБК приводит также к относительно равновыраженной активации СОД в тканях при ГБО, составляющей 95-170% относительно гипероксического контроля (табл. 6, А5, В5, Д5, Ж5, И5). При этом активность фермента каталазы, повышенная при ГБО, нормализуется во всех тканях, достоверных изменений ее уровня по сравнению с интактными животными не зарегистрировано (табл. 6, Б5, Г5, Е5, З5, К5).
Отсюда следует, что применение смеси аллантоина и ПАБК способствует нормализации функционирования важнейших ферментов антиоксидантной защиты – СОД и каталазы – в тканях при ГБО-индуцированном окислительном стрессе.
По сравнению с ПАБК (прототипом) смесь ПАБК с аллантоином предотвращает чрезмерную активацию СОД в легких (табл. 6, Д5) и отсутствие нормализации функционирования фермента в печени и почках, что показано в случае применения только ПАБК (табл. 6, Д5, Ж5). Применение смеси нормализует также содержание ШО в печени и почках (табл. 5, З5, К5).
По сравнению с аллантоином смесь ПАБК и аллантоина предотвращает снижение активности каталазы в эритроцитах при ГБО (табл. 6, Б5).
Таким образом, смесь аллантоина и ПАБК обладает большей антиоксидантной емкостью и мощностью, чем отдельные ее компоненты. Это подтверждается ингибирующим влиянием смеси на интенсивность ПОЛ в тканях интактных крыс, а также падением уровня продуктов ПОЛ – МДА и ШО – в условиях ГБО-индуцированного окислительного стресса ниже значений интактного контроля.
Введение смеси аллантоина и ПАБК оказывает нормализующее влияние на активность СОД и каталазы, восстанавливая оптимальное соотношение активности сопряженных антиоксидантных ферментов и согласованность их действия, снимает напряженность и дисбаланс ферментов антиоксидантной системы при окислительном стрессе.
Состав смеси определяет ее более высокий антиоксидантный потенциал, чем составляющих компонентов – аллантоина и ПАБК, которые в сочетании проявляют синергизм действия.
Источники информации
1. Патент US 6015548, от 18. 01.2000, МПК А 61 К 7/42, А 61 К 7/44, А 61 К 7/00, А 61 К 31/355, А 61 К 31/34 Roberts R.L. et al. High effeciency skin protection formulation with sunscreen agents and antioxidants.
2. Патент WO 9823152, от 4.06.1998, МПК A 01 N 43/08, А 61 К 31/34 Potini Chim Stabilized ascorbyl composition.
3. Патент WO 9918814 от 22.04.1999, МПК A 23 L 1/302, A 23 L 1/304, A 23 L 1/305, А 61 К 45/06 Z. Hendrik Janetal Preparation for enhancement of the antioxidant status of cells.
4. Патент US 5498434, от 12.03.1996, МПК A 23 D 7/00 Jonston J.D. Synergistic compositions for extending animal feed shelf life.
5. Патент RU 2176910 C1 7A 61 K 31/00, 31/52, 35/00, 35/22 от 20.12.2001 “Антиоксидант”.
9. Патент US 5620682 от 15.04.1997, МПК А 61 К 7/42; А 61 К 7/44 Fogel Arnold W Sunscreen compositions.
10. Патент RU 93056336 А 6 А 01 К 61/00, от 17.12.93. Способ стимуляции икры осетровых рыб.
11. Патент RU 2132681 С1 6 А 61 К 31/195, от 21.10.98. Индуктор интерферона.
12. Патент RU 96113786 А 6 А 61 К 31/245, от 08.07.96. Антикоагулянтное средство.
13. Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421 – прототип.
14. Патент RU 96113753, А 6 А 61 К 31/195, 31/245 от 08.07.1996. Антиоксидант.
15. Шерстнев М.П., Атапаев Т.Б., Владимиров Ю.А. Активированная родомином Ж хемилюминисценция плазмы крови в присутствии ионов двухвалентного железа. Биофизика, 1989, т.XXXIV, в.4, стр.684-687.
16. Владимиров Ю.А. Свечение, сопровождающее биохимические реакции. Соросовский образовательный журнал, №6,1999, стр.25-32. 10-3 мл смеси на 1 г массы животного.
Испытания проводились на белых крысах-самцах весом 200 грамм. Антиоксидант вводили в концентрациях в пересчете на вес животного внутрибрюшинно за 1, 12 и 24 часа до обработки ГБО. Условия окислительного стресса моделировались повышенным давлением кислорода 0,5 МПа в течение 2 часов. Сразу после окончания действия повышенного давления кислорода животных декапитировали и готовили гомогенаты из тканей мозга, печени, легких и почек. Гепаринизированную кровь ценрифугировали в течение 10 минут при 3000 об/мин. Интенсивность перекисного окисления липидов (ПОЛ) оценивали по уровню шиффовых оснований (ШО) и малонового диальдегида (МДА). Антиоксидантный статус тканей оценивали по активности ферментов СОД и каталазы.
В условиях ГБО-индуцированного окислительного стресса наблюдается повышение интенсивности ПОЛ во всех тканях: уровень МДА повышается на 43-90% (табл. 1, А4, В4, Д4, Ж4, И4), содержание ШО возрастает на 50-103% (табл. 1, Б4, Г4, Е4, З4, К4). При этом наблюдалось нарушение скоординированности в работе сопряженных антиоксидантных ферментов – СОД и каталазы. В условиях ГБО наблюдается ингибирование активности СОД на 53-60% в различных тканях крыс (табл.4, В4, Д4, Ж4, И4), тогда как активность каталазы возрастает на 24-77% в тканях (табл. 4, Г4, Е4, 34, К4), а в эритроцитах снижается на 38% относительно интактного контроля (табл. 4, Б4).
Таким образом, ГБО-индуцированный окислительный стресс, использованный нами в качестве экспериментальной модели, сопровождается существенной интенсификацией ПОЛ, напряженностью и нарушением функционирования компонентов антиоксидантной ферментной системы в тканях крыс.
Анализ результатов проведенных исследований показал, что смесь аллантоина и ПАБК проявляет выраженные антиоксидантные свойства при ГБО-индуцированном окислительном стрессе, что выражается в существенном снижении интенсивности ПОЛ в эритроцитах, мозге, легких, печени и почках животных. При этом в тканях животных зарегистрировано снижение уровня вторичного молекулярного продукта ПОЛ – МДА на 35-47% по сравнению с интактным контролем (табл. 3, А5, В5, Д5, Ж5, И5). Снижение содержания ШО составляет 32-50% относительно интактного контроля и 54-74% относительно гипероксического контроля (табл. 3, Б5, Г5, Е5, З5, К5). Отсюда следует, что уровень ПОЛ при применении смеси аллантоина и ПАБК не просто нормализуется, а опускается ниже нормы. Это свидетельствует о высокой антиоксидантной емкости и мощности изучаемой смеси.
Применение смеси аллантоина и ПАБК приводит также к относительно равновыраженной активации СОД в тканях при ГБО, составляющей 95-170% относительно гипероксического контроля (табл. 6, А5, В5, Д5, Ж5, И5). При этом активность фермента каталазы, повышенная при ГБО, нормализуется во всех тканях, достоверных изменений ее уровня по сравнению с интактными животными не зарегистрировано (табл. 6, Б5, Г5, Е5, З5, К5).
Отсюда следует, что применение смеси аллантоина и ПАБК способствует нормализации функционирования важнейших ферментов антиоксидантной защиты – СОД и каталазы – в тканях при ГБО-индуцированном окислительном стрессе.
По сравнению с ПАБК (прототипом) смесь ПАБК с аллантоином предотвращает чрезмерную активацию СОД в легких (табл. 6, Д5) и отсутствие нормализации функционирования фермента в печени и почках, что показано в случае применения только ПАБК (табл. 6, Д5, Ж5). Применение смеси нормализует также содержание ШО в печени и почках (табл. 5, З5, К5).
По сравнению с аллантоином смесь ПАБК и аллантоина предотвращает снижение активности каталазы в эритроцитах при ГБО (табл. 6, Б5).
Таким образом, смесь аллантоина и ПАБК обладает большей антиоксидантной емкостью и мощностью, чем отдельные ее компоненты. Это подтверждается ингибирующим влиянием смеси на интенсивность ПОЛ в тканях интактных крыс, а также падением уровня продуктов ПОЛ – МДА и ШО – в условиях ГБО-индуцированного окислительного стресса ниже значений интактного контроля.
Введение смеси аллантоина и ПАБК оказывает нормализующее влияние на активность СОД и каталазы, восстанавливая оптимальное соотношение активности сопряженных антиоксидантных ферментов и согласованность их действия, снимает напряженность и дисбаланс ферментов антиоксидантной системы при окислительном стрессе.
Состав смеси определяет ее более высокий антиоксидантный потенциал, чем составляющих компонентов – аллантоина и ПАБК, которые в сочетании проявляют синергизм действия.
Источники информации
1. Патент US 6015548, от 18. 01.2000, МПК А 61 К 7/42, А 61 К 7/44, А 61 К 7/00, А 61 К 31/355, А 61 К 31/34 Roberts R.L. et al. High effeciency skin protection formulation with sunscreen agents and antioxidants.
2. Патент WO 9823152, от 4.06.1998, МПК A 01 N 43/08, А 61 К 31/34 Potini Chim Stabilized ascorbyl composition.
3. Патент WO 9918814 от 22.04.1999, МПК A 23 L 1/302, A 23 L 1/304, A 23 L 1/305, А 61 К 45/06 Z. Hendrik Janetal Preparation for enhancement of the antioxidant status of cells.
4. Патент US 5498434, от 12.03.1996, МПК A 23 D 7/00 Jonston J.D. Synergistic compositions for extending animal feed shelf life.
5. Патент RU 2176910 C1 7A 61 K 31/00, 31/52, 35/00, 35/22 от 20.12.2001 “Антиоксидант”.
9. Патент US 5620682 от 15.04.1997, МПК А 61 К 7/42; А 61 К 7/44 Fogel Arnold W Sunscreen compositions.
10. Патент RU 93056336 А 6 А 01 К 61/00, от 17.12.93. Способ стимуляции икры осетровых рыб.
11. Патент RU 2132681 С1 6 А 61 К 31/195, от 21.10.98. Индуктор интерферона.
12. Патент RU 96113786 А 6 А 61 К 31/245, от 08.07.96. Антикоагулянтное средство.
13. Акберова С.И., Мусаев П.И., и др. Парааминобензойная кислота как антиоксидант. Доклады Академии наук, 1998, т.361, №3. – С.419-421 – прототип.
14. Патент RU 96113753, А 6 А 61 К 31/195, 31/245 от 08.07.1996. Антиоксидант.
15. Шерстнев М.П., Атапаев Т.Б., Владимиров Ю.А. Активированная родомином Ж хемилюминисценция плазмы крови в присутствии ионов двухвалентного железа. Биофизика, 1989, т.XXXIV, в.4, стр.684-687.
16. Владимиров Ю.А. Свечение, сопровождающее биохимические реакции. Соросовский образовательный журнал, №6,1999, стр.25-32.



Формула изобретения Антиоксидантное средство, содержащее водный раствор парааминобензойной кислоты, отличающееся тем, что средство дополнительно содержит аллантоин при следующем соотношении компонентов, мас.%: Парааминобензойная кислота 1,37  10-5 – 1,37
Аллантоин 1,58 10-5 – 1,37
Аллантоин 1,58 10-5 – 1,58
Вода Остальное 10-5 – 1,58
Вода Остальное
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.06.2007
Извещение опубликовано: 20.02.2009 БИ: 05/2009
|
||||||||||||||||||||||||||
