Патент на изобретение №2228527
|
||||||||||||||||||||||||||
(54) СПОСОБ ОПРЕДЕЛЕНИЯ АНТИПИРИНА
(57) Реферат: Изобретение относится к медицине, а именно к биохимии. Сущность способа: исследуемую биопробу и стандартный раствор антипирина наносят на силикагелевую пластину марки Сорбфил, осуществляют хроматографирование в системе растворителей вода:уксусная кислота, взятых в объемном соотношении 3:1, в течение 10 минут, после чего выдерживают в течение 2-3 минут при температуре 50  С, обрабатывают реагентом, содержащим реактив Эрлиха в смеси с уксусной и фосфорной кислотой, после чего повторно выдерживают при температуре 50 С, обрабатывают реагентом, содержащим реактив Эрлиха в смеси с уксусной и фосфорной кислотой, после чего повторно выдерживают при температуре 50 С в течение 2-3 минут и определяют содержание антипирина в исследуемом образце по площадям пятен пробы и стандарта. Способ обеспечивает высокую точность и чувствительность определения содержания антипирина в биологических объектах, основан на использовании дешевых и доступных реагентов. 2 табл.
Изобретение относится к области медицины, а именно к биохимии, и может быть использовано для оценки функционального состояния печени.
Известен способ определения метаболической функции печени путем проведения антипиринового теста с получением показателей времени полувыведения (Т 1/2) и клиренса антипирина (Clir). Количественное определение антипирина проводят одним из методов: спектрофотометрически [1], фотоколориметрически [2], газожидкостной хроматографией [3], жидкостной хроматографией [4].
К недостаткам каждого из этих методов следует отнести многостадийность и длительность определения. Существенным недостатком спектрофотометрического и фотоколориметрического определения антипирина является необходимость химической модификации препарата при подготовке образца биологической жидкости к анализу, зависимость интенсивности окраски анализируемого раствора от времени и температуры. Данные способы недостаточно чувствительны и требуют больших затрат времени на проведение анализа. При газожидкостном хроматографировании дополнительным ухудшающим фактором служит использование высокой температуры. Все это приводит к нарушению воспроизводимости результатов анализа, а значит к снижению точности определения количества антипирина. Длительность анализа в среднем составляет 1-1,5 часа.
Наиболее близким по технической сущности к предлагаемому является способ определения антипирина методом тонкослойной хроматографии (ТСХ).
Известный способ осуществляют следующим образом.
На пластину для тонкослойной хроматографии с закрепленным слоем силикагеля наносят стандартные растворы антипирина различной концентрации и супернатант слюны обследуемого пациента и высушивают. Хроматографирование проводят в системе растворителей хлороформ:этиловый спирт в соотношении 80:20, пятна антипирина окрашивают парами йода. Концентрацию антипирина в образце определяют при помощи денситометра или методом планиметрии [5].
К недостаткам данного способа следует отнести получение размытых, нечетко выраженных пятен на пластине, поскольку обязательное увлажнение часто вызывает их расплывание и смыв с пластины, что влияет на точность и чувствительность способа.
Кроме этого, к недостаткам известного способа следует также отнести многостадийность и использование летучих реагентов – йода, ледяной уксусной кислоты, хлороформа. Длительность анализа составляет около часа.
Авторы заявляемого способа пользовались этим методом для определения антипирина, но при этом столкнулись с рядом сложностей:
1. Неэффективностью разделения метаболитов антипирина в системе растворителей хлороформ:спирт.
2. Частой размытостью пятен.
3. Проявитель – пары йода – являются летучими и высокотоксичными соединениями.
4. Невоспроизводимостью результатов, стандартное отклонение (ошибка определения) выходило за пределы допустимого (2 С в течение 2-3 минут и определяют содержание антипирина в исследуемом образце по площадям пятен пробы и стандарта. Способ обеспечивает высокую точность и чувствительность определения содержания антипирина в биологических объектах, основан на использовании дешевых и доступных реагентов. 2 табл.
Изобретение относится к области медицины, а именно к биохимии, и может быть использовано для оценки функционального состояния печени.
Известен способ определения метаболической функции печени путем проведения антипиринового теста с получением показателей времени полувыведения (Т 1/2) и клиренса антипирина (Clir). Количественное определение антипирина проводят одним из методов: спектрофотометрически [1], фотоколориметрически [2], газожидкостной хроматографией [3], жидкостной хроматографией [4].
К недостаткам каждого из этих методов следует отнести многостадийность и длительность определения. Существенным недостатком спектрофотометрического и фотоколориметрического определения антипирина является необходимость химической модификации препарата при подготовке образца биологической жидкости к анализу, зависимость интенсивности окраски анализируемого раствора от времени и температуры. Данные способы недостаточно чувствительны и требуют больших затрат времени на проведение анализа. При газожидкостном хроматографировании дополнительным ухудшающим фактором служит использование высокой температуры. Все это приводит к нарушению воспроизводимости результатов анализа, а значит к снижению точности определения количества антипирина. Длительность анализа в среднем составляет 1-1,5 часа.
Наиболее близким по технической сущности к предлагаемому является способ определения антипирина методом тонкослойной хроматографии (ТСХ).
Известный способ осуществляют следующим образом.
На пластину для тонкослойной хроматографии с закрепленным слоем силикагеля наносят стандартные растворы антипирина различной концентрации и супернатант слюны обследуемого пациента и высушивают. Хроматографирование проводят в системе растворителей хлороформ:этиловый спирт в соотношении 80:20, пятна антипирина окрашивают парами йода. Концентрацию антипирина в образце определяют при помощи денситометра или методом планиметрии [5].
К недостаткам данного способа следует отнести получение размытых, нечетко выраженных пятен на пластине, поскольку обязательное увлажнение часто вызывает их расплывание и смыв с пластины, что влияет на точность и чувствительность способа.
Кроме этого, к недостаткам известного способа следует также отнести многостадийность и использование летучих реагентов – йода, ледяной уксусной кислоты, хлороформа. Длительность анализа составляет около часа.
Авторы заявляемого способа пользовались этим методом для определения антипирина, но при этом столкнулись с рядом сложностей:
1. Неэффективностью разделения метаболитов антипирина в системе растворителей хлороформ:спирт.
2. Частой размытостью пятен.
3. Проявитель – пары йода – являются летучими и высокотоксичными соединениями.
4. Невоспроизводимостью результатов, стандартное отклонение (ошибка определения) выходило за пределы допустимого (2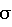 ).
Задачей заявляемого технического решения является разработка способа, позволяющего быстро, объективно и количественно оценить содержание антипирина в биологических объектах.
Техническим результатом предлагаемого способа является повышение точности и чувствительности определения содержания антипирина в биологических объектах и сокращение времени проведения анализа.
Технический результат достигается тем, что способ определения антипирина проводят путем взятия пробы, нанесения образца и стандартного раствора антипирина на силикагелевую пластину, хроматографирования в системе растворителей и определения содержания антипирина в исследуемом образце по площадям пятен пробы и стандарта.
Отличительными приемами заявляемого способа являются: нанесение пробы и стандарта на силикагелевую пластину марки “Сорбфил”; хроматографирование в течение 10 минут в системе растворителей вода:уксусная кислота, взятых в объемном соотношении 3:1; пластины с анализируемыми образцами в течение 2-3 минут выдерживают при температуре 50 ).
Задачей заявляемого технического решения является разработка способа, позволяющего быстро, объективно и количественно оценить содержание антипирина в биологических объектах.
Техническим результатом предлагаемого способа является повышение точности и чувствительности определения содержания антипирина в биологических объектах и сокращение времени проведения анализа.
Технический результат достигается тем, что способ определения антипирина проводят путем взятия пробы, нанесения образца и стандартного раствора антипирина на силикагелевую пластину, хроматографирования в системе растворителей и определения содержания антипирина в исследуемом образце по площадям пятен пробы и стандарта.
Отличительными приемами заявляемого способа являются: нанесение пробы и стандарта на силикагелевую пластину марки “Сорбфил”; хроматографирование в течение 10 минут в системе растворителей вода:уксусная кислота, взятых в объемном соотношении 3:1; пластины с анализируемыми образцами в течение 2-3 минут выдерживают при температуре 50 С; обработка реагентом, содержащим ароматический альдегид – реактив Эрлиха – в смеси с уксусной и фосфорной кислотой; повторное выдерживание анализируемой пластины при температуре 50 С; обработка реагентом, содержащим ароматический альдегид – реактив Эрлиха – в смеси с уксусной и фосфорной кислотой; повторное выдерживание анализируемой пластины при температуре 50 С в течение 2-3 минут.
Использование пластины марки “Сорбфил” дает возможность эффективно разделить анализируемые вещества – антипирин и его метаболиты, ускорить процесс хроматографирования; при этом стоимость анализа уменьшается в два раза по сравнению со способом-прототипом.
Использование для проведения элюирования дистиллированной воды, модифицированной концентрированной уксусной кислотой, позволяет упростить способ, сократить время проведения анализа и сделать его более экономичным.
Отличие способа также заключается и в том, что проявление антипирина проводят реагентом, представляющим собой реактив Эрлиха, растворенный в смеси уксусной и фосфорной кислот. Использование предложенного реагента позволяет получить устойчивое окрашивание пятен исследуемых веществ, которое не изменяется при длительном хранении.
Авторам заявляемого способа неизвестно и в доступной литературе не найдено использование подобного реагента для проведения анализа антипирина.
Все эти отличия позволяют сделать вывод о соответствии заявляемого технического решения критерию изобретения “новизна”.
Сравнение заявляемого технического решения не только с прототипом, но и другими техническими решениями в биохимии не позволило выявить в них признаки, отличающие заявленное решение не только от способа-прототипа, но и от других аналогичных технических решений.
Нами не найдена информация, в которой бы говорилось об определении антипирина приемами заявляемого способа.
Предлагаемый способ позволяет получить усматриваемый заявителем технический результат – повышение точности и чувствительности определения содержания антипирина в биологических объектах и сокращение времени проведения анализа.
Это позволяет сделать вывод о соответствии технического решения критерию “изобретательский уровень”.
Способ, составляющий заявляемое изобретение, предназначен для использования в медицине, а именно в биохимии. Возможность его осуществления подтверждена описанными в заявке приемами и средствами следовательно, предлагаемое решение соответствует критерию изобретения “промышленная применимость”.
Заявляемый способ осуществляют следующим образом.
Исследуемую биопробу параллельно со стандартными растворами антипирина наносят на пластину марки Сорбфил”. Далее пластину хроматографируют в системе растворителей вода:уксусная кислота при объемном соотношении 3:1 в течение 10 минут. После чего пластину выдерживают в течение 2-3 минут при температуре 50 С в течение 2-3 минут.
Использование пластины марки “Сорбфил” дает возможность эффективно разделить анализируемые вещества – антипирин и его метаболиты, ускорить процесс хроматографирования; при этом стоимость анализа уменьшается в два раза по сравнению со способом-прототипом.
Использование для проведения элюирования дистиллированной воды, модифицированной концентрированной уксусной кислотой, позволяет упростить способ, сократить время проведения анализа и сделать его более экономичным.
Отличие способа также заключается и в том, что проявление антипирина проводят реагентом, представляющим собой реактив Эрлиха, растворенный в смеси уксусной и фосфорной кислот. Использование предложенного реагента позволяет получить устойчивое окрашивание пятен исследуемых веществ, которое не изменяется при длительном хранении.
Авторам заявляемого способа неизвестно и в доступной литературе не найдено использование подобного реагента для проведения анализа антипирина.
Все эти отличия позволяют сделать вывод о соответствии заявляемого технического решения критерию изобретения “новизна”.
Сравнение заявляемого технического решения не только с прототипом, но и другими техническими решениями в биохимии не позволило выявить в них признаки, отличающие заявленное решение не только от способа-прототипа, но и от других аналогичных технических решений.
Нами не найдена информация, в которой бы говорилось об определении антипирина приемами заявляемого способа.
Предлагаемый способ позволяет получить усматриваемый заявителем технический результат – повышение точности и чувствительности определения содержания антипирина в биологических объектах и сокращение времени проведения анализа.
Это позволяет сделать вывод о соответствии технического решения критерию “изобретательский уровень”.
Способ, составляющий заявляемое изобретение, предназначен для использования в медицине, а именно в биохимии. Возможность его осуществления подтверждена описанными в заявке приемами и средствами следовательно, предлагаемое решение соответствует критерию изобретения “промышленная применимость”.
Заявляемый способ осуществляют следующим образом.
Исследуемую биопробу параллельно со стандартными растворами антипирина наносят на пластину марки Сорбфил”. Далее пластину хроматографируют в системе растворителей вода:уксусная кислота при объемном соотношении 3:1 в течение 10 минут. После чего пластину выдерживают в течение 2-3 минут при температуре 50 С, затем обрабатывают реагентом, содержащим ароматический альдегид в смеси уксусной и фосфорной кислот, после чего повторно выдерживают при температуре 50 С, затем обрабатывают реагентом, содержащим ароматический альдегид в смеси уксусной и фосфорной кислот, после чего повторно выдерживают при температуре 50 С в течение 2-3 минут. В результате проведенного анализа антипирин проявляется на пластинах в виде четких, красиво окрашенных розовых пятен.
Содержание антипирина рассчитывают по площадям пятен пробы и стандарта. Общее время анализа составляет не более 30 минут.
Предложенный способ поясняется примерами конкретного выполнения.
Пример 1.
Больной К., история болезни №43434, диагноз: атеросклероз сосудов головного мозга и коронарных артерий, ишемическая болезнь сердца, III функциональный класс, стенокардия напряжения и покоя. При поступлении в клинику больному была выполнена антипириновая проба. Концентрацию антипирина определяли методом, взятым за прототип, и предлагаемым способом. Определение по способу прототипу показало, что клиренс (Clir) антипирина составил 36,7 мл/мин, период полувыведения (Т 1/2) – 11,6 ч. Время, затраченное на проведение указанного анализа, составило 70 минут.
По предлагаемому способу: Clir – 33,8 мл/мин, Т 1/2 – 12,61 ч. Время, затраченное на проведение указанного анализа, составило 30 минут.
Эти же показатели у практически здоровых людей-доноров составили: Clir – 52,25 мл/мин, Т 1/2 – 8,53 ч.
На основании проведенных исследований установлено у больного К снижение клиренса антипирина на 35%, что свидетельствует о выраженном нарушении биотрансформационной функции печени.
Пример 2.
Больной О., история болезни №40153, диагноз: острый миелоидный лейкоз. При поступлении клиренс антипирина, определенный по предлагаемому способу, составил 42 мл/мин, Т 1/2 – 10,38 ч. Время, затраченное на проведение указанного анализа, составило 25 минут.
По способу-прототипу: Сlir – 40,5 мл/мин, Т 1/2 – 11 ч. Время, затраченное на проведение указанного анализа, составило 60 минут.
Эти же показатели у практически здоровых людей-доноров составили: Clir – 52,25 мл/мин, Т 1/2 – 8,53 ч.
Антипириновая проба позволила выявить нарушение метаболической функции печени по снижению клиренса антипирина на 19,6%, Т 1/2 на 21,6%, что можно оценить как не резко выраженное нарушение функции печени.
Пример 3.
Больная К., история болезни №23124, диагноз: хронический персистирующий гепатит средней тяжести.
Данные антипириновой пробы, проведенной по предлагаемому способу: Clir – 39,74 мл/мин, Т 1/2 – 9,09 ч.
Антипириновая проба позволила выявить резкое снижение биотрансформационной функции печени на основании снижения клиренса антипирина на 24%.
Пример 4.
Больная М., история болезни №56017, диагноз – железодефицитная анемия средней тяжести. Проведенный антипириновый тест позволил обнаружить умеренное нарушение биотрансформационной функции печени по результатам снижения клиренса антипирина и времени его полувыведения на 18,6% и 33,4% соответственно.
Всего было обследовано 25 доноров, 40 больных коронарным атеросклерозом и 18 пациентов с железодефицитной анемией и миелоидным лейкозом. Исследования проводили при поступлении в клинику и в процессе лечения. Полученные данные представлены в табл.1 и 2. С в течение 2-3 минут. В результате проведенного анализа антипирин проявляется на пластинах в виде четких, красиво окрашенных розовых пятен.
Содержание антипирина рассчитывают по площадям пятен пробы и стандарта. Общее время анализа составляет не более 30 минут.
Предложенный способ поясняется примерами конкретного выполнения.
Пример 1.
Больной К., история болезни №43434, диагноз: атеросклероз сосудов головного мозга и коронарных артерий, ишемическая болезнь сердца, III функциональный класс, стенокардия напряжения и покоя. При поступлении в клинику больному была выполнена антипириновая проба. Концентрацию антипирина определяли методом, взятым за прототип, и предлагаемым способом. Определение по способу прототипу показало, что клиренс (Clir) антипирина составил 36,7 мл/мин, период полувыведения (Т 1/2) – 11,6 ч. Время, затраченное на проведение указанного анализа, составило 70 минут.
По предлагаемому способу: Clir – 33,8 мл/мин, Т 1/2 – 12,61 ч. Время, затраченное на проведение указанного анализа, составило 30 минут.
Эти же показатели у практически здоровых людей-доноров составили: Clir – 52,25 мл/мин, Т 1/2 – 8,53 ч.
На основании проведенных исследований установлено у больного К снижение клиренса антипирина на 35%, что свидетельствует о выраженном нарушении биотрансформационной функции печени.
Пример 2.
Больной О., история болезни №40153, диагноз: острый миелоидный лейкоз. При поступлении клиренс антипирина, определенный по предлагаемому способу, составил 42 мл/мин, Т 1/2 – 10,38 ч. Время, затраченное на проведение указанного анализа, составило 25 минут.
По способу-прототипу: Сlir – 40,5 мл/мин, Т 1/2 – 11 ч. Время, затраченное на проведение указанного анализа, составило 60 минут.
Эти же показатели у практически здоровых людей-доноров составили: Clir – 52,25 мл/мин, Т 1/2 – 8,53 ч.
Антипириновая проба позволила выявить нарушение метаболической функции печени по снижению клиренса антипирина на 19,6%, Т 1/2 на 21,6%, что можно оценить как не резко выраженное нарушение функции печени.
Пример 3.
Больная К., история болезни №23124, диагноз: хронический персистирующий гепатит средней тяжести.
Данные антипириновой пробы, проведенной по предлагаемому способу: Clir – 39,74 мл/мин, Т 1/2 – 9,09 ч.
Антипириновая проба позволила выявить резкое снижение биотрансформационной функции печени на основании снижения клиренса антипирина на 24%.
Пример 4.
Больная М., история болезни №56017, диагноз – железодефицитная анемия средней тяжести. Проведенный антипириновый тест позволил обнаружить умеренное нарушение биотрансформационной функции печени по результатам снижения клиренса антипирина и времени его полувыведения на 18,6% и 33,4% соответственно.
Всего было обследовано 25 доноров, 40 больных коронарным атеросклерозом и 18 пациентов с железодефицитной анемией и миелоидным лейкозом. Исследования проводили при поступлении в клинику и в процессе лечения. Полученные данные представлены в табл.1 и 2.

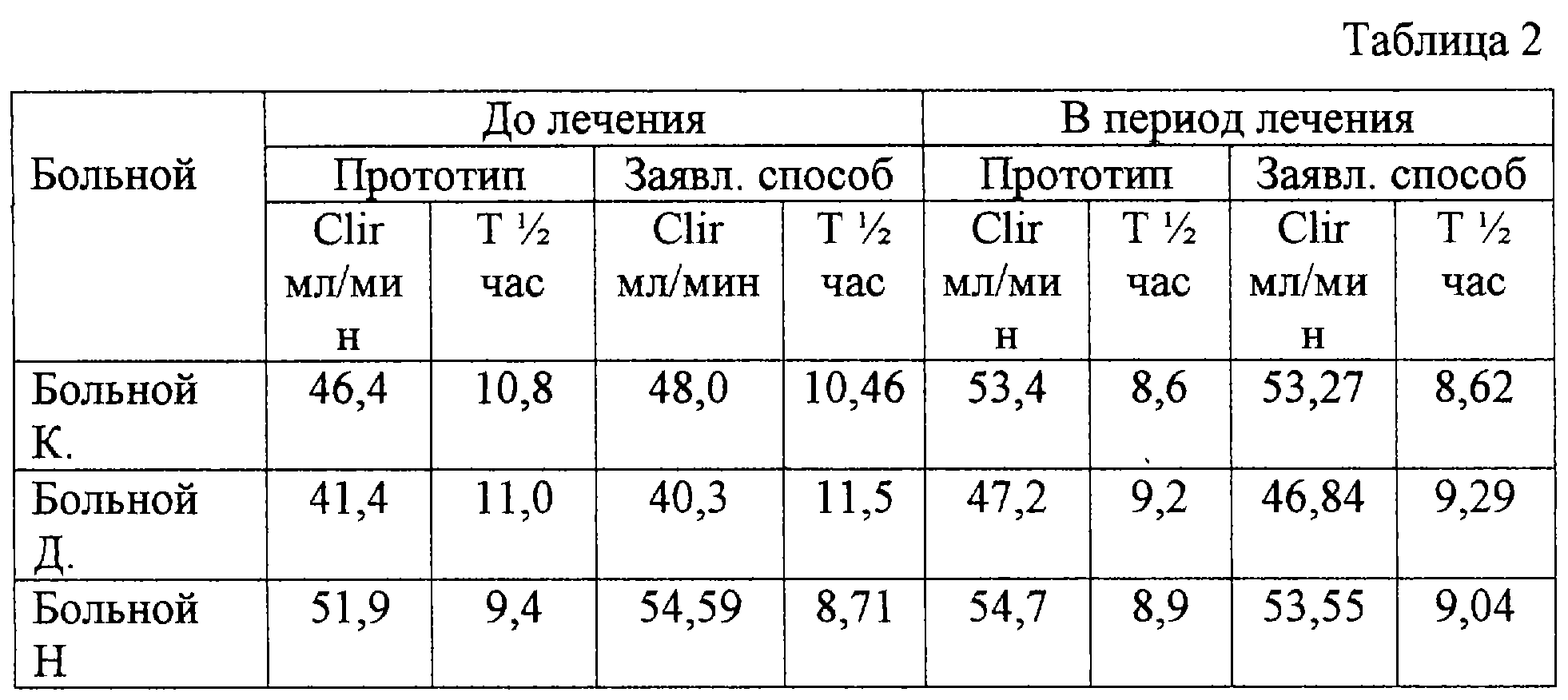 Таким образом, из данных, приведенных в табл.1, следует, что определение концентрации антипирина осуществимо как у практически здоровых людей, так и у больных с разными нозологическими заболеваниями. Табл.2 показывает, что под влиянием медикаментозной терапии показатели антипиринового теста изменяются в положительную сторону. Фармакокинетические параметры – клиренс антипирина и время полувыведения, определенные известным и предлагаемым способами, – близки по абсолютной величине, и разница между показателями не превышает 5%, т.е. находится в пределах ошибки метода.
Таким образом, заявляемый способ позволяет сократить время проведения анализа по сравнению с известными техническими решениями в 2-3 раза, исключает применение органических растворителей, основан на применении только водных растворов. Используемый для проявления антипирина реагент подлежит длительному хранению, в отличие от используемых в прототипе йода и ледяной уксусной кислоты, требующих ежедневного приготовления. Использованием проявляющего реагента предложенного состава достигается длительная и устойчивая окраска пятен антипирина. Немаловажным является и то, что способ основан на использовании дешевых и доступных реагентов.
Литература:
1. Новый метод оценки функционального состояния печени в клинике внутренних болезней и при диспансеризации некоторых контингентов населения: Метод, рекомендации. – М., 1990, с.25.
2. D. Mendelsohn and N.V. Levin. S. Afr. J. Med. Sci. 25, 13-18 (1960).
3. L.F. Prescott, K.K. Adjepon – Yamoah. E. Roberts. J. Pharm. Pharmacol. 25, 205-207 (1973).
5. RU 2140637, МКИ6 G 01 N 33/48, опубл. 27.10.1999 – прототип.
Таким образом, из данных, приведенных в табл.1, следует, что определение концентрации антипирина осуществимо как у практически здоровых людей, так и у больных с разными нозологическими заболеваниями. Табл.2 показывает, что под влиянием медикаментозной терапии показатели антипиринового теста изменяются в положительную сторону. Фармакокинетические параметры – клиренс антипирина и время полувыведения, определенные известным и предлагаемым способами, – близки по абсолютной величине, и разница между показателями не превышает 5%, т.е. находится в пределах ошибки метода.
Таким образом, заявляемый способ позволяет сократить время проведения анализа по сравнению с известными техническими решениями в 2-3 раза, исключает применение органических растворителей, основан на применении только водных растворов. Используемый для проявления антипирина реагент подлежит длительному хранению, в отличие от используемых в прототипе йода и ледяной уксусной кислоты, требующих ежедневного приготовления. Использованием проявляющего реагента предложенного состава достигается длительная и устойчивая окраска пятен антипирина. Немаловажным является и то, что способ основан на использовании дешевых и доступных реагентов.
Литература:
1. Новый метод оценки функционального состояния печени в клинике внутренних болезней и при диспансеризации некоторых контингентов населения: Метод, рекомендации. – М., 1990, с.25.
2. D. Mendelsohn and N.V. Levin. S. Afr. J. Med. Sci. 25, 13-18 (1960).
3. L.F. Prescott, K.K. Adjepon – Yamoah. E. Roberts. J. Pharm. Pharmacol. 25, 205-207 (1973).
5. RU 2140637, МКИ6 G 01 N 33/48, опубл. 27.10.1999 – прототип.
Формула изобретения Способ определения антипирина, включающий взятие пробы, нанесение образца и стандартного раствора антипирина на силикагелевую пластинку, хроматографирование в системе растворителей и определение содержания антипирина в исследуемом образце по площадям пятен пробы и стандарта, отличающийся тем, что пробу наносят на силикагелевую пластину марки Сорбфил, хроматографирование проводят в системе растворителей вода:уксусная кислота, взятых в объемном соотношении 3:1 в течение 10 мин, после чего выдерживают в течение 2-3 мин при температуре 50  С, обрабатывают реагентом, содержащим реактив Эрлиха в смеси с уксусной и фосфорной кислотой, после чего повторно выдерживают при температуре 50 С, обрабатывают реагентом, содержащим реактив Эрлиха в смеси с уксусной и фосфорной кислотой, после чего повторно выдерживают при температуре 50 С в течение 2-3 мин. С в течение 2-3 мин.
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 28.05.2004
Извещение опубликовано: 10.06.2006 БИ: 16/2006
|
||||||||||||||||||||||||||
