Патент на изобретение №2223946
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ L-ЛИЗИНА
(57) Реферат: Изобретение относится к способу получения L-лизина из лизинсодержащих растворов, включающий обработку рацемата L-винной кислотой с получением солей D- и L-лизина, удаления D-формы, разложение гидротартрата лизина методом электродиализа в электродиализаторе с чередующимися катионообменными и биполярными мембранами в интенсивном токовом режиме, перезаряжая L-лизин в катионную форму, при этом процесс электродиализа ведут при плотности электрического тока от 12 до 18 мА/см2, а освобождающийся из гидротартрата разделяющий агент направляют повторно на стадию разделения рацемата. Способ позволяет исключить использование для ионообменника концентрированных растворов кислот, разделяющий агент (L-винную кислоту) используют многократно, достигается высокий коэффициент разделения смеси от 950 до 1100. 3 з. п. ф-лы, 3 ил. Изобретение относится к выделению и очистке индивидуальных аминокислот из их смесей, в частности к получению L-лизина из рацемической смеси, и может быть использовано в различных отраслях производства, предпочтительно в пищевой, фармацевтической и медицинской промышленности. В настоящее время для выделения или очистки L-лизина от примесей все более частое применение находят электромембранные методы [1]. Так известен способ получения и очистки L-лизина от сопутствующих примесей электромембранно-сорбционным методом, который заключается в пропускании солянокислого раствора лизина через сульфокатионит КУ-2-8 в Н+-форме путем пропускания через ионообменник электрического тока [2]. Для этого ионообменник помещается в колонку прямоугольного сечения, двумя боковыми противоположными стенками которой являются катионитовые мембраны МК-40. С внешней стороны колонки, напротив мембран устанавливаются электроды, тем самым образуя катодную и анодную секции. В катодной секции находится дистиллированная вода, а в секцию, содержащую анод, помещается раствор серной кислоты. В результате анодной электродной реакции (разложение воды с выделением ионов водорода) происходит регенерация ионообменного слоя за счет замены ионов лизина катионами водорода. В параллельно протекающей катодной электродной реакции (разложение воды с выделением газообразного водорода и генерацией гидроксильных ионов) происходит десорбция аминокислоты из фазы ионообменника в раствор с образованием основного лизина. Главный недостаток этого способа заключается в ограниченном его использовании и промышленном применении, поскольку им может быть очищено только небольшое количество лизина, полученного методом микробиологического синтеза. (Микроорганизмы селективно синтезируют индивидуальный L-лизин на сахаросодержащих средах.) Однако таким образом невозможно организовать крупнотоннажное производство L-аминокислоты из-за высокой сложности и стоимости процесса. В промышленности лизин получают в любых количествах более дешевым методом химического синтеза с образованием его рацемической смеси из D- и L-равновесных форм, а поскольку D-форма лизина оказывает на живые организмы отрицательное воздействие, то ее необходимо отделять от L-формы. Однако задача разделения рацематов лизина достаточно сложна, а все известные ее решения недостаточно экономически эффективны или экологически нецелесообразны. Известен способ получения L-лизина из лизинсодержащего водно-метанолового раствора путем обработки рацемата лизина винной кислотой L-формы (L-BK) [3]. При взаимодействии рацемата лизина с L-BK в водно-метанольном растворе в зависимости от соотношения компонентов могут получаться кислые или нейтральные соли лизина с L-BK. Выделение кислой соли L-лизин-L-ВК происходит удовлетворительно количественно и качественно лишь при избытке L-лизина в исходной смеси, который создается за счет предварительного выделения D-лизина в виде нейтральной соли с L-BK. Из маточного раствора, полученного после отделения кристаллов соли 2D-лизин-L-ВК, выделяют кислую соль L-лизин-L-ВК путем добавления в него L-BK в количестве, необходимом для образования кислой соли. Соль L-лизин-L-BK обычно выделяется из 25-50%-ного водного раствора метилового спирта. Выделенные кристаллы промывают 50%-ным метиловым спиртом и сушат при температуре 60-70oС. Для получения L-лизина в свободном состоянии выделенные соли растворяют в воде и пропускают через ионообменные колонны с катионитом КУ-2-8 в H+-форме. Основная масса L-лизин-L-BK соли выделяется за 3 ч. Данный способ по технической сущности, достигаемому результату и решаемой задаче наиболее близок к предлагаемому изобретению и принят за прототип. Однако и этот способ не лишен недостатков, один из которых заключается в том, что в процессе его реализации необходимо осуществлять регенерацию слоя концентрированным раствором кислоты, при сбросе которого наносится вред окружающей среде, затрачиваются химические реагенты, а кроме того, способ достаточно сложен операционно. Задача по устранению отмеченных недостатков известного способа решена за счет создания оригинального способа выделения чистого L-лизина методом электродиализа, при котором используется интенсивный токовый режим (область нелинейной концентрационной поляризации). При этом полное выделение L-лизина происходит за счет его перезарядки в катионную форму и эффективной электромиграции через катионообменную мембрану. Технический результат – исключение использования для регенерации ионообменника концентрированных растворов кислот; упрощение способа достигается тем, что разложение гидротартрата лизина и выделение чистого L-лизина осуществляют методом электродиализа в электродиализаторе с чередующимися катионообменными и биполярными мембранами, производя перезарядку L-лизина в катионную форму, при этом процесс электродиализа ведут в интенсивном токовом режиме при плотности тока 12-18 мА/см2, а освобождающийся разделяющий агент повторно направляют на стадию разделения рацемата. В качестве разделяющего агента используют винную кислоту, а процесс в указанном режиме тока приводит к коэффициенту разделения смесей, изменяющемуся в диапазоне от 950 до 1100. Принципиальная схема реализации способа получения L-лизина методом электродиализа изображена на фиг.1. Для наглядности протекания техпроцесса получения L-лизина на фиг.1 действующие компоненты (вещества) обозначены общепринятыми символами: О2 – кислород, H2 – водород, Vin – винная кислота, Lys – лизин, ОН– и Н+ – ионы гидроксильной группы и водорода,  – анод и – анод и  – катод, катионообменная мембрана – К и биполярная мембрана – АК.
Способ осуществляется следующим образом.
Полученный химическим синтезом из циклогексанона высокой чистоты рацемат D- и L-форм лизина разделяют с помощью L-винной кислоты. Разделение основано на различной растворимости солей, получаемых при взаимодействии рацемата с L-винной кислотой. Соль D-лизина и винной кислоты наименее растворима. После ее отделения известным способом разрушение оставшейся соли L-лизина и L-винной кислоты осуществляют с помощью электродиализа.
В качестве разделяющего агента возможно использование камфорной кислоты, однако ее высокая стоимость, на порядок выше винной, делают ее применение в техпроцессе весьма проблематичным.
В электродиализатор с чередующимися катионообменными мембранами (К) и биполярными мембранами (АК), в частности МК-40 и МБ-3, которые образуют секции 1-7, подают: в четные секции 2, 4, 6 – тартрат L-лизина, а в нечетные 1, 3, 5, 7 – дистиллированную воду. Под действием градиента электрического потенциала ионы H+ и ОН–, генерируемые биполярными мембранами АК, переносятся в смежные секции, при этом находящийся в четных секциях 2, 4 и 6 лизин в форме однозарядного катиона перезаряжается по нижеуказанной схеме в двухзарядный катион: – катод, катионообменная мембрана – К и биполярная мембрана – АК.
Способ осуществляется следующим образом.
Полученный химическим синтезом из циклогексанона высокой чистоты рацемат D- и L-форм лизина разделяют с помощью L-винной кислоты. Разделение основано на различной растворимости солей, получаемых при взаимодействии рацемата с L-винной кислотой. Соль D-лизина и винной кислоты наименее растворима. После ее отделения известным способом разрушение оставшейся соли L-лизина и L-винной кислоты осуществляют с помощью электродиализа.
В качестве разделяющего агента возможно использование камфорной кислоты, однако ее высокая стоимость, на порядок выше винной, делают ее применение в техпроцессе весьма проблематичным.
В электродиализатор с чередующимися катионообменными мембранами (К) и биполярными мембранами (АК), в частности МК-40 и МБ-3, которые образуют секции 1-7, подают: в четные секции 2, 4, 6 – тартрат L-лизина, а в нечетные 1, 3, 5, 7 – дистиллированную воду. Под действием градиента электрического потенциала ионы H+ и ОН–, генерируемые биполярными мембранами АК, переносятся в смежные секции, при этом находящийся в четных секциях 2, 4 и 6 лизин в форме однозарядного катиона перезаряжается по нижеуказанной схеме в двухзарядный катион:+NH3-(CH2)4-CH(NH2)-COOH+H+–>+NH3-(CH2)4-CH(NH3 +)-COOH Двухзарядные катионы L-лизина переносятся через катионообменные мембраны К в нечетные секции 1, 3, 5 и 7, где взаимодействуют с гидроксильными ионами ОН–, образуя биполярные ионы основного лизина, т.е.: +NH3-(CH2)4-CH(NH3 +)-COOH+2OH––>+NH3-(CH2)4-CH(NH2)-COO–+2H2O Процесс электродиализа ведут при плотности тока 12-18 мА/см2 с концентрацией компонентов раствора 0,02-0,10 моль/л и с линейной скоростью, равной 0,1-0,3 см/с. Освобождающийся разделяющий агент – винная кислота из четных секций 2, 4 и 6 возвращается на разделение рацемической смеси лизина D- и L-форм лизина. Определяющим фактором для разделения лизина и винной кислоты является плотность электрического тока, что подтверждается полученными опытными результатами. От плотности тока зависят прежде всего концентрационный фактор (SF) и относительная конверсия (   ) лизина. На графике отражена зависимость концентрационного фактора (SF) от плотности электрического тока (i).
Фактор разделения лизина и винной кислоты представляет собой отношение концентраций компонентов в пермеате (perm) к отношению концентрации этих компонентов в ретентате (ret): ) лизина. На графике отражена зависимость концентрационного фактора (SF) от плотности электрического тока (i).
Фактор разделения лизина и винной кислоты представляет собой отношение концентраций компонентов в пермеате (perm) к отношению концентрации этих компонентов в ретентате (ret): где CLys и СVin – концентрации лизина и винной кислоты соответственно. В свою очередь концентрации компонентов в пермеате и ретентате по абсолютной величине определяются исходной концентрацией составляющих разделяемой смеси, однако их отношения зависят от плотности электрического тока. Из графика I (фиг.2) видно, что наибольшие значения фактора разделения исходных компонентов (SF=950-1100) достигаются при плотности тока от 12 до 18 мА/см2, при этом степень выделения L-лизина удовлетворяет требованиям техпроцесса. При значениях плотности тока менее 12 мА/см2 величина потока лизина через мембрану МК-40 будет значительно падать, а при плотности тока i<5 мА/см2 SF практически не будет изменяться и составляет менее 200 единиц. Использование значения плотности тока более 18 мА/см2 экономически нецелесообразно, т.к. приводит к проявлению побочных эффектов концентрационной поляризации, перегреву обрабатываемой среды и, как следствие, повышенному расходу электроэнергии. Плотность электрического тока оказывает значительное влияние и на относительную конверсию лизина. На графике II (фиг.3) показана зависимость относительной конверсии (   ) лизина от плотности электрического тока (i) при электродиализе. Относительная конверсия представляет собой отношение концентрации лизина, выделенного в виде целевого продукта (CLys)perm, к концентрации лизина, вступающего в процесс (СLys)0 [4], и выражается формулой: ) лизина от плотности электрического тока (i) при электродиализе. Относительная конверсия представляет собой отношение концентрации лизина, выделенного в виде целевого продукта (CLys)perm, к концентрации лизина, вступающего в процесс (СLys)0 [4], и выражается формулой: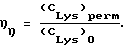 Из приведенного графика II следует, что максимальная степень выделения лизина из гидротартрата осуществляется также при значениях плотности тока (i) в пределах от 12 до 18 мА/см2. Дальнейшее увеличение плотности тока фактически не дает прироста конверсии свободного L-лизина, а приводит лишь к излишнему расходу электроэнергии. При выделении L-лизина из его гидротартрата методом электродиализа при высоких плотностях тока рН пермеата также следует выбирать оптимально, потому что сдвиг в щелочную среду приведет к снижению электромиграции за счет уменьшения количества катионов, а в более кислую обусловит конкурирующий транспорт ионов водорода. При технологических значениях плотности тока, равных 12-18 мА/см2, наиболее оптимальная величина рН раствора будет находиться в пределах 4,0-5,0. Линейная скорость потока от 0,1 до 0,3 см/с определяется технологической необходимостью, т. е. при скорости подачи раствора насосом менее 0,1 см/с будет мала производительность процесса, при скорости же более 0,3 см/с будет наблюдаться недостаточное выделение L-лизина из исходного раствора. Таким образом, при использовании интенсивного токового режима электродиализа происходит наиболее полное выделение L-лизина за счет его перезарядки в форму двухзарядных катионов и эффективной электромиграции через катионообменную мембрану. При этом гидротартрат-ионы полностью остаются в ретентате. Пермеат представляет собой индивидуальный раствор L-лизина, содержащий в результате проведения процесса в одну стадию 58% от исходного количества аминокислоты, введенной в систему. Проведение второй стадии позволяет увеличить относительную конверсию до 96%. Пример 1 Эксперимент по выделению L-лизина с разрушением его гидротартрата проводили в семикамерной электродиализной ячейке под действием градиента электрического потенциала с линейной скоростью потока 0,1 см/с при плотности тока 12 мА/см2 в непрерывном режиме. В секции 2, 4, 6 насосом подают раствор гидротартрата L-лизина, а в секции 1, 3, 5, 7 – дистиллированную воду. Рабочая площадь мембран МК-40 и МБ-3 составляла 20 см2. Концентрация исходного раствора по лизину и по гидротартрат-ионам – 0,025 моль/л. Поток лизина через катионообменную мембрану в данных условиях процесса составляет 2,6  10-8 моль/см2 10-8 моль/см2 с в отличие от условий линейной концентрационной поляризации, когда его величина практически на порядок меньше. Фактор разделения лизина и винной кислоты имел величину 950, при этом относительная конверсия лизина составила 0,54 (54%). Процесс позволяет получать непрерывно на выходе из нечетных секций аппарата содержание L-лизина 1,97 г/л, а оставшуюся винную кислоту из четных секций направить на повторное использование.
Пример 2 с в отличие от условий линейной концентрационной поляризации, когда его величина практически на порядок меньше. Фактор разделения лизина и винной кислоты имел величину 950, при этом относительная конверсия лизина составила 0,54 (54%). Процесс позволяет получать непрерывно на выходе из нечетных секций аппарата содержание L-лизина 1,97 г/л, а оставшуюся винную кислоту из четных секций направить на повторное использование.
Пример 2Процесс проводят как в примере 1, но электродиализное разрушение гидротартрата лизина осуществляют при плотности тока 15 мА/см2 с линейной скоростью потока 0,3 см/с. По данным содержания L-лизина и L-винной кислоты в пермеате и ретентате был рассчитан фактор разделения SF, который имеет значение 1080. Рассчитана также относительная конверсия лизина, составившая 58% при осуществлении процесса электродиализа в одну ступень. Такие условия дают возможность в непрерывном режиме получать целевой раствор L-лизина с концентрацией 2,11 г/л. Величина   = 96% достигается при проведении электромембранного разделения в две ступени.
Пример 3 = 96% достигается при проведении электромембранного разделения в две ступени.
Пример 3Процесс проводят так же, как и в примере 1, но при плотности тока 18 мА/см2. Фактор разделения SF L-лизина и L-винной кислоты увеличивается совсем незначительно и составляет 1100, однако при данной плотности тока уже зафиксирован ощутимый разогрев в секциях электродиализатора (  Т=15oС). В то же время относительная конверсия остается на том же уровне, что и при плотности тока 15 мА/см2.
На выходе из нечетных секций получено 2,15 г/л L-лизина.
Таким образом, используя предложенный способ получения L-лизина, можно несложно реализуемым технологическим процессом выпускать промышленным путем в достаточно больших объемах L-лизин высокого качества из лизинсодержащих растворов с выходом до 96%.
Источники информации Т=15oС). В то же время относительная конверсия остается на том же уровне, что и при плотности тока 15 мА/см2.
На выходе из нечетных секций получено 2,15 г/л L-лизина.
Таким образом, используя предложенный способ получения L-лизина, можно несложно реализуемым технологическим процессом выпускать промышленным путем в достаточно больших объемах L-лизин высокого качества из лизинсодержащих растворов с выходом до 96%.
Источники информации1. Патент США 6110342, В 01 D 61/44, 29.08.2002 г. “Процесс получения гидрохлорида аминокислоты и щелочи электродиализом и разложением воды”. 2. Патент РФ 2163905, С 07 С 229/02, 10.03.2001 г. “Способ очистки L-лизина от сопутствующих примесей электромембранно-сорбционным методом”. 3. Московец О.Ф., Эсливанова Г.А. Разделение рацемата лизина на оптические изомеры через соли с L-винной кислотой. – В сб.: Разработка химических способов получения аминокислот. Л.: ГИПХ, 1984 г., с.45, 46 (прототип). 4. Международная терминология по мембранам и мембранным процессам. Рекомендации Международного Союза по теоретической и прикладной химии (IUPAC, 1996). Формула изобретения 1. Способ получения L-лизина из лизинсодержащих растворов, включающий обработку рацемата разделяющим агентом с получением солей лизина D- и L-форм, удаление D-формы, разложение гидротартрата лизина и выделение чистого L-лизина, отличающийся тем, что разложение гидротартрата лизина осуществляют методом электродиализа в электродиализаторе с чередующимися катионообменными и биполярными мембранами в интенсивном токовом режиме, перезаряжая L-лизин в катионную форму, при этом процесс электродиализа ведут при плотности электрического тока от 12 до 18 м А/см2, а освобождающийся из гидротартрата разделяющий агент направляют повторно на стадию разделения рацемата. 2. Способ по п.1, отличающийся тем, что в качестве разделяющего агента используют L-винную кислоту. 3. Способ по п.1, отличающийся тем, что процесс электродиализа проводят в режиме, приводящем к величине коэффициента разделения смеси, изменяющемся в диапазоне 950-1100. 4. Способ по п.1, отличающийся тем, что рН исходного раствора устанавливается в пределах 4-5. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 18.10.2004
Извещение опубликовано: 20.05.2006 БИ: 14/2006
|
||||||||||||||||||||||||||
