Патент на изобретение №2220910
|
||||||||||||||||||||||||||
(54) СМЕШАННЫЙ ФЕРРАТ (YI) КАЛИЯ-НАТРИЯ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ
(57) Реферат: Изобретение относится к области неорганической химии, конкретно к синтезу ферратов щелочных металлов. Смешанный феррат (VI) калия-натрия, отвечающий формуле K3Na(FeО4)2, получен прибавлением 30-45%-ного раствора гидроксида калия к равному объему 30-45%-ного раствора гидроксида натрия, который содержит 0,1-0,3 моль/л феррат (VI) иона. Новое соединение обладает свойствами мощного и селективного окислителя и может быть использовано, например, в производстве химических источников тока, при очистке сточных вод, в органическом синтезе и других областях. 2 с.п.ф-лы. Изобретение относится к области неорганической химии, конкретно к синтезу ферратов щелочных металлов, и может найти применение в различных отраслях промышленности, где используются мощные и селективные окислители. Общим методом синтеза ферратов (VI) щелочных металлов является окисление газообразным хлором оксопроизводных железа (III) в концентрированной щелочи или, альтернативно, окисление порошкообразных оксидов железа или металлического железа оксидами или нитратами щелочных металлов (Ф. Коттон, Дж. Уилкинсон. Основы неорганической химии. – М.: Мир, 1979, с. 473). Известен, кроме того, смешанный феррат калия-стронция, осаждающийся из раствора феррата калия при добавлении хлорида стронция (S. Ogasawara, М. Таkаnо and Y. Bando, Bull. hist. Chem. Res. Kyoto Univ. (1988), vol. 66, p. 64). В литературе, однако, отсутствует упоминание о смешанных ферратах, содержащих только катионы щелочных металлов. Задачей настоящего изобретения является расширение арсенала существующих ферратов (VI) щелочных металлов, обладающих полезными свойствами в качестве окислителей. Поставленная задача решена благодаря получению смешанного феррата (VI) калия-натрия, имеющего химическую брутто-формулу K3Na(FeO4)2, путем прибавления 30-45%-ного раствора гидроксида калия к равному объему 30-45% раствора гидроксида натрия, содержащего 0,1-0,3 моль/л феррат (VI)-иона (FeO4 2--иoнa), с последующим отделением выпавшего осадка известным образом, например фильтрованием или центрифугированием, промыванием его спиртом и эфиром и высушиванием в вакууме. Приведенные выше величины концентрации и объемные соотношения не являются произвольными – их выбор продиктован тем обстоятельством, что при выходе за указанные выше пределы образуются окрашенные продукты неопределенного состава, по-видимому, относящиеся к классу бертолидов (соединений переменного состава). Напротив, смешанный феррат (VI) калия-натрия, K3Na(FeO4)2, получаемый в виде кристаллического вещества темно-бордового цвета, является истинным дальтонидом – индивидуальным химическим соединением, а не смесью солей или двойной солью, и имеет кристаллическую решетку, построенную, согласно данным рентгеноструктурного анализа, по типу глассерита с гексагональной сингонией и параметрами элементарной ячейки а=5,827 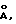 с=7,541 с=7,541 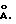 Изучение вещества методом мессбауэровской спектроскопии свидетельствует о том, что железо в полученном соединении находится в степени окисления +6, поскольку его спектр при комнатной температуре представляет собой дублет с изомерным сдвигом относительно альфа-железа  =-0,85 =-0,85 0,01 мм 0,01 мм с-1, квадрупольным расщеплением с-1, квадрупольным расщеплением  =0,21 =0,21 0,01 мм 0,01 мм с-1 и шириной линий поглощения на половине высоты Г=0,23 с-1 и шириной линий поглощения на половине высоты Г=0,23 0,01 мм 0,01 мм с-1.
Полученный смешанный феррат калия-натрия проявляет свойства сильного окислителя, превосходящего в этом отношении хроматы и перманганаты, и может быть использован в процессах очистки воды, в том числе сточных вод, в качестве селективного окислителя в органическом синтезе, получении химических источников тока.
К достоинствам полученного вещества можно отнести его меньшую токсичность по сравнению с ферратом калия, поскольку ион Na+ в 10 раз менее токсичен, чем ион К+, а в К3Nа(FеO4)2 четвертая часть всех ионов калия замещена ионами натрия (З. Франке. Химия отравляющих веществ. – М.: Химия, 1973. – Т. 1. – С. 411). Кроме того, плотность нового вещества, по меньшей мере, в 1,4 раза больше, чем у любого из известных к настоящему времени ферратов (VI) щелочных металлов, что представляет несомненное достоинство с точки зрения фасовки и транспортировки этого вещества, поскольку при этом требуется тара меньшего объема.
Детально изобретение иллюстрируется следующими примерами его осуществления.
Пример 1.
В трехгорлую круглодонную колбу емкостью 2500 мл, снабженную мешалкой, термометром и капельной воронкой, поместили 1000 мл 40% раствора едкого натра, содержащего 150 г феррата (VI) натрия Na2FeO4, и при интенсивном перемешивании и охлаждении колбы льдом в течение 15 минут из капельной воронки прибавили 1000 мл 40% раствора едкого кали. После введения всего количества КОН перемешивание продолжили еще 30 минут, затем полученную суспензию перенесли на воронку Бюхнера, собранные на фильтре темно-бордовые кристаллы промыли спиртом и эфиром и высушили в вакууме над твердым КОН. Выход 163 г (95%).
Данные элементного анализа (в скобках указаны вычисленные значения): с-1.
Полученный смешанный феррат калия-натрия проявляет свойства сильного окислителя, превосходящего в этом отношении хроматы и перманганаты, и может быть использован в процессах очистки воды, в том числе сточных вод, в качестве селективного окислителя в органическом синтезе, получении химических источников тока.
К достоинствам полученного вещества можно отнести его меньшую токсичность по сравнению с ферратом калия, поскольку ион Na+ в 10 раз менее токсичен, чем ион К+, а в К3Nа(FеO4)2 четвертая часть всех ионов калия замещена ионами натрия (З. Франке. Химия отравляющих веществ. – М.: Химия, 1973. – Т. 1. – С. 411). Кроме того, плотность нового вещества, по меньшей мере, в 1,4 раза больше, чем у любого из известных к настоящему времени ферратов (VI) щелочных металлов, что представляет несомненное достоинство с точки зрения фасовки и транспортировки этого вещества, поскольку при этом требуется тара меньшего объема.
Детально изобретение иллюстрируется следующими примерами его осуществления.
Пример 1.
В трехгорлую круглодонную колбу емкостью 2500 мл, снабженную мешалкой, термометром и капельной воронкой, поместили 1000 мл 40% раствора едкого натра, содержащего 150 г феррата (VI) натрия Na2FeO4, и при интенсивном перемешивании и охлаждении колбы льдом в течение 15 минут из капельной воронки прибавили 1000 мл 40% раствора едкого кали. После введения всего количества КОН перемешивание продолжили еще 30 минут, затем полученную суспензию перенесли на воронку Бюхнера, собранные на фильтре темно-бордовые кристаллы промыли спиртом и эфиром и высушили в вакууме над твердым КОН. Выход 163 г (95%).
Данные элементного анализа (в скобках указаны вычисленные значения):К 30,7% (30,9%) Na 6,1% (6,1%) Fe 29,8% (29,3%) Пример 2 (использование смешанного феррата калия-натрия в качестве компонента электролита в химическом источнике тока). В пасте для формования электродов стандартной феррат-литиевой щелочной батареи обычно используемый феррат (VI) калия заменили равным весовым количеством феррата (VI) калия-натрия, полученного согласно примеру 1. Емкость батареи возросла с 18 до 24 пикофарад, т.е. на треть. Пример 3 (использование смешанного феррата калия-натрия для очистки воды). К 1 литру водного раствора, имитирующего сточные воды в процессе получения золота цианидным методом и содержавшего 0,9 ммоль/л цианид-иона, добавили 0,2 л раствора феррата калия с концентрацией 10 ммоль/л. После перемешивания раствора в течение 3 минут качественные реакции на цианид-ион дали отрицательный результат (количественное превращение высокотоксичного цианида в относительно безопасный цианат-ион OCN). Формула изобретения 1. Смешанный феррат (VI) калия-натрия формулы K3Na(FeО4)2. 2. Способ получения смешанного феррата калия-натрия по п.1, отличающийся тем, что к 35-40%-ному водному раствору гидроксида натрия, содержащего 0,1-0,3 моль/л феррат-иона (FeО2-4), прибавляют равный объем водного 35-40%-ного раствора гидроксида калия, выпавшие кристаллы отделяют известным способом, последовательно промывают спиртом и эфиром и сушат. MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 01.02.2004
Извещение опубликовано: 27.08.2005 БИ: 24/2005
NF4A Восстановление действия патента Российской Федерации на изобретение
Извещение опубликовано: 20.03.2006 БИ: 08/2006
|
||||||||||||||||||||||||||
