Патент на изобретение №2217145
|
||||||||||||||||||||||||||
(54) 2-ГЕТЕРОАРИЛАЛКЕНИЛПРОИЗВОДНЫЕ ЦИКЛОПЕНТАНГЕПТАН(ЕН)ОВОЙ КИСЛОТЫ
(57) Реферат: Изобретение относится к области медицины и органической химии и касается новых производных простагландинов F-типа, используемых в качестве глазных гипотензивных средств, а также к способу лечения глаукомы с их помощью, офтальмологическим растворам и наборам, включающим указанные растворы. Новые простагландины обладают существенно более высокой активностью, чем известные соединения. 4 с. и 20 з. п. ф-лы, 1 табл. , 5 ил. Таблицыр Формула изобретения 1. 2-Гетероарилалкенилпроизводные циклопентан(ен)овой кислоты, представленные общей формулой I 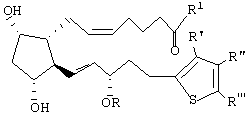 где R представляет собой водород или низший алкил;
R1 представляет собой гидрокси, низший алкокси или амидогруппу;
R’, R” и R”’ независимо представляют собой водород, хлор, бром или низший алкил.
2. Соединение по п.1, где по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
3. Соединение по п.1, где по меньшей мере два из R’, R” и R”’ представляют собой бром.
4. Соединение по п.1, где по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
5. Соединение по п.1, где по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
6. Соединение по п.1, где указанное соединение выбрано из группы, включающей:
7-[3
где R представляет собой водород или низший алкил;
R1 представляет собой гидрокси, низший алкокси или амидогруппу;
R’, R” и R”’ независимо представляют собой водород, хлор, бром или низший алкил.
2. Соединение по п.1, где по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
3. Соединение по п.1, где по меньшей мере два из R’, R” и R”’ представляют собой бром.
4. Соединение по п.1, где по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
5. Соединение по п.1, где по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
6. Соединение по п.1, где указанное соединение выбрано из группы, включающей:
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
7. Способ лечения глаукомы, который включает введение млекопитающему, страдающему глаукомой, терапевтически эффективного количества соединения формулы I по п.1 или его фармацевтически приемлемой соли.
8. Способ по п.7, где в указанном соединении по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
9. Способ по п.7, где в указанном соединении по меньшей мере два из R’, R” и R”’ представляют собой бром.
10. Способ по п.7, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
11. Способ по п.7, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
12. Способ по п.7, где указанное соединение выбрано из группы, включающей:
7-[3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
7. Способ лечения глаукомы, который включает введение млекопитающему, страдающему глаукомой, терапевтически эффективного количества соединения формулы I по п.1 или его фармацевтически приемлемой соли.
8. Способ по п.7, где в указанном соединении по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
9. Способ по п.7, где в указанном соединении по меньшей мере два из R’, R” и R”’ представляют собой бром.
10. Способ по п.7, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
11. Способ по п.7, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
12. Способ по п.7, где указанное соединение выбрано из группы, включающей:
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 , 5 , 5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
13. Офтальмологический раствор, включающий терапевтически эффективное количество соединения формулы I по п.1 или его фармацевтически приемлемой соли в смеси с нетоксичным офтальмологически приемлемым жидким носителем, расфасованный в емкость, подходящую для дозированного применения.
14. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
15. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере два из R’, R” и R”’ представляют собой бром.
16. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
17. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
18. Офтальмологический раствор по п.13, где указанное соединение выбрано из группы, включающей:
7-[3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
13. Офтальмологический раствор, включающий терапевтически эффективное количество соединения формулы I по п.1 или его фармацевтически приемлемой соли в смеси с нетоксичным офтальмологически приемлемым жидким носителем, расфасованный в емкость, подходящую для дозированного применения.
14. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
15. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере два из R’, R” и R”’ представляют собой бром.
16. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
17. Офтальмологический раствор по п.13, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
18. Офтальмологический раствор по п.13, где указанное соединение выбрано из группы, включающей:
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
19. Фармацевтический продукт для лечения глаукомы, включающий контейнер, приспособленный для высвобождения содержимого указанного контейнера в дозированной форме, и офтальмологический раствор в указанном контейнере, включающий соединение формулы I по п.1 или его фармацевтически приемлемую соль в смеси с нетоксичным офтальмологически приемлемым жидким носителем.
20. Продукт по п.19, где в указанном соединении по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
21. Продукт по п.19, где в указанном соединении по меньшей мере два из R’, R” и R”’ представляют собой бром.
22. Продукт по п.19, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
23. Продукт по п.19, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
24. Продукт по п.19, где указанное соединение выбрано из группы, включающей:
7-[3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
19. Фармацевтический продукт для лечения глаукомы, включающий контейнер, приспособленный для высвобождения содержимого указанного контейнера в дозированной форме, и офтальмологический раствор в указанном контейнере, включающий соединение формулы I по п.1 или его фармацевтически приемлемую соль в смеси с нетоксичным офтальмологически приемлемым жидким носителем.
20. Продукт по п.19, где в указанном соединении по меньшей мере один из R’, R” и R”’ выбран из группы, включающей хлор, бром и метил.
21. Продукт по п.19, где в указанном соединении по меньшей мере два из R’, R” и R”’ представляют собой бром.
22. Продукт по п.19, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой хлор и по меньшей мере один из R’, R” и R”’ представляет собой метил.
23. Продукт по п.19, где в указанном соединении по меньшей мере один из R’, R” и R”’ представляет собой бром и по меньшей мере один из R’, R” и R”’ представляет собой метил.
24. Продукт по п.19, где указанное соединение выбрано из группы, включающей:
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(2,4-дибром)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 -гидрокси-5-(5-(3-хлор-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту;
амид 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
изопропиловый эфир 7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 -гидрокси-5-(5-(3-бром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновой кислоты;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z гептеновую кислоту;
7-[3 -метокси-5-(5-(2-бром-3-метил)тиенил)-1E-пентенил)циклопентил]-5Z гептеновую кислоту;
7-[3 ,5 ,5 -дигидрокси-2-(3 -дигидрокси-2-(3 -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту. -гидрокси-5-(5-(3,4-дибром-2-метил)тиенил)-1E-пентенил)циклопентил]-5Z-гептеновую кислоту.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 18.11.2008
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
