Патент на изобретение №2215747
|
||||||||||||||||||||||||||
(54) АГОНИСТЫ АПОЛИПОПРОТЕИНА А-I И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДИСЛИПИДЕМИЕЙ
(57) Реферат: Изобретение относится к агонисту АроА-I, включающему пептид или пептидный аналог, содержащий от 15 до 29 аминокислотных остатков, который образует амфипатическую  -спираль в присутствии липидов и который характеризуется следующей формулой: Z1-X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20-X21-X22-X23-Z2, -спираль в присутствии липидов и который характеризуется следующей формулой: Z1-X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20-X21-X22-X23-Z2,или его фармацевтически приемлемая соль, значения радикалов см. формулу изобретения. Соединения по изобретению обладают высокой агонистической активностью в отношении аполипопротеина А-I и могут использоваться для лечения заболеваний, связанных с дислипопротеинемией, включая гиперхолестеринемию, сердечно-сосудистые заболевания, атеросклероз, рестеноз и септический шок. Описаны также мультимерный агонист АроА-I, комплекс агониста АроА-I и липида, фармацевтические композиции, включающие соединения по изобретению, а также способ лечения с помощью агонистов АроА-I. 14 с. и 48 з.п. ф-лы, 19 табл., 30 ил. Текст описания в факисимильном виде (см. графическую часть). Формула изобретения 1. Агонист АроА-I, включающий: (i) пептид или пептидный аналог, содержащий от 15 до 29 аминокислотных остатков, который образует амфипатическую  -спираль в присутствие липидов и который характеризуется следующей формулой (I): -спираль в присутствие липидов и который характеризуется следующей формулой (I):Z1-X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20Х21-Х22-Х23-Z2, или его фармацевтически приемлемая соль, где X1 представлен пролином (Р), аланином (А), глицином (G), глутамином (Q), аспарагином (N), аспарагиновой кислотой (D) или D-пролином (р); Х2 представлен алифатической аминокислотой; Х3 представлен лейцином (L) или фенилаланином (F); Х4 представлен кислой аминокислотой; Х5 представлен лейцином (L) или фенилаланином (F); Х6 представлен лейцином (L) или фенилаланином (F); Х7 представлен гидрофильной аминокислотой; X8 представлен кислой или основной аминокислотой; Х9 представлен лейцином (L) или глицином (G); Х10 представлен лейцином (L), триптофаном (W) или глицином (G) Х11 представлен гидрофильной аминокислотой; X12 представлен гидрофильной аминокислотой; Х13 представлен глицином (G) или алифатической аминокислотой; Х14 представлен лейцином (L), триптофаном (W), глицином, (G) или Nal; Х15 представлен гидрофильной аминокислотой; Х16 представлен гидрофобной аминокислотой; Х17 представлен гидрофобной аминокислотой; X18 представлен основной аминокислотой, глутамином (Q) или аспарагином (N); X19 представлен основной аминокислотой, глутамином (Q) или аспарагином (N); Х20 представлен основной аминокислотой; X21 представлен алифатической аминокислотой; Х22 представлен основной аминокислотой; Х23 отсутствует или представлен основной аминокислотой; Z1 представлен H2N- или RC(O)NH-; Z2 представлен -C(O)NRR, -C(O)OR, или -С(O)ОН, или соответствующей солью; каждый R независимо друг от друга представлен -Н, С1-6-алкилом, С1-6-алкенилом, С1-6-алкинилом, С5-20-арилом, С6-26-алкарилом, 5-20-атомным гетероарилом, 6-26-атомным алкгетероарилом или 1-7-аминокислотным пептидом или пептидным аналогом; каждый знак “-” между остатками Хn независимо друг от друга обозначает амидную связь, замещенную амидную связь, изостер амида или миметик амида; или (ii) делетированную форму формулы (I), в которой по крайней мере одна и вплоть до восьми остатков из X1, Х2, Х3, Х4, Х5, Х6, Х7, Х8, X9, Х10, Х11, X12, X13, X14, X15, X16, X17, X18, X19, Х20, Х21 и Х22 делетированы; или (iii) измененную форму формулы (I), в которой по крайней мере одна и вплоть до восьми остатков из 1, Х2, Х3, Х4, Х5, Х6, Х7, X8, X9, Х10, Х11, Х12, X13, X14, Х15, X16, X17, X18, X19, Х20, Х21, Х22 и Х23 по консервативному типу заменены на другие аминокислотные остатки. 2. Агонист АроА-I по п. 1, который проявляет по крайней мере 38%-ную активность по активации фермента LCAT по сравнению с АроА-I человека. 3. Агонист АроА-I по п. 1, который является измененной формой формулы (I). 4. Агонист АроА-I по п. 3, в составе которого гидрофобные остатки зафиксированы в соответствии с формулой (I), а по крайней мере один нефиксированный остаток заменен по консервативному типу на другой аминокислотный остаток. 5. Агонист АроА-I по п. 4, в котором: X1 представлен пролином (Р), D-пролином (р), глицином (G) или аланином (А); Х2 представлен аланином (А), лейцином (L) или валином (V); Х3 представлен лейцином (L) или фенилаланином (F); Х5 представлен лейцином (L) или фенилаланином (F); Х6 представлен лейцином (L) или фенилаланином (F’); X9 представлен лейцином (L) или глицином (G); Х10 представлен лейцином (L), триптофаном (W) или глицином (G); X13 представлен лейцином (L), глицином (G) или Aib; Х14 представлен лейцином, Nal, триптофаном (W) или глицином (G); Х16 представлен аланином (А), Nal, триптофаном (W), глицином (G), лейцином (L) или фенилаланином (F); Х17 представлен лейцином (L), глицином (G) или Nal; X21 представлен лейцином (L) и по крайней мере один из остатков Х4, Х7, Х8, Х11, X12, X15, X18, X19, Х20, Х22 и Х23 заменен по консервативному типу на другой аминокислотный остаток. 6. Агонист АроА-I по п. 3, в котором гидрофильные остатки зафиксированы в соответствии с формулой (I), а по крайней мере один нефиксированный остаток заменен по консервативному типу на другой аминокислотный остаток. 7. Агонист АроА-I по п. 6, в котором Х4 представлен аспарагиновой кислотой (D) или глутаминовой кислотой (Е); Х7 представлен лизином (К), аргинином (R) или орнитином; X8 представлен аспарагиновой кислотой (D) или глутаминовой кислотой (Е); Х11 представлен аспарагином (N) или глутамином (Q); Х12 представлен глутаминовой кислотой (Е) или аспарагиновой кислотой (D); Х15 представлен аспарагиновой кислотой (D) или глутаминовой кислотой (Е); X18 представлен глутамином (Q), аспарагином (N), лизином (К) или орнитином; X19 представлен глутамином (Q), аспарагином (N), лизином (К) или орнитином; Х20 представлен лизином (К) или орнитином; Х22 представлен лизином (К) или орнитином; Х23 отсутствует или представлен лизином (К) и по крайней мере один из остатков X1, Х2, Х3, Х5, Х6, Х9, Х10, X13, X14, X16, X17 и Х21 заменен по консервативному типу на другой аминокислотный остаток. 8. Агонист АроА-I по п. 7, в составе которого Х3 представлен лейцином (L) или фенилаланином (F), Х6 представлен фенилаланином (F), Х9 представлен лейцином (L) или глицином (G), Х10 представлен лейцином (L), или триптофаном (W), или глицином (G) и по крайней мере один из остатков X1, Х2, Х5, Х13, Х14, Х16, X17 и X21 заменен по консервативному типу на другой аминокислотный остаток. 9. Агонист АроА-I по п. 5 или 7, в составе которого заменяющий остаток классифицируется в ту же подгруппу, что и заменяемый остаток. 10. Агонист АроА-I по п. 1, являющийся делегированной формой формулы (I). 11. Агонист АроА-I по п. 10, в составе которого один виток спирали пептида или пептидного аналога делетирован. 12. Агонист АроА-I по п. 1, являющийся состоящим из 22-23 аминокислот пептидом или пептидным аналогом формулы (I). 13. Агонист АроА-I по п. 12, в составе которого знак “-” между остатками обозначает группу -C(O)NH-, Z1 представлен H2N-, и Z2 представлен -С(O)ОН или его солью. 14. Агонист АроА-I по п. 13, в составе которого Х1 представлен пролином (Р), аланином (А), глицином (G), аспарагином (N), глутамином (Q), аспарагиновой кислотой (D) или D-пролином (р); Х2 представлен аланином (А), валином (V) или лейцином (L); X3 представлен лейцином (L) или фенилаланином (F); Х4 представлен аспарагиновой кислотой (D) или глутаминовой кислотой (Е); X5 представлен лейцином (L) или фенилаланином (F); Х6 представлен лейцином (L) или фенилаланином (F); Х7 представлен лизином (К), аргинином (R) или орнитином; X8 представлен аспарагиновой кислотой (D) или глутаминовой кислотой (Е); Х9 представлен лейцином (L) или глицином (G); X10 представлен лейцином (L), триптофаном (W) или глицином (G); Х11 представлен аспарагином (N) или глутамином (Q); X12 представлен глутаминовой кислотой (Е) или аспарагиной кислотой (D); Х13 представлен глицином (G), лейцином (L) или Aib; Х14 представлен лейцином (L), Nal, триптофаном (W) или глицином (G); X15 представлен аспарагиновой кислотой (D) или глутаминовой кислотой (Е); Х16 представлен аланином (А), Nal, триптофаном (W), лейцином (L), фенилаланином (F) или глицином (G); Х17 представлен глицином (G), лейцином (L) или Nal; X18 представлен глутамином (Q), аспарагином (N), лизином (К) или орнитином; Х19 представлен глутамином (Q), аспарагином (N), лизином (К) или орнитином; Х20 представлен лизином (К) или орнитином; Х21 представлен лейцином (L); Х22 представлен лизином (К) или орнитином и Х23 отсутствует или представлен лизином (К). 15. Агонист АроА-I по п. 14, в составе которого аминокислота Х23 отсутствует. 16. Агонист АроА-I по п. 13 или 14, в составе которого один из остатков X18 или X19 представлен глутамином (Q) или аспарагином (N), а при этом другой остаток X18 или X19 представлен лизином (К) или орнитином. 17. Агонист АроА-I по п. 14, в составе которого каждый из остатков Х9, Х10, Х13, X14, Х15 и X17 не является глицином (G). 18. Агонист АроА-I по п. 14, в составе которого один из остатков Х9, Х10, Х13, X14, X15 и X17 представлен глицином (G), а остальные не являются глицином (G). 19. Агонист АроА-I по п. 1, который выбирают из группы, включающей: пептид 1 PVLDLFRELLNELLEZLKQKLK (SEQIDN01); пептид 2 GVLDLFRELLNELLEALKQKLKK (SEQ ID NO 2); пептид 3 PVLDLFRELLNELLEWLKQKLK (SEQ ID NO 3); пептид 4 PVLDLFRELLNELLEALKQKLK (SEQ ID NO 4); пептид 5 PVLDLFRELLNELLEALKQKLKK (SEQ ID NO 5); пептид 6 PVLDLFRELLNEXLEALKQKLK (SEQ ID NO 6); пептид 7 PVLDLFKELLNELLEALKQKLK (SEQ ID NO 7); пептид 8 PVLDLFRELLNEGLEALKQKLK (SEQ ID NO 8); пептид 9 PVLDLFRELGNELLEALKQKLK (SEQ ID NO 9); пептид 10 PVLDLFRELLNELLEAZKQKLK (SEQ ID NO 10); пептид 11 PVLDLFKELLQELLEALKQKLK (SEQ ID NO 11); пептид 12 PVLDLFRELLNELLEAGKQKLK (SEQ ID NO 12); пептид 13 GVLDLFRELLNEGLEALKQKLK (SEQ ID NO 13); пептид 14 PVLDLFRELLNELLEALOQOLO (SEQ ID NO 14); пептид 15 PVLDLFRELWNELLEALKQKLK (SEQ ID NO 15); пептид 16 PVLDLLRELLNELLEALKQKLK (SEQ ID NO 16); пептид 17 PVLELFKELLQELLEALKQKLK (SEQ ID NO 17); пептид 18 GVLDLFRELLNELLEALKQKLK (SEQ ID NO 18); пептид 19 PVLDLFRELLNEGLEALKQKLK (SEQ ID NO 19); пептид 20 PVLDLFREGLNELLEALKQKLK (SEQ ID NO 20); пептид 21 PVLDLFRELLNELLEALKQKLK (SEQ ID NO 21); пептид 22 PVLDLFRELLNELLEGLKQKLK (SEQ ID NO 22); пептид 23 PLLELFKELLQELLEALKQKLK (SEQ ID NO 23); пептид 24 PVLDLFRELLNELLEALQKKLK (SEQ ID NO 24); пептид 25 PVLDFFRELLNEXLEALKQKLK (SEQ ID NO 25); пептид 26 PVLDLFRELLNELLELLKQKLK (SEQ ID NO 26); пептид 27 PVLDLFRELLNELZEALKQKLK (SEQ ID NO 27); пептид 28 PVLDLFRELLNELWEALKQKLK (SEQ ID NO 28); пептид 29 AVLDLFRELLNELLEALKQKLK (SEQ ID NO 29); пептид 123 QVLDLFRELLNELLEALKQKLK (SEQ ID NO 123); пептид 124 PVLDLFOELLNELLEALOQOLO (SEQ ID NO 124); пептид 125 NVLDLFRELLNELLEALKQKLK (SEQ ID NO 125) пептид 126 PVLDLFRELLNELGEALKQKLK (SEQ ID NO 126); пептид 127 PVLDLFRELLNELLELLKQKLK (SEQ ID NO 127); пептид 128 PVLDLFRELLNELLEFLKQKLK (SEQ ID NO 128); пептид 129 PVLELFNDLLRELLEALQKKLK (SEQ ID NO 129); пептид 130 PVLELFNDLLRELLEALKQKLK (SEQ ID NO 130); пептид 131 PVLELFKELLNELLDALRQKLK (SEQ ID NO 131); пептид 132 PVLDLFRELLENLLEALQKKLK (SEQ ID NO 132); пептид 133 PVLELFERLLEDLLQALNKKLK (SEQ ID NO 133); пептид 134 PVLELFERLLEDLLKALNQKLK (SEQ ID NO 134); пептид 135 DVLDLFRELLNELLEALKQKLK (SEQ ID NO 135); пептид 136 PALELFKDLLQELLEALKQKLK (SEQ ID NO 136); пептид 137 PVLDLFRELLNEGLEAZKQKLK (SEQ ID NO 137); пептид 138 PVLDLFRELLNEGLEWLKQKLK (SEQ ID NO 138); пептид 139 PVLDLFRELWNEGLEALKQKLK (SEQ ID NO 139); пептид 140 PVLDLFRELLNEGLEALOQOLO (SEQ ID NO 140); пептид 141 PVLDFFRELLNEGLEALKQKLK (SEQ ID NO 141); пептид 142 PVLELFRELLNEGLEALKQKLK (SEQ ID NO 142); и ацилированные по N-концу, и(или) амидированные по С-концу, или этерифицированные их формы, при том, что Х обозначает Aib, Z обозначает Nal, а О обозначает орнитин. 20. Мультимерный агонист АроА-I, который проявляет по крайней мере 38%-ную активность по активации фермента LCAT по сравнению с АроА-1 человека и который характеризуется формулой (II) НН [LLm-HH] n LLm-HH (II), или его фармацевтически приемлемая соль, где каждый показатель m независимо друг от друга является целым числом от 0 до 1; n является целым числом от 0 до 10; каждый НН независимо представляет пептид или пептидный аналог по п. 1; каждый LL независимо представляет бифункциональный линкер; каждый знак “-” независимо обозначает ковалентную связь. 21. Мультимерный агонист АроА-I, который проявляет по крайней мере 38%-ную активность по активации фермента LCAT по сравнению с АроА-I человека и который характеризуется формулой (III) X-Nya-Х(ya-1)-(Nyb-X(yb-1))p (III) или его фармацевтически приемлемая соль, где каждый Х независимо представлен HH[LLm-HH] n LLm-HH; каждый НН независимо представлен базовым пептидом формулы (I) или его аналогом, или мутированным, укороченным, делетированным по внутреннему положению или достроенным вариантом в соответствии с описанным в данном тексте; каждый LL независимо представлен бифункциональным линкером; каждый m независимо является целым числом от 0 до 1; каждый n независимо является целым числом от 0 до 8; Nya и Nyb независимо друг от друга являются многофункциональной связывающей составляющей, где уa и уb представляют число функциональных групп, соответственно, в ya и Nyb; каждый уa или уb независимо является целым числом от 3 до 8; р является целым числом от 0 до 7; каждый знак “-” независимо обозначает ковалентную связь. 22. Мультимерный агонист АроА-I, который проявляет по крайней мере 38%-ную активность по активации фермента LCAT по сравнению с АроА-I человека и который характеризуется формулой (IV) или (V) 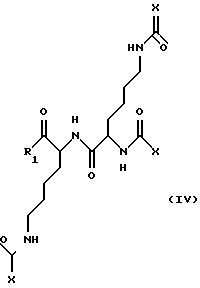 -OR- 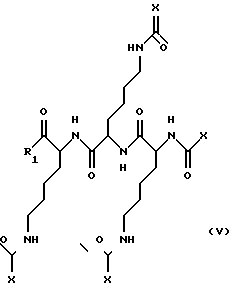 или его фармацевтически приемлемая соль, где каждый Х независимо представлен HH[LLm-HH] n LLm-HH; каждый НH независимо представлен пептидом или пептидным аналогом по п. 1; каждый LL независимо представлен бифункциональным линкером; каждый n независимо является целым числом от 0 до 1; каждый m независимо является целым числом от 0 до 8; R1 является -OR или -NRR; каждый R независимо представлен -Н, С1-6-алкилом, С1-6-алкенилом, С1-6-алкинилом, С5-20-арилом, С6-26-алкарилом, 5-20-атомным гетероарилом или 6-26-атомным алкгетероарилом. 23. Мультимерный агонист АроА-I по любому из пп. 20, 21 или 22, в составе которого бифункциональный линкер является расщепляемым. 24. Мультимерный агонист АроА-I по любому из пп. 20, 21 или 22, у которого n равно 0. 25. Мультимерный агонист АроА-I по п. 24, у которого m равно 0. 26. Мультимерный агонист АроА-I по любому из пп. 20, 21 или 22, у которого каждый НН независимо друг от друга является пептидом по п. 13. 27. Мультимерный агонист АроА-I по любому из пп. 20, 21 или 22, у которого каждый НН независимо друг от друга является пептидом по п. 14. 28. Мультимерный агонист АроА-I по любому из пп. 20, 21 или 22, у которого каждый НН независимо друг от друга является пептидом по п. 19. 29. Комплекс агониста АроА-I и липида, состоящий из агониста АроА-I и липида, притом, что агонист АроА-I является пептидом или пептидным аналогом по п. 1. 30. Комплекс агониста АроА-1 и липида по п. 29, в котором агонист АроА-I является пептидом по п. 12. 31. Комплекс агониста АроА-1 и липида по п. 29, в котором агонист АроА-I является пептидом по п. 13. 32. Комплекс агониста АроА-1 и липида по п. 29, в котором агонист АроА-I является пептидом по п. 14. 33. Комплекс агониста АроА-1 и липида по п. 29, в котором агонист АроА-I является пептидом по п. 19. 34. Комплекс агониста АроА-I и липида, состоящий из агониста АpoА-I АроА-I и липида, притом, что агонисту АроА-I является мультимерным агонистом по п. 20. 35. Комплекс агониста АроА-I и липида, состоящий из агониста АроА-I и липида, при том, что агонист является мультимерным агонистом АроА-I по п. 21. 36. Комплекс агониста АроА-I и липида, состоящий из агониста АроА-I и липида, при том, что агонист АроА-I является мультимерным агонистом по п. 22. 37. Комплекс агониста АроА-I и липида по любому из пп. 29-36, в котором липидом является сфингомиелин. 38. Комплекс агониста АроА-I и липида по любому из пп. 29-36, который находится в форме лиофилизованного порошка. 39. Комплекс агониста АроА-I и липида по любому из пп. 29-36, который находится в форме раствора. 40. Фармацевтическая композиция, содержащая агонист АроА-I и фармацевтически приемлемый носитель, наполнитель или растворитель, при том, что агонист АроА-I является пептидом или пептидным аналогом по п. 1. 41. Фармацевтическая композиция по п. 40, в которой агонист АроА-I является пептидом по п. 12. 42. Фармацевтическая композиция по п. 40, в которой агонист АроА-I является пептидом по п. 13. 43. Фармацевтическая композиция по п. 40, в которой агонист АроА-I является пептидом по п. 14. 44. Фармацевтическая композиция по п. 40, в которой агонист АроА-I является пептидом по п. 19. 45. Фармацевтическая композиция, содержащая агонист АроА-I и фармацевтически приемлемый носитель, наполнитель или растворитель, при том, что агонист АроА-I является мультимерным агонистом АроА-I по п. 20. 46. Фармацевтическая композиция, содержащая агонист АроА-I и фармацевтически приемлемый носитель, наполнитель или растворитель, при том, что агонист АроА-I является мультимерным агонистом АроА-I по п. 21. 47. Фармацевтическая композиция, содержащая агонист АроА-I и фармацевтически приемлемый носитель, наполнитель или растворитель, при том, что агонист АроА-I является мультимерным агонистом АроА-I по п. 22. 48. Фармацевтическая композиция по любому из пп. 40-47, в которой агонист АроА-I находится в форме комплекса с липидом, при том, что упомянутый комплекс состоит из агониста АроА-I и липида. 49. Фармацевтическая композиция по п. 48, в которой комплекс агониста АроА-I и липида находится в форме лиофилизованного порошка. 50. Способ лечения пациента, страдающего от заболевания, связанного с дислипидемией, при том, что упомянутый способ включает этап введения такому пациенту эффективного количества агониста АроА-I по п. 1. 51. Способ по п. 50, при том, что агонист АроА-I находится в форме фармацевтической композиции, а упомянутая композиция содержит агонист АроА-I и фармацевтически приемлемый носитель, наполнитель или растворитель. 52. Способ по п. 50, при том, что агонист АроА-I находится в форме комплекса агониста АроА-I и липида, а упомянутый комплекс состоит из агониста АроА-I и липида. 53. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является гиперхолестеринемия. 54. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является сердечно-сосудистое заболевание. 55. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является атеросклероз. 56. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является рестеноз. 57. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является дефицит HDL или АроА-I. 58. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является гипертриглицеридемия. 59. Способ по п. 50, при том, что связанным с дислипидемией заболеванием является метаболический синдром. 60. Способ лечения пациента, страдающего от септического шока, при том, что упомянутый способ включает этап введения такому пациенту эффективного количества агониста АроА-I по п. 1. 61. Способ по п. 50 или 60, при том, что упомянутым пациентом является человек. 62. Способ по п. 50 или 60, при том, что упомянутому пациенту вводят примерно 0,5-100 мг/кг агониста АроА-I. РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 29.09.2009
Извещение опубликовано: 20.09.2010 БИ: 26/2010
|
||||||||||||||||||||||||||
