Патент на изобретение №2215004
|
||||||||||||||||||||||||||
(54) КОНДЕНСИРОВАННОЕ ПРОИЗВОДНОЕ 1,2,4-ТИАДИАЗИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
(57) Реферат: Настоящее изобретение относится к конденсированным производным 1,2,4-тиадиазина, содержащим в системе тиофеновое и 1,2,4-тиадиазольное кольца. Описаны также фармацевтическая композиция и способ получения лекарственного препарата на основе соединений. Соединения обладают способностью воздействия на КАТФ-регулируемые калиевые каналы, что делает их полезными при лечении эндокринной системы, в частности их можно применять для снижения гиперинсулинемии и тем самым предотвращать диабет. 3 с. и 5 з.п. ф-лы. Настоящее изобретение касается конденсированных производных 1,2,4-тиадиазина, способов их получения, композиций, включающих эти соединения, применения этих соединений в качестве лекарственных препаратов и их использования при лечении, например, заболеваний центральной нервной системы, сердечно-сосудистой системы, легочной системы, желудочно-кишечной системы и эндокринной системы. ПРОТОТИПЫ ИЗОБРЕТЕНИЯ Калиевые каналы играют важную роль в физиологической и фармакологической регуляции клеточного мембранного потенциала. Среди различных типов калиевых каналов есть АТФ-чувствительные (КАТФ)-каналы, которые регулируются изменениями внутриклеточной концентрации аденозинтрифосфата (АТФ). КАТФ-каналы обнаружены в клетках из различных тканей, таких как клетки сердца, поджелудочной железы, скелетных мышц, гладких мышц, центральные нейроны и клетки аденогипофиза. Эти каналы связаны с различными клеточными функциями, например секрецией гормонов (инсулина из панкреатических бета-клеток, гормона роста и пролактина из клеток аденогипофиза), расширением кровеносных сосудов (в клетках гладких мышц), длительностью потенциала сердечного действия, выделением нейротрасмиттеров в центральной нервной системе. Обнаружено, что для лечения различных заболеваний важны модуляторы КАТФ-каналов. Определенные сульфонилмочевины, которые используют для лечения инсулиннезависимого сахарного диабета, действуют, стимулируя выделение инсулина посредством ингибирования КАТФ-каналов на панкреатических бета-клетках. Обнаружено, что вещества, открывающие калиевые каналы (potassium channel openers), которые включают гетерогенную группу соединений, способны расслаблять гладкие мышцы сосудов, и, следовательно, их можно применять для лечения гипертензии. Кроме того, вещества, открывающие калиевые каналы, можно применять в качестве бронхолитических средств при лечении астмы и разных других заболеваний. Показано также, что вещества, открывающие калиевые каналы, промотируют рост волос, и их можно применять для лечения облысения. Вещества, открывающие калиевые каналы, также могут расслаблять гладкую мышцу мочевого пузыря, и, следовательно, их можно применять для лечения недержания мочи. Вещества, открывающие калиевые каналы, которые расслабляют гладкую мышцу, можно применять для предотвращения преждевременных родов. Посредством воздействия на калиевые каналы центральной нервной системы можно применять эти соединения для лечения различных неврологических и психиатрических заболеваний, таких как болезнь Альцгеймера, эпилепсия и церебральная ишемия. Обнаружено также, что эти соединения полезны при лечении доброкачественной простатической гипертензии, эректильной дисфункции и для контрацепции. Соединения настоящего изобретения, которые ингибируют секрецию инсулина посредством активации калиевых каналов бета-клеток, можно применять в комбинации с другими соединениями, которые можно использовать для лечения инсулиннезависимого сахарного диабета и инсулинзависимого сахарного диабета. Примерами таких соединений являются инсулин, сенсибилизаторы инсулина, такие как триазолидиндионы, средства, усиливающие секрецию инсулина, такие как (repaglinide), толбутамид (tolbutamide), глибенкламид (glibenclamide) и глюкагонподобный пептид (GLP1), ингибиторы  -глюкозидазы и печеночные ферменты, ответственные за биосинтез глюкозы.
В настоящее время показано, что диазоксид (7-хлор-3-метил-2Н-1,2,4-бензотиадиазин 1,1-диоксид) и некоторые производные 3-(алкиламино)-4Н-пиридо[4,3-е] -1,2,4-тиадиазин 1,1-диоксида ингибируют выделение инсулина посредством активации КАТФ-каналов панкреатических бета-клеток (Pirotte В. и др. Biochem. Pharmacol., 47, 1381-1386 (1994); (Pirotte B. и др. Med. Chem., 36, 3211-3213 (1993)). Показано также, что диазоксид задерживает приступ диабета у ВВ-крыс (Vlahos W. D. и др. Metabolism, 40, 39-46 (1991)). На ожиревших крысах (obese zucker rats) показано, что диазоксид снижает секрецию инсулина и увеличивает связывание рецепторов инсулина и, следовательно, улучшает толерантность к глюкозе и снижает увеличение веса (Alemzadeh R. и др. Endocrinol., 133, 705-712, 1993). Ожидается, что соединения, которые активируют КАТФ-каналы, можно применять для лечения заболеваний, характеризующихся чрезмерным продуцированием инсулина, и для лечения и профилактики диабета.
Европейский Патент 618209 раскрывает класс производных пиридотиадиазина, имеющих алкильную или алкиламиногруппу в положении 3 тиадиазинового кольца. Заявлено, что эти соединения являются агонистами рецепторов АМРА-глутамата.
В J. Med. Chem., 1980, 23, 575-577, описан синтез 4(5)-амино- и формиламиноимидазо-5(4) карбоксамида и их свойства как агентов химиотерапевтического значения. Показано, главным образом, соединения 3-аминоимидазо[4,5-е] -1,2,4-тиадиазин 1,1-диоксид и N-бензоиламиноимидазо[4,5-е] -1,2,4-тиадиазин 1,1-диоксид.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ -глюкозидазы и печеночные ферменты, ответственные за биосинтез глюкозы.
В настоящее время показано, что диазоксид (7-хлор-3-метил-2Н-1,2,4-бензотиадиазин 1,1-диоксид) и некоторые производные 3-(алкиламино)-4Н-пиридо[4,3-е] -1,2,4-тиадиазин 1,1-диоксида ингибируют выделение инсулина посредством активации КАТФ-каналов панкреатических бета-клеток (Pirotte В. и др. Biochem. Pharmacol., 47, 1381-1386 (1994); (Pirotte B. и др. Med. Chem., 36, 3211-3213 (1993)). Показано также, что диазоксид задерживает приступ диабета у ВВ-крыс (Vlahos W. D. и др. Metabolism, 40, 39-46 (1991)). На ожиревших крысах (obese zucker rats) показано, что диазоксид снижает секрецию инсулина и увеличивает связывание рецепторов инсулина и, следовательно, улучшает толерантность к глюкозе и снижает увеличение веса (Alemzadeh R. и др. Endocrinol., 133, 705-712, 1993). Ожидается, что соединения, которые активируют КАТФ-каналы, можно применять для лечения заболеваний, характеризующихся чрезмерным продуцированием инсулина, и для лечения и профилактики диабета.
Европейский Патент 618209 раскрывает класс производных пиридотиадиазина, имеющих алкильную или алкиламиногруппу в положении 3 тиадиазинового кольца. Заявлено, что эти соединения являются агонистами рецепторов АМРА-глутамата.
В J. Med. Chem., 1980, 23, 575-577, описан синтез 4(5)-амино- и формиламиноимидазо-5(4) карбоксамида и их свойства как агентов химиотерапевтического значения. Показано, главным образом, соединения 3-аминоимидазо[4,5-е] -1,2,4-тиадиазин 1,1-диоксид и N-бензоиламиноимидазо[4,5-е] -1,2,4-тиадиазин 1,1-диоксид.
ОПИСАНИЕ ИЗОБРЕТЕНИЯНастоящее изобретение касается производных конденсированного 1,2,4-тиадиазина и конденсированного 1,4-тиазина общей формулы I: 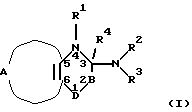 где В представляет >NR5 или >CR5R6, где R5 и R6 независимо являются водородом; гидроксилом; C1-6-алкоксигруппой или C1-6-алкилом, С3-6-циклоалкилом, С2-6-алкенилом или С2-6-алкинилом, необязательно моно- или полизамещенным галогеном, или R5 и R4 вместе представляют одну из связей в двойной связи между атомами 2 и 3 формулы I; D представляет -S(=O)2– или независимо -S(=O)- или D-B представляет -S(=O)(R7)= N-, где R7 является C1-6-алкилом; или арилом или гетероарилом, необязательно моно- или полизамещенным галогеном, гидроксилом, C1-6-алкоксигруппой, арилоксигруппой, арилалкоксигруппой, нитрогруппой, аминогруппой, C1-6-моноалкил- или диалкиламиногруппой, цианогруппой, ацилом или C1-6-алкоксикарбонилом; R1 является водородом; гидроксилом; C1-6-алкоксигруппой или C1-6-алкилом, С3-6-циклоалкилом, C2-6-алкенилом или С2-6-алки-нилом, необязательно моно- или полизамещенным галогеном, и R4 является водородом; или R4 вместе с R5 представляют одну связь из двойной связи между атомами 2 и 3 формулы I; или R1 вместе с R4 представляют одну связь из двойной связи между атомами 3 и 4 формулы I; R2 является водородом; гидроксилом; C1-6-алкоксигруппой или C1-6-алкилом, С3-6-циклоалкилом, С2-6-алкенилом или С2-6-алки-нилом, необязательно моно- или полизамещенным галогеном; R3 является R8; -OR8; -C(=X)R8; -NR8R9; бициклоалкилом, арилом, гетероарилом, арилалкилом или гетероарилалкилом, необязательно моно- или полизамещенным галогеном, C1-6-алкоксигруппой, арилоксигруппой, арилалкоксигруппой, нитрогруппой, аминогруппой, C1-6-моноалкил- или диалкиламиногруппой, цианогруппой, оксогруппой, ацилом или C1-6-алкоксикарбонилом; или арилом, замещенным C1-6-алкилом; где R8 является водородом; С3-6-циклоалкилом или (С3-6-циклоалкил)С3-6-алкилом, при этом С3-6-циклоалкильная группа необязательно моно- или полизамещена 1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой; 3-6-членной насыщенной циклической системой, включающей один или более атомов азота, кислорода или серы; или линейным или разветвленным C1-18-алкилом, необязательно моно- или полизамещенным галогеном, гидроксилом или C1-6-алкоксигруппой, C1-6-алкилтиогруппой, С3-6-циклоалкилом, арилом, арилоксигруппой, арилалкоксигруппой, нитрогруппой, аминогруппой, C1-6-моноалкил- или диалкиламиногруппой, цианогруппой, оксогруппой, формильной группой, ацилом, карбоксилом, C1-6-алкоксикарбонилом или карбамоилом; Х представляет О или S; R8 является водородом; C1-6-алкилом; С2-6-алкенилом; С3-6-циклоалкилом, необязательно моно- или полизамещенным C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой; или R8 и R9 вместе с атомом азота образуют 3-12-членную моно- или бициклическую систему, в которой один или более атомов углерода могут быть замещены азотом, кислородом или серой, при этом каждая из этих циклических систем необязательно моно- или полизамещена галогеном, C1-6-алкилом, гидроксилом, C1-6-алкоксигруппой, С1-6-алкокси-С1-6-алкилом, нитрогруппой, аминогруппой, цианогруппой, трифторметилом, C1-6-моноалкил- или диалкиламиногруппой, оксогруппой; или R3 представляет 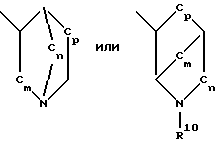 где n, m, p независимо равны 0, 1, 2, 3, и R10 является водородом; гидроксилом; C1-6-алкоксигруппой, С3-6-циклоалкилом, необязательно моно- или полизамещенным C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой; C1-6-алкилом, С2-6-алкенилом или С2-6-алкинилом, необязательно моно- или полизамещенным галогеном; или R2 и R3 вместе с атомом азота образуют 3-12-членную моно- или бициклическую систему, в которой один или более атомов углерода могут быть замещены азотом, кислородом или серой, при этом каждая из этих циклических систем необязательно моно- или полизамещена галогеном, C1-6-алкилом, гидроксилом, C1-6-алкоксигруппой, С1-6-алкокси-С1-6-алкилом, нитрогруппой, аминогруппой, цианогруппой, трифторметилом, C1-6-моноалкил- или диалкиламиногруппой или оксогруппой; А вместе с атомами углерода 5 и 6 формулы I представляет 5- или 6-членную гетероциклическую систему, включающую один или более атомов азота, кислорода или серы, при этом гетероциклическая система необязательно моно- или полизамещена галогеном, C1-12-алкилом, С3-6-циклоалкилом; гидроксилом, C1-6-алкоксигруппой; С1-6-алкокси-С1-6-алкилом; нитрогруппой, аминогруппой; цианогруппой; цианометилом; пергалогенметилом; C1-6-моноалкил- или диалкиламиногруппой; сульфамоильной группой; C1-6-алкилтиогруппой; C1-6-алкилсульфонильной группой; C1-6-алкилсульфинильной группой; C1-6-алкилкарбониламиногруппой; арилтиогруппой; арилсульфинильной группой; арилсульфонильной группой, при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой; C1-6-алкоксикарбонилом; C1-6-алкоксикарбонил-C1-6-алкилом; карбамилом; карбамилметилом; C1-6-моноалкил- или диалкиламинокарбонилом; C1-6-моноалкил- или диалкиламинотиокарбонилом; уреидогруппой; C1-6-моноалкил- или диалкиламинокарбониламиногруппой; тиоуреидогруппой; C1-6-моноалкил- или диалкиламинотиокарбониламиногруппой; C1-6-моноалкил- или диалкиламиносульфонилом; карбоксилом; карбокси-С1-6-алкилом; ацилом; арилом, арилалкилом, арилоксигруппой, при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой; (1,2,4-оксадиазол-5-ил)- или (1,2,4-оксадиазол-3-ил)-C1-6-алкилом, при этом оксадиазолильная группа необязательно замещена C1-6-алкилом или С3-6-циклоалкилом; или 5-6-членным циклом, содержащим азот, необязательно замещенным фенилом или C1-6-алкилом; при условии, что А вместе с атомами углерода 5 и 6 формулы I не образуют пиридинового кольца и что не включены следующие соединения: 3-аминоимидазо[4,5-е] -1,2,4-тиадиазин 1,1-диоксид и 3-бензоиламиноимидазо[4,5-е] -1,2,4-тиадиазин 1,1-диоксид, или их солей с фармацевтически приемлемой кислотой или основанием. В область данного изобретения включены все оптические изомеры соединений формулы I, некоторые из которых оптически активны, а также их смеси, включая их рацемические смеси. Область данного изобретения включает также таутомерные формы соединений формулы I. Соли включают фармацевтически приемлемые соли присоединения кислот, таких как соляная, бромистоводородная, иодистоводородная, фосфорная, серная, трифторуксусная, трихлоруксусная, щавелевая, малеиновая, пировиноградная, малоновая, янтарная, лимонная, винная, фумаровая, миндальная, бензойная, коричная, метансульфоновая, этансульфоновая, пикриновая и подобные, и включают кислоты, имеющие отношение к фармацевтически приемлемым солям, которые перечислены в Journal of Pharmaceutical Science, 66, 2 (1977), и включены здесь в качестве ссылки, фармацевтически приемлемые соли металлов, таких как литий, натрий, калий, магний и подобные, или соли необязательно алкилированного аммония. Использованный здесь термин “C1-6-алкоксигруппа”, сам по себе или в комбинации, относится к линейному или разветвленному моновалентному заместителю, включающему C1-6-алкильную группу, связанную через эфирный кислород, со свободной валентной связью от эфирного кислорода и имеющую от 1 до 6 атомов углерода, например метокси-, этокси-, пропокси-, изопропокси-, бутокси-, пентоксигруппе. Использованный здесь термин “C1-6-алкилтиогруппа”, сам по себе или в комбинации, относится к линейному или разветвленному моновалентному заместителю, включающему низшую алкильную группу, связанную через атом бивалентной серы, со свободной валентной связью от атома серы и имеющую от 1 до 6 атомов углерода, например метилтио-, этилтио-, пропилтио-, бутилтио-, пентилтиогруппе. Использованный здесь термин “С2-6-алкенил”‘ относится к ненасыщенной углеводородной цепи, имеющей 2-6 атомов углерода и одну двойную связь, такой как, например, винил, 1-пропенил, аллил, изопропенил, н-бутенил, н-пентенил и н-гексенил. Использованный здесь термин “С3-6-циклоалкил” относится к радикалу насыщенного циклического углеводорода с указанным количеством углеродов, такому как циклопропил, циклобутил, циклопентил или циклогексил. Использованный здесь термин “С2-6-алкинил” относится к ненасыщенным углеводородам, которые содержат тройную связь, таким как, например, -С  СН, -С СН, -С ССН3, -CH2C ССН3, -CH2C CH, -CH2CH2C CH, -CH2CH2C CH, (СН3)С CH, (СН3)С СН и подобные.
Использованный здесь термин “С1-6-алкокси-С1-6-алкил” относится к группе из 2-12 атомов углерода, разъединенной атомом кислорода, такой как, например, -CH2-O-СН3, -СН2-O-СН2-, СН3, -СН2-О-СН-(СН3)2 и подобные.
Термин “галоген” обозначает фтор, хлор, бром или йод.
Термин “пергалогенметил” обозначает трифторметил, трихлорметил, трибромметил или трийодметил.
Использованные здесь термины “C1-6-алкил”, “C1-12-алкил” и “C1-18-алкил”, сами по себе или в комбинации, относятся к линейной или разветвленной насыщенной углеводородной цепи, имеющей указанное количество атомов углерода, такой как, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, 2-метилбутил, 3-метилбутил, 4-метилбутил, неопентил, н-гексил, 1,2-диметилпропил, 2,2-диметилпропил, 1,2,2-триметилпропил и подобные. Использованный здесь термин “C1-18-алкил”, включает также вторичный С3-6-алкил и третичный С4-6-алкил.
Использованный здесь термин “C1-6-моноалкиламиногруппа” относится к аминогруппе, в которой один из атомов водорода замещен линейной или разветвленной насыщенной углеводородной цепью, имеющей указанное количество атомов углерода, такой как, например, метиламино-, этиламино-, пропиламино-, н-бутиламино-, втор-бутиламино-, изобутиламино-, трет-бутиламино-, н-пентиламино-, 2-метилбутиламино-, н-гексиламино-, 4-метилпентиламино-, неопентиламино-, н-гексиламино-, 2,2-диметилпропиламиногруппа и подобные.
Использованный здесь термин “C1-6-диалкиламиногруппа” относится к аминогруппе, в которой два атома водорода независимо замещены линейной или разветвленной насыщенной углеводородной цепью, имеющей указанное количество атомов углерода, такой как, например, диметиламино-, N-этил-N-метиламино-, диэтиламино-, дипропиламино-, N-(н-бутил)-N-метиламино-, ди(н-пентил)аминогруппа и подобные.
Использованный здесь термин “ацил” относится к моновалентному заместителю, который включает C1-6-алкильную группу, связанную через карбонильную группу, такому как, например, ацетил, пропионил, бутирил, изобутирил, пивалоил, валерил и подобные.
Использованный здесь термин “C1-6-алкоксикарбонил” относится к моновалентному заместителю, включающему C1-6-алкокси-группу, связанную через карбонильную группу, такому как, например, метоксикарбонил, карбоэтоксигруппа, пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, 3-метилбутоксикарбонил, н-гексоксикарбонил и подобные.
Использованный здесь термин “3-12-членная моно- или бициклическая система” относится к моновалентному заместителю формулы -NR2R3 или -NR8R9, где R2 и R3 или R8 и R9 вместе с атомом азота образуют 3-12-членную моно- или бициклическую систему, в которой один или более атомов углерода могут быть замещены азотом, кислородом или серой, такому как 1-пирро-лидин, пиперидино, морфолино, тиоморфолино, 4-метилпиперазин-1-ил, 7-азабицикло[2.2.1]гептан-7-ил и подобные.
Использованный здесь термин “3-6-членная насыщенная циклическая система” относится к моновалентному заместителю, который включает моноциклическую насыщенную систему, содержащую один или более гетероатомов, выбранных из азота, кислорода и серы, и 3-6 членов, и имеют свободную валентность от атома углерода, такому как, например, 2-пирролидин, 4-пиперидил, 3-морфолинил, 1,4-диоксан-2-ил, 5-оксазолидинил, 4-изоксазолидинил или 2-тиоморфолинил.
Использованный здесь термин “бициклоалкил” относится к моновалентному заместителю, который включает бициклическую структуру, составленную из 6-12 атомов углерода, такому как, например, 2-норборнил, 7-норборнил, 2-бицикло[2.2.2]октил и 9-бицикло[3.3.1]нонанил.
Использованный здесь термин “арил” относится к фенилу, 1-нафтилу или 2-нафтилу.
Использованный здесь термин “гетероарил” один или в комбинации относится к моновалентному заместителю, который включает 5-6-членную моноциклическую ароматическую систему или 9-10-членную бициклическую ароматическую систему, содержащую один или более гетероатомов, выбранных из азота, кислорода и серы, такому как, например, пиррол, имидазол, пиразол, триазол, пиридин, пиразин, пиримидин, пиридазин, изотиазол, изоксазол, оксазол, оксадиазол, тиадиазол, хинолин, изохинолин, хиназолин, хиноксалин, индол, бензимидазол, бензофуран, птеридин и пурин.
Использованный здесь термин “арилалкил” относится к линейной или разветвленной насыщенной углеродной цепи, содержащей от 1 до 6 углеродов и замещенной ароматическим карбогидридом, такой как бензил, фенетил, 3-фенилпропил, 1-нафтилметил, 2-(1-нафтил)этил и подобные.
Использованный здесь термин “арилоксигруппа” относится к феноксигруппе, 1-нафтилоксигруппе или 2-нафтилоксигруппе.
Использованный здесь термин “арилалкоксигруппа” относится к C1-6-алкоксигруппе, замещенной ароматическим карбогидридом, такой как бензилокси-, фенэтокси-, 3-фенилпропокси-, 1-нафтилметокси-, 2-(1-нафтил)этоксигруппа и подобные.
Использованный здесь термин “гетероарилалкил” относится к линейной или разветвленной насыщенной углеродной цепи, содержащей от 1 до 6 углеродов и замещенной гетероарильной группой, такой как (2-фурил)метил, (3-фурил)метил, (2-тиенил)метил, (3-тиенил)метил, (2-пиридил)метил, 1-метил-1-(2-пиримидил)этил и подобные.
Использованный здесь термин “С1-6-алкилсульфонил” относится к моновалентному заместителю, включающему C1-6-алкильную группу, связанную через сульфонильную группу, такому как, например, метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, втор-бутилсульфонил изо-бутилсульфонил, трет-бутилсульфонил, н-пентилсульфонил, 2-метилбутилсульфонил, 3-метилбутилсульфонил, н-гексилсульфонил, 4-метилпентилсульфонил, неопентилсульфонил, н-гексилсульфонил и 2,2-диметилпропилсульфонил.
Использованный здесь термин “C1-6-моноалкиламиносульфонил” относится к моновалентному заместителю, включающему C1-6-моноалкиламиногруппу, связанную через сульфонильную группу, такому как, например, метиламиносульфонил, этиламиносульфонил, н-пропиламиносульфонил, изопропиламиносуль-фонил, н-бутиламиносульфонил, втор-бутиламиносульфонил, изо-бутиламиносульфонил, трет-бутиламиносульфонил, н-пентиламиносульфонил, 2-метилбутиламиносульфонил, 3-метилбутиламиносульфонил, н-гексиламиносульфонил, 4-метилпентиламиносульфонил, неопентиламиносульфонил, н-гексиламиносульфонил и 2,2-диметилпропиламиносульфонил.
Использованный здесь термин “C1-6-диалкиламиносульфонил” относится к моновалентному заместителю, включающему C1-6-диалкиламиногруппу, связанную через сульфонильную группу, такому как диметиламиносульфонил, N-этил-N-метиламиносульфонил, диэтиламиносульфонил, дипропиламиносульфонил, N-(н-бутил)-N-метиламиносульфонил, ди(н-пентил)аминосульфонил и подобные.
Использованный здесь термин “C1-6-алкилсульфинил” относится к моновалентному заместителю, включающему линейную или разветвленную C1-6-алкильную группу, связанную через сульфинильную группу (-S(=O)-), такому как, например, метилсульфинил, этилсульфинил, изопропилсульфинил, бутилсульфинил, пентилсульфинил и подобные.
Использованный здесь термин “C1-6-алкилкарбониламиногруппа” относится к аминогруппе, в которой один атом водорода замещен ацильной группой, такой как, например, ацетамидопропионамидо-, изопропилкарбониламиногруппа и подобные.
Использованный здесь термин “(С3-6-циклоалкил)C1-6-алкил”, сам по себе или в комбинации, относится к линейной или разветвленной насыщенной углеводородной цепи, которая имеет от 1 до 6 атомов углерода и является монозамещенной С3-6-циклоалкильной группой, при этом циклоалкильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, такой как, например, циклопропилметил, (1-метилциклопропил)метил, 1-(циклопропил)этил, циклопентилметил, циклогексилметил и подобные.
Использованный здесь термин “арилтиогруппа”, относится к арильной группе, связанной через атом дивалентной серы и имеющей свободную валентную связь от атома серы, при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, например фенилтио-, (4-метилфенил)тио-, (2-хлорфенил)тиогруппе и подобным.
Использованный здесь термин “арилсульфинил” относится к арильной группе, связанной через сульфинильную группу (S(=O)-), при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, такой как фенилсульфинил, (4-хлорфенил)сульфинил и подобные.
Использованный здесь термин “арилсульфонил” относится к арильной группе, связанной через сульфонильную группу, при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, такой как фенилсульфонил, тозил и подобные.
Использованный здесь термин “C1-6-моноалкиламинокарбонил” относится к моновалентному заместителю, который включает C1-6-моноалкиламиногруппу, связанную через карбонильную группу, такому как, например, метиламинокарбонил, этиламинокарбонил, н-пропиламинокарбонил, изопропиламинокарбонил, н-бутиламинокарбонил, втор-бутиламинокарбонил, изобутиламинокарбонил, трет-бутиламинокарбонил, н-пентиламинокарбонил, 2-метилбутиламинокарбонил, 3-метилбутиламинокарбонил, н-гексиламинокарбонил, 4-метиламинокарбонил, неопентиламинокарбонил, н-гексиламинокарбонил и 2,2-диметилпропиламинокарбонил.
Использованный здесь термин “С1-6-диалкиламинокарбонил” относится к моновалентному заместителю, который включает C1-6-диалкиламиногруппу, связанную через карбонильную группу, такому как диметиламинокарбонил, N-этил-N-метиламинокар-бонил, диэтиламинокарбонил, дипропиламинокарбонил, N-(н-бутил)-N-метиламинокарбонил, ди(н-пентил)аминокарбонил и подобные.
Использованный здесь термин “C1-6-моноалкиламинокарбониламиногруппа” относится к аминогруппе, в которой один из атомов водорода замещен C1-6-моноалкиламинокарбонильной группой, такой как, например, метиламинокарбониламино-, этиламинокарбониламино-, н-пропиламинокарбониламино-, изопропиламинокарбониламино-, н-бутиламинокарбониламино-, втор-бутиламинокарбониламино-, изобутиламинокарбониламино-, трет-бутиламинокарбониламино- и 2-метилбутиламинокарбониламиногруппа.
Использованный здесь термин “C1-6-диалкиламинокарбониламиногруппа” относится к аминогруппе, в которой один из атомов водорода замещен C1-6-диалкиламинокарбонильной группой, такой как, например, диметиламинокарбониламино-, N-этил-N-метиламинокарбониламино-, диэтиламинокарбониламино-, дипропиламинокарбониламино-, N-(н-бутил)-N-метиламинокарбониламино-, ди(н-пентил)аминокарбониламиногруппа и подобные.
Использованный здесь термин “5- или 6-членная гетероциклическая система” относится к моноциклической ненасыщенной или насыщенной системе, содержащей один, два или три гетероатома, выбранных из азота, кислорода и серы и имеющей 5 членов, такой как, например, пиррол, фуран, тиофен, пирролин, дигидрофуран, дигидротиофен, имидазол, имидазолин, пиразол, пиразолин, оксазол, тиазол, изоксазол, изотиазол, 1,2,3-оксадиазол, фуразан, 1,2,3-триазол, 1,2,3-тиадиазол или 2,1,3- тиадиазол; ароматической моноциклической системе, содержащей два или более атомов азота и имеющей 6 членов, такой как, например, пиразин, пиримидин, пиридазин, 1,2,4-триазин, 1,2,3-триазин или тетразин; неароматической моноциклической системе, содержащей один или более гетероатомов, выбранных из азота, кислорода и серы, и имеющей 6 членов, такой как, например, пиран, тиопиран, пиперидин, диоксан, оксазин, изоксазин, дитиан, оксатин, тиазин, пиперазин, тиадиазин, дитиазин или оксадиазин.
Использованный здесь термин “5- или 6-членный азотсодержащий цикл” относится к моновалентному заместителю, который включает моноциклическую ненасыщенную или насыщенную систему, содержащую один или более атомов азота и имеющую 5 или 6 членов, такому как, например, пирролидинил, пирролинил, имидазолидинил, пиразолидинил, пиразолинил, пиперидил, пиперазинил, пирролил, 2-пирролил, имидазолил, пиразолил, триазолил, пиридил, пиразинил, пиримидинил, пиридизинил, морфолино, тиоморфолино, изотиазолил, изоксазолил, оксазолил, оксадиазолил, тиадиазолил, 1,3-диоксоланил и 1,4-диоксоланил.
В предпочтительном варианте данного изобретения соединение общуей формулы I выбирают из СН и подобные.
Использованный здесь термин “С1-6-алкокси-С1-6-алкил” относится к группе из 2-12 атомов углерода, разъединенной атомом кислорода, такой как, например, -CH2-O-СН3, -СН2-O-СН2-, СН3, -СН2-О-СН-(СН3)2 и подобные.
Термин “галоген” обозначает фтор, хлор, бром или йод.
Термин “пергалогенметил” обозначает трифторметил, трихлорметил, трибромметил или трийодметил.
Использованные здесь термины “C1-6-алкил”, “C1-12-алкил” и “C1-18-алкил”, сами по себе или в комбинации, относятся к линейной или разветвленной насыщенной углеводородной цепи, имеющей указанное количество атомов углерода, такой как, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, 2-метилбутил, 3-метилбутил, 4-метилбутил, неопентил, н-гексил, 1,2-диметилпропил, 2,2-диметилпропил, 1,2,2-триметилпропил и подобные. Использованный здесь термин “C1-18-алкил”, включает также вторичный С3-6-алкил и третичный С4-6-алкил.
Использованный здесь термин “C1-6-моноалкиламиногруппа” относится к аминогруппе, в которой один из атомов водорода замещен линейной или разветвленной насыщенной углеводородной цепью, имеющей указанное количество атомов углерода, такой как, например, метиламино-, этиламино-, пропиламино-, н-бутиламино-, втор-бутиламино-, изобутиламино-, трет-бутиламино-, н-пентиламино-, 2-метилбутиламино-, н-гексиламино-, 4-метилпентиламино-, неопентиламино-, н-гексиламино-, 2,2-диметилпропиламиногруппа и подобные.
Использованный здесь термин “C1-6-диалкиламиногруппа” относится к аминогруппе, в которой два атома водорода независимо замещены линейной или разветвленной насыщенной углеводородной цепью, имеющей указанное количество атомов углерода, такой как, например, диметиламино-, N-этил-N-метиламино-, диэтиламино-, дипропиламино-, N-(н-бутил)-N-метиламино-, ди(н-пентил)аминогруппа и подобные.
Использованный здесь термин “ацил” относится к моновалентному заместителю, который включает C1-6-алкильную группу, связанную через карбонильную группу, такому как, например, ацетил, пропионил, бутирил, изобутирил, пивалоил, валерил и подобные.
Использованный здесь термин “C1-6-алкоксикарбонил” относится к моновалентному заместителю, включающему C1-6-алкокси-группу, связанную через карбонильную группу, такому как, например, метоксикарбонил, карбоэтоксигруппа, пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, 3-метилбутоксикарбонил, н-гексоксикарбонил и подобные.
Использованный здесь термин “3-12-членная моно- или бициклическая система” относится к моновалентному заместителю формулы -NR2R3 или -NR8R9, где R2 и R3 или R8 и R9 вместе с атомом азота образуют 3-12-членную моно- или бициклическую систему, в которой один или более атомов углерода могут быть замещены азотом, кислородом или серой, такому как 1-пирро-лидин, пиперидино, морфолино, тиоморфолино, 4-метилпиперазин-1-ил, 7-азабицикло[2.2.1]гептан-7-ил и подобные.
Использованный здесь термин “3-6-членная насыщенная циклическая система” относится к моновалентному заместителю, который включает моноциклическую насыщенную систему, содержащую один или более гетероатомов, выбранных из азота, кислорода и серы, и 3-6 членов, и имеют свободную валентность от атома углерода, такому как, например, 2-пирролидин, 4-пиперидил, 3-морфолинил, 1,4-диоксан-2-ил, 5-оксазолидинил, 4-изоксазолидинил или 2-тиоморфолинил.
Использованный здесь термин “бициклоалкил” относится к моновалентному заместителю, который включает бициклическую структуру, составленную из 6-12 атомов углерода, такому как, например, 2-норборнил, 7-норборнил, 2-бицикло[2.2.2]октил и 9-бицикло[3.3.1]нонанил.
Использованный здесь термин “арил” относится к фенилу, 1-нафтилу или 2-нафтилу.
Использованный здесь термин “гетероарил” один или в комбинации относится к моновалентному заместителю, который включает 5-6-членную моноциклическую ароматическую систему или 9-10-членную бициклическую ароматическую систему, содержащую один или более гетероатомов, выбранных из азота, кислорода и серы, такому как, например, пиррол, имидазол, пиразол, триазол, пиридин, пиразин, пиримидин, пиридазин, изотиазол, изоксазол, оксазол, оксадиазол, тиадиазол, хинолин, изохинолин, хиназолин, хиноксалин, индол, бензимидазол, бензофуран, птеридин и пурин.
Использованный здесь термин “арилалкил” относится к линейной или разветвленной насыщенной углеродной цепи, содержащей от 1 до 6 углеродов и замещенной ароматическим карбогидридом, такой как бензил, фенетил, 3-фенилпропил, 1-нафтилметил, 2-(1-нафтил)этил и подобные.
Использованный здесь термин “арилоксигруппа” относится к феноксигруппе, 1-нафтилоксигруппе или 2-нафтилоксигруппе.
Использованный здесь термин “арилалкоксигруппа” относится к C1-6-алкоксигруппе, замещенной ароматическим карбогидридом, такой как бензилокси-, фенэтокси-, 3-фенилпропокси-, 1-нафтилметокси-, 2-(1-нафтил)этоксигруппа и подобные.
Использованный здесь термин “гетероарилалкил” относится к линейной или разветвленной насыщенной углеродной цепи, содержащей от 1 до 6 углеродов и замещенной гетероарильной группой, такой как (2-фурил)метил, (3-фурил)метил, (2-тиенил)метил, (3-тиенил)метил, (2-пиридил)метил, 1-метил-1-(2-пиримидил)этил и подобные.
Использованный здесь термин “С1-6-алкилсульфонил” относится к моновалентному заместителю, включающему C1-6-алкильную группу, связанную через сульфонильную группу, такому как, например, метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, втор-бутилсульфонил изо-бутилсульфонил, трет-бутилсульфонил, н-пентилсульфонил, 2-метилбутилсульфонил, 3-метилбутилсульфонил, н-гексилсульфонил, 4-метилпентилсульфонил, неопентилсульфонил, н-гексилсульфонил и 2,2-диметилпропилсульфонил.
Использованный здесь термин “C1-6-моноалкиламиносульфонил” относится к моновалентному заместителю, включающему C1-6-моноалкиламиногруппу, связанную через сульфонильную группу, такому как, например, метиламиносульфонил, этиламиносульфонил, н-пропиламиносульфонил, изопропиламиносуль-фонил, н-бутиламиносульфонил, втор-бутиламиносульфонил, изо-бутиламиносульфонил, трет-бутиламиносульфонил, н-пентиламиносульфонил, 2-метилбутиламиносульфонил, 3-метилбутиламиносульфонил, н-гексиламиносульфонил, 4-метилпентиламиносульфонил, неопентиламиносульфонил, н-гексиламиносульфонил и 2,2-диметилпропиламиносульфонил.
Использованный здесь термин “C1-6-диалкиламиносульфонил” относится к моновалентному заместителю, включающему C1-6-диалкиламиногруппу, связанную через сульфонильную группу, такому как диметиламиносульфонил, N-этил-N-метиламиносульфонил, диэтиламиносульфонил, дипропиламиносульфонил, N-(н-бутил)-N-метиламиносульфонил, ди(н-пентил)аминосульфонил и подобные.
Использованный здесь термин “C1-6-алкилсульфинил” относится к моновалентному заместителю, включающему линейную или разветвленную C1-6-алкильную группу, связанную через сульфинильную группу (-S(=O)-), такому как, например, метилсульфинил, этилсульфинил, изопропилсульфинил, бутилсульфинил, пентилсульфинил и подобные.
Использованный здесь термин “C1-6-алкилкарбониламиногруппа” относится к аминогруппе, в которой один атом водорода замещен ацильной группой, такой как, например, ацетамидопропионамидо-, изопропилкарбониламиногруппа и подобные.
Использованный здесь термин “(С3-6-циклоалкил)C1-6-алкил”, сам по себе или в комбинации, относится к линейной или разветвленной насыщенной углеводородной цепи, которая имеет от 1 до 6 атомов углерода и является монозамещенной С3-6-циклоалкильной группой, при этом циклоалкильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, такой как, например, циклопропилметил, (1-метилциклопропил)метил, 1-(циклопропил)этил, циклопентилметил, циклогексилметил и подобные.
Использованный здесь термин “арилтиогруппа”, относится к арильной группе, связанной через атом дивалентной серы и имеющей свободную валентную связь от атома серы, при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, например фенилтио-, (4-метилфенил)тио-, (2-хлорфенил)тиогруппе и подобным.
Использованный здесь термин “арилсульфинил” относится к арильной группе, связанной через сульфинильную группу (S(=O)-), при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, такой как фенилсульфинил, (4-хлорфенил)сульфинил и подобные.
Использованный здесь термин “арилсульфонил” относится к арильной группе, связанной через сульфонильную группу, при этом арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой, такой как фенилсульфонил, тозил и подобные.
Использованный здесь термин “C1-6-моноалкиламинокарбонил” относится к моновалентному заместителю, который включает C1-6-моноалкиламиногруппу, связанную через карбонильную группу, такому как, например, метиламинокарбонил, этиламинокарбонил, н-пропиламинокарбонил, изопропиламинокарбонил, н-бутиламинокарбонил, втор-бутиламинокарбонил, изобутиламинокарбонил, трет-бутиламинокарбонил, н-пентиламинокарбонил, 2-метилбутиламинокарбонил, 3-метилбутиламинокарбонил, н-гексиламинокарбонил, 4-метиламинокарбонил, неопентиламинокарбонил, н-гексиламинокарбонил и 2,2-диметилпропиламинокарбонил.
Использованный здесь термин “С1-6-диалкиламинокарбонил” относится к моновалентному заместителю, который включает C1-6-диалкиламиногруппу, связанную через карбонильную группу, такому как диметиламинокарбонил, N-этил-N-метиламинокар-бонил, диэтиламинокарбонил, дипропиламинокарбонил, N-(н-бутил)-N-метиламинокарбонил, ди(н-пентил)аминокарбонил и подобные.
Использованный здесь термин “C1-6-моноалкиламинокарбониламиногруппа” относится к аминогруппе, в которой один из атомов водорода замещен C1-6-моноалкиламинокарбонильной группой, такой как, например, метиламинокарбониламино-, этиламинокарбониламино-, н-пропиламинокарбониламино-, изопропиламинокарбониламино-, н-бутиламинокарбониламино-, втор-бутиламинокарбониламино-, изобутиламинокарбониламино-, трет-бутиламинокарбониламино- и 2-метилбутиламинокарбониламиногруппа.
Использованный здесь термин “C1-6-диалкиламинокарбониламиногруппа” относится к аминогруппе, в которой один из атомов водорода замещен C1-6-диалкиламинокарбонильной группой, такой как, например, диметиламинокарбониламино-, N-этил-N-метиламинокарбониламино-, диэтиламинокарбониламино-, дипропиламинокарбониламино-, N-(н-бутил)-N-метиламинокарбониламино-, ди(н-пентил)аминокарбониламиногруппа и подобные.
Использованный здесь термин “5- или 6-членная гетероциклическая система” относится к моноциклической ненасыщенной или насыщенной системе, содержащей один, два или три гетероатома, выбранных из азота, кислорода и серы и имеющей 5 членов, такой как, например, пиррол, фуран, тиофен, пирролин, дигидрофуран, дигидротиофен, имидазол, имидазолин, пиразол, пиразолин, оксазол, тиазол, изоксазол, изотиазол, 1,2,3-оксадиазол, фуразан, 1,2,3-триазол, 1,2,3-тиадиазол или 2,1,3- тиадиазол; ароматической моноциклической системе, содержащей два или более атомов азота и имеющей 6 членов, такой как, например, пиразин, пиримидин, пиридазин, 1,2,4-триазин, 1,2,3-триазин или тетразин; неароматической моноциклической системе, содержащей один или более гетероатомов, выбранных из азота, кислорода и серы, и имеющей 6 членов, такой как, например, пиран, тиопиран, пиперидин, диоксан, оксазин, изоксазин, дитиан, оксатин, тиазин, пиперазин, тиадиазин, дитиазин или оксадиазин.
Использованный здесь термин “5- или 6-членный азотсодержащий цикл” относится к моновалентному заместителю, который включает моноциклическую ненасыщенную или насыщенную систему, содержащую один или более атомов азота и имеющую 5 или 6 членов, такому как, например, пирролидинил, пирролинил, имидазолидинил, пиразолидинил, пиразолинил, пиперидил, пиперазинил, пирролил, 2-пирролил, имидазолил, пиразолил, триазолил, пиридил, пиразинил, пиримидинил, пиридизинил, морфолино, тиоморфолино, изотиазолил, изоксазолил, оксазолил, оксадиазолил, тиадиазолил, 1,3-диоксоланил и 1,4-диоксоланил.
В предпочтительном варианте данного изобретения соединение общуей формулы I выбирают из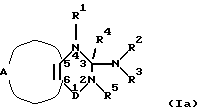 где R1 и R5 независимо являются водородом; гидроксилом; C1-6-алкоксигруппой или C1-6-алкилом, С3-6-циклоалкилом, С2-6-алкенилом или С2-6-алкинилом, необязательно моно- или полизамещенным галогеном, и R4 является водородом; или R4 вместе с R5 представляют одну из связей в двойной связи между атомами 2 и 3 формулы I, и R1 такой, как определено выше; или R4 вместе с R1 представляют одну из связей в двойной связи между атомами 3 и 4 формулы I, и R5 такой, как определено выше; D представляет -S(=O)2– или -S(=O)-. В другом предпочтительном варианте данного изобретения общую формулу I выбирают из 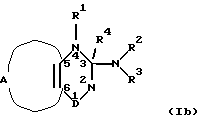 где R1 является водородом; C1-6-алкоксигруппой или C1-6-алкилом, С3-6-циклоалкилом, С2-6-алкенилом или С2-6-алкинилом, необязательно моно- или полизамещенным галогеном, и R4 является водородом; или R4 вместе с R1 представляют одну из связей в двойной связи между атомами 3 и 4 формулы I; D представляет -S(=O)(R7)=, где R7 является C1-6-алкилом; или арилом или гетероарилом, необязательно моно- или полизамещенным галогеном, гидроксилом, C1-6-алкоксигруппой, арилоксигруппой, арилалкоксигруппой, нитрогруппой, аминогруппой, C1-6-моноалкил- или диалкиламиногруппой, цианогруппой, ацилом или C1-6-алкоксикарбонилом. В другом предпочтительном варианте данного изобретения соединение общей формулы I выбирают из 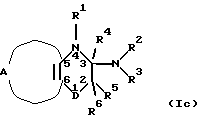 где R1, R5 и R6 независимо являются водородом; гидроксилом; C1-6-алкоксигруппой или C1-6-алкилом, С3-6-циклоалкилом, С2-6-алкенилом или С2-6-алкинилом, необязательно моно- или полизамещенным галогеном, и R4 является водородом; или R4 вместе с R5 представляют одну из связей в двойной связи между атомами 2 и 3 формулы I, и R1 и R6 такие, как определено выше; или R4 вместе с R1 представляют одну из связей в двойной связи между атомами 3 и 4 формулы I, и R5 и R6 такие, как определено выше; D представляет -S(=O)2– или -S(=O)-. Предпочтительной общей формулой I является (Ia). В другом предпочтительном варианте данного изобретения D представляет -S(=O)2-. В другом предпочтительном варианте данного изобретения R1 выбирают из водорода, C1-6-алкила, С3-6-циклоалкила или С2-6-алкенила. Предпочтительно R1 является водородом или C1-6-алкилом. В другом предпочтительном варианте данного изобретения R1 вместе с R4 представляют одну из связей в двойной связи между атомами 3 и 4 формулы I. В другом предпочтительном варианте данного изобретения R4 вместе с R5 представляют одну из связей в двойной связи между атомами 2 и 3 формулы I. В другом предпочтительном варианте данного изобретения R2 выбирают из водорода, гидроксила, C1-6-алкила, С3-6-циклоалкила или С2-6-алкенила. Предпочтительно R3 является водородом или C1-6-алкилом. В другом предпочтительном варианте данного изобретения R3 выбирают из R8, -OR8, -NR8R9 или арила, при этом арильная группа необязательно замещена 1-6-алкилом, где R8 является водородом; С3-6-циклоалкилом; (С3-6-циклоалкил)C1-6-алкилом, причем 3-6-членная система включает один, два или три атома азота, кислорода или серы; или линейным или разветвленным C1-18-алкилом, необязательно замещенным галогеном, гидроксилом, C1-6-алкоксигруппой, C1-6-алкилтиогруппой, С3-6-циклоалкилом, арил; R9 является водородом, C1-6-алкилом или С3-6-циклоалкилом; или R8 и R9 вместе с атомом азота образуют 4-6-членный цикл, преимущественно 1-пирролидил, пиперидин или морфолиновый цикл. Еще в одном предпочтительном варианте данного изобретения R3 выбирают из вторичного С3-6-алкила, третичного С4-6-алкила, С3-6-циклоалкила или (С3-6-циклоалкил)метила, необязательно моно- или полизамещенного 1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой. R3 предпочтительно выбирают из изопропила, 1-метилпропила, 2-метилпропила, трет-бутила, 1,1-диметилпропила, 1,2-диметилпропила, 1,2,2-триметилпропила, 2,3-диметилбутила, 1-этилпропила, 1-этил-2-метилпропила, 1-этил-2,2-диметилпропила, 2,3,3-триметилбутила, 2-метилбутила, 1,5-диметилгексила, 3-метилбутила, 3-метилгексила, циклопропила, 1-метилциклопропила, циклобутила, циклопентила, циклогексила, циклопропилметила, 1-(циклопропил)этила, циклобутилметила, циклопентилметила или циклогексилметила. Еще в одном предпочтительном варианте данного изобретения R2 и R3 вместе с атомом азота образуют шестичленный цикл, необязательно замещенный по 2 положению C1-6-алкильной группой, предпочтительно выбранной из метила, этила или изопропила. Шестичленный цикл преимущественно является пиперидином, пиперазином или тиоморфолиновым циклом. Еще в одном предпочтительном варианте данного изобретения R7 выбирают из C1-6-алкила, фенила или пиридила. Еще в одном предпочтительном варианте данного изобретения А вместе с атомами углерода 5 и 6 формулы I образует 5-членную гетероциклическую систему, содержащую один гетероатом, выбранный из азота и серы, 5-членную гетероциклическую систему, содержащую два гетероатома, выбранных из азота, кислорода и серы, 6-членную ароматическую гетероциклическую систему, содержащую два или три атома азота, 6-членную неароматическую гетероциклическую систему, содержащую один или два атома, выбранных из азота, кислорода и серы; при этом гетероциклические системы необязательно моно- или дизамещены галогеном; C1-12-алкилом, С3-6-циклоалкилом; цианогруппой, цианометилом; пергалогенметилом; сульфамоилом; C1-6-алкилтиогруппой; C1-6-алкилсульфонилом; C1-6-алкилсульфинилом; арилтиогруппой, арилсульфинилом, причем арильная группа необязательно моно- или полизамещена C1-6-алкилом, галогеном, гидроксилом или C1-6-алкоксигруппой; С1-6-алкоксикарбонил-С1-6-алкилом; карбамилметилом; карбокси-С1-6-алкилом; арилоксигруппой; (1,2,4-оксадиазол-5-ил)- или (1,2,4-оксадиазол-3-ил)C1-6-алкилом, при этом оксадиазолильная группа необязательно замещена C1-6-алкилом или С3-6-циклоалкилом, или 5-6-членным азотсодержащим циклом, необязательно замещенным фенилом или C1-6-алкилом. А вместе с атомами углерода 5 и 6 предпочтительно образует тиено[3,2-е] -цикл или пирроло[3,2-е]-цикл, тиофен, имидазол, тиазол, пиразол, изоксазол или изотиазол, пиразино[2,3-е]-, пиримидо[4,5-е]-, пиримидо[5,4-е]-, пиридазино[4,5-е]- или пиридазино[4,3-е]-цикл, тиопиран, пиперидин, диоксан, оксазин или дитиан. Предпочтительными соединениями данного изобретения являются 7-циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид; 7-циано-6-метил-3-пропиламино-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-изопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-метилгептил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-этилпентил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(2-метилбутил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-метилгексил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклогексилметиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; этил-3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е]-1  6,2,4-тиадиазин-3-иламино)бутаноат; 6,2,4-тиадиазин-3-иламино)бутаноат;3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3, 2-е] -1  6,2, 4-тиадиазин-3-иламино)масляная кислота; 6,2, 4-тиадиазин-3-иламино)масляная кислота;6-хлор-3-(3-гидрокси-1-метилпропил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; (R)-6-хлор-3-(фенилэтил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; (S)-3-втор-бутиламино-6-хлор-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-изопропиламино-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклопентиламино-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-бром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-фтор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-циклобутиламино-5,6-диметил-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 3-циклопентиламино-5,6-диметил-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-изопропиламино-6,7-диметил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид; 3-циклобутиламино-6,7-диметил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид; 3-циклопентиламино-6,7-диметил-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-3-пропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-6-метил-3-изопропиламино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-изопропиламино-5-метил-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклопентиламино-5-метил-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-фтор-3-пропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-фтор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-фтор-3-пропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-фтор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-изопропиламино-7-метил-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклобутиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(2-гидроксиэтил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; (  )-3-экзо-бицикло[2.2.1]гепт-2-иламино-6-хлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; )-3-экзо-бицикло[2.2.1]гепт-2-иламино-6-хлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид;(R)-6-хлор-3-(2-гидроксипропил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-бром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5,6-дибром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклогексиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(фуран-2-илметил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-этилпропил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-бром-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(2-метилаллил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид или 6-циано-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид. Соединения настоящего изобретения взаимодействуют с калиевыми каналами и, следовательно, действуют как открывающие вещества или как блокаторы КАТФ-регулируемых калиевых каналов, что делает их полезным при лечении различных заболеваний сердечно-сосудистой системы, например церебральной ишемии, гипертензии, ишемической болезни сердца, стенокардии и коронарной болезни сердца; заболеваний легочной системы; желудочно-кишечной системы; церебральной нервной системы и эндокринной системы. Так как некоторые КАТФ-открывающие вещества способны бороться с вазоспазмами в базилярных и церебральных артериях, то соединения настоящего изобретения можно использовать для лечения вазоспазматических нарушений, таких как субарахноидальное кровоизлияние и мигрень. Соединения настоящего изобретения можно также применять для лечения заболеваний, связанных с пониженным кровотоком скелетных мышц, таких как болезнь Рейно и перемежающаяся хромота. Кроме того, соединения настоящего изобретения можно также применять для лечения хронических заболеваний дыхательных путей, включая астму, и для лечения нестабильности мышц (detrusor muscle instability), производной синдрома инфравезикальной обструкции, а следовательно, камней в почках, способствуя их прохождению через мочеиспускательный канал. Соединения настоящего изобретения можно также применять для лечения симптомов, связанных с нарушениями желудочно-кишечной мобильности, таких как синдром раздраженной толстой кишки. Кроме того, соединения можно применять для предотвращения преждевременных родов и лечения дисменореи. Вещества, открывающие калиевые каналы, гиперполяризуют нейроны и ингибируют выделение нейротрансмиттеров, и ожидается, что такие соединения можно применять для лечения различных заболеваний центральной нервной системы, например эпилепсии, ишемии и нейродегенеративных заболеваний, и для устранения боли. Кроме того, вещества, открывающие калиевые каналы, промотируют рост волос, следовательно, соединения настоящего изобретения можно применять для лечения облысения. Также вещества, открывающие калиевые каналы, расслабляют гладкие мышцы, следовательно, соединения настоящего изобретения можно применять для лечения недержания мочи. При таких заболеваниях как гиперплазия панкреатических островков и инсулинома, при которых гиперсекреция инсулина вызывает тяжелую гипогликемию, соединения настоящего изобретения можно применять для снижения секреции инсулина. При ожирении часто встречается гиперинсулинемия и невосприимчивость к инсулину. Это состояние может вести к развитию инсулиннезависимого сахарного диабета (NIDDM). Ожидают, что вещества, открывающие калиевые каналы, и, следовательно, соединения настоящего изобретения можно применять для снижения гиперинсулинемии и тем самым предотвращать диабет и уменьшать ожирение. При явном NIDDM лечение гиперинсулинемии при помощи веществ, открывающих калиевые каналы, и следовательно, соединений настоящего изобретения может быть полезным для восстановления чувствительности к глюкозе и нормальной секреции инсулина. В случае раннего инсулинзависимого сахарного диабета (IDDM) или преддиабетических случаях можно применять вещества, открывающие калиевые каналы, и, следовательно, соединения настоящего изобретения для индуцирования покоя панкреатических клеток, что может предотвратить развитие аутоиммунного заболевания. Вещества настоящего изобретения, открывающие калиевые каналы, можно принимать в комбинации с иммуносупрессантом или агентом типа никотинамида, который будет снижать аутоиммунную дегенерацию бета-клеток. Объединение покоя бета-клеток с лечением, защищающим бета-клетки против цитокин-опосредованной бета-клеточной недостаточности/цитотоксичности, является еще одним аспектом данного изобретения. Инсулиновая зависимость или диабет типа 1 (IDDM), а также последующий приступ IDDM (известный также как тип 1,5, например, пациенты с инсулиннезависимым диабетом типа 2 (NIDDM) с аутореактивностью против эпитопов бета-клеток, что затем вызывает инсулиновую зависимость) имеют циркулирующие аутореактивные моноциты/лимфоциты, которые возвращаются к островкам/бета-клеткам и выделяют свои цитокины. Некоторые из этих цитокинов (например, интерлейкин-l  (IL-1 (IL-1 ), фактор а некроза опухоли (TNFa) и интерферон ), фактор а некроза опухоли (TNFa) и интерферон  (IFN (IFN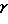 ) являются специфически токсичными относительно бета-клеток, например, через индуцирование оксида азота (NO) и других свободных радикалов. Ингибирование такой цитотоксичности, например, посредством введения никотинамида (NA), его производных или других цитокинзащитных соединений преддиабетическим/диабетическим пациентам, принимающим лечение РСО-соединением, является примером данного аспекта изобретения. Никотинамид принадлежит к семейству В-витаминов и является производным никотиновой кислоты в результате амидирования карбоксильной группы. Он не влияет на фармакологические свойства никотина. NA превращается в NAD+, который действует как коэнзим для белков, включенных в тканевое дыхание. Предполагают, что NA влияет на многие предполагаемые внутриклеточные молекулярные процессы после иммунной атаки на бета-клетки. Эксперименты на животных и ранние неслепые эксперименты на людях показали защитную роль такого соединения против IDDM, а также в цитокин/иммунно-опосредованной деструкции бета-клеток.
Еще один аспект данной заявки касается применения РСО-соединения, самого по себе или в комбинации с ингибитором цитокин/иммунно-опосредованного повреждения бета-клеток, при трансплантации, например, островковой трансплантации у диабетических пациентов. Применение одного или обоих из этих способов лечения может снизить риск отторжения трансплантированных островков/бета-клеток/поджелудочной железы.
Соединения настоящего изобретения, которые действуют как блокаторы КАТФ-каналов, можно применять для лечения NIDDM.
Предпочтительно соединения настоящего изобретения можно применять для лечения или профилактики заболеваний эндокринной системы, таких как гиперинсулинемия и диабет.
Таким образом, другой аспект данного изобретения касается соединения общей формулы I или его фармацевтически приемлемой соли присоединения кислоты для применения в качестве терапевтически приемлемого вещества, предпочтительно для применения в качестве терапевтически приемлемого вещества при лечении гиперинсулинемии или при лечении или профилактике диабета.
Кроме того, данное изобретение касается также применения заявленных соединений формулы I в виде лекарственных средств, полезных для лечения гиперинсулинемии или для лечения или профилактики диабета.
Еще в одном аспекте настоящее изобретение касается способов получения указанных выше соединений. Эти способы включают ) являются специфически токсичными относительно бета-клеток, например, через индуцирование оксида азота (NO) и других свободных радикалов. Ингибирование такой цитотоксичности, например, посредством введения никотинамида (NA), его производных или других цитокинзащитных соединений преддиабетическим/диабетическим пациентам, принимающим лечение РСО-соединением, является примером данного аспекта изобретения. Никотинамид принадлежит к семейству В-витаминов и является производным никотиновой кислоты в результате амидирования карбоксильной группы. Он не влияет на фармакологические свойства никотина. NA превращается в NAD+, который действует как коэнзим для белков, включенных в тканевое дыхание. Предполагают, что NA влияет на многие предполагаемые внутриклеточные молекулярные процессы после иммунной атаки на бета-клетки. Эксперименты на животных и ранние неслепые эксперименты на людях показали защитную роль такого соединения против IDDM, а также в цитокин/иммунно-опосредованной деструкции бета-клеток.
Еще один аспект данной заявки касается применения РСО-соединения, самого по себе или в комбинации с ингибитором цитокин/иммунно-опосредованного повреждения бета-клеток, при трансплантации, например, островковой трансплантации у диабетических пациентов. Применение одного или обоих из этих способов лечения может снизить риск отторжения трансплантированных островков/бета-клеток/поджелудочной железы.
Соединения настоящего изобретения, которые действуют как блокаторы КАТФ-каналов, можно применять для лечения NIDDM.
Предпочтительно соединения настоящего изобретения можно применять для лечения или профилактики заболеваний эндокринной системы, таких как гиперинсулинемия и диабет.
Таким образом, другой аспект данного изобретения касается соединения общей формулы I или его фармацевтически приемлемой соли присоединения кислоты для применения в качестве терапевтически приемлемого вещества, предпочтительно для применения в качестве терапевтически приемлемого вещества при лечении гиперинсулинемии или при лечении или профилактике диабета.
Кроме того, данное изобретение касается также применения заявленных соединений формулы I в виде лекарственных средств, полезных для лечения гиперинсулинемии или для лечения или профилактики диабета.
Еще в одном аспекте настоящее изобретение касается способов получения указанных выше соединений. Эти способы включаюта) реакцию соединения формулы II 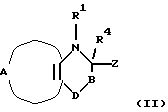 где А, В, D, R1 и R4 такие, как определено выше, и Z представляет отщепляемую группу, такую как алкоксигруппа, алкилтиогруппа, галоген, предпочтительно хлор, бром, йод, триметиламиногруппа или метилсульфонил, с соединением формулы III 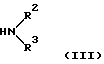 где R2 и R3 определены выше, с образованием соединения общей формулы I; б) реакцию соединения формулы IV 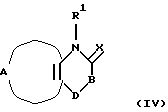 где R1 представляет водород, и А, В, D и Х такие, как определено выше, или В представляет NH и R1, A, D и Х такие, как определено выше, с соединением формулы III или его подходящей солью в присутствии Р2O5 и высококипящего третичного амина или его подходящей соли с образованием соединения общей формулы I; с) реакцию соединения формулы IV 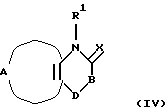 где R1 представляет водород и А, В, D и Х такие, как определено выше, или В представляет NH и R1, А, D и Х такие, как определено выше, с соединением формулы III или его подходящей солью в присутствии тетрахлорида титана и растворителя, с которым он может образовывать комплекс, такого как, например, тетрагидрофуран или смесь толуола и анизола, с образованием соединения общей формулы I; г) реакцию соединения формулы V 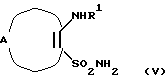 где R1 и А такие, как определено выше, с соединением формулы IV R3NCO, где R3 такой, как определено выше, с образованием соединения общей формулы I, где D представляет SO2, В представляет >NR5, R2 представляет Н, и R4 и R5 вместе образуют связь; д) реакцию соединения формулы V 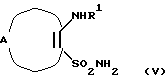 где R1 и А такие, как определено выше, с соединением формулы VII R3NНC(=O)Cl (VII), где R3 определен выше, с образованием соединения общей формулы I, где D представляет SO2, В представляет >NR5, R2 представляет Н, и R4 и R5 вместе образуют связь; е) реакцию соединения формулы V 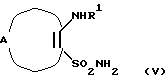 где R1 и А такие, как определено выше, с соединением формулы VIII 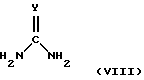 где Y представляет NH или S, или его подходящей солью с образованием соединения общей формулы I, где D представляет SO2, В представляет >NR5, R4 и R5 вместе образуют связь, и R2 и R3 представляют Н; ж) реакцию соединения формулы IX 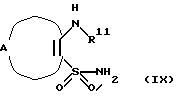 или его подходящей соли, где R11 представляет R1 или EtOC(=O), где R1 и А такие, как определено выше, с соединением формулы Х R3N=C=S (X), где R3 такой, как определено выше, с образованием аддукта, который может иметь любую из двух структур XI или XII или представлять смесь обоих 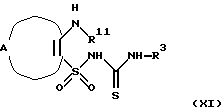 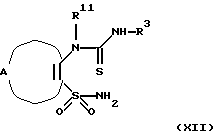 любая из которых при замыкании цикла, например, при обработке фосгеном в подходящем растворителе, образует соединение общей формулы I, если R11 представляет R1, где D представляет S(=O)2, В представляет >NR5, R2 представляет Н и R4 и R5 вместе образуют связь, и соединение общей формулы XIII, если R11 представляет EtOC(=O); 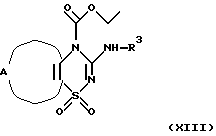 з) гидролиз и последующее декарбоксилирование соединения общей формулы XIII 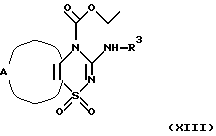 с образованием соединения общей формулы I, где D представляет S(=O)2, В представляет >NR5, R1 и R2 представляет Н и R4 и R5 вместе образуют связь, например, при нагревании исходного соединения в водном основании. Исходные материалы являются либо известными соединениями, либо соединениями, которые можно получить по аналогии с получением известных соединений или по аналогии с известными способами, как описано, например, в работах Huang B.-S. и др., J. Med. Chem., 23, 575-7 (1980), Ofitserov V.I. и др. , Khim. Geterotsiki. Soedin., 1119-22 (русск.) (1976), Torliss J.G., US 3641017 (1972), Kotovskaya S.K. и др., Khim-Farm. Zh., 13, 54-57 (русск.) (1979), Meyer R. F. , J. Heterocycl. Chem., 6, 407-408 (1969), Hattori M., Yoneda M. и Goto M., Bull. Chem. Soc. Jap., 46, 1890-1 (1973), Williams T.R. и Cram D.J., J. Org. Chem., 38, 20-26 (1973), Barnes А.С., Kennewell P.D. И Taylor J.B., J. Chem. Soc. Chem. Commun., 1973, 776-777, Stoss и Satzinger, Chem. Ber., 109., 2097 (1976), Kresze G., Hatjiissaak A., Phosphorus Sulfur, 29, 41-47 (1987), Dillard R. D., Yen T.T., Stark P., Pavey D.E., J. Med. Chem., 23, 717-722 (1980). ФАРМАКОЛОГИЧЕСКИЕ СПОСОБЫ Способность соединений взаимодействовать с калиевыми каналами можно определить различными способами. Если применяют методику с повязкой-зажимом (patch-clamp) (Hamin О.Р., Marty A., Neher E., Sakmann В. и Sigworth F.J., Plugers Arch., 391, 85-100 (1981)), то можно регистрировать ионный ток через отдельный канал клетки. Активность данных соединений в качестве веществ, открывающих калиевые каналы, можно измерять как релаксацию колец аорты крысы в соответствии со следующей процедурой. Вырезают секцию крысиной грудной аорты между дугой аорты и диафрагмой и готовят препараты для исследования в виде колец, как описано у Taylor P.D. и др., Britt. J. Pharmacol., 111, 42-48 (1994). Через 45 минут установления равновесия при натяжении 2 г осуществляют сокращение препаратов, достигая 80% максимального отклика, используя необходимую концентрацию фенилэфрина. Когда реакция на фенилэфрин достигает плато, добавляют к бане сильнодействующие сосудорасширяющие агенты, кумулятивно небольшими объемами, используя полулогарифмические молярные инкременты с интервалом 2 минуты. Релаксацию выражают в процентах от растяжения при сокращении (contracted tension). Возможность соединения выражают как концентрацию, необходимую для достижения 50% релаксации ткани. Релаксация колец крысиной аорты Пример – ЭК50 микро М 4 – 2,8 6 – 20,5 В  -клетке поджелудочной железы можно определить открытие КАТФ-каналов, измеряя последующее изменение концентрации свободного Са2+ в цитоплазме согласно способу Arkhammar P. и др., J. Biol. Chem., 262, 5448-5454 (1987).
Отток 86Rb+ из -клетке поджелудочной железы можно определить открытие КАТФ-каналов, измеряя последующее изменение концентрации свободного Са2+ в цитоплазме согласно способу Arkhammar P. и др., J. Biol. Chem., 262, 5448-5454 (1987).
Отток 86Rb+ из  -клеточной линии -клеточной линииКлеточную линию RIN 5F культивируют в питательной среде RPMI 1640 с Glutamax I, снабженной 10% сывороткой плода коровы (от GibcoBRL, Scotland, UK), поддерживая в атмосфере 5% СO2/95% воздуха при 37oС. Клетки отделяют раствором Трипсин-ЭДТА (от GibcoBRL, Scotland, UK), ресуспендируют в питательной среде, добавляют 1 милликюри/мл 86Rb+ и повторно высевают в пластины для микротитрования (набор 3596 на 96 ячеек, стерильный, от Costar Corporation, MA, USA) при плотности 50000 клеток/ячейка в 100  л/ячейка и культивируют 24 часа перед использованием в исследовании.
Пластины промывают 4 раза буфером Рингера (Ringer) (150 мМ NaCl, 10 мМ Hepes, 3,0 мМ КСl 1,0 мМ CaCl2, 20 мМ сахарозы, рН 7,1). Добавляют 80 л/ячейка и культивируют 24 часа перед использованием в исследовании.
Пластины промывают 4 раза буфером Рингера (Ringer) (150 мМ NaCl, 10 мМ Hepes, 3,0 мМ КСl 1,0 мМ CaCl2, 20 мМ сахарозы, рН 7,1). Добавляют 80  л буфера Рингера и 1 л буфера Рингера и 1  л контрольного или исследуемого соединения, растворенного в ДМСО. После инкубации с крышкой в течение 1 часа при комнатной температуре переносят 50 л контрольного или исследуемого соединения, растворенного в ДМСО. После инкубации с крышкой в течение 1 часа при комнатной температуре переносят 50  л супернатанта в PicoPlates (Packard Instrument Company, CT, USA) и добавляют 100 л супернатанта в PicoPlates (Packard Instrument Company, CT, USA) и добавляют 100  л MicroScint40 (Packard Instrument Company, CT, USA). Пластины считают в TopCount (Packard Instrument Company, CT, USA) в течение 1 мин/ячейка по программе 32P.
Расчет ЭК50 и Емакс производят посредством SlideWrite (Advanced Graphics Software, Inc., CA, USA), используя расчетный график с четырьмя параметрами: у = (а-d)/(1+(х/с)b)+d, где а = активность, определенная при нулевой концентрации, b = угловой коэффициент, с = концентрация на середине кривой и d = активность, определенная при очень больших концентрациях.
Повышенный Rb-отток в клетках RIN 5F л MicroScint40 (Packard Instrument Company, CT, USA). Пластины считают в TopCount (Packard Instrument Company, CT, USA) в течение 1 мин/ячейка по программе 32P.
Расчет ЭК50 и Емакс производят посредством SlideWrite (Advanced Graphics Software, Inc., CA, USA), используя расчетный график с четырьмя параметрами: у = (а-d)/(1+(х/с)b)+d, где а = активность, определенная при нулевой концентрации, b = угловой коэффициент, с = концентрация на середине кривой и d = активность, определенная при очень больших концентрациях.
Повышенный Rb-отток в клетках RIN 5FПример – ЭК50 микро М 4 – 5,5 6 – 31 Соединения данного изобретения эффективны при дозировке в широком диапазоне. В основном, удовлетворительные результаты получают при дозировке примерно от 0,05 до 1000 мг, предпочтительно примерно от 0,1 до 500 мг, в день. Наиболее предпочтительная доза составляет примерно от 1 до 100 мг в день. Точная доза будет зависеть от способа приема, принимаемой формы, пациента, подлежащего лечению, веса тела подлежащего лечению пациента и предпочтений и опыта лечащего врача или ветеринара. Способ приема может быть любым способом, который эффективно доставляет активное соединение к подходящему или необходимому месту действия, таким как оральный способ или парентеральный, например ректальный, трансдермальный, подкожный, внутривенный, внутримышечный или внутриносовой, при этом предпочтителен оральный способ приема. Типичные композиции включают соединение формулы I или его фармацевтически приемлемую соль присоединения кислоты вместе с фармацевтически приемлемым наполнителем, который может быть носителем или разбавителем, или это соединение можно разбавить носителем, или можно заключить внутрь носителя, который может представлять собой капсулу, саше, бумажку или другой контейнер. При составлении композиций можно использовать любую технологию для получения фармацевтических композиций. Например, активное соединение обычно смешивают с носителем или разбавляют носителем, или заключают внутрь носителя, который может представлять собой ампулу, капсулу, саше, бумажку или другой контейнер. Если носитель служит в качестве разбавителя, он может быть твердым, полутвердым или жидким материалом, который действует в качестве носителя, наполнителя или среды для активного соединения. Активное соединение может быть адсорбировано на гранулярном твердом контейнере, например, в саше. Некоторыми примерами подходящих носителей являются вода, раствор соли, спирты, полиэтиленгликоли, полигидроксиэтоксилироованное касторовое масло, желатин, лактоза, амилоза, стеарат магния, тальк, кремниевая кислота, моноглицериды жирных кислот и поливинилпирролидон. Препараты могут также включать смачивающие агенты, эмульгаторы и суспендирующие агенты, консерванты, подслащающие агенты или ароматизаторы. Препараты данного изобретения можно составить таким образом, чтобы обеспечить быстрое, длительное или замедленное выделение активного ингредиента после введения пациенту, применяя хорошо известные специалистам процедуры. Фармацевтические препараты можно стерилизовать и смешать, если требуется, со вспомогательными агентами, эмульгаторами, солями, влияющими на осмотическое давление, буферами и/или подкрашивающими веществами и подобными материалами, которые не вступают во вредные взаимодействия с активными соединениями. Для парентерального применения особенно подходят растворы или суспензии для инъекций, преимущественно водные растворы с активным соединением, растворенным в полигидроксилированном касторовом масле. Для орального применения особенно подходят таблетки, драже или капсулы, имеющие тальк и/или карбогидрат в качестве носителя, связующего или подобного. Предпочтительные носители для таблеток, драже или капсул включают лактозу, кукурузный крахмал и/или картофельный крахмал. В случаях, когда можно применять подслащенный носитель, можно использовать сироп или эликсир. Обычно соединения распределяют в виде стандартных форм, примерно по 1-100 мг на стандартную дозированную форму в фармацевтически приемлемом носителе. Типичная таблетка, подходящая для использования в данном способе, может быть приготовлена обычными способами таблетирования и содержит: Активное соединение – 5,0 мг Лактоза (Lactosum) – 67,8 мг Ph.Eur. Avicel  – 31,4 мг – 31,4 мгAmberlite  – 0,25 мг Ph.Eur.
ПРИМЕРЫ – 0,25 мг Ph.Eur.
ПРИМЕРЫДалее способ получения соединений формулы I проиллюстрирован следующими примерами, которые, однако, не являются ограничительными. ПРИМЕР 1 7-Циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксан а) 4-Циано-2-гидразинокарбонил-5-метилтиофен-3-сульфонамид Метил-4-циано-5-метил-3-сульфамоилтиофен-2-карбоксилат (2,9 г), полученный из метил-3-амино-4-циано-5-метилтиофен-2-карбоксилата по аналогии с известными процедурами, например работы F. Junquera и др., Eur. J. Med. Chem. , 23, 329 (1988), суспендируют в 10 мл этанола. Добавляют гидразинмоногидрат (2 мл) и смесь перемешивают в течение 1 часа при комнатной температуре, а затем выпаривают. Маслянистый остаток (3,3 г) растирают с 10 мл воды и осадившиеся кристаллы собирают фильтрованием, промывают водой и сушат, получая желтые кристаллы указанного в заголовке соединения (выход 1,63 г); т.пл. 186-191oС. 1H ЯМР (ДМСО-d6),  (м. д. ): 7,25 (широкий, 5Н, NH/NH2), 2,51 (с, 3Н, СН3).
б) 4-Циано-5-метил-3-сульфамоилтиофен-2-карбонилазид (м. д. ): 7,25 (широкий, 5Н, NH/NH2), 2,51 (с, 3Н, СН3).
б) 4-Циано-5-метил-3-сульфамоилтиофен-2-карбонилазидРаствор нитрита натрия (0,47 г) в 5 мл воды добавляют по капле к перемешиваемому раствору 4-циано-2-гидразинокарбонил-5-метилтиофен-3-сульфонамида (1,6 г) в 38 мл 1 М соляной кислоты при 0oС. Полученную смесь перемешивают в течение 30 минут при 0oС и затем фильтруют. Остаток на фильтре промывают водой и сушат в вакууме, получая 1,35 г указанного в заголовке соединения. 1H ЯМР (ДМСО-d6),  (м.д.): 7,75 (широкий, 1Н, NH2), 2,75 (с, 1Н, СН3).
в) 4-Циано-2-этоксикарбониламино-5-метилтиофен-3-сульфонамид (м.д.): 7,75 (широкий, 1Н, NH2), 2,75 (с, 1Н, СН3).
в) 4-Циано-2-этоксикарбониламино-5-метилтиофен-3-сульфонамид4-Циано-5-метил-3-сульфамоилтиофен-2-карбонилазид (1,35 г) добавляют небольшими порциями за 5 минут к 50 мл абсолютного этанола при температуре кипения с обратным холодильником. Полученный раствор кипятят с обратным холодильником в течение 5 минут затем выпаривают. Затем кристаллизовавшийся остаток растирают с 20 мл этилацетата. Кристаллы отфильтровывают, промывают этилацетатом и сушат, получая указанное в заголовке соединение. 1H ЯМР (ДМСО-d6),  (м.д.): 9,45 (широкий, 1Н, NH) 7,82 (широкий, 2Н, NH2), 4,23 (квартет, 2Н, СН2), 2,51 (с, 3Н, СН3), 1,25 (т, 3H, CH3).
г) N-(4-Циано-2-этоксикарбониламино-5-метил-3-тиенилсульфонил)-N’-изопропилтиомочевина (м.д.): 9,45 (широкий, 1Н, NH) 7,82 (широкий, 2Н, NH2), 4,23 (квартет, 2Н, СН2), 2,51 (с, 3Н, СН3), 1,25 (т, 3H, CH3).
г) N-(4-Циано-2-этоксикарбониламино-5-метил-3-тиенилсульфонил)-N’-изопропилтиомочевинаСмесь 4-циано-2-этоксикарбониламино-5-метилтиофен-3-сульфонамида (0,50 г), карбонат калия (0,36 г) и изопропилизотиоцианата (300  л) в 10 мл сухого ацетона нагревают при 55oС в течение 18 часов и затем выпаривают до сухости. Остаток растворяют в 10 мл воды и доводят рН до 2, добавляя по капле 1 М соляную кислоту. Осадок отфильтровывают, промывают небольшим количеством воды и сушат, получая 0,34 г указанного в заголовке соединения; т.пл. 169-171oС.
д) Этил-7-циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е]-1,2,4-тиадиазин-4-карбоксилат 1,1-диоксид л) в 10 мл сухого ацетона нагревают при 55oС в течение 18 часов и затем выпаривают до сухости. Остаток растворяют в 10 мл воды и доводят рН до 2, добавляя по капле 1 М соляную кислоту. Осадок отфильтровывают, промывают небольшим количеством воды и сушат, получая 0,34 г указанного в заголовке соединения; т.пл. 169-171oС.
д) Этил-7-циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е]-1,2,4-тиадиазин-4-карбоксилат 1,1-диоксидК перемешиваемому раствору N-(4-циано-2-этоксикарбониламино-5-метил-3-тиенилсульфонил)-N’-изопропилтиомочевины (0,3 г) и триэтиламина (320  л) в 10 мл сухого ТГФ при 0oС добавляют 750 л) в 10 мл сухого ТГФ при 0oС добавляют 750  л 20% раствора фосгена в толуоле. Смесь перемешивают при 0oС в течение 1 часа и затем выпаривают до сухости. Остаток растирают с 10 мл воды, отфильтровывают, промывают на фильтре водой и сушат, получая 0,24 г сырого соединения, указанного в заголовке; т.пл. 116-119oС. Продукт используют для следующей стадии без очистки.
е) 7-Циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид л 20% раствора фосгена в толуоле. Смесь перемешивают при 0oС в течение 1 часа и затем выпаривают до сухости. Остаток растирают с 10 мл воды, отфильтровывают, промывают на фильтре водой и сушат, получая 0,24 г сырого соединения, указанного в заголовке; т.пл. 116-119oС. Продукт используют для следующей стадии без очистки.
е) 7-Циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксидСмесь 7-циано-3-изопропиламино-6-метил-4Н-тиено[2,3-е] -1,2,4-тиадиазин-4-карбоксилат 1,1-диоксида (0,15 г) и 5 мл 1 М водного гидроксида натрия перемешивают при комнатной температуре течение 1 часа. Затем смесь фильтруют и доводят рН до 1-2, добавляя по капле 4 М соляную кислоту. После перемешивания в течение 30 минут осадок отфильтровывают, промывают небольшим количеством воды и сушат, получая указанное в заголовке соединение; т.пл. 235-238oС. 1Н ЯМР (ДМСО-d6),  (м.д.): 11,35 (с, 1Н, NH), 7,55 (широкий д, 1Н, NH), 3,98-3,77 (м, 1Н, СН), 2,50 (с, 1Н, СН3), 1,15 (д, 6Н, СН3).
ПРИМЕР 2 (м.д.): 11,35 (с, 1Н, NH), 7,55 (широкий д, 1Н, NH), 3,98-3,77 (м, 1Н, СН), 2,50 (с, 1Н, СН3), 1,15 (д, 6Н, СН3).
ПРИМЕР 27-Циано-6-метил-3-пропиламино-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид a) N-(4-Циано-2-этоксикарбониламино-5-метил-3-тиенилсульфонил)-N’-пропилтиомочевина Указанное в заголовке соединение получают из 4-циано-2-этоксикарбониламино-5-метилтиофен-3-сульфонамида и пропилизотиоцианата по аналогии с синтезом, описанным в примере 1-г; т.пл. 167-168oС. б) Этил-7-циано-6-метил-3-пропиламино-4Н-тиено[2,3-е]-1,2,4-тиадиазин-4-карбоксилат 1,1-диоксид Указанное в заголовке соединение получают из N-(4-циано-2-этоксикарбониламино-5-метил-3-тиенилсульфонил)-N’-пропилтиомочевины по аналогии с процедурой, описанной в примере 1-д; т.пл. 175-179oС. в) 7-Циано-6-метил-3-пропиламино-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид Указанное в заголовке соединение получают путем гидролиза и последующего декарбоксилирования этил-7-циано-6-метил-3-пропиламино-4Н-тиено[2,3-е]-1,2, -тиадиазин-4-карбоксилат 1,1-диоксида по аналогии с синтезом, описанным в примере 1-е; т.пл. 293-298oС. 1H ЯМР (ДМСО-d6),  (м.д.): 11,6 (с, 1Н, NH), 7,65 (широкий, 1Н, NH), 3,14 (дд, 2Н, СН2), 2,58 (с, 1Н, СН3), 1,65-1,4 (м, 2Н, СН2), 0,89 (т, 3Н, СН3).
ПРИМЕР 3 (м.д.): 11,6 (с, 1Н, NH), 7,65 (широкий, 1Н, NH), 3,14 (дд, 2Н, СН2), 2,58 (с, 1Н, СН3), 1,65-1,4 (м, 2Н, СН2), 0,89 (т, 3Н, СН3).
ПРИМЕР 36-Хлор-3-(3-метилбутил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1- диоксид a) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(3-метилбутил)тиомочевина Трет-бутоксид калия (0,49 г, 4,4 ммоль) добавляют к раствору 5-амино-5-хлортиофен-2-сульфонамида (5 мл) при перемешивании на бане со льдом. Через 10 минут к полученной суспензии добавляют по капле 3-метилбутилизотиоцианат (0,31 г, 2,4 ммоль) и смесь перемешивают при 0-20oС в течение 3,5 часов. Большую часть растворителя выпаривают при 40oС и остаток помещают в 25 мл воды, обрабатывают обесцвечивающим углем и фильтруют. Подкисление фильтрата уксусной кислотой до рН 3-4 и фильтрование дают 0,21 г указанного в заголовке соединения; т.пл. 114-115oС (разлагается). 1H ЯМР (ДМСО-d6),  (м. д.): 0,85 (д, 6Н, 2хСН3), 1,40 (квартет, 2Н, СН2), 1,50 (м, 1Н, СН), 3,45 (квартет, 2Н, CH2), 6,45 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,30 (широкий т, 1H, NH), 11,3 (шир. c, 1H).
б) 6-Хлор-3-(3-метилбутил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м. д.): 0,85 (д, 6Н, 2хСН3), 1,40 (квартет, 2Н, СН2), 1,50 (м, 1Н, СН), 3,45 (квартет, 2Н, CH2), 6,45 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,30 (широкий т, 1H, NH), 11,3 (шир. c, 1H).
б) 6-Хлор-3-(3-метилбутил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидФосген (0,242 мл, 20% в толуоле) добавляют к раствору N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(3-метилбутил)тиомочевины (0,153 г, 0,42 ммоль) и сухого триэтиламина (0,118 мл, 0,85 ммоль) в сухом тетрагидрофуране (3 мл) при перемешивании при 0oС. Смесь перемешивают в течение 2 часов при 0oС и выпаривают до сухости. Проводят кристаллизацию из этилацетата и осадок выделяют фильтрованием, промывают водой и сушат, получая 38 мг (27%) указанного в заголовке соединения; т.пл. 230-231oС. 1H ЯМР (ДМСО-d6),  (м.д.): 0,90 (д, 6Н, 2хСН3), 1,40 (квартет, 2Н, СН2), 1,60 (м, 1Н, СН), 3,20 (квартет, 2Н, CH2), 7,05 (с, 1Н, Н-5), 7,25 (широкий с, 1Н, NH), 10,95 (с, 1Н, NH).
Масс-спектр: m/е 307 (М+).
ПРИМЕР 4 (м.д.): 0,90 (д, 6Н, 2хСН3), 1,40 (квартет, 2Н, СН2), 1,60 (м, 1Н, СН), 3,20 (квартет, 2Н, CH2), 7,05 (с, 1Н, Н-5), 7,25 (широкий с, 1Н, NH), 10,95 (с, 1Н, NH).
Масс-спектр: m/е 307 (М+).
ПРИМЕР 46-Хлор-3-(1-метилгептил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(3-метилгептил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и 1-метилгептилизотиоцианата по аналогии с процедурой, описанной в примере 3-а; получают сироп (выход 29%). 1H ЯМР (ДМСО-d6),  (м.д.): 0,90 (т, 3Н, СН3), 1,10 (д, 3Н, СН3), 1,25 (м, 8Н), 1,47 (квинтет, 1Н, СН), 6,5 (широкий с, 2Н, NH2), 6,65 (с, 1Н, Н-4), 7,95 (широкий, 1Н, NH), 11,2 (широкий, с, 1Н).
б) 6-Хлор-3-(1-метилгептил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м.д.): 0,90 (т, 3Н, СН3), 1,10 (д, 3Н, СН3), 1,25 (м, 8Н), 1,47 (квинтет, 1Н, СН), 6,5 (широкий с, 2Н, NH2), 6,65 (с, 1Н, Н-4), 7,95 (широкий, 1Н, NH), 11,2 (широкий, с, 1Н).
б) 6-Хлор-3-(1-метилгептил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(1-метилгептил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 71%); т.пл. 179-181oС. 1H ЯМР (ДМСО-d6),  (м.д.): 0,85 (т, 3Н, СН3), 1,15 (д, 3Н, СН3), 1,30 (м, 8Н), 1,45 (м, 2Н, СН2), 3,75 (квинтет, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,10 (широкий с, 1Н, NH), 10,65 (с, 1Н, NH).
Масс-спектр: m/е 349 (М+).
ПРИМЕР 5 (м.д.): 0,85 (т, 3Н, СН3), 1,15 (д, 3Н, СН3), 1,30 (м, 8Н), 1,45 (м, 2Н, СН2), 3,75 (квинтет, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,10 (широкий с, 1Н, NH), 10,65 (с, 1Н, NH).
Масс-спектр: m/е 349 (М+).
ПРИМЕР 56-Хлор-3-(1-этилпентил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(3-этилпентил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и 1-этилпентилизотиоцианата по аналогии с процедурой, описанной в примере 3-а; получают сироп (выход 36%). lH ЯМР (ДМСО-d6),  (м.д.): 0,8 (2 квартета, 6Н, 2хСН3), 1,2 (м, 4Н), 1,5 (м, 4Н), 4,20 (секстет, 1Н, СН), 6,55 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 7,85 (широкий д, 1Н, NH), 11,3 (широкий с, 1Н, NH).
б) 6-Хлор-3-(1-этилпентил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м.д.): 0,8 (2 квартета, 6Н, 2хСН3), 1,2 (м, 4Н), 1,5 (м, 4Н), 4,20 (секстет, 1Н, СН), 6,55 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 7,85 (широкий д, 1Н, NH), 11,3 (широкий с, 1Н, NH).
б) 6-Хлор-3-(1-этилпентил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(3-этилпентил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 35%); т.пл. 165-167,5oС. 1H ЯМР (ДМСО-d6),  (м.д.): 0,85 (2 квартета, 6Н, 2хСН3), 1,25 (м, 4Н), 3,65 (м, 1Н, СН), 7,0 (широкий, 1Н, NH), 7,05 (с, 1Н, Н-5), 10,65 (широкий с, 1Н, NH).
Масс-спектр: m/е 335 (М+).
ПРИМЕР 6 (м.д.): 0,85 (2 квартета, 6Н, 2хСН3), 1,25 (м, 4Н), 3,65 (м, 1Н, СН), 7,0 (широкий, 1Н, NH), 7,05 (с, 1Н, Н-5), 10,65 (широкий с, 1Н, NH).
Масс-спектр: m/е 335 (М+).
ПРИМЕР 66-Хлор-3-(2-метилбутил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(3-метилбутил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и 2-метилбутил изотиоцианата по аналогии с процедурой, описанной в примере 3-а (выход 28%); т.пл. 116,5-118oС. 1H ЯМР (ДМСО-d6),  (м.д.): 0,8 (2 д, 6Н, 2хСН3), 1,10 (м, 1Н), 1,30 (м, 1Н), 1,65 (м, 1Н), 3,40 (м, 2Н + HDO, CH2), 6,45 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,25 (широкий т, 1Н, NH), 11,3 (широкий с, 1Н).
б) 6-Хлор-3-(2-метилбутил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м.д.): 0,8 (2 д, 6Н, 2хСН3), 1,10 (м, 1Н), 1,30 (м, 1Н), 1,65 (м, 1Н), 3,40 (м, 2Н + HDO, CH2), 6,45 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,25 (широкий т, 1Н, NH), 11,3 (широкий с, 1Н).
б) 6-Хлор-3-(2-метилбутил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(3-метилбутил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 39%); т.пл. 232-234oС. 1H ЯМР (ДМСО-d6),  (м.д.): 0,85 (2 д, 6Н, 2хСН3), 1,15 (м, 1Н), 1,40 (м, 1Н), 1,60 (м, 1Н), 3,10 (м, 2Н, СН2), 7,05 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,85 (широкий с, 1Н, NH).
Масс-спектр: m/е 307 (М+).
Элементный анализ (м.д.): 0,85 (2 д, 6Н, 2хСН3), 1,15 (м, 1Н), 1,40 (м, 1Н), 1,60 (м, 1Н), 3,10 (м, 2Н, СН2), 7,05 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,85 (широкий с, 1Н, NH).
Масс-спектр: m/е 307 (М+).
Элементный анализРассчитано для C10H14ClN3O2S2,%: С 39,02; Н 4,58; N 13,65. Найдено,%: С 38,98; Н 4,72; N 13,40. ПРИМЕР 7 6-Хлор-3-(2-метилгексил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(1-метилгексил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и 1-метилгексилизотиоцианата по аналогии с процедурой, описанной в примере 3-а; получают сироп (выход 43%). 1H ЯМР (ДМСО-d6),  (м.д.): 0,85 (т, 3Н, СН3), 1,10 (д, 3Н, СН3), 1,25 (м, 6Н), 1,45 (м, 2Н), 4,25 (м, 1Н, СН), 6,50 (шир. 2H, NH2), 6,66 (c. 1H, H-4), 7,93 (широкий, 1Н, NH), 11,3 (широкий с, 1Н, NH).
б) 6-Хлор-3-(2-метилгексил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м.д.): 0,85 (т, 3Н, СН3), 1,10 (д, 3Н, СН3), 1,25 (м, 6Н), 1,45 (м, 2Н), 4,25 (м, 1Н, СН), 6,50 (шир. 2H, NH2), 6,66 (c. 1H, H-4), 7,93 (широкий, 1Н, NH), 11,3 (широкий с, 1Н, NH).
б) 6-Хлор-3-(2-метилгексил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(1-метилгексил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 63%); т.пл. 158-162oС. 1H ЯМР (ДМСO-d6),  (м.д.): 0,85 (т, 3Н, СН3), 1,15 (д, 3Н, СН3), 1,25 (м, 6Н), 1,45 (м, 2Н), 3,45 (м, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,15 (широкий с, 1Н, NH), 10,75 (широкий с, 1Н, NH).
Масс-спектр: m/е 335 (М+).
ПРИМЕР 8 (м.д.): 0,85 (т, 3Н, СН3), 1,15 (д, 3Н, СН3), 1,25 (м, 6Н), 1,45 (м, 2Н), 3,45 (м, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,15 (широкий с, 1Н, NH), 10,75 (широкий с, 1Н, NH).
Масс-спектр: m/е 335 (М+).
ПРИМЕР 86-Хлор-3-(циклопентил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-циклопентилтиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и циклопентилизотиоцианата по аналогии с процедурой, описанной в примере 3-а (выход 46%). 1H ЯМР (ДМСО-d6),  (м. д. ): 1,30-1,70 (м, 6Н), 1,90 (м, 2Н), 4,40 (секстет, 1Н, СН), 6,55 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,15 (широкий д, 1Н, NH), 11,2 (широкий с, 1Н, NH).
б) 6-Хлор-3-(2-циклопент)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м. д. ): 1,30-1,70 (м, 6Н), 1,90 (м, 2Н), 4,40 (секстет, 1Н, СН), 6,55 (широкий, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,15 (широкий д, 1Н, NH), 11,2 (широкий с, 1Н, NH).
б) 6-Хлор-3-(2-циклопент)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(1-циклопентил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 57%); т.пл. 291-292oС. 1H ЯМР (ДМСО-d6),  (м.д.): 1,40-1,70 (м, 6Н, СН3), 1,90 (м, 2Н), 3,95 (секстет, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,3 (широкий, 1Н, NH), 10,70 (сл.с, 1Н, NH).
Масс-спектр: m/е 305 (М+).
ПРИМЕР 9 (м.д.): 1,40-1,70 (м, 6Н, СН3), 1,90 (м, 2Н), 3,95 (секстет, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,3 (широкий, 1Н, NH), 10,70 (сл.с, 1Н, NH).
Масс-спектр: m/е 305 (М+).
ПРИМЕР 96-Хлор-3-(циклогексилметил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-циклогексилметилтиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и циклогексилметилизотиоцианата по аналогии с процедурой, описанной в примере 3-а; получают сироп (выход 8%). 1H ЯМР (ДМСО-d6),  (м.д.): 0,95 (м, 2Н), 1,25 (м, 3Н), 1,70 (м, 6Н), 3,45 (д, 2Н, СН2), 4,45 (широкий, HDO+NH), 6,65 (с, 1Н, Н-4).
б) 6-Хлор-3-(циклогексилметил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м.д.): 0,95 (м, 2Н), 1,25 (м, 3Н), 1,70 (м, 6Н), 3,45 (д, 2Н, СН2), 4,45 (широкий, HDO+NH), 6,65 (с, 1Н, Н-4).
б) 6-Хлор-3-(циклогексилметил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(1-циклогексилметил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 68%); т.пл. >200oС (разлагается). 1H ЯМР (ДМСО-d6),  (м.д.): 0,90 (м, 2Н), 1,15 (м, 3Н), 1,70 (м, 6Н), 3,05 (т, 2Н, СН2), 7,05 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,95 (широкий с, 1Н, NH).
Масс-спектр: m/e 333 (М+).
ПРИМЕР 10 (м.д.): 0,90 (м, 2Н), 1,15 (м, 3Н), 1,70 (м, 6Н), 3,05 (т, 2Н, СН2), 7,05 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,95 (широкий с, 1Н, NH).
Масс-спектр: m/e 333 (М+).
ПРИМЕР 10Этил-3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е] -1  2,2,4-тиадиазин-3-иламино)бутаноат 2,2,4-тиадиазин-3-иламино)бутаноата) Этил 3-{3[(3-амино-5-хлортиен-2-ил)сульфонил]тиоуреидо}бутаноат Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и 3-изотиоцианатобутирата по аналогии с процедурой, описанной в примере 3-а (выход 93%). 1H ЯМР (ДМСО-d6),  (м.д.): 1,18 (д, 3Н, СН3), 1,20 (т, 3Н, СН3), 2,61 (м, 2Н, СН2), 4,08 (квартет, 2Н, СН2), 4,58 (м, 1Н, СН), 6,46 (широкий с, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,34 (широкий д, 1Н, NH), 11,35 (широкий с, 1Н).
б) Этил-3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е] -1 (м.д.): 1,18 (д, 3Н, СН3), 1,20 (т, 3Н, СН3), 2,61 (м, 2Н, СН2), 4,08 (квартет, 2Н, СН2), 4,58 (м, 1Н, СН), 6,46 (широкий с, 2Н, NH2), 6,65 (с, 1Н, Н-4), 8,34 (широкий д, 1Н, NH), 11,35 (широкий с, 1Н).
б) Этил-3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е] -1 2,2,4-тиадиазин-3-иламино)бутаноат 2,2,4-тиадиазин-3-иламино)бутаноатУказанное в заголовке соединение получают из этил-3-{3[(3-амино-5-хлортиен-2-ил)сульфонил] тиоуреидо} бутаноата по аналогии с процедурой, описанной в примере 3-б, за исключением того, что продукт чистят способом колоночной хроматографии (выход 71%); т.пл. 151-155oС (этилацетат). 1H ЯМР (ДМСО-d6),  (м.д.): 1,18 (т, 3Н, СН3), 1,20 (д, 3Н, СН3), 2,57 (м, 2Н, СН2), 4,07 (квартет, 2Н, СН2), 4,17 (м, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,99 (с, 1Н, NH).
Масс-спектр: m/e 351/353 (М+).
Элементный анализ (м.д.): 1,18 (т, 3Н, СН3), 1,20 (д, 3Н, СН3), 2,57 (м, 2Н, СН2), 4,07 (квартет, 2Н, СН2), 4,17 (м, 1Н, СН), 7,05 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,99 (с, 1Н, NH).
Масс-спектр: m/e 351/353 (М+).
Элементный анализРассчитано для C11H14Cl1O4S2  0,2 этилацетат,%: С 38,36; Н 4,26; N 11,37.
Найдено,%: С 38,35; Н 4,18; N 11,58.
ПРИМЕР 11 0,2 этилацетат,%: С 38,36; Н 4,26; N 11,37.
Найдено,%: С 38,35; Н 4,18; N 11,58.
ПРИМЕР 113-(6-Хлор-1,4-дигидро-1,1-диоксотиено[3,2-е] –  2,4-тиадиазин-3-иламино)бутановая кислота 2,4-тиадиазин-3-иламино)бутановая кислотаЭтил-3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е] -1  2,2,4-тиадиазин-3-иламино)бутаноат (0,5 г, 1,42 ммоль) гидролизуют до кислоты, перемешивая в 5 мл 2 н. гидроксида натрия в течение 2 часов при комнатной температуре. Раствор обрабатывают обесцвечивающим углем, фильтруют и подкисляют 4 М соляной кислотой до рН 2. Полученный осадок выделяют фильтрованием, промывают водой и сушат, получая 294 мг (64%) указанного в заголовке соединения; т.пл. 218-223oС.
1H ЯМР (ДМСО-d6), 2,2,4-тиадиазин-3-иламино)бутаноат (0,5 г, 1,42 ммоль) гидролизуют до кислоты, перемешивая в 5 мл 2 н. гидроксида натрия в течение 2 часов при комнатной температуре. Раствор обрабатывают обесцвечивающим углем, фильтруют и подкисляют 4 М соляной кислотой до рН 2. Полученный осадок выделяют фильтрованием, промывают водой и сушат, получая 294 мг (64%) указанного в заголовке соединения; т.пл. 218-223oС.
1H ЯМР (ДМСО-d6),  (м.д.): 1,19 (д, 3Н, СН3), 2,49 (м, 2Н, СН2), 4,10 (м, 1Н, СН), 7,06 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,99 (с, 1Н, NH), 12,38 (широкий с, 1Н, ОН).
Масс-спектр: m/е 305/307 (М-Н2O)+.
Элементный анализ (м.д.): 1,19 (д, 3Н, СН3), 2,49 (м, 2Н, СН2), 4,10 (м, 1Н, СН), 7,06 (с, 1Н, Н-5), 7,25 (широкий, 1Н, NH), 10,99 (с, 1Н, NH), 12,38 (широкий с, 1Н, ОН).
Масс-спектр: m/е 305/307 (М-Н2O)+.
Элементный анализРассчитано для C9H10N3Cl1O4S2,%: С 33,39; Н 3,11; N 12,98. Найдено,%: С 33,62; Н 3,11; N 12,81. ПРИМЕР 12 6-Хлор-3-(3-гидрокси-1-метилпропил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Толуол (5 мл) охлаждают до 10oС и добавляют литийалюминийгидрид (114 мг, 3 ммоль), а затем 0,53 мл тетрагидрофурана. Этил-3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е] -1  2,2,4-тиадиазин-3-иламино)бутаноат (352 мг, 1 ммоль) добавляют к этому охлажденному раствору и смесь перемешивают в течение 2 часов при 0oС и затем при комнатной температуре в течение ночи. Эту смесь охлаждают на бане со льдом и добавляют по капле 10 мл воды, а затем 5-10 мл 20% серной кислоты. Смесь экстрагируют эфиром (3 х 30 мл) и органическую фазу промывают водой, сушат и выпаривают до сухости. Сырой продукт смешивают с твердым веществом, которое образовалось в водной фазе, и окончательно чистят способом колоночной хроматографии на диоксиде кремния со смесью этилацетат/метанол (9: 1) в качестве элюента, получая 120 мг (39%) указанного в заголовке соединения; т.пл. 199-203oС.
1H ЯМР (ДМСО-d6), 2,2,4-тиадиазин-3-иламино)бутаноат (352 мг, 1 ммоль) добавляют к этому охлажденному раствору и смесь перемешивают в течение 2 часов при 0oС и затем при комнатной температуре в течение ночи. Эту смесь охлаждают на бане со льдом и добавляют по капле 10 мл воды, а затем 5-10 мл 20% серной кислоты. Смесь экстрагируют эфиром (3 х 30 мл) и органическую фазу промывают водой, сушат и выпаривают до сухости. Сырой продукт смешивают с твердым веществом, которое образовалось в водной фазе, и окончательно чистят способом колоночной хроматографии на диоксиде кремния со смесью этилацетат/метанол (9: 1) в качестве элюента, получая 120 мг (39%) указанного в заголовке соединения; т.пл. 199-203oС.
1H ЯМР (ДМСО-d6),  (м.д.): 1,14 (д, 3Н, СН3), 1,65 (м, 2Н, СН2), 3,48 (м, 1Н, СН2), 3,90 (м, 1Н, СН), 4,60 (широкий с, 1Н, ОН), 7,06 (с, 1Н, Н-5), 7,17 (широкий, 1Н, NH), 10,86 (с, 1Н, NH).
Масс-спектр: m/е 309/311 (М+).
Элементный анализ (м.д.): 1,14 (д, 3Н, СН3), 1,65 (м, 2Н, СН2), 3,48 (м, 1Н, СН2), 3,90 (м, 1Н, СН), 4,60 (широкий с, 1Н, ОН), 7,06 (с, 1Н, Н-5), 7,17 (широкий, 1Н, NH), 10,86 (с, 1Н, NH).
Масс-спектр: m/е 309/311 (М+).
Элементный анализРассчитано для C9H12N3Cl1O3S2  0,15 этилацетат, %: С 35,70; Н 4,12; N 13,01.
Найдено,%: С 35,7; Н 4,1; N 13,1.
ПРИМЕР 13 0,15 этилацетат, %: С 35,70; Н 4,12; N 13,01.
Найдено,%: С 35,7; Н 4,1; N 13,1.
ПРИМЕР 13(R)-6-Хлор-3-(1-фенилэтил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид а) (R)-N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(1-фенилэтил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и D-  -метилбензили изотиоцианата по аналогии с процедурой, описанной в примере 3-а (выход 96%, грязный продукт).
1H ЯМР (ДМСО-d6), -метилбензили изотиоцианата по аналогии с процедурой, описанной в примере 3-а (выход 96%, грязный продукт).
1H ЯМР (ДМСО-d6),  (м.д.): 1,46 (д, 3Н, СН3), 5,36 (квинтет, 1Н, СН), 6,45 (широкий с, 2Н, NH2), 6,64 (с, 1Н, Н-4), 7,2-7,4 (м, 5Н, АrН), 8,53 (широкий д, 1Н, NH), 11,3 (широкий с, 1Н).
б) (R)-6-Хлор-3-(1-фенилэтил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид (м.д.): 1,46 (д, 3Н, СН3), 5,36 (квинтет, 1Н, СН), 6,45 (широкий с, 2Н, NH2), 6,64 (с, 1Н, Н-4), 7,2-7,4 (м, 5Н, АrН), 8,53 (широкий д, 1Н, NH), 11,3 (широкий с, 1Н).
б) (R)-6-Хлор-3-(1-фенилэтил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из сырой (R)-N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(1-фенилэтил)тиомочевины по аналогии с процедурой, описанной в примере 3-б, за исключением того, что продукт чистят способом колоночной хроматографии на диоксиде кремния со смесью дихлорметан/метанол (19:1) в качестве элюента (выход 17%); т.пл. 218-220oС (этилацетат). 1H ЯМР (ДМСО-d6),  (м.д.): 1,48 (д, 3Н, СН3), 4,97 (квинтет, 1Н, СН), 7,10 (с, 1Н, Н-5), 7,2-7,4 (м, 5Н, АrН), 7,73 (широкий, 1Н, NH), 10,81 (с, 1Н, NH).
Масс-спектр: m/е 341/343 (М+).
Элементный анализ (м.д.): 1,48 (д, 3Н, СН3), 4,97 (квинтет, 1Н, СН), 7,10 (с, 1Н, Н-5), 7,2-7,4 (м, 5Н, АrН), 7,73 (широкий, 1Н, NH), 10,81 (с, 1Н, NH).
Масс-спектр: m/е 341/343 (М+).
Элементный анализРассчитано для С13Н12N3Cl1О2S2,%: С 45,68; Н 3,54; N 12,29. Найдено,%: С 45,83; Н 3,55; N 12,04. ПРИМЕР 14 (S)-3-втор-Бутиламино-6-хлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Раствор 3,6-дихлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксида (257 мг, 1,0 ммоль) и (S)-(+)-втор-бутиламина (0,31 мл, 3,0 ммоль) перемешивают в 10 мл абсолютного этанола в течение 4 дней при 80oС в закупоренной склянке. Охлажденный раствор концентрируют в вакууме и остаток перемешивают с водой (10 мл), а затем доводят рН до 2 при помощи 4 М соляной кислоты. Первоначально образовавшийся смолистый продукт кристаллизуют при перемешивании при 0oС. Осадок выделяют фильтрованием, промывают водой и перекристаллизовывают из смеси этилацетат/метанол, а затем сушат в течение ночи в вакууме при 30oС, получая 181 мг (62%) чистого соединения, указанного в заголовке; т.пл. 228-230oС (этилацетат). 1H ЯМР (ДМСО-d6),  (м.д.): 0,88 (т, 3Н, СН3), 1,14 (д, 3Н, СН3), 1,49 (м, 2Н, CH2), 3,68 (м, 1Н, СН), 7,08 (с, 1Н, Н-5), 7,13 (широкий, 1Н, NH), 10,73 (широкий с, 1Н, NH).
Масс-спектр: m/е 293/295 (M+).
Элементный анализ (м.д.): 0,88 (т, 3Н, СН3), 1,14 (д, 3Н, СН3), 1,49 (м, 2Н, CH2), 3,68 (м, 1Н, СН), 7,08 (с, 1Н, Н-5), 7,13 (широкий, 1Н, NH), 10,73 (широкий с, 1Н, NH).
Масс-спектр: m/е 293/295 (M+).
Элементный анализРассчитано для С9Н12N3Cl1O2S2,%: С 36,79; Н 4,12; N 14,30. Найдено,%: С 36,79; Н 4,1; N 14,2. ПРИМЕР 15 6-Хлор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид a) N-[5-хлор-3-(изопропилтиокарбамоил)сульфамоилтиофен-2-ил]ацетамид трет-Бутоксид калия (135 мг, 1,2 ммоль) добавляют к раствору N-(5-хлор-3-сульфамоилтиофен-2-ил)ацетамида (255 мг, 1,0 ммоль) в сухом N,N-диметилформамиде (5 мл) при перемешивании на бане со льдом. Через 5 минут добавляют по капле изопропилизотиоцианат (0,128 мл, 1,2 ммоль) и раствор перемешивают при 0oС в течение 30 минут, а затем при комнатной температуре в течение 3 часов. К раствору добавляют дополнительное количество трет-бутоксида калия (135 мг, 1,2 ммоль) и перемешивание продолжают при комнатной температуре в течение 1 часа. Растворитель выпаривают при температуре <50oС, а остаток помещают в 10 мл воды и доводят рН до 2 при помощи 4 М соляной кислоты. Полученный осадок отделяют фильтрованием, промывают водой и сушат, получая 274 мг (77%) сырого соединения, указанного в заголовке. 1H ЯМР (ДМСО-d6),  (м.д.):1,12 (д, 6Н, 2хСН3), 2,28 (с, 3Н, СОСН3), 4,21 (м, 1Н, NCH), 7,15 (с, 1Н, Н-4), 8,34 (широкий д, 1Н, NH), 10,26 (с, 1Н, NH).
б) 6-Хлор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид (м.д.):1,12 (д, 6Н, 2хСН3), 2,28 (с, 3Н, СОСН3), 4,21 (м, 1Н, NCH), 7,15 (с, 1Н, Н-4), 8,34 (широкий д, 1Н, NH), 10,26 (с, 1Н, NH).
б) 6-Хлор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксидФосген (0,416 мл, 20% в толуоле) добавляют по капле к раствору N-[5-хлор-3-(изопропилтиокарбамоил)сульфамоилтиофен-2-ил] ацетамида (261 мг, 0,73 ммоль) и сухого триэтиламина (0,209 мл, 1,5 ммоль) в сухом тетрагидрофуране (5 мл) при перемешивании при 0oС. Смесь перемешивают в течение 1 часа при 0oС и выпаривают до сухости. Остаток растирают с 10 мл воды и осадок отделяют фильтрованием, промывают водой и в завершение деацетилируют при перемешивании в 2 мл 2 н. гидроксида натрия в течение 90 минут при комнатной температуре. Раствор подкисляют до рН 2 4 М соляной кислотой и осадок отфильтровывают и переклисталлизовывают из этилацетата с обесцвечивающим углем, получая 44 мг (21%) чистого соединения, указанного в заголовке; т.пл. 272-274oС (этилацетат). 1H ЯМР(ДМСО-d6),  (м.д.): 1,16 (д, 6Н, 2хСН3), 3,85 (м, 1Н, NCH), 7,23 (с, 1Н, Н-7), 7,48 (широкий д, 1Н, NH), 11,12 (с, 1Н, NH).
Масс-спектр: m/е 279/281 (М+).
ПРИМЕР 16 (м.д.): 1,16 (д, 6Н, 2хСН3), 3,85 (м, 1Н, NCH), 7,23 (с, 1Н, Н-7), 7,48 (широкий д, 1Н, NH), 11,12 (с, 1Н, NH).
Масс-спектр: m/е 279/281 (М+).
ПРИМЕР 166-Хлор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид а) N-[5-Хлор-3-(циклопентилтиокарбамоил)сульфамоилтиофен-2-ил]ацетамид Указанное в заголовке соединение получают из N-(5-хлор-3-сульфамоилтиофен-2-ил)ацетамида и циклопентилизотиоцианата по аналогии с процедурой, описанной в примере 15-а (выход сырого продукта (93%). 1H ЯМР (ДМСО-d6),  (м.д.): 1,3-2,0 (м, 8Н, (CH2)4), 2,28 (с, 3Н, СН3), 4,32 (секстет, 1Н, СН), 7,16 (с, 1Н, Н-4), 8,48 (широкий д, 1Н, NH), 10,23 (широкий с, 1Н, NH).
б) 6-Хлор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид (м.д.): 1,3-2,0 (м, 8Н, (CH2)4), 2,28 (с, 3Н, СН3), 4,32 (секстет, 1Н, СН), 7,16 (с, 1Н, Н-4), 8,48 (широкий д, 1Н, NH), 10,23 (широкий с, 1Н, NH).
б) 6-Хлор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-[5-хлор-3-(циклопентилтиокарбамоил)сульфамоилтиофен-2-ил] ацетамида по аналогии с процедурой, описанной в примере 15-б (выход 32%); т.пл. 280-282oС (водный этанол). 1H ЯМР (ДMCO-d6),  (м.д.): 1,4-2,0 (м, 8Н, СН2)4), 3,96 (секстет, 1Н, СН), 7,23 (с, 1Н, Н-7), 7,62 (широкий, 1Н, NH), 11,09 (с, 1Н, NH).
Масс-спектр: m/е 305/307 (М+).
ПРИМЕР 17 (м.д.): 1,4-2,0 (м, 8Н, СН2)4), 3,96 (секстет, 1Н, СН), 7,23 (с, 1Н, Н-7), 7,62 (широкий, 1Н, NH), 11,09 (с, 1Н, NH).
Масс-спектр: m/е 305/307 (М+).
ПРИМЕР 176-Бром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Бром (0,12 мл, 2,3 ммоль) добавляют по капле к раствору 6-хлор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазина 1,1-диоксида (280 мг, 1,0 ммоль) в 10 мл уксусной кислоты и смесь перемешивают в течение 24 часов при 100oС в закупоренной склянке. Охлажденную смесь выпаривают до сухости, а остаток растирают с водой, получая твердое вещество, которое перекристаллизовывают из смеси этанол/вода (1: 1), получая 118 мг (39%) указанного в заголовке, загрязненного 10% исходного вещества; т.пл. примерно 279oС (водный этанол). 1H ЯМР (ДМСО-d6),  (м.д.): 1,16 (д, 6Н, 2хСН3), 3,86 (м, 1Н, СН), 7,14 (с, 1Н, Н-5), 7,18 (широкий, 1Н, NH), 10,74 (с, 1Н, NH).
Масс-спектр: m/е 323/325 (М+).
ПРИМЕР 18 (м.д.): 1,16 (д, 6Н, 2хСН3), 3,86 (м, 1Н, СН), 7,14 (с, 1Н, Н-5), 7,18 (широкий, 1Н, NH), 10,74 (с, 1Н, NH).
Масс-спектр: m/е 323/325 (М+).
ПРИМЕР 183-Изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Порошкообразный гидроксид калия (128 мг, 2,28 ммоль) добавляют к раствору 6-хлор-3-изопропиламино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксида (319 мг, 1,14 ммоль) в 25 мл метанола и смесь гидрируют при комнатной температуре и атмосферном давлении в течение 3 дней со 150 г 10% палладия на углероде. Катализатор удаляют фильтрованием и промывают этанолом и водой. Объединенный фильтрат подкисляют 4 М соляной кислотой и выпаривают до сухости. Остаток перекристаллизовывают из смеси этанол/вода и в заключение из этилацетата с обесцвечивающим углем, получая указанное в заголовке соединение, загрязненное исходным веществом, которое можно удалить способом колоночной хроматографии на силикагеле. 1H ЯМР (ДМСО-d6),  (м.д.): 1,16 (д, 6Н, 2хСН3), 3,88 (м, 1Н, СН), 6,95 (д, 1Н, Н-5), 7,03 (широкий д, 1Н, NH), 7,88 (с, 1Н, Н-6), 10,70 (широкий с, 1Н).
ПРИМЕР 19 (м.д.): 1,16 (д, 6Н, 2хСН3), 3,88 (м, 1Н, СН), 6,95 (д, 1Н, Н-5), 7,03 (широкий д, 1Н, NH), 7,88 (с, 1Н, Н-6), 10,70 (широкий с, 1Н).
ПРИМЕР 193-Изопропиламино-7-метил-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид а) Цианометансульфонамид Сухой ТГФ (200 мл) насыщают аммиаком при -10oС, затем добавляют небольшими порциями за 20 минут при -10oС раствор цианометансульфонилхлорида (13,9 г, получен согласно работе Sammes и др., J. Chem. Sоc., 1971, 2151-5155) в 10 мл сухого ТГФ. После добавления поднимают температуру до 0oС и фильтруют реакционную смесь. Удаление из фильтрата растворителя и очистка остатка способом колоночной хроматографии на силикагеле с элюированием этилацетатом дают указанное в заголовке соединение в виде бежевых кристаллов; т.пл. 97-99oС. ИК (KBr),  (см-1): 3316, 3328 (N-H), 2266 (C (см-1): 3316, 3328 (N-H), 2266 (C N), 1371, 1151 (SO2).
б) 2-Амино-4-метилтиофен-3-сульфонамид N), 1371, 1151 (SO2).
б) 2-Амино-4-метилтиофен-3-сульфонамидСмесь цианометансульфонамида (1,0 г), 2,5-дигидрокси-2,5-диметил-1,4-дитиана (0,75 г) и триэтиламина (100  л) в абсолютном этаноле (7 мл) нагревают при 45-50oС под азотом в течение 3 часов. Затем выпаривают растворитель и остаток порционируют в воде (30 мл) и этилацетате (50 мл). Водную фазу экстрагируют этилацетатом, 4 х 50 мл. Объединенные этилацетатные фазы сушат над сульфатом натрия и выпаривают. Остаток чистят способом колоночной хроматографии на силикагеле при элюировании этилацетатом. Получают указанное в заголовке соединение в виде желтого твердого вещества, выход 0,65 г (41%); т.пл. 142-144oС.
1H ЯМР (СD3OD), л) в абсолютном этаноле (7 мл) нагревают при 45-50oС под азотом в течение 3 часов. Затем выпаривают растворитель и остаток порционируют в воде (30 мл) и этилацетате (50 мл). Водную фазу экстрагируют этилацетатом, 4 х 50 мл. Объединенные этилацетатные фазы сушат над сульфатом натрия и выпаривают. Остаток чистят способом колоночной хроматографии на силикагеле при элюировании этилацетатом. Получают указанное в заголовке соединение в виде желтого твердого вещества, выход 0,65 г (41%); т.пл. 142-144oС.
1H ЯМР (СD3OD),  (м. д. ): 7,19 (с, 1Н, С(5)Н), 4,88 (широкий, 4Н, SO2NH2+H2O), 4,71 (с, 2Н, NH2), 2,41 (с, 3Н, NH2).
Масс-спектр: 192(M+), 112 (М+ -SO2NH2), 72(СН3-С2НS+).
в) N-(2-Амино-4-метил-3-тиенилсульфонил)-N’-изопропилтиомочевин (м. д. ): 7,19 (с, 1Н, С(5)Н), 4,88 (широкий, 4Н, SO2NH2+H2O), 4,71 (с, 2Н, NH2), 2,41 (с, 3Н, NH2).
Масс-спектр: 192(M+), 112 (М+ -SO2NH2), 72(СН3-С2НS+).
в) N-(2-Амино-4-метил-3-тиенилсульфонил)-N’-изопропилтиомочевинСмесь 2-амино-4-метилтиофен-3-сульфонамида (0,30 г), карбоната калия (0,32 г) и изопропилизотиоцианата (271  л) в сухом ацетоне (5 мл) нагревают при 50-55oС в течение ночи. Затем выпаривают растворитель, а остаток растворяют в воде (15 мл); доводят рН до 2, добавляя 4 М соляную кислоту, и смесь перемешивают в течение 30 минут. Осадившиеся кристаллы отфильтровывают, промывают небольшим количеством воды и сушат, получая 0,24 г (выход 54%) указанного в заголовке соединения; т.пл. 118-120oС.
г) 3-Изопропиламино-7-метил-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид л) в сухом ацетоне (5 мл) нагревают при 50-55oС в течение ночи. Затем выпаривают растворитель, а остаток растворяют в воде (15 мл); доводят рН до 2, добавляя 4 М соляную кислоту, и смесь перемешивают в течение 30 минут. Осадившиеся кристаллы отфильтровывают, промывают небольшим количеством воды и сушат, получая 0,24 г (выход 54%) указанного в заголовке соединения; т.пл. 118-120oС.
г) 3-Изопропиламино-7-метил-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид20% раствор фосгена в толуоле (175  л) добавляют к перемешиваемому и охлажденному раствору N-(2-амино-4-метил-3-тиенилсульфонил)-N’-изопропилтиомочевины (0,22 г) и триэтиламина (313 л) добавляют к перемешиваемому и охлажденному раствору N-(2-амино-4-метил-3-тиенилсульфонил)-N’-изопропилтиомочевины (0,22 г) и триэтиламина (313  л) в сухом ТГФ (5 мл), при этом поддерживают температуру ниже 5oС. После перемешивания в течение 1,5 часов смесь выпаривают и растирают с 10 мл воды. Осадок собирают фильтрованием и сушат, получая 0,14 г сырого продукта. Кристаллы нагревают при 70oС с 5 мл этилацетата и полученную смесь охлаждают в течение 10 минут до 0oС и затем фильтруют. Остаток на фильтре промывают небольшим количеством этилацетата и сушат, получая 0,087 г (выход 45%) указанного в заголовке соединения в виде рыжевато-коричневых кристаллов; т.пл. 152-154oС.
1H ЯМР (ДМСО-d6), л) в сухом ТГФ (5 мл), при этом поддерживают температуру ниже 5oС. После перемешивания в течение 1,5 часов смесь выпаривают и растирают с 10 мл воды. Осадок собирают фильтрованием и сушат, получая 0,14 г сырого продукта. Кристаллы нагревают при 70oС с 5 мл этилацетата и полученную смесь охлаждают в течение 10 минут до 0oС и затем фильтруют. Остаток на фильтре промывают небольшим количеством этилацетата и сушат, получая 0,087 г (выход 45%) указанного в заголовке соединения в виде рыжевато-коричневых кристаллов; т.пл. 152-154oС.
1H ЯМР (ДМСО-d6),  (м. д. ): 7,10 (широкий д, 1Н, NH), 6,61 (с, 1Н, N(4)Н), 6,52 (с, 1Н, С(6)Н), 3,89 (м, 1Н, CH2), 2,32 (с, 3Н, СН3), 1,18 (д, 6Н, СН3).
ПРИМЕР 20 (м. д. ): 7,10 (широкий д, 1Н, NH), 6,61 (с, 1Н, N(4)Н), 6,52 (с, 1Н, С(6)Н), 3,89 (м, 1Н, CH2), 2,32 (с, 3Н, СН3), 1,18 (д, 6Н, СН3).
ПРИМЕР 206-Хлор-3-циклобутиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Раствор 3,6-дихлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксида (257 мг, 1,0 ммоль) в циклобутиламине (1,0 мл) перемешивают в течение 18 часов при 90oС в закупоренной склянке. Этот охлажденный раствор концентрируют в вакууме и остаток перемешивают с водой (10 мл) при 0oС, затем доводят рН до 2 при помощи 4 М соляной кислоты. Продукт выделяют фильтрованием, промывают водой и перекристаллизовывают из смеси метанол/этилацетат, а затем сушат в вакууме при комнатной температуре, получая 155 мг (53%) чистого соединения, указанного в заголовке; т.пл. 315-317oС (разлагается). 1H ЯМР (ДМСО-d6),  (м.д.): 1,58-1,75 (м, 2Н), 1,89-2,05 (м, 2Н), 2,19-2,30 (м, 2Н), 4,16 (м, 1Н), 7,06 (с, 1Н), 7,62 (широкий с, 1Н), 10,83 (широкий с, 1Н).
Масс-спектр: m/е 291/293 (М+).
Элементный анализ (м.д.): 1,58-1,75 (м, 2Н), 1,89-2,05 (м, 2Н), 2,19-2,30 (м, 2Н), 4,16 (м, 1Н), 7,06 (с, 1Н), 7,62 (широкий с, 1Н), 10,83 (широкий с, 1Н).
Масс-спектр: m/е 291/293 (М+).
Элементный анализРассчитано для C9H10N3Cl1O2S2,%: С 37,05; Н 3,45; N 14,40. Найдено,%: С 37,18; Н 3,48; N 14,19. ПРИМЕР 21 6-Хлор-3-(2-гидроксиэтил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Раствор 3,6-дихлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксида (206 мг, 0,8 ммоль) в этаноламине (1,0 мл) перемешивают в течение 18 часов при 100oС в закупоренной склянке. Этот охлажденный раствор концентрируют в вакууме и остаток перемешивают с водой (5 мл) при 0oС, затем доводят рН до 2 при помощи 4 М соляной кислоты. Продукт выделяют фильтрованием, промывают водой и перекристаллизовывают из смеси этанол/вода, получая 135 мг (60%) чистого соединения, указанного в заголовке; т.пл. 260-261oС (разлагается). 1H ЯМР (ДМСО-d6),  (м.д.): 3,26 (искаженный квартет, 2Н), 3,50 (т, 2Н), 4,85 (широкий с, 1Н), 7,07 (с, 1Н), 7,20 (широкий с, 1Н), 10,9 (широкий с, 1Н).
Масс-спектр: m/е 281/283 (М+).
Элементный анализ (м.д.): 3,26 (искаженный квартет, 2Н), 3,50 (т, 2Н), 4,85 (широкий с, 1Н), 7,07 (с, 1Н), 7,20 (широкий с, 1Н), 10,9 (широкий с, 1Н).
Масс-спектр: m/е 281/283 (М+).
Элементный анализРассчитано для С7Н8N3Сl1O3S2,%: С 29,84; Н 2,86; N 14,91. Найдено,%: С 30,13; Н 2,84; N 14,79. ПРИМЕР 22 (  )-3-экзо-бицикло[2.2.1] гепт-2-иламино-6-хлор-4Н-тиено-[3,2-е]-1,2,4-тиадиазин 1,1-диоксид )-3-экзо-бицикло[2.2.1] гепт-2-иламино-6-хлор-4Н-тиено-[3,2-е]-1,2,4-тиадиазин 1,1-диоксидРаствор 3,6-дихлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксида (206 мг, 0,8 ммоль) в экзо-2-аминонорборнане (1,0 мл) перемешивают в течение 20 часов при 100oС в закупоренной склянке. Эту смесь перемешивают с водой (10 мл) при 0oС, затем доводят рН до 2 при помощи 4 М соляной кислоты. Продукт выделяют фильтрованием, промывают водой и перекристаллизовывают из смеси этилацетат/метанол, получая 168 мг (60%) чистого соединения, указанного в заголовке; т.пл. 323-324oС (разлагается). 1H ЯМР (ДМСО-d6),  (м.д.): 1,05-1,55 (м, 7Н), 1,68-1,77 (м, 1Н), 2,18-2,28 (м, 2Н), 7,09 (с, 1Н), 7,2 (широкий с, 1Н), примерно 10,5 (широкий с, 1Н), (м.д.): 1,05-1,55 (м, 7Н), 1,68-1,77 (м, 1Н), 2,18-2,28 (м, 2Н), 7,09 (с, 1Н), 7,2 (широкий с, 1Н), примерно 10,5 (широкий с, 1Н),Масс-спектр: m/е 331/333 (М+). Элементный анализ Рассчитано для C12H14N3Cl1O2S2,%: С 43,43; Н 4,25; N 12,66. Найдено,%: С 43,67; Н 4,26; N 12,55. ПРИМЕР 23 (R)-6-Хлор-3-(2-гидроксипропил)амино-4Н-тиено-[3,2-е] -1,2,4-тиадиазин 1,1-диоксид Раствор 3,6-дихлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксида (200 мг, 0,78 ммоль) в (R)-(-)-1-амино-2-пропаноле (1,0 мл) перемешивают в течение 18 часов при 100oС в закупоренной склянке. Этот охлажденный раствор перемешивают с водой (3 мл) при 0oС, затем доводят рН до 2 при помощи 4 М соляной кислоты. Продукт выделяют фильтрованием, промывают водой и сушат в вакууме при комнатной температуре, получая 170 мг (74%) чистого соединения, указанного в заголовке; т.пл. 210-211oС. 1H ЯМР (ДМСО-d6),  (м.д.): 1,08 (д, 3Н), 3,0-3,1 (м, 1Н), 3,15-3,25 (м, 1Н), 3,72-3,82 (м, 1Н), 4,91 (широкий с, 1Н), 7,09 (с, 1Н), 7,14 (широкий с, 1Н), 10,95 (широкий с, 1Н).
Масс-спектр: m/е 297/295 (М+).
Элементный анализ (м.д.): 1,08 (д, 3Н), 3,0-3,1 (м, 1Н), 3,15-3,25 (м, 1Н), 3,72-3,82 (м, 1Н), 4,91 (широкий с, 1Н), 7,09 (с, 1Н), 7,14 (широкий с, 1Н), 10,95 (широкий с, 1Н).
Масс-спектр: m/е 297/295 (М+).
Элементный анализРассчитано для C8H10N3Cl1O3S2  0,5 Н2О,%: С 31,53; Н 3,64; N 13,79.
Найдено,%: С 31,57; Н 3,58; N 13,58.
ПРИМЕР 24 0,5 Н2О,%: С 31,53; Н 3,64; N 13,79.
Найдено,%: С 31,57; Н 3,58; N 13,58.
ПРИМЕР 246-Бром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Бром (1,26 мл, 25 ммоль) добавляют по капле к раствору 6-хлор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,3-тиадиазин 1,1-диоксида (2,3 г, 8,2 ммоль) в 25 мл уксусной кислоты и смесь перемешивают в течение 24 часов при 100oС в закупоренной склянке. Охлажденную смесь выпаривают до сухости, а остаток, который состоит из двух основных продуктов, растирают с водой, получая твердое вещество, которое перекристаллизовывают из смеси этилацетат/метанол с обесцвечивающим углем, получая 538 мг (20%) указанного в заголовке соединения. Аналитически чистый образец можно получить путем препаративной высокоэффективной жидкостной хроматографии на колонке Source RPC 15, используя в качестве элюента смесь ацетонитрил/вода (20:80) с 0,1 TFA (трифторуксусная кислота); т.пл. 282-283oС (водный этанол). 1H ЯМР (ДМСО-d6),  (м. д.): 1,16 (д, 6Н), 3,86 (м, 1Н), 7,14 (с, 1Н), 7,18 (широкий, 1Н), 10,74 (с, 1Н), (м. д.): 1,16 (д, 6Н), 3,86 (м, 1Н), 7,14 (с, 1Н), 7,18 (широкий, 1Н), 10,74 (с, 1Н),Масс-спектр: m/е 323/325 (М+). Элементный анализ Рассчитано для C8H10N3Br1O2S2,%: С 29,64; Н 3,11; N 12,96. Найдено,%: С 29,49; Н 3,04; N 12,59. ПРИМЕР 25 3,6-Дибром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Маточник от кристаллизации 6-бром-3-изопропиламино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксида, описанной выше, выпаривают до сухости, а остаток чистят хроматографически в диоксиде кремния со смесью дихлорметан/метанол (95: 5) в качестве элюента. Перекристаллизация из этилацетата дает 270 мг (8%) чистого соединения, указанного в заголовке; т.пл. 250-251oС. 1H ЯМР (ДМСО-d6),  (м.д.): 1,18 (д, 6Н), 3,86 (м, 1Н), 7,18 (широкий, 1Н), 10,31 (с, 1Н).
Масс-спектр: m/е 405/403/401 (М+).
Элементный анализ (м.д.): 1,18 (д, 6Н), 3,86 (м, 1Н), 7,18 (широкий, 1Н), 10,31 (с, 1Н).
Масс-спектр: m/е 405/403/401 (М+).
Элементный анализРассчитано для С8Н9N3Вr2O2S2,%: С 23,84; Н 2,25; N 10,42. Найдено,%: С 24,14; Н 2,18; N 10,25. ПРИМЕР 26 6-Хлор-3-циклогексиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид a) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(3-циклогексил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и циклогексилизотиоцианата по аналогии с процедурой, описанной в примере 3-а (выход 78%). 1H ЯМР (ДМСО-d6),  (м.д.): 1,1-1,9 (м, 10Н), 4,0 (м, 1Н), 6,45 (широкий с, 2Н), 6,66 (с, 1Н), 8,05 (широкий д, 1Н), 11,2 (широкий с, 1Н).
б) 6-Хлор-3-циклогексиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид (м.д.): 1,1-1,9 (м, 10Н), 4,0 (м, 1Н), 6,45 (широкий с, 2Н), 6,66 (с, 1Н), 8,05 (широкий д, 1Н), 11,2 (широкий с, 1Н).
б) 6-Хлор-3-циклогексиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксидУказанное в заголовке соединение получают из N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(циклогексил)тиомочевины по аналогии с процедурой, описанной в примере 3-б (выход 66%); т.пл. 282-284oС (этилацетат/метанол). 1H ЯМР (ДМСО-d6),  (м.д.):1,1-1,9 (м, 10Н), 3,55 (м, 1Н), 7,08 (с, 1Н), 7,19 (широкий, 1Н), 10,73 (широкий с, 1Н).
Масс-спектр: m/е 321/319 (М+).
Элементный анализ (м.д.):1,1-1,9 (м, 10Н), 3,55 (м, 1Н), 7,08 (с, 1Н), 7,19 (широкий, 1Н), 10,73 (широкий с, 1Н).
Масс-спектр: m/е 321/319 (М+).
Элементный анализРассчитано для C11H14N3Cl1O2S2,%: С 41,31; Н 4,41; N 13,14. Найдено,%: С 41,66; Н 4,45; N 12,99. ПРИМЕР 27 6-Хлор-3-(фуран-2-илметил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид а) N-(3-Амино-5-хлор-2-тиенилсульфонил)-N’-(фуран-2-илметил)тиомочевина Указанное в заголовке соединение получают из 3-амино-5-хлортиофен-2-сульфонамида гидрохлорида и фурфурилизотиоцианата по аналогии с процедурой, описанной в примере 3-а (выход сырого продукта 92%). б) 6-Хлор-3-(фуран-2-илметил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид Указанное в заголовке соединение получают из сырого N-(3-амино-5-хлор-2-тиенилсульфонил)-N’-(фуран-2-илметил)тиомочевины по аналогии с процедурой, описанной в примере 3-б, за исключением того, что продукт чистят способом колоночной хроматографии на диоксиде кремния со смесью дихлорметан/метанол (9:1) в качестве элюента (выход 11%); т.пл. 224-225oС. 1H ЯМР (ДМСО-d6),  (м. д.): 4,41 (д, 2Н), 6,33 (м, 1Н), 6,41 (м, 1Н), 7,05 (с, 1Н), 7,62 (широкий с, 1Н), 7,75 (широкий т, 1Н), 11,2 (широкий с, 1Н).
Элементный анализ (м. д.): 4,41 (д, 2Н), 6,33 (м, 1Н), 6,41 (м, 1Н), 7,05 (с, 1Н), 7,62 (широкий с, 1Н), 7,75 (широкий т, 1Н), 11,2 (широкий с, 1Н).
Элементный анализРассчитано для С10Н8N3Сl1O3S2,%: С 37,80; Н 2,54; N 13,22. Найдено,%: С 37,87; Н 2,51; N 13,10. ПРИМЕР 28 6-Циано-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид К раствору 6-бром-3-изопропиламино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксида (243 мг, 0,75 ммоль) в сухом N,N-диметилформамиде (2 мл) добавляют цианид меди(I) (135 мг, 1,5 ммоль) и смесь нагревают при 150oС в течение 2 часов под азотом. Темной смеси дают охладиться до комнатной температуры и добавляют воду. Эту суспензию подщелачивают до основного рН, добавляя 1 н. гидроксид натрия, фильтруют и фильтрат подкисляют, добавляя 4 М соляную кислоту. Полученный осадок чистят способом препаративной высокоэффективной жидкостной хроматографии на колонке Source RPC 15, используя в качестве элюента смесь ацетонитрил/вода (20: 80) с 0,1 TFA (трифторуксусная кислота), получают 4 мг (2%) чистого соединения, указанного в заголовке. Масс-спектрометрия с жидкостной хроматографией (LC-MS): m/е 271 (М+1)+. ПРИМЕР 29 6-Бром-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Бром (0,12 мл, 2,3 ммоль) добавляют по капле к раствору 6-хлор-3-циклопентиламино-4Н-тиено[3,2-е] -1,2,4-тиадиазина (305 мг, 1,0 ммоль) в уксусной кислоте (10 мл) и смесь перемешивают в течение 21 часа при 100oС в закупоренной склянке. Охлажденную смесь выпаривают до сухости, а остаток растирают с водой, получая твердое вещество, которое перекристаллизовывают из этилацетата и этанола, получая указанное в заголовке соединение (166 мг, 47%), загрязненное 33% исходного вещества. Очистка способом препаративной высокоэффективной жидкостной хроматографии дает указанное в заголовке соединение (65 мг, 18%), загрязненное 3% исходного материала. Разлагается при 287-294oC. 1H ЯМР (ДМСО-d6),  (м.д.): 10,7 (с, 1Н, NH), 7,35 (широкий с, 1Н, NH), 7,13 (с, 1Н, Н-7), 4,00 (секстет, 1Н), 1,9 (м, 2Н), 1,7-1,4 (м, 6Н).
ПРИМЕР 30 (м.д.): 10,7 (с, 1Н, NH), 7,35 (широкий с, 1Н, NH), 7,13 (с, 1Н, Н-7), 4,00 (секстет, 1Н), 1,9 (м, 2Н), 1,7-1,4 (м, 6Н).
ПРИМЕР 306-Хлор-3-(2-метилаллил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид Раствор 3,6-дихлор-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксида (128 мг, 0,5 ммоль) в металлиламине (0,5 мл) перемешивают при 90oС в течение 48 часов в закупоренной склянке. Охлажденный раствор концентрируют в вакууме и остаток перемешивают с водой (3 мл), затем доводят рН до 2 при помощи 4 М соляной кислоты. Продукт выделяют фильтрованием и промывают, получая 92 мг (64%) чистого соединения, указанного в заголовке; т.пл. 224-226oС (разлагается). 1H ЯМР (ДМСО-d6),  (м. д.): 1,72 (с, 3Н), 3,75 (д, 2Н), 4,83 (с, 2Н), 7,05 (с, 1Н), 7,45 (широкий с, 1Н), 11,0 (широкий с, 1Н). (м. д.): 1,72 (с, 3Н), 3,75 (д, 2Н), 4,83 (с, 2Н), 7,05 (с, 1Н), 7,45 (широкий с, 1Н), 11,0 (широкий с, 1Н).
Формула изобретения 1. Конденсированное производное 1,2,4-тиадиазина, выбранное из следующих: 7-циано-6-метил-3-пропиламино-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-изопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-метилгептил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-этилпентил)амино-4Н-тиено(3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(2-метилбутил)амино-4Н-тиено[3,2-е]-1,2,4тиадиазин 1,1-диоксид; 6-хлор-3-(1-метилгексил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклопентиламино-4Н-тиено [3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-ииклогексилметиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; этил3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-е]-1  6,2,4-тиадиазин-3-иламино)бутаноат; 6,2,4-тиадиазин-3-иламино)бутаноат;3-(6-хлор-1,4-дигидро-1,1-диоксотиено[3,2-e] -1  6, 2,4-тиадиазин-3-иламино)масляная кислота; 6, 2,4-тиадиазин-3-иламино)масляная кислота;6-хлор-3-(3-гидрокси-1-метилпропил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; (R)-6-хлор-3-(1-фенилэтил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; (S)-3-втор-бутиламино-6-хлор-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-изопропиламино-4Н-тиено [2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклопентиламино-4Н-тиено [2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-бром-3-изопропиламино-4Н-тиено [3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-фтор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-циклобутиламино-5,6-диметил-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 3-циклопентиламино-5,6-диметил-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-изопропиламино-6,7-диметил-4Н-тиено [2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 3-циклобутиламино-6,7-диметил-4Н-тиено[2,3-е] -1,2,4-тиадиазин 1,1-диоксид; 3-циклопeнтиламино-6,7-диметил-4Н-тиено[2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-3-изопропиламино-4Н-тиено [3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-3-пропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1 диоксид; 5-хлор-3-циклопентиламино-4Н-тиено [3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-хлор-6-метил-3-изопропиламино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-изопропиламино-5-метил-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклопентиламино-5-метил-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-фтор-3-пропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-фтор-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5-фтор-3-пропиламино-4Н-тиено [3,2-е]-1,2,4-тиадиазин 1,1диоксид; 5-фтор-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 3-изопропиламино-7-метил-4Н-тиено [2,3-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклобутиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(2-гидроксиэтил)амино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; (  )-3-экзо-бицикло-[2.2.1] гепт-2-иламино-6-хлор-4Н-тиено-[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; )-3-экзо-бицикло-[2.2.1] гепт-2-иламино-6-хлор-4Н-тиено-[3,2-е] -1,2,4-тиадиазин 1,1-диоксид;(R)-6-хлор-3-(2-гидроксипропил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-бром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 5,6-дибром-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-циклогексиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(фуран-2-илметил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(1-этилпропил)амино-4Н-тиено[3,2-е] -1,2,4-тиадиазин 1,1-диоксид; 6-бром-3-циклопентиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид; 6-хлор-3-(2-метилаллил)амино-4Н-тиено[3, 2-е]-1,2,4-тиадиазин 1,1-диоксид или 6-циано-3-изопропиламино-4Н-тиено[3,2-е]-1,2,4-тиадиазин 1,1-диоксид, его соль с фармацевтически приемлемой кислотой или основанием, или любой оптический изомер или смесь оптических изомеров, включая смесь рацематов, или любая таутомерная форма. 2. Фармацевтическая композиция, воздействующая на КАТФ – регулируемые калиевые каналы, включающая соединение по п.1 или его фармацевтически приемлемую соль с фармацевтически приемлемой кислотой или основанием, или любой его оптический изомер, или смесь оптических изомеров, включая рацемическую смесь, или любую таутомерную форму с одним или большим количеством фармацевтически приемлемых носителей или разбавителей. 3. Фармацевтическая композиция по п.2, отличающаяся тем, что она пригодна для лечения или предотвращения заболеваний эндокринной системы, таких, как гиперинсулинемия и диабет. 4. Фармацевтическая композиция по п.2 или 3 в виде стандартной дозированной формы для орального или парентерального приема. 5. Фармацевтическая композиция по п.2 или 3, где указанное соединение принимают как дозу в диапазоне от 0,05 до 1000 мг в день, предпочтительно от 0,1 до 500 мг в день, и особо предпочтительно от 50 до 200 мг в день. 6. Соединение по п.1 или его фармацевтически приемлемая соль с фармацевтически приемлемой кислотой или основанием, или любой его оптический изомер, или смесь оптических изомеров, включая рацемическую смесь, или любая таутомерная форма, воздействующее на КАТФ – регулируемые калиевые каналы. 7. Соединение по п.1 или его фармацевтически приемлемая соль с фармацевтически приемлемой кислотой или основанием, или любой его оптический изомер, или смесь оптических изомеров, включая рацемическую смесь, или любая таутомерная форма, воздействующее на КАТФ – регулируемые калиевые каналы, пригодное для лечения или предотвращения заболеваний эндокринной системы, таких, как гиперинсулинемия и диабет. 8. Способ получения лекарственного препарата на основе соединения по п. 1, отличающийся тем, что включает внесение соединения формулы I по п.1 или его фармацевтически приемлемой соли в дозированную форму галенова препарата. Приоритет по пунктам: 16.07.1997 – соединения с 1 по 33 в п.1, пп.2-8; 17.03.1998 – соединения с 34 по 42 в п.1; 30.06.1998 – соединения с 43 по 45 в п.1. MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 01.07.2004
Извещение опубликовано: 20.04.2006 БИ: 11/2006
|
||||||||||||||||||||||||||
