Патент на изобретение №2209078
|
||||||||||||||||||||||||||
(54) СОСТАВ ДЛЯ УНИЧТОЖЕНИЯ ФНО-
(57) Реферат: Изобретение относится к медицине и ветеринарии и может быть использовано при терапии опухолей у людей и животных. Заявленный состав для уничтожения ФНО-  -чувствительных клеток опухоли содержит цитостатик и ФНО- -чувствительных клеток опухоли содержит цитостатик и ФНО- , в качестве цитостатика содержит интерколирующие в ДНК препараты и дополнительно биологически активный мурамилпептид при массовом соотношении цитостатика, мурамилпептида и ФНО- , в качестве цитостатика содержит интерколирующие в ДНК препараты и дополнительно биологически активный мурамилпептид при массовом соотношении цитостатика, мурамилпептида и ФНО- 1: 0,06-300: 0,00001-0,1. Изобретение обеспечивает повышение эффективности состава дня уничтожения ФНО- 1: 0,06-300: 0,00001-0,1. Изобретение обеспечивает повышение эффективности состава дня уничтожения ФНО- -чувствительных клеток опухоли и снижение токсичности препарата.
Изобретение относится к медицине и ветеринарии и может быть использовано при терапии опухолей у людей и животных.
Известно широкое применение в терапии опухолей цитотоксических препаратов, таких как цисплатин, доксорубицин.
Цисплатин – цис-Платина(II)-диамин, дихлорид – синтетический противоопухолевый препарат широкого спектра действия [Машковский М.Д. Лекарственные средства. – М.: Медицина, 1993, с. 523].
Доксорубицин – противоопухолевый антибиотик антрациклинового ряда. Обладает способностью к блокированию матричной активности ДНК [Машковский М.Д. Лекарственные средства. – М.: Медицина, 1993 с. 534-535].
Известно также применение для терапии опухолей антибиотика актиномицина-D-акриноциклин-ди(треонин-D-валинил-пролинил-саркозил-N-метил-валинил)-лактон [Машковский М. Д. Лекарственные средства. – М.: Медицина, 1993, с. 532-533].
В последние годы делаются активные попытки использовать в терапии опухолей природные цитотоксические агенты, в частности фактор некроза опухолей- -чувствительных клеток опухоли и снижение токсичности препарата.
Изобретение относится к медицине и ветеринарии и может быть использовано при терапии опухолей у людей и животных.
Известно широкое применение в терапии опухолей цитотоксических препаратов, таких как цисплатин, доксорубицин.
Цисплатин – цис-Платина(II)-диамин, дихлорид – синтетический противоопухолевый препарат широкого спектра действия [Машковский М.Д. Лекарственные средства. – М.: Медицина, 1993, с. 523].
Доксорубицин – противоопухолевый антибиотик антрациклинового ряда. Обладает способностью к блокированию матричной активности ДНК [Машковский М.Д. Лекарственные средства. – М.: Медицина, 1993 с. 534-535].
Известно также применение для терапии опухолей антибиотика актиномицина-D-акриноциклин-ди(треонин-D-валинил-пролинил-саркозил-N-метил-валинил)-лактон [Машковский М. Д. Лекарственные средства. – М.: Медицина, 1993, с. 532-533].
В последние годы делаются активные попытки использовать в терапии опухолей природные цитотоксические агенты, в частности фактор некроза опухолей- (ФНО- (ФНО- ). ФНО- ). ФНО- – белок, имеющий молекулярную массу 17,1 кДa, является цитотоксическим фактором активированных макрофагов и нормальных киллеров. Природный и рекомбинантный ФНО- – белок, имеющий молекулярную массу 17,1 кДa, является цитотоксическим фактором активированных макрофагов и нормальных киллеров. Природный и рекомбинантный ФНО- показали хорошие результаты при испытаниях в качестве противоопухолевого агента на животных [Agier et al., 1988, Факторы некроза опухолей. Справочник по цитолитическим лимфоцитам и компонентам: Эффекторы иммунной системы, Е.R. Podak, ed., CRC Press Inc. Boca Raton, Fla. , p. 105]. Они вызывали некроз ряда экспериментальных опухолей на сингенных мышах и продемонстрировали высокую эффективность на человеческих опухолях, перевитых бестимусным мышам [Asher A. 1987, Studies on the anti-tumor efficacy of systemically administered recombinant tumor necrosis factor against several murine tumors in vivo. J. Immunol. 138(3):963-74.; Kuroda K. et al., 2000, Human tumor necrosis factor-alpha mutant RGD-V29 (F4614) shows potent antitumor activity and reduced toxicity against human tumor xenografted nude mice. Cancer Lett 2000 Oct 16;159(1):33-41]. Были предприняты попытки использовать ФНО- показали хорошие результаты при испытаниях в качестве противоопухолевого агента на животных [Agier et al., 1988, Факторы некроза опухолей. Справочник по цитолитическим лимфоцитам и компонентам: Эффекторы иммунной системы, Е.R. Podak, ed., CRC Press Inc. Boca Raton, Fla. , p. 105]. Они вызывали некроз ряда экспериментальных опухолей на сингенных мышах и продемонстрировали высокую эффективность на человеческих опухолях, перевитых бестимусным мышам [Asher A. 1987, Studies on the anti-tumor efficacy of systemically administered recombinant tumor necrosis factor against several murine tumors in vivo. J. Immunol. 138(3):963-74.; Kuroda K. et al., 2000, Human tumor necrosis factor-alpha mutant RGD-V29 (F4614) shows potent antitumor activity and reduced toxicity against human tumor xenografted nude mice. Cancer Lett 2000 Oct 16;159(1):33-41]. Были предприняты попытки использовать ФНО- для воздействия на опухоли в клинике [Terlikowski S.J. 2001, Tumour necrosis factor and cancer treatment: a historical review and perspectives. Rocz Akad Med Bialymst. , 46:5-18; Lejeune F.J., et al., 2001, Isolated limb perfusion: the European experience. Surg Oncol Clin N Am, 10(4): 821-32; Nashan D. , Luger Т.А. 2001, Cytokines: current status and prospects in the treatment of skin tumors. Hautarzt; 52(8):691-6].
Применение перечисленных выше цитотоксических препаратов осложняется побочными эффектами. Для подавления роста опухолевых клеток требуются высокие дозы этих агентов, токсичные для нормальных клеток и органов. Например, цисплатин негативно влияет на почки. Доксорубицин обладает кумулятивной кардиотоксичностью. При применении ФНО- для воздействия на опухоли в клинике [Terlikowski S.J. 2001, Tumour necrosis factor and cancer treatment: a historical review and perspectives. Rocz Akad Med Bialymst. , 46:5-18; Lejeune F.J., et al., 2001, Isolated limb perfusion: the European experience. Surg Oncol Clin N Am, 10(4): 821-32; Nashan D. , Luger Т.А. 2001, Cytokines: current status and prospects in the treatment of skin tumors. Hautarzt; 52(8):691-6].
Применение перечисленных выше цитотоксических препаратов осложняется побочными эффектами. Для подавления роста опухолевых клеток требуются высокие дозы этих агентов, токсичные для нормальных клеток и органов. Например, цисплатин негативно влияет на почки. Доксорубицин обладает кумулятивной кардиотоксичностью. При применении ФНО- у пациентов наблюдается гипотензия, отек легких, внутрисосудистые тромбы и другие тяжелые побочные эффекты. Другая проблема – приобретение опухолевыми клетками резистентности к цитотоксическим агентам.
К иммуномодуляторам относятся цитокины иммунной системы, пептиды тимуса и костного мозга, низкомолекулярные биорегуляторы бактериального происхождения. В число последних входят мурамилпептиды [Ivanov V. et al., 1987, Structure, design, and synthesis immunoactive peptides. Pure & Appl. Chem. 59, 317-324].
Известен состав для терапии опухолей, содержащий мурамилпептид и цитостатик – цисплатин или доксорубицин [MacEwen E.G., Kurzman, Helfand S., Vail D., London C., Kisseberth W., Rosenthal R.C., Fox L.E., Keller E.T., Obradovich J., et al. Current studies of liposome murarmyl tripeptide (COP 19835A lipid) therapy for metastasis in spontaneous tumors: a progress review. (1994) J. Drug Target, 2(5), 391-6]. Лечение остеосарком у собак проводится с помощью внутривенного раздельного и последовательного введения мурамилпептида(N-ацетилмурамоил-аланил-D-изоглутаминил-аланил-2-(1′, 2’дипальмитоил)-sn-глицеро-3′-фосфорил-этиламида) и цисплатина: курс многоразового введения цисплатина завершается курсом многоразового введения мурамилпептида. При лечении гемангиом у собак применяется многоразовое внутривенное введение доксорубицина с циклофосфамидом параллельно с многоразовым внутривенным введением мурамилпептида. В обоих описанных выше случаях удается добиться значительного увеличения срока жизни животных, существенно превышающего аналогичный показатель при химиотерапии и монотерапии остеосарком и гемангиом у собак с применением одного мурамилпептица. Недостатком данных составов для лечения является прежде всего необходимость многоразового введения препаратов. Лечение существенно осложняется обязательным предварительным оперативным удалением основной опухоли.
Известен состав, содержащий ФНО- у пациентов наблюдается гипотензия, отек легких, внутрисосудистые тромбы и другие тяжелые побочные эффекты. Другая проблема – приобретение опухолевыми клетками резистентности к цитотоксическим агентам.
К иммуномодуляторам относятся цитокины иммунной системы, пептиды тимуса и костного мозга, низкомолекулярные биорегуляторы бактериального происхождения. В число последних входят мурамилпептиды [Ivanov V. et al., 1987, Structure, design, and synthesis immunoactive peptides. Pure & Appl. Chem. 59, 317-324].
Известен состав для терапии опухолей, содержащий мурамилпептид и цитостатик – цисплатин или доксорубицин [MacEwen E.G., Kurzman, Helfand S., Vail D., London C., Kisseberth W., Rosenthal R.C., Fox L.E., Keller E.T., Obradovich J., et al. Current studies of liposome murarmyl tripeptide (COP 19835A lipid) therapy for metastasis in spontaneous tumors: a progress review. (1994) J. Drug Target, 2(5), 391-6]. Лечение остеосарком у собак проводится с помощью внутривенного раздельного и последовательного введения мурамилпептида(N-ацетилмурамоил-аланил-D-изоглутаминил-аланил-2-(1′, 2’дипальмитоил)-sn-глицеро-3′-фосфорил-этиламида) и цисплатина: курс многоразового введения цисплатина завершается курсом многоразового введения мурамилпептида. При лечении гемангиом у собак применяется многоразовое внутривенное введение доксорубицина с циклофосфамидом параллельно с многоразовым внутривенным введением мурамилпептида. В обоих описанных выше случаях удается добиться значительного увеличения срока жизни животных, существенно превышающего аналогичный показатель при химиотерапии и монотерапии остеосарком и гемангиом у собак с применением одного мурамилпептица. Недостатком данных составов для лечения является прежде всего необходимость многоразового введения препаратов. Лечение существенно осложняется обязательным предварительным оперативным удалением основной опухоли.
Известен состав, содержащий ФНО- (16000 ед/мышь) в комбинации с химиотерапевтическими агентами: доксорубицином (1-10 мг/кг), 5-фторурацилом (3-100 мг/кг) циклофосфамидом (50-200 мг/кг), для терапии опухолей Meth A, трансплантированных в сингенных мышей. Наиболее эффективные комбинации индуцируют полную регрессию опухоли. [Regenass U., Muller M., Curschellas E., Matter A. Anti-tumor effects of tumor necrosis factor in combination with chemotherapeutic agents. Int J Cancer. 1987;39(2):266-73]. К недостаткам данного состава относится внутривенная инфузия вводимой композиции. Данный способ введения обеспечивает максимальное проявление цитотоксичности при высоких дозах химиотерапевтических агентов 5 мг/кг доксорубицина, 100 мг/кг цитоксана и 100 мг/кг фторурацила.
Известен состав для лечения онкологических больных, содержащий актиномицин D совместно с ФНО- (16000 ед/мышь) в комбинации с химиотерапевтическими агентами: доксорубицином (1-10 мг/кг), 5-фторурацилом (3-100 мг/кг) циклофосфамидом (50-200 мг/кг), для терапии опухолей Meth A, трансплантированных в сингенных мышей. Наиболее эффективные комбинации индуцируют полную регрессию опухоли. [Regenass U., Muller M., Curschellas E., Matter A. Anti-tumor effects of tumor necrosis factor in combination with chemotherapeutic agents. Int J Cancer. 1987;39(2):266-73]. К недостаткам данного состава относится внутривенная инфузия вводимой композиции. Данный способ введения обеспечивает максимальное проявление цитотоксичности при высоких дозах химиотерапевтических агентов 5 мг/кг доксорубицина, 100 мг/кг цитоксана и 100 мг/кг фторурацила.
Известен состав для лечения онкологических больных, содержащий актиномицин D совместно с ФНО- [Seibel N.L., Dinndorf P.A., Bauer M., Sondel P.M. , Hammond G.D., Reaman G.H. Phase I study of tumor necrosis factor-alpha and actinomycin D in pediatric patients with cancer: a Children’s Cancer Group study. (1994), J. Immunother Emphasis Tumor Immunol, 16(2), 125-31, и Sella A. , Aggarwal B.B., Kilboum R.G., Bui .CA., Zukiwski A.A., Logothetis C.J. Phase I study of tumor necrosis factor plus actinomycin D in patients with androgen-independent prostate cancer. (1995) Cancer Biother, 10(3), 225-35]. Однако широкое применение актиномицина D в онкологии ограничивается тяжелыми побочными реакциями у пациентов.
Известен наиболее близкий к заявленному состав, содержащий цисплатин и ФHО- [Seibel N.L., Dinndorf P.A., Bauer M., Sondel P.M. , Hammond G.D., Reaman G.H. Phase I study of tumor necrosis factor-alpha and actinomycin D in pediatric patients with cancer: a Children’s Cancer Group study. (1994), J. Immunother Emphasis Tumor Immunol, 16(2), 125-31, и Sella A. , Aggarwal B.B., Kilboum R.G., Bui .CA., Zukiwski A.A., Logothetis C.J. Phase I study of tumor necrosis factor plus actinomycin D in patients with androgen-independent prostate cancer. (1995) Cancer Biother, 10(3), 225-35]. Однако широкое применение актиномицина D в онкологии ограничивается тяжелыми побочными реакциями у пациентов.
Известен наиболее близкий к заявленному состав, содержащий цисплатин и ФHО- , который может быть успешно использован для уничтожения клеток пассируемых линий OVCAR-3 и SK-OV-3 аденокарциномы яичника человека, резистентных к цитотоксическому действию цисплатины и ФНО- , который может быть успешно использован для уничтожения клеток пассируемых линий OVCAR-3 и SK-OV-3 аденокарциномы яичника человека, резистентных к цитотоксическому действию цисплатины и ФНО- , используемых по отдельности [Mutch D., Powell С., Kao M., Collins J. In vitro analysis of the anticancer potential of tumor necrosis factor in combination with cisplatin. Gynecol Oncol. 1989 Sep.; 34(3):328-33].
К недостаткам известного состава относится ограниченный цитолиз опухолевых клеток в культуре, максимальный уровень которого не превышает 56%.
Изобретение решает задачу повышения эффективности состава для уничтожения ФНО- , используемых по отдельности [Mutch D., Powell С., Kao M., Collins J. In vitro analysis of the anticancer potential of tumor necrosis factor in combination with cisplatin. Gynecol Oncol. 1989 Sep.; 34(3):328-33].
К недостаткам известного состава относится ограниченный цитолиз опухолевых клеток в культуре, максимальный уровень которого не превышает 56%.
Изобретение решает задачу повышения эффективности состава для уничтожения ФНО- -чувствительных опухолевых клеток и снижения токсичности препарата.
Поставленная задача решается за счет того, что состав для уничтожения ФНО- -чувствительных опухолевых клеток и снижения токсичности препарата.
Поставленная задача решается за счет того, что состав для уничтожения ФНО- -чувствительных опухолевых клеток, содержащий цитостатик и ФНО- -чувствительных опухолевых клеток, содержащий цитостатик и ФНО- , в качестве цитостатика содержит интерколирующие в ДНК препараты и дополнительно биологически активный мурамилпептид при массовом соотношении мурамилпептида, цитостатика и ФНО- , в качестве цитостатика содержит интерколирующие в ДНК препараты и дополнительно биологически активный мурамилпептид при массовом соотношении мурамилпептида, цитостатика и ФНО- 1:0,06-300:0,00001-0,1.
Заявляемый состав, предназначенный для уничтожения ФНО- 1:0,06-300:0,00001-0,1.
Заявляемый состав, предназначенный для уничтожения ФНО- -чувствительных клеток, содержит цитостатик из группы интерколирующих в ДНК препаратов, взаимодействующих с хроматином, в частности цисплатин, доксорубицин или актиномицин D, цитокин ФНО- -чувствительных клеток, содержит цитостатик из группы интерколирующих в ДНК препаратов, взаимодействующих с хроматином, в частности цисплатин, доксорубицин или актиномицин D, цитокин ФНО- и мурамилпептид: ГМДП (N-ацетилглюкозаминил- и мурамилпептид: ГМДП (N-ацетилглюкозаминил- 1–>4-N-ацетилмурамоил-аланил-D-изоглутамин), ГМДП-К (N-ацетилглюкозаминил- 1–>4-N-ацетилмурамоил-аланил-D-изоглутамин), ГМДП-К (N-ацетилглюкозаминил- 1–>4-N-ацетилмурамоил-аланил-D-изоглутаминовая кислота) или другой иммунологически активный мурамилпептид.
Преимущество предлагаемой тройной комбинации препаратов (цитостатик, ФНО- 1–>4-N-ацетилмурамоил-аланил-D-изоглутаминовая кислота) или другой иммунологически активный мурамилпептид.
Преимущество предлагаемой тройной комбинации препаратов (цитостатик, ФНО- и мурамилпептид) состоит в использовании реагентов, взаимоусиливающих противоопухолевое действие каждого из составляющих композицию. Это позволяет снизить эффективные концентрации реагентов. Например, в комбинации (цисплатин, ФНО- и мурамилпептид) состоит в использовании реагентов, взаимоусиливающих противоопухолевое действие каждого из составляющих композицию. Это позволяет снизить эффективные концентрации реагентов. Например, в комбинации (цисплатин, ФНО- и мурамилпептид) для достижения 100% выживаемости мышей линии Ваlb/с с асцитной карциномой Эрлиха используются в 4 раза более низкие дозы цисплатина и в 5-20 раз более низкие дозы ФНО- и мурамилпептид) для достижения 100% выживаемости мышей линии Ваlb/с с асцитной карциномой Эрлиха используются в 4 раза более низкие дозы цисплатина и в 5-20 раз более низкие дозы ФНО- , чем приводимые в литературе при монотерапии перевиваемых опухолей у мышей цисплатином (Landrito J. E. , Yoshiga К., Sakurai К., Takada К. Effects of intralesional injection of cisplatin dissolved in urografin and lipiodol on Ehrlich ascites tumor and normal tissues of CD-1 mice. (1994) Cancer Chemother Pharmacol; 34(4): 323-30 и Krug H., Taubert G., Lenschow S. Proliferation kinetics of Ehrlich ascites tumors during cisplatin administration. (1990) Acta Histochem Suppl; 39:61-65) и ФНО- , чем приводимые в литературе при монотерапии перевиваемых опухолей у мышей цисплатином (Landrito J. E. , Yoshiga К., Sakurai К., Takada К. Effects of intralesional injection of cisplatin dissolved in urografin and lipiodol on Ehrlich ascites tumor and normal tissues of CD-1 mice. (1994) Cancer Chemother Pharmacol; 34(4): 323-30 и Krug H., Taubert G., Lenschow S. Proliferation kinetics of Ehrlich ascites tumors during cisplatin administration. (1990) Acta Histochem Suppl; 39:61-65) и ФНО- (Obrador E, Navarro J, Mompo J, Asensi M, Pellicer JA, Estrela JM. Glutathione and the rate of cellular proliferation determine tumour cell sensitivity to tumour necrosis factor in vivo. (1997) Biochem J; 325 (Pt 1), 183-189 и Krosnick J., Mule J., Mctosh J., Rosenberg S. Augmentation of antitumor efficacy by the combination of recombinant TNF and chemotherapeutic agents in vivo. (1989) Cancer Res., 49, 3729-3733). Несомненным преимуществом является однократное введение препаратов. Следует отметить, что в предлагаемой противоопухолевой комбинации используют доступный отечественный препарат ГМДП и широко применяемые в онкологической практике цитостатики цисплатин и доксорубицин.
В описываемом составе используют препарат рекомбинантного ФНО- (Obrador E, Navarro J, Mompo J, Asensi M, Pellicer JA, Estrela JM. Glutathione and the rate of cellular proliferation determine tumour cell sensitivity to tumour necrosis factor in vivo. (1997) Biochem J; 325 (Pt 1), 183-189 и Krosnick J., Mule J., Mctosh J., Rosenberg S. Augmentation of antitumor efficacy by the combination of recombinant TNF and chemotherapeutic agents in vivo. (1989) Cancer Res., 49, 3729-3733). Несомненным преимуществом является однократное введение препаратов. Следует отметить, что в предлагаемой противоопухолевой комбинации используют доступный отечественный препарат ГМДП и широко применяемые в онкологической практике цитостатики цисплатин и доксорубицин.
В описываемом составе используют препарат рекомбинантного ФНО- человека, (лаборатория химии генов ИБХ им. М.М. Шемякина и Ю.А. Овчинникова РАН) с активностью 4х107 ед. на 1 мг белка, ГМДП (фирма “Пептек”), Россия, цисплатин, доксорубицин и актиномицин D-(фирма “Sigma”, США), ЗФР-0,1 М фосфатный буфер, рН 7,4, содержащий 0,15 М NaСl), приготовленный из коммерческих солей марки хч на бидистиллированной воде.
Изобретение иллюстрируют примеры.
Пример 1.
Навеску препарата цисплатина 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Полученный раствор цисплатина разводят стерильным физиологическим раствором до концентрации 9 мкг/мл. Раствор рекомбинантного ФНО- человека, (лаборатория химии генов ИБХ им. М.М. Шемякина и Ю.А. Овчинникова РАН) с активностью 4х107 ед. на 1 мг белка, ГМДП (фирма “Пептек”), Россия, цисплатин, доксорубицин и актиномицин D-(фирма “Sigma”, США), ЗФР-0,1 М фосфатный буфер, рН 7,4, содержащий 0,15 М NaСl), приготовленный из коммерческих солей марки хч на бидистиллированной воде.
Изобретение иллюстрируют примеры.
Пример 1.
Навеску препарата цисплатина 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Полученный раствор цисплатина разводят стерильным физиологическим раствором до концентрации 9 мкг/мл. Раствор рекомбинантного ФНО- (0,6 мг/мл) в ЗФР 0,1% бычьим сывороточным альбумином разводят стерильным физиологическим раствором до концентрации 3,75х10-3 мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологического раствора или ЗФР и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают приготовленные препараты цисплатина, ФНО- (0,6 мг/мл) в ЗФР 0,1% бычьим сывороточным альбумином разводят стерильным физиологическим раствором до концентрации 3,75х10-3 мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологического раствора или ЗФР и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают приготовленные препараты цисплатина, ФНО- и ГМДП в равных объемах и по 100 мкл добавляют в чашки Петри с опухолевыми клетками, культивируемыми в 900 мкл среды RPMI-1640 (фирмы “Flow Laboratories”, Шотландия), содержащей 10% FCS (эмбриональная телячья сыворотка фирмы “Gibco BRL”), создавая тем самым концентрацию ГМДП 5 мкг/мл, цисплатина 0,3 мкг/мл и ФНО- и ГМДП в равных объемах и по 100 мкл добавляют в чашки Петри с опухолевыми клетками, культивируемыми в 900 мкл среды RPMI-1640 (фирмы “Flow Laboratories”, Шотландия), содержащей 10% FCS (эмбриональная телячья сыворотка фирмы “Gibco BRL”), создавая тем самым концентрацию ГМДП 5 мкг/мл, цисплатина 0,3 мкг/мл и ФНО- 0,125х10-3 мкг/мл, (массовое соотношение 1:0,06:0,000025).
Для тестирования цитолиза клеток линии L929 под влиянием исследуемого состава препаратов клетки, культивируемые во флаконах в атмосфере 5% СO2 при 37oС, снимают раствором трипсина (0,5%) и помещают в центрифужные стаканы объемом 50 мл, содержащие 30 мл среды RPMI-1640 с FCS. После центрифугирования при 300g клеточный осадок суспендируют в культуральной среде с 10% FCS. Отбирают из образца аликвоту, пользуясь камерой Горяева, определяют концентрацию клеток, доводят клеточную суспензию до плотности 500 кл/мл и помещают в чашки с диаметром 30 мм. Через 24 часа культивирования добавляют тестируемые препараты. Инкубацию продолжают в течение 7 дней в атмосфере 5% СО2 при 37oС. После чего среду отбирают пастеровской пипеткой, прикрепленные к пластику клетки промывают 3 раза ЗФР (0,1 М фосфатный буфер, рН 7,4, содержащий 0,15 М NaCl). Отмытые клетки фиксируют, заливая их 0,5 мл смеси метанол:уксусная кислота (объемное отношение 3:1) и оставляя на 20 мин при комнатной температуре. Затем фиксирующий раствор отбирают пастеровской пипеткой, добавляют 0,5 мл 0,5% раствор кристаллического фиолетового красителя (коммерческий краситель “Sigma”) в 20% метаноле и инкубируют при комнатной температуре в течение 20 мин. Окрашенные клетки отмывают от избытка красителя дистиллированной водой, процедуру отмывания повторяют 7 раз. Чашки высушивают и производят подсчет окрашенных колоний визуально в проходящем свете. Процент мертвых клеток определяют по формуле 0,125х10-3 мкг/мл, (массовое соотношение 1:0,06:0,000025).
Для тестирования цитолиза клеток линии L929 под влиянием исследуемого состава препаратов клетки, культивируемые во флаконах в атмосфере 5% СO2 при 37oС, снимают раствором трипсина (0,5%) и помещают в центрифужные стаканы объемом 50 мл, содержащие 30 мл среды RPMI-1640 с FCS. После центрифугирования при 300g клеточный осадок суспендируют в культуральной среде с 10% FCS. Отбирают из образца аликвоту, пользуясь камерой Горяева, определяют концентрацию клеток, доводят клеточную суспензию до плотности 500 кл/мл и помещают в чашки с диаметром 30 мм. Через 24 часа культивирования добавляют тестируемые препараты. Инкубацию продолжают в течение 7 дней в атмосфере 5% СО2 при 37oС. После чего среду отбирают пастеровской пипеткой, прикрепленные к пластику клетки промывают 3 раза ЗФР (0,1 М фосфатный буфер, рН 7,4, содержащий 0,15 М NaCl). Отмытые клетки фиксируют, заливая их 0,5 мл смеси метанол:уксусная кислота (объемное отношение 3:1) и оставляя на 20 мин при комнатной температуре. Затем фиксирующий раствор отбирают пастеровской пипеткой, добавляют 0,5 мл 0,5% раствор кристаллического фиолетового красителя (коммерческий краситель “Sigma”) в 20% метаноле и инкубируют при комнатной температуре в течение 20 мин. Окрашенные клетки отмывают от избытка красителя дистиллированной водой, процедуру отмывания повторяют 7 раз. Чашки высушивают и производят подсчет окрашенных колоний визуально в проходящем свете. Процент мертвых клеток определяют по формуле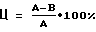 где А – число колоний в контроле (в чашке, в которую вместо препаратов вносят ЗФР) В – число колоний в образце, обработанном препаратами. Ц=87  5% 5%Эффект комбинации препаратов сравнивают с рядом контрольных образцов клеточных культуры, инкубированных с: – физиологическим раствором или ЗФР Ц=0%; – одним цисплатином в концентрации 0,3 мкг/мл Ц=45  2%; 2%;– одним ФНО-  в концентрации 0,125 х10-3 мкг/мл Ц=25 в концентрации 0,125 х10-3 мкг/мл Ц=25 2%; 2%;– одним ГМДП в концентрации 5 мкг/мл Ц=2  2%; 2%;– комбинацией цисплатина в концентрации 0,3 мкг/мл с ФНО-  в концентрации 0,125 х 10-3 мкг/мл Ц=64 в концентрации 0,125 х 10-3 мкг/мл Ц=64 3%; 3%;– комбинацией цисплатина в концентрации 0,3 мкг/мл с ГМДП в концентрации 5 мкг/мл Ц=67  3%; 3%;– комбинацией ФНО-  в концентрации 0,125 х 10-3 мкг/мл с ГМДП в концентрации 5 мкг/мл Ц=44 в концентрации 0,125 х 10-3 мкг/мл с ГМДП в концентрации 5 мкг/мл Ц=44 2%.
Пример 2.
Состав готовят по примеру 1, но используют растворы ГМДП и ФНО- 2%.
Пример 2.
Состав готовят по примеру 1, но используют растворы ГМДП и ФНО- с концентрациями 30 мкг/мл и 0,375х с концентрациями 30 мкг/мл и 0,375х10-3 мкг/мл соответственно. Смешивают в равных объемах ГМДП, цисплатин и ФНО-  , добавляют в культуральную среду и получают раствор, содержащий 1 мкг/мл ГМДП, 0,3 мкг/мл цисплатина и 0,0125х10-3 мкг/мл ФНО- , добавляют в культуральную среду и получают раствор, содержащий 1 мкг/мл ГМДП, 0,3 мкг/мл цисплатина и 0,0125х10-3 мкг/мл ФНО- (массовое соотношение 1:0,3:0,0000125). Испытания проводят по примеру 1. Ц=72%.
Пример 3.
Состав готовят по примеру 1, но используют растворы ГМДП с концентрацией 3 мкг/мл, цисплатина с концентрацией 900 мкг/мл, ФНО- (массовое соотношение 1:0,3:0,0000125). Испытания проводят по примеру 1. Ц=72%.
Пример 3.
Состав готовят по примеру 1, но используют растворы ГМДП с концентрацией 3 мкг/мл, цисплатина с концентрацией 900 мкг/мл, ФНО- с концентрацией 0,0375 мкг/мл и получают рабочий раствор, содержащий 0,1 мкг/мл ГМДП, 30 мкг/мл цисплатина и 1,25х10-3мкг/мл ФНО- с концентрацией 0,0375 мкг/мл и получают рабочий раствор, содержащий 0,1 мкг/мл ГМДП, 30 мкг/мл цисплатина и 1,25х10-3мкг/мл ФНО- (массовое соотношение 1:300: 0,0125). Испытания проводят по примеру 1. Ц=100%.
Пример 4.
Состав готовят по примеру 1, но в качестве цитостатика используют доксорубицин. Препарат доксорубицина 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Полученный раствор доксорубицина разводят стерильным физиологическим раствором до концентрации 30 мкг/м. Раствор рекомбинантного ФНО- (массовое соотношение 1:300: 0,0125). Испытания проводят по примеру 1. Ц=100%.
Пример 4.
Состав готовят по примеру 1, но в качестве цитостатика используют доксорубицин. Препарат доксорубицина 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Полученный раствор доксорубицина разводят стерильным физиологическим раствором до концентрации 30 мкг/м. Раствор рекомбинантного ФНО- (0,6 мг/мл) разводят стерильным физиологическим раствором до концентрации 7,5х10-3мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологического раствора или ЗФР и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают приготовленные препараты доксорубицина, ФНО- (0,6 мг/мл) разводят стерильным физиологическим раствором до концентрации 7,5х10-3мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологического раствора или ЗФР и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают приготовленные препараты доксорубицина, ФНО- и ГМДП в равных объемах и по 20 мкл добавляют в лунки 96-луночного планшета с опухолевыми клетками, культивируемыми в 180 мкл среды RPMI-1640, содержащей 10% FCS, создавая тем самым концентрацию 1 мкг/мл ГМДП, 1 мкг/мл докорубицина и 0,25х10-3 мкг/мл ФНО- и ГМДП в равных объемах и по 20 мкл добавляют в лунки 96-луночного планшета с опухолевыми клетками, культивируемыми в 180 мкл среды RPMI-1640, содержащей 10% FCS, создавая тем самым концентрацию 1 мкг/мл ГМДП, 1 мкг/мл докорубицина и 0,25х10-3 мкг/мл ФНО- (массовое соотношение 1:1:0,00025).
Оценку уровня цитолиза производят в тесте с кристаллическим фиолетовым: клетки (2х104 кл./лунку) в 100 мкл RPMI-1640, содержащей 10% FCS, помещают в 96-луночный планшет. После 48 часовой инкубации клеточных культур с составом препаратов в атмосфере 5% СО2 при 37oС среду убирают, клетки промывают 3 раза ЗФР, фиксируют в смеси метанол/уксусная кислота 3/1 в течение 20 мин и окрашивают 0,5% раствором кристаллического фиолетового в 20% метаноле в течение 20 мин. Затем ячейки планшета отмывают 7 раз водой и высушивают. Краситель, связавшийся с клетками, растворяют в 1% SDS и уровень его поглощения при 540 нм измеряют на спектрофотометре Titertek Multiskan MCC/340. Процент цитотоксичности определяют по формуле (массовое соотношение 1:1:0,00025).
Оценку уровня цитолиза производят в тесте с кристаллическим фиолетовым: клетки (2х104 кл./лунку) в 100 мкл RPMI-1640, содержащей 10% FCS, помещают в 96-луночный планшет. После 48 часовой инкубации клеточных культур с составом препаратов в атмосфере 5% СО2 при 37oС среду убирают, клетки промывают 3 раза ЗФР, фиксируют в смеси метанол/уксусная кислота 3/1 в течение 20 мин и окрашивают 0,5% раствором кристаллического фиолетового в 20% метаноле в течение 20 мин. Затем ячейки планшета отмывают 7 раз водой и высушивают. Краситель, связавшийся с клетками, растворяют в 1% SDS и уровень его поглощения при 540 нм измеряют на спектрофотометре Titertek Multiskan MCC/340. Процент цитотоксичности определяют по формуле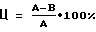 где А – показатель экстинкции в контроле (в образце, в который вместо препаратов вносили ЗФР), В – показатель экстинкции в образце, обработанном препаратами. Ц=90  3%.
Пример 5.
Состав готовят по примеру 1, но в качестве цитостатика используют актиномицин D. Препарат актиномицина D 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Полученный раствор актиномицина D разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают растворы актиномицина D (30 мкг/мл), ФНО- 3%.
Пример 5.
Состав готовят по примеру 1, но в качестве цитостатика используют актиномицин D. Препарат актиномицина D 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Полученный раствор актиномицина D разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают растворы актиномицина D (30 мкг/мл), ФНО- и ГМДП в равных объемах и по 20 мкл добавляют в лунки 96-луночного планшета с опухолевыми клетками, культивируемыми в 180 мкл среды RPMI-1640 с 10% FCS, и получают раствор, содержащий 0,1 мкг/мл ГМДП, 1 мкг/мл, актиномицина D и 0,01 мкг/мл ФНО- и ГМДП в равных объемах и по 20 мкл добавляют в лунки 96-луночного планшета с опухолевыми клетками, культивируемыми в 180 мкл среды RPMI-1640 с 10% FCS, и получают раствор, содержащий 0,1 мкг/мл ГМДП, 1 мкг/мл, актиномицина D и 0,01 мкг/мл ФНО- (массовое соотношение 1:10:0,1). Испытания проводят по примеру 4. Ц=100% (массовое соотношение 1:10:0,1). Испытания проводят по примеру 4. Ц=100%Пример 6. Состав готовят по примеру 1, но используют в качестве мурамилпептида ГМДП-К в концентрации 300 мкг/мл, цисплатин берут в концентрации 90 мкг/мл, ФНО-  – 0,375 мкг/мл и получают раствор, содержащий 10 мкг/мл ГМДП-К, 3 мкг/мл цисплатина и 0,0125 мкг/мл ФНО- – 0,375 мкг/мл и получают раствор, содержащий 10 мкг/мл ГМДП-К, 3 мкг/мл цисплатина и 0,0125 мкг/мл ФНО- (массовое соотношение 1:0,3: 0,00125). Испытания проводят по примеру 4. Ц=100%.
Пример 7.
Навеску препарата цисплатина 1 мг растворяют в 1 мл физиологического раствора на магнитной мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Цисплатин разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Раствор рекомбинантного ФНО- (массовое соотношение 1:0,3: 0,00125). Испытания проводят по примеру 4. Ц=100%.
Пример 7.
Навеску препарата цисплатина 1 мг растворяют в 1 мл физиологического раствора на магнитной мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Цисплатин разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Раствор рекомбинантного ФНО- (0,6 мг/мл) разводят стерильным физиологическим раствором до концентрации 37,5 х10-3 мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологического раствора и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают приготовленные препараты цисплатина, ФНО- (0,6 мг/мл) разводят стерильным физиологическим раствором до концентрации 37,5 х10-3 мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологического раствора и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 30 мкг/мл. Смешивают приготовленные препараты цисплатина, ФНО- и ГМДП в равных объемах. Добавляют по 20 мкл смеси в лунки 96-луночного планшета с опухолевыми клетками линии MCF7, культивируемыми в 180 мкл RPMI-1640 с 10% FCS, создавая тем самым концентрацию ГМДП 1 мкг/мл, цисплатина 1 мкг/м и ФНО- и ГМДП в равных объемах. Добавляют по 20 мкл смеси в лунки 96-луночного планшета с опухолевыми клетками линии MCF7, культивируемыми в 180 мкл RPMI-1640 с 10% FCS, создавая тем самым концентрацию ГМДП 1 мкг/мл, цисплатина 1 мкг/м и ФНО- 0,0125 мкг/мл (массовое соотношение 1:1:0,0125).
Тестирование влияния комбинации препаратов на жизнеспособность опухолевых клеток клетки линии аденокарциномы молочной железы человека MCF7, культивируемых во флаконах в атмосфере 5% СO2 при 37oС. Клетки снимают с поверхности флаконов раствором трипсина (0,5%) и помещают в центрифужные стаканы объемом 50 мл, содержащие 30 мл среды RPMI-1640 с 10% FCS. После центрифугирования при 300g клеточный осадок суспендируют в культуральной среде RPMI-1640 с 10% FCS. Отбирают из образца аликвоту, пользуясь камерой Горяева, определяют концентрацию клеток, доводят клеточную суспензию до плотности 1х105 кл/мл и помещают в планшеты. Через 24 часа культивирования добавляют тестируемые препараты. Клетки инкубируют с комбинацией препаратов в течение 120 часов в атмосфере 5% СО2 при 37oС. Затем определяют жизнеспособность клеток в опытных и контрольных культурах.
Жизнеспособность клеток оценивают колориметрическим методом по степени восстановления красителя МТТ – [3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолиумбромид] – окрашенного субстрата для митохондриальных дегидрогеназ (“Sigma” США) – до формазона. Для этого за 2,5 часа до окончания культивирования в каждую лунку добавляют 20 мкл краски МТТ с концентрацией 2,5 мг/мл. По окончании инкубации планшеты центрифугируют при 300 g в течение 10 мин. Надосадочную жидкость удаляют из лунок, осадок растворяют в 100 мкл диметилсульфоксида при непрерывном встряхивании в течение 15 мин. Оптическую плотность содержимого лунок измеряют на приборе Titertek Multiskan MCC/340 при длине волны 540 нм. Процент цитотоксичности определяют по формуле 0,0125 мкг/мл (массовое соотношение 1:1:0,0125).
Тестирование влияния комбинации препаратов на жизнеспособность опухолевых клеток клетки линии аденокарциномы молочной железы человека MCF7, культивируемых во флаконах в атмосфере 5% СO2 при 37oС. Клетки снимают с поверхности флаконов раствором трипсина (0,5%) и помещают в центрифужные стаканы объемом 50 мл, содержащие 30 мл среды RPMI-1640 с 10% FCS. После центрифугирования при 300g клеточный осадок суспендируют в культуральной среде RPMI-1640 с 10% FCS. Отбирают из образца аликвоту, пользуясь камерой Горяева, определяют концентрацию клеток, доводят клеточную суспензию до плотности 1х105 кл/мл и помещают в планшеты. Через 24 часа культивирования добавляют тестируемые препараты. Клетки инкубируют с комбинацией препаратов в течение 120 часов в атмосфере 5% СО2 при 37oС. Затем определяют жизнеспособность клеток в опытных и контрольных культурах.
Жизнеспособность клеток оценивают колориметрическим методом по степени восстановления красителя МТТ – [3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолиумбромид] – окрашенного субстрата для митохондриальных дегидрогеназ (“Sigma” США) – до формазона. Для этого за 2,5 часа до окончания культивирования в каждую лунку добавляют 20 мкл краски МТТ с концентрацией 2,5 мг/мл. По окончании инкубации планшеты центрифугируют при 300 g в течение 10 мин. Надосадочную жидкость удаляют из лунок, осадок растворяют в 100 мкл диметилсульфоксида при непрерывном встряхивании в течение 15 мин. Оптическую плотность содержимого лунок измеряют на приборе Titertek Multiskan MCC/340 при длине волны 540 нм. Процент цитотоксичности определяют по формуле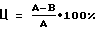 где А – показатель экстинкции в контроле (в образце, в который вместо препаратов вносили ЗФР), “ В – показатель экстинкции в образце, обработанном препаратами. Ц=69  3%.
Эффект комбинации препаратов сравнивают с рядом контрольных образцов: клеточные культуры инкубированные с 3%.
Эффект комбинации препаратов сравнивают с рядом контрольных образцов: клеточные культуры инкубированные с– физиологическим раствором или ЗФР. Ц=0%; – одним цисплатином в концентрации 1 мкг/мл. Ц=28  1%; 1%;– одним ФНО-  в концентрации 0,0125 мкг/мл. Ц=42 в концентрации 0,0125 мкг/мл. Ц=42 2%; 2%;– одним ГМДП в концентрации 1 мкг/мл. Ц=2  1%; 1%;– комбинацией цисплатина в концентрации 1 мкг/мл с ФНО-  в концентрации 0,0125 мкг/мл. Ц=61 в концентрации 0,0125 мкг/мл. Ц=61 3%; 3%;– комбинацией цисплатина в концентрации 0,3 мкг/мл с ГМДП в концентрации 1 мкг/мл. Ц=32  2%; 2%;– комбинацией ФНО-  в концентрации 0,0125 мкг/мл с ГМДП в концентрации 1 мкг/мл Ц=60 в концентрации 0,0125 мкг/мл с ГМДП в концентрации 1 мкг/мл Ц=60 3%.
Пример 8.
Состав готовят по примеру 7, но в качестве цитостатика используют доксорубицин в концентрации 120 мкг/мл и получают раствор, содержащий 1 мкг/мл ГМДП, 4,0 мкг/мл доксорубицина и 0,0125 мкг/мл ФНО- 3%.
Пример 8.
Состав готовят по примеру 7, но в качестве цитостатика используют доксорубицин в концентрации 120 мкг/мл и получают раствор, содержащий 1 мкг/мл ГМДП, 4,0 мкг/мл доксорубицина и 0,0125 мкг/мл ФНО-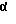 (массовое соотношение 1:4:0,0125). Испытания проводят по примеру 7. Ц=82 (массовое соотношение 1:4:0,0125). Испытания проводят по примеру 7. Ц=82 3%.
Пример 9.
Состав готовят по примеру 7, но используют цисплатин в концентрации 90 мкг/мл и получают раствор, содержащий 1 мкг/мл ГМДП, 3,0 мкг/мл цисплатина, 0,0125 мкг/мл ФНО- 3%.
Пример 9.
Состав готовят по примеру 7, но используют цисплатин в концентрации 90 мкг/мл и получают раствор, содержащий 1 мкг/мл ГМДП, 3,0 мкг/мл цисплатина, 0,0125 мкг/мл ФНО- (массовое соотношение 1:3:0,0125). Испытания проводят на клетках линии гистиоцитарной лимфомы человека U937 как на линии MCF7 со следующими изменениями. Для разнесения клеток по 96-луночному планшету клетки линии U937 из флаконов собирают пипетированием их в культуральной среде. Время инкубации клеток с комбинациями препаратов составляет 72 часа. Ц= 90 (массовое соотношение 1:3:0,0125). Испытания проводят на клетках линии гистиоцитарной лимфомы человека U937 как на линии MCF7 со следующими изменениями. Для разнесения клеток по 96-луночному планшету клетки линии U937 из флаконов собирают пипетированием их в культуральной среде. Время инкубации клеток с комбинациями препаратов составляет 72 часа. Ц= 90 3%.
Пример 10.
Состав, полученный по примеру 4, добавляют по 20 мкл смеси в лунки 96-луночного планшета с опухолевыми клетками, взятыми от онкологических больных, Экссудаты из плевральной полости онкологических больных получают из ОНЦ РАМН, Москва. Клетки экссудата центрифугируют при 300g и осадок ресуспендируют в среде RPMI-1640 в объеме в 10 раз меньше первоначального. Полученную суспензию (по 7 мл) осторожно наслаивают на лимфоцит разделяющую среду (фиколл/диатризоат с плотностью 1,077 г/мл), разлитую по 4 мл в 15-ти мл центрифужные пробирки. Затем суспензию центрифугируют 25 мин при 600g при комнатной температуре. Опухолевые клетки и лейкоциты локализуются в интерфазе градиента. Интерфазу отбирают пастеровской пипеткой. Клетки отмывают дважды, центрифугируя при 300g 10 мин в культуральной среде без FCS. Затем клетки суспендируют в среде RPMI-1640 с 10% FCS при плотности 1х105 клеток/мл и помещают по 180 мкл суспензии в ячейки 96-луночного планшета. Время инкубации клеток с составом препаратов составляет 72 часа.
Оценку уровня цитолиза проводят в тесте с трипановым синим: клетки снимают резиновым скребком, промывают 2 раза средой без сыворотки. Снятые клетки и смывы объединяют в один образец. Из образца отбирают аликвоту 50 мкл, добавляют к ней 10 мкл 0,4% раствора трипанового синего и сразу помещают в камеру Горяева для подсчета живых и мертвых клеток (мертвые клетки в отличие от живых включали краску). При этом считают не менее 100 опухолевых клеток. Процент цитотоксичности определяют по формуле 3%.
Пример 10.
Состав, полученный по примеру 4, добавляют по 20 мкл смеси в лунки 96-луночного планшета с опухолевыми клетками, взятыми от онкологических больных, Экссудаты из плевральной полости онкологических больных получают из ОНЦ РАМН, Москва. Клетки экссудата центрифугируют при 300g и осадок ресуспендируют в среде RPMI-1640 в объеме в 10 раз меньше первоначального. Полученную суспензию (по 7 мл) осторожно наслаивают на лимфоцит разделяющую среду (фиколл/диатризоат с плотностью 1,077 г/мл), разлитую по 4 мл в 15-ти мл центрифужные пробирки. Затем суспензию центрифугируют 25 мин при 600g при комнатной температуре. Опухолевые клетки и лейкоциты локализуются в интерфазе градиента. Интерфазу отбирают пастеровской пипеткой. Клетки отмывают дважды, центрифугируя при 300g 10 мин в культуральной среде без FCS. Затем клетки суспендируют в среде RPMI-1640 с 10% FCS при плотности 1х105 клеток/мл и помещают по 180 мкл суспензии в ячейки 96-луночного планшета. Время инкубации клеток с составом препаратов составляет 72 часа.
Оценку уровня цитолиза проводят в тесте с трипановым синим: клетки снимают резиновым скребком, промывают 2 раза средой без сыворотки. Снятые клетки и смывы объединяют в один образец. Из образца отбирают аликвоту 50 мкл, добавляют к ней 10 мкл 0,4% раствора трипанового синего и сразу помещают в камеру Горяева для подсчета живых и мертвых клеток (мертвые клетки в отличие от живых включали краску). При этом считают не менее 100 опухолевых клеток. Процент цитотоксичности определяют по формуле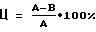 где А – число мертвых клеток в образце, “ В – общее число клеток. Ц=100%. Пример 11. Навеску препарата цисплатина 1 мг растворяют в 1 мл физиологического раствора на мешалке при комнатной температуре и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. Цисплатин разводят стерильным физиологическим раствором до концентрации 200 мкг/мл. Раствор рекомбинантного ФНО-  (0,6 мг/мл) разводят стерильным физиологическим раствором до концентрации 0,625 мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологическим раствора и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 750 мкг/мл. Смешивают приготовленные растворы цисплатина, ФНО- (0,6 мг/мл) разводят стерильным физиологическим раствором до концентрации 0,625 мкг/мл. Навеску ГМДП (1 мг) растворяют в 1 мл физиологическим раствора и стерилизуют, используя мембранный фильтр с диаметром пор 0,2 мкм. ГМДП разводят стерильным физиологическим раствором до концентрации 750 мкг/мл. Смешивают приготовленные растворы цисплатина, ФНО- и ГМДП в равных объемах и вводят полученный препарат по 0,6 мл в мышь внутрибрюшинно. Таким образом, в каждую особь с асцитной карциномой Эрлиха, имплантированной внутрибрюшинно мышам линии Ваlb/с, вводят состав, включающий 41,7 мкг/мл ГМДП, 66,7 мкг/мл цисплатина и 0,210 мкг/мл ФНО- и ГМДП в равных объемах и вводят полученный препарат по 0,6 мл в мышь внутрибрюшинно. Таким образом, в каждую особь с асцитной карциномой Эрлиха, имплантированной внутрибрюшинно мышам линии Ваlb/с, вводят состав, включающий 41,7 мкг/мл ГМДП, 66,7 мкг/мл цисплатина и 0,210 мкг/мл ФНО- (массовое соотношение 1: 1,6: 0,0050). Изменяя конечный объем композиции препаратов от 0,04 до 4 мл, пропорционально изменяют концентрацию вводимых агентов, сохраняя их массовое соотношение. Доза препаратов составляет 25 мкг/мышь ГМДП (6,25 мг/м2), 0,125 мкг/мышь ФНО- (массовое соотношение 1: 1,6: 0,0050). Изменяя конечный объем композиции препаратов от 0,04 до 4 мл, пропорционально изменяют концентрацию вводимых агентов, сохраняя их массовое соотношение. Доза препаратов составляет 25 мкг/мышь ГМДП (6,25 мг/м2), 0,125 мкг/мышь ФНО- (0,031 мкг/м2) и 40 мкг/мышь цисплатина (10 мг/м2). Группа мышей состоит из 10 особей. Оценивают среднюю продолжительность жизни и выживаемость. Средняя продолжительность жизни определяют как сумму продолжительности жизни в днях всех умерших в группе животных, деленную на количество этих животных. Выживаемость определяют по формуле (0,031 мкг/м2) и 40 мкг/мышь цисплатина (10 мг/м2). Группа мышей состоит из 10 особей. Оценивают среднюю продолжительность жизни и выживаемость. Средняя продолжительность жизни определяют как сумму продолжительности жизни в днях всех умерших в группе животных, деленную на количество этих животных. Выживаемость определяют по формуле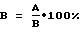 где А – число живых мышей через 7 мес. после перевивания им опухолей, В – первоначальное число мышей в группе (10 особей). В группе мышей, в которой проводилась описанная терапия, выживаемость составила 100%. Эффект комбинации препаратов, оцениваемый выживаемости мышей и продолжительности жизни, сравнивают с аналогичными параметрами животных контрольных групп, каждая из которых состоит из 10 особей с имплантированными клетками асцита карциномы Эрлиха. Контрольные группы состоят из опухоленосителей, которым вводили следующие препараты: – физиологический раствор – у всех мышей развивается асцит и они погибают. Средняя продолжительность жизни составляет 32 дня. – цисплатт в дозе 40 мкг/мышь – выживаемость мышей составляет 30%. – ФНО-  в дозе 0,125 мкг/мышь – у всех мышей развивается асцит и они погибают. Средняя продолжительность жизни мышей составляет 37 дней в дозе 0,125 мкг/мышь – у всех мышей развивается асцит и они погибают. Средняя продолжительность жизни мышей составляет 37 дней– ГМДП в дозе 25 мкг/мышь – выживаемость 20%. – комбинация цисплатина в дозе 40 мкг/мышь с ФНО-  в дозе 0,125 мкг/мышь – выживаемость 80%.
– комбинация цисплатина в дозе 40 мкг/мышь с ГМДП в дозе 25 мкг/мышь – выживаемость 80%.
– комбинация ФНО- в дозе 0,125 мкг/мышь – выживаемость 80%.
– комбинация цисплатина в дозе 40 мкг/мышь с ГМДП в дозе 25 мкг/мышь – выживаемость 80%.
– комбинация ФНО- в дозе 0,125 мкг/мышь с ГМДП в дозе 25 мкг/мышь – выживаемость 30%.
Следует отметить, что в группе мышей, которым не имплантировали опухолевые клетки, но вводили комбинацию препаратов, выживаемость 100%. в дозе 0,125 мкг/мышь с ГМДП в дозе 25 мкг/мышь – выживаемость 30%.
Следует отметить, что в группе мышей, которым не имплантировали опухолевые клетки, но вводили комбинацию препаратов, выживаемость 100%.
Формула изобретения Состав для уничтожения ФНО-  -чувствительных опухолевых клеток, содержащий цитостатик и ФНО- -чувствительных опухолевых клеток, содержащий цитостатик и ФНО- , отличающийся тем, что в качестве цитостатика состав содержит интерколирующие в ДНК препараты и дополнительно биологически активный мурамилпептид при массовом соотношении, мурамилпептида, цитостатика и ФНО- , отличающийся тем, что в качестве цитостатика состав содержит интерколирующие в ДНК препараты и дополнительно биологически активный мурамилпептид при массовом соотношении, мурамилпептида, цитостатика и ФНО- 1:0,06 – 300:0,00001-0,1. 1:0,06 – 300:0,00001-0,1.
|
||||||||||||||||||||||||||
