|
(21), (22) Заявка: 98112109/14, 18.06.1998
(24) Дата начала отсчета срока действия патента:
18.06.1998
(30) Конвенционный приоритет:
20.06.1997 DE 19726167.1
(43) Дата публикации заявки: 20.06.2000
(45) Опубликовано: 10.07.2003
(15) Информация о коррекции:
Версия коррекции № 1 (
Текст описания приведен в факсимильном виде.
Формула изобретения
1. Производное инсулина или его физиологически приемлемая соль формулы I
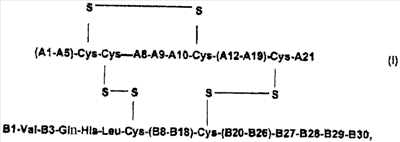
в которой (А1-А5) – аминокислотные остатки в положениях А1-А5 цепи А человеческого (ср. SEQ ID NO 1) или животного инсулина;
(А12-А19) – аминокислотные остатки в положениях А12-А19 цепи А человеческого (ср. SEQ ID NO 1) или животного инсулина;
А21 – Asn, Asp, Gly, Ser, Thr или Ala;
(В8-В18) – аминокислотные остатки в положениях В8-В18 цепи В человеческого (ср. SEQ ID NO 2) или животного инсулина;
(В20-В26) – аминокислотные остатки в положениях В20-В26 цепи В человеческого (ср. SEQ ID NO 2) или животного инсулина;
А8, А9, А10 – аминокислотные остатки в положениях А8, А9 и А10 цепи А человеческого (ср. SEQ ID NO 1) или животного инсулина;
В30 – гидроксил или аминокислотный остаток в положении В30 цепи В человеческого (ср. SEQ ID NO 2) или животного инсулина,
В1 – фенилаланиновый (Phe) остаток или атом водорода,
В3 – природный основной аминокислотный остаток,
В27, В28 и В29 – аминокислотные остатки в положениях В27, В28 и В29 цепи В человеческого (ср. SEQ ID NO 2) или животного инсулина или соответственно другой природный аминокислотный остаток, причем, по меньшей мере, один из аминокислотных остатков в положениях В27, В28 и В29 цепи В является природным аминокислотным остатком, выбранным из группы изолейцин (Ile), аспарагиновая кислота (Asp) и глутаминовая кислота (Glu) и, по меньшей мере, один из аминокислотных остатков в положениях В27, В28 и В29 цепи В заменен на другой природный аминокислотный остаток, выбранный в отношении В29 из группы нейтральных или кислых аминокислот, и в отношении В27 и В28 из группы нейтральных аминокислот.
2. Производное инсулина или его физиологически приемлемая соль согласно п.1, в котором (которой) обозначают: А8 – аланин (Ala); А9 – серин (Ser); А10 – валин (Val) и В30 – аланин (Ala).
3. Производное инсулина или его физиологически приемлемая соль согласно п.1, в котором (которой) обозначают А8 – треонин (Thr); А9 – серин (Ser) и А10 – изолейцин (Ile).
4. Производное инсулина или его физиологически приемлемая соль согласно п.3, в котором (которой) В30 обозначает аланин (Ala) или треонин (Thr).
5. Производное инсулина или его физиологически приемлемая соль согласно п.3 с В30 = треонин (Thr), в котором (которой) обозначают: (А1-А5) – аминокислотные остатки в положениях А1-А5 цепи А человеческого инсулина; (А12-А19) – аминокислотные остатки в положениях А12-А19 цепи А человеческого инсулина; (В8-В18) – аминокислотные остатки в положениях В8-В18 цепи В человеческого инсулина, и (В20-В26) – аминокислотные остатки в положениях В20-В26 цепи В человеческого инсулина.
6. Производное инсулина или его физиологически приемлемая соль по любому из пп.1-5, в котором (которой) аминокислотный остаток в положении В1 цепи В является фенилаланиновым (Phe) остатком.
7. Производное инсулина или его физиологически приемлемая соль по любому из пп.1-6. в котором (которой) аминокислотный остаток в положении В3 цепи В является гистидиновым (His), лизиновым (Lys) или аргининовым (Arg) остатком.
8. Производное инсулина или его физиологически приемлемая соль по любому из пп.1-7, у которого (которой) цепь В имеет последовательность

9. Производное инсулина или его физиологически приемлемая соль по любому из пп.1-7, у которого (которой) по меньшей мере один из аминокислотных остатков в положениях В27, В28 и В29 цепи В является изолейциновым (Ile) остатком.
10. Производное инсулина или его физиологически приемлемая соль по п.9, у которого (которой) цепь В имеет последовательность
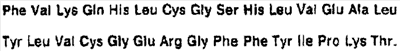
11. Производное инсулина или его физиологически приемлемая соль по п.9, у которого (которой) цепь В имеет последовательность
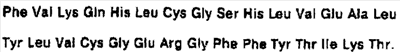
12. Производное инсулина или его физиологически приемлемая соль согласно одному из пп.1-7 и 9, у которого (которой) аминокислотный остаток в положении А21 цепи А является аспарагиновым (Asp) остатком.
13. Производное инсулина или его физиологически приемлемая соль по п.12, у которого (которой) цепь А имеет последовательность

14. Производное инсулина или его физиологически приемлемая соль согласно одному из пп.1-9, у которого (которой) по меньшей мере один из аминокислотных остатков в положениях В27, В28 и В29 цепи В является природным аминокислотным остатком, выбранным из группы кислых аминокислот.
15. Производное инсулина или его физиологически приемлемая соль по п.14, у которого (которой) аминокислотный остаток в положении А21 цепи А является аспарагиновым (Asp) остатком.
16. Предшественник производного инсулина по п.1, имеющий последовательность
 
17. ДНК-Последовательность, кодирующая предшественник производного инсулина согласно п.16.
18. Вектор экспрессии, содержащий ДНК-последовательность согласно п.17, выбранная из группы плазмид plNT 329, 332 и 333.
19. Штамм Е.coli К12 W3110, трансформированный вектором экспрессии согласно п.18.
20. Фармацевтическая композиция с понижающей, соответственно регулирующей уровень глюкозы в крови эффективностью, содержащая производное инсулина в качестве активного вещества и физиологически приемлемый носитель, отличающаяся тем, что она содержит в качестве производного инсулина по меньшей мере одно производное инсулина и/или одну его физиологически приемлемую соль согласно одному или нескольким из пп.1-15 в эффективном количестве.
21. Фармацевтическая композиция согласно п.20, отличающаяся тем, что она содержит производное инсулина и/или его физиологически приемлемую соль в растворенной, аморфной и/или кристаллической форме.
22. Фармацевтическая композиция согласно п.20, отличающаяся тем, что она дополнительно содержит вспомогательное вещество продленного действия.
23. Фармацевтическая композиция согласно п.22, отличающаяся тем, что вспомогательным веществом продленного действия является протаминсульфат, причем производное инсулина и/или его физиологически приемлемая соль присутствует в форме сокристаллизата с протаминсульфатом.
РИСУНКИ
PD4A – Изменение наименования обладателя патента Российской Федерации на изобретение
(73) Новое наименование патентообладателя:
Санофи-Авентис Дойчланд ГмбХ (DE)
Извещение опубликовано: 10.06.2006 БИ: 16/2006
TZ4A – Поправки к описаниям изобретений
Часть описания, где обнаружена ошибка: Текст опис., с.36 Протокол последовательностей
Напечатано: К п. 1 формулы ( I ) 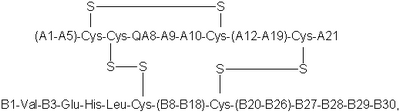
Следует читать: К п. 1 формулы ( I ) 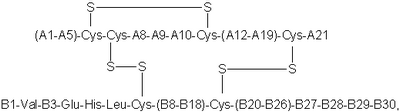
Номер и год публикации бюллетеня: 19-2003
Извещение опубликовано: 20.06.2007 БИ: 17/2007
TH4A – Переиздание описания изобретения к патенту Российской Федерации
Причина переиздания: Коррекция текстов формулы и описания изобретения
Извещение опубликовано: 20.12.2007 БИ: 35/2007
ND4A Продление срока действия патента Российской Федерации на изобретение
Дата, до которой продлен срок действия: 07.10.2021
(пп. 1, 3 – 8, 12, 14, 15, 20 – 22)
Извещение опубликовано: 10.02.2008 БИ: 04/2008
|