Патент на изобретение №2207343
|
||||||||||||||||||||||||||
(54) ЗАМЕЩЕННЫЕ АММОНИЕВЫЕ СОЛИ 5′-Н-ФОСФОНАТА 3′-АЗИДО-3′-ДЕЗОКСИТИМИДИНА, ЯВЛЯЮЩИЕСЯ СЕЛЕКТИВНЫМИ ИНГИБИТОРАМИ ПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ВИЧ-1 И ВИЧ-2
(57) Реферат: Изобретение относится к замещенным аммониевым солям 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина общей формулы (1), где RR’R”N представляют собой L-аланин, этаноламин, триэтаноламин, 6-аминокапроновую кислоту, пиридоксиламин или диметиламиноэтанол, являющимся селективными ингибиторами продукции вируса иммунодефицита человека ВИЧ-1 и ВИЧ-2. Соединения по изобретению обладают улучшенной способностью к кристаллизации и меньшей гигроскопичностью по сравнению с солями 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина с щелочными и щелочноземельными металлами. 3 табл. 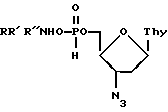 Изобретение относится к вирусологии и касается новых биологически активных соединений, а именно замещенных аммониевых солей 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина общей формулы:
Изобретение относится к вирусологии и касается новых биологически активных соединений, а именно замещенных аммониевых солей 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина общей формулы: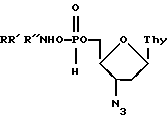 где RR’R”N – представляют собой L-аланин, этаноламин, триэтаноламин, 6-аминокапроновую кислоту, пиридоксиламин или диметиламиноэтанол. Новые соединения обладают способностью селективно ингибировать продукцию вирусов иммунодефицита человека (ВИЧ), что позволяет предполагать возможность их использования в медицине для лечения людей, инфицированных ВИЧ и больных СПИД. В настоящее время известны различные соединения, ингибирующие продукцию вируса иммунодефицита человека. Наибольшее распространение из них получил 3′-азидо-3′-дезокситимидин (АЗТ) [Mitsuya Н. et al., Proc. Natl. Acad. Sci. USA, 1985, 82, 7096-7070]. Известны также 5′-фосфонаты 3′-азидо-2′,3′-дидезоксинуклеозидов, в том числе, 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина [Патент СССР 1548182, кл. С 07 Н 19/073, 1987], которые обладают ингибирующей активностью в отношении ВИЧ-1 и ВИЧ-2, но при этом менее токсичны, чем АЗТ. Однако создание лекарственной формы на основе 3′-азидо-2′,3′-дидезоксинуклеозидов крайне затруднено из-за их высокой гигроскопичности. Известны также соли щелочных и щелочноземельных металлов 5′-фосфонатов 3′-азидо-2′, 3′-дидезоксинуклеозидов [Патент РФ 2106353, кл. С 07 Н 19/073, 1996], однако не все из них по разным причинам удовлетворяют требованиям к созданию хорошей лекарственной формы. Заявляемые замещенные аммониевые соли 5′-фосфоната 3′-азидо-3′-дезокситимидина по активности и токсичности не уступают солям щелочных и щелочноземельных металлов, а также кислотной форме 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина, но в то же время им присуща лучшая способность к кристаллизации, большая чистота и меньшая гигроскопичность. Кроме того, новые соли расширяют круг соединений, обладающих ингибирующей активностью в отношении ВИЧ-1 и ВИЧ-2. Новые вещества представляют собой белые кристаллические порошки, хорошо растворимые в воде, ограниченно растворимые в спиртах, хлороформе, хлористом метилене. Их получение проводят добавлением эквимолярного количества соответствующего аминосоединения к кислотной форме 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. Образующиеся соли упаривают до малых объемов, из которых начинается самопроизвольная кристаллизация, и оставляют при 4oС на 5-6 ч до окончания кристаллизации, выпавшие осадки отфильтровывают, промывают малыми объемами охлажденной до 4oС воды и сушат. Выход целевых веществ составляет 95-98%. Чистота и структура новых соединений подтверждены данными ВЭЖХ, УФ- и ЯМР-спектроскопии. Ниже приводятся примеры получения замещенных аммониевых солей 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. Пример 1. Синтез соли L-аланилата 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (I) К раствору 165 г (0,5 моля) кислой формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина в 200 мл дистиллированной воды при охлаждении водой со льдом и перемешивании в течение 20 мин приливают 200 мл (0,5 моля) 2,5 н. раствора L-аланина. Образовавшийся прозрачный бесцветный раствор упаривают на роторном испарителе при температуре бани не более 45oС до 130-150 мл суммарного объема и оставляют на 6 ч при 4oС. Выпавший мелкокристаллический осадок отделяют на стеклянном фильтре, промывают 40 мл охлажденной до 4oС дистиллированной воды и сушат в вакууме. Выход 201 г (95,8%), т.пл. >300oС (с разложением). Вещество не гигроскопично. Время удерживания нуклеотидной компоненты на колонке Nucleosil 120-7 NH2 в линейном градиенте КН2РO4 (0,05-1 М) 7,2 мин, скорость потока 1 мл/мин. УФ-спектр (вода):  max 266 нм ( max 266 нм ( 9600). 1Н ЯМР (D2О; 9600). 1Н ЯМР (D2О;  , м.д.; J, Гц): 1.33 д (3Н, СН3 (аланин), JCH3-CH 6,5 Гц); 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 4,65-3,90 м (5Н, Н3’+Н4’+2Н5’+СН (аланин)); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O, , м.д.; J, Гц): 1.33 д (3Н, СН3 (аланин), JCH3-CH 6,5 Гц); 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 4,65-3,90 м (5Н, Н3’+Н4’+2Н5’+СН (аланин)); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O,  , м.д.; J, Гц): 6,5 д (1Н, НP JH-P 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 2. Синтез этаноламмониевой соли 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (II) , м.д.; J, Гц): 6,5 д (1Н, НP JH-P 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 2. Синтез этаноламмониевой соли 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (II)К раствору 165 г (0,5 моля) кислой формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина в 200 мл дистиллированной воды при охлаждении водой со льдом и перемешивании в течение 20 мин приливают 100 мл (0,5 моля) 5 н. раствора этаноламина. Образовавшийся прозрачный бесцветный раствор упаривают на роторном испарителе при температуре бани не более 45oС до 130-150 мл суммарного объема и оставляют на 6 ч при 4oС. Выпавший мелкокристаллический осадок отделяют на стеклянном фильтре, промывают 40 мл охлажденной до 4oС дистиллированной воды и сушат в вакууме. Выход 186 г (94,9%), т.пл. >300oС (с разложением). Вещество не гигроскопично. Время удерживания нуклеотидной компоненты на колонке Nucleosil 120-7 NH2 в линейном градиенте КН2РO4 (0,05-1 М) 7,2 мин, скорость потока 1 мл/мин. УФ-спектр (вода):  max 266 нм ( max 266 нм ( 9600). 1H ЯМР (D2О): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 3,19 т (2Н, CH2N (этаноламин), JCH2-CH2 5 Гц); 3,61 т (2Н, СН2O (этаноламин), JCH2-CH2 5 Гц); 4,65-3,90 м (4Н, Н3’+Н4’+2Н5′); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-P 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 3. Синтез триэтаноламмониевой соли 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (III) 9600). 1H ЯМР (D2О): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 3,19 т (2Н, CH2N (этаноламин), JCH2-CH2 5 Гц); 3,61 т (2Н, СН2O (этаноламин), JCH2-CH2 5 Гц); 4,65-3,90 м (4Н, Н3’+Н4’+2Н5′); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-P 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 3. Синтез триэтаноламмониевой соли 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (III)К раствору 165 г (0,5 моля) кислой формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина в 200 мл дистиллированной воды при охлаждении водой со льдом и перемешивании в течение 20 мин приливают 100 мл (0,5 моля) 5 н. раствора триэтаноламина. Образовавшийся прозрачный бесцветный раствор упаривают на роторном испарителе при температуре бани не более 45oС до 130-150 мл суммарного объема и оставляют на 6 ч при 4oС. Выпавший мелкокристаллический осадок отделяют на стеклянном фильтре, промывают 40 мл охлажденной до 4oС дистиллированной воды и сушат в вакууме. Выход 233 г (97,1%), т.пл. >300oС (с разложением). Вещество не гигроскопично. Время удерживания нуклеотидной компоненты на колонке Nucleosil 120-7 NH2 в линейном градиенте KH2PO4 (0,05-1 М) 7,2 мин, скорость потока 1 мл/мин. УФ-спектр (вода):  max 266 нм ( max 266 нм ( 9600). 1Н ЯМР (D2О): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 3,22 т (6Н, 3CH2N (триэтаноламин), JCH2-CH2 5 Гц); 4,65-3,90 м (10Н, Н3’+Н4’+2Н5’+3CH2O (триэтаноламин)); 6,15 т (1Н, Н1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-Ch3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-P 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 4. Синтез 6-аминогексаноата 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (IV) 9600). 1Н ЯМР (D2О): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 3,22 т (6Н, 3CH2N (триэтаноламин), JCH2-CH2 5 Гц); 4,65-3,90 м (10Н, Н3’+Н4’+2Н5’+3CH2O (триэтаноламин)); 6,15 т (1Н, Н1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-Ch3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-P 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 4. Синтез 6-аминогексаноата 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (IV)К раствору 165 г (0,5 моля) кислой формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина в 200 мл дистиллированой воды при охлаждении водой со льдом и перемешивании в течение 20 мин приливают 200 мл (0,5 моля) 2,5 н. раствора 6-аминокапроновой кислоты. Образовавшийся прозрачный бесцветный раствор упаривают на роторном испарителе при температуре бани не более 45oС до 130-150 мл суммарного объема и оставляют на 6 ч при 4oС. Выпавший мелкокристаллический осадок отделяют на стеклянном фильтре, промывают 40 мл охлажденной до 4oС дистиллированной воды и сушат в вакууме. Выход 195 г (84,2%), т.пл. >300oС (с разложением). Вещество не гигроскопично. Время удерживания нуклеотидной компоненты на колонке Nucleosil 120-7 NH2 в линейном градиенте КН2РO4 (0,05-1 М) 7,2 мин, скорость потока 1 мл/мин. УФ-спектр (вода):  max 266 нм ( max 266 нм ( 9600). 1Н ЯМР (D2O): 1,34-1,69 м (6Н, 3CH2 (аминокапроновая кислота)); 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,36 т (2Н, СН2СООН (аминокапроновая кислота), JCH2-CH2 7 Гц); 2,55 м (2Н, Н2′); 3,02 т (2Н, CH2N (аминокапроновая кислота), JCH2-CH2 7 Гц); 4,65-3,90 м (4Н, Н3’+Н4’+2Н5′); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-p 626 Гц, JР-Н5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 5. Синтез пиридоксиламмониевой соли 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (V) 9600). 1Н ЯМР (D2O): 1,34-1,69 м (6Н, 3CH2 (аминокапроновая кислота)); 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,36 т (2Н, СН2СООН (аминокапроновая кислота), JCH2-CH2 7 Гц); 2,55 м (2Н, Н2′); 3,02 т (2Н, CH2N (аминокапроновая кислота), JCH2-CH2 7 Гц); 4,65-3,90 м (4Н, Н3’+Н4’+2Н5′); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-p 626 Гц, JР-Н5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 5. Синтез пиридоксиламмониевой соли 5′-Н-фосфонат 3′-азидо-3′-дезокситимидина (V)К раствору 165 г (0,5 моля) кислой формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина в 200 мл дистиллированной воды при охлаждении водой со льдом и перемешивании в течение 20 мин приливают 250 мл (0,5 моля) 2 н. раствора пиридоксиламина. Образовавшийся прозрачный бесцветный раствор упаривают на роторном испарителе при температуре бани не более 45oС до 130-150 мл суммарного объема и оставляют на 6 ч при 4oС. Выпавший мелкокристаллический осадок отделяют на стеклянном фильтре, промывают 40 мл охлажденной до 4oС дистиллированной воды и сушат в вакууме. Выход 237 г (94,9%), т.пл. >300oС (с разложением). Вещество не гигроскопично. Время удерживания нуклеотидной компоненты на колонке Nucleosil 120-7 NH2 в линейном градиенте КН2РO4 (0,05-1 М) 7,2 мин, скорость потока 1 мл/мин. УФ-спектр (вода):  max 261 нм ( max 261 нм ( 14300). 1Н ЯМР (D2O): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 2,77 с (3Н, СН3 (пиридоксиламин)); 4,65-3,90 м (6Н, Н3’+Н4’+2Н5’+CH2NH2 (пиридоксиламин)); 4,84 с (2Н, CH2OH (пиридоксиламин)); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц); 7,66 д (1Н, Н6, JH6-CH3 1 Гц); 8,08 с (1Н, Аr (пиридоксиламин)). 31Р-ЯМР-спектр (D2О): 6,5 д (1Н, НP, JH-p 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 6. Синтез (гидроксиэтил)диметиламмониевой соли 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина (VI) 14300). 1Н ЯМР (D2O): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 2,77 с (3Н, СН3 (пиридоксиламин)); 4,65-3,90 м (6Н, Н3’+Н4’+2Н5’+CH2NH2 (пиридоксиламин)); 4,84 с (2Н, CH2OH (пиридоксиламин)); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц); 7,66 д (1Н, Н6, JH6-CH3 1 Гц); 8,08 с (1Н, Аr (пиридоксиламин)). 31Р-ЯМР-спектр (D2О): 6,5 д (1Н, НP, JH-p 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Пример 6. Синтез (гидроксиэтил)диметиламмониевой соли 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина (VI)К раствору 165 г (0,5 моля) кислой формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина в 200 мл дистиллированной воды при охлаждении водой со льдом и перемешивании в течение 20 мин приливают 100 мл (0,5 моля) 5 н. раствора диметиламиноэтанола. Образовавшийся прозрачный бесцветный раствор упаривают на роторном испарителе при температуре бани не более 45oС до 130-150 мл суммарного объема и оставляют на 6 ч при 4oС. Выпавший мелкокристаллический осадок отделяют на стеклянном фильтре, промывают 40 мл охлажденной до 4oС дистиллированной воды и сушат в вакууме. Выход 199 г (94,9%), т.пл. >300oС (с разложением). Вещество не гигроскопично. Время удерживания нуклеотидной компоненты на колонке Nucleosil 120-7 NH2 в линейном градиенте КН2РO4 (0,05-1 М) 7,2 мин, скорость потока 1 мл/мин. УФ-спектр (вода):  max 266 нм ( max 266 нм ( 9600). 1Н ЯМР (D2О): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 2,84 с (3Н, СН3 (диметиламиноэтанол)); 3,21 т (2Н, CH2N (диметиламиноэтанол), JCH2-CH2 5 Гц); 3.93 т (2Н, СН2О (диметиламиноэтанол), JCH2-CH2 5 Гц); 4,65-3,90 м (4Н, Н3’+Н4’+2Н5′); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-p 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Были изучены биологические свойства новых соединений, а именно их способность селективно ингибировать продукцию ВИЧ и токсичность для клеток. Исследования проводили на культурах лимфоцитов человека – перевиваемых лимфобластоидных линиях клеток человека H9/IIIB, МТ-4 и PBL. Продукция вируса клетками определялась методами непрямой иммунофлуоресценции и иммуноферментного анализа по [Тарусова Н. Б., Хорлин А.А., Краевский А.А. и др. Мол. Биол. 1989, 23, 1716-1723, Краевский А.А., Тарусова Н.Б., Жу К.-Ю, и др.. Мол. Биол. 1992, 26, 624-633,. Dyatkina N., Arzumanov A., Krayevsky A. at al. , Nucleosides & Nucleotides, 1994, 13, 325-337]. Активность соединений характеризовали величиной ЭД – концентрации, подавляющей продукцию ВИЧ-1 и ВИЧ-2 на 50%, токсичность – величиной ТД, а именно концентрации, подавляющей рост неинфицированных клеток на 50%. Индекс селективности вычисляли как отношение ТД к ЭД. Для сравнения использовали кислотную форму 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. Данные экспериментов приведены в табл. 1-3.
Таким образом, новые вещества – замещенные соли 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина ингибируют репродукцию ВИЧ-1 и ВИЧ-2 в культурах лимфоцитов человека Н9, МТ-4 и PBL примерно с той же активностью, с которой это наблюдалось и для кислотной формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. Токсичность заявляемых замещенных аммониевых солей 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина также находится в пределах токсичности кислотной формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. В то же время новые соединения позволяют сделать процесс получения лекарственных форм на их основе более технологичным. 9600). 1Н ЯМР (D2О): 1,93 д (3Н, СН3, JCH3-H6 0,5 Гц); 2,55 м (2Н, Н2′); 2,84 с (3Н, СН3 (диметиламиноэтанол)); 3,21 т (2Н, CH2N (диметиламиноэтанол), JCH2-CH2 5 Гц); 3.93 т (2Н, СН2О (диметиламиноэтанол), JCH2-CH2 5 Гц); 4,65-3,90 м (4Н, Н3’+Н4’+2Н5′); 6,15 т (1Н, H1′, JH1′-H2′ 6 Гц), 7,66 д (1Н, Н6, JH6-CH3 1 Гц). 31Р-ЯМР-спектр (D2O): 6,5 д (1Н, НP, JH-p 626 Гц, JP-H5′ 6,3 Гц, JP-H4′ 1,6 Гц).
Были изучены биологические свойства новых соединений, а именно их способность селективно ингибировать продукцию ВИЧ и токсичность для клеток. Исследования проводили на культурах лимфоцитов человека – перевиваемых лимфобластоидных линиях клеток человека H9/IIIB, МТ-4 и PBL. Продукция вируса клетками определялась методами непрямой иммунофлуоресценции и иммуноферментного анализа по [Тарусова Н. Б., Хорлин А.А., Краевский А.А. и др. Мол. Биол. 1989, 23, 1716-1723, Краевский А.А., Тарусова Н.Б., Жу К.-Ю, и др.. Мол. Биол. 1992, 26, 624-633,. Dyatkina N., Arzumanov A., Krayevsky A. at al. , Nucleosides & Nucleotides, 1994, 13, 325-337]. Активность соединений характеризовали величиной ЭД – концентрации, подавляющей продукцию ВИЧ-1 и ВИЧ-2 на 50%, токсичность – величиной ТД, а именно концентрации, подавляющей рост неинфицированных клеток на 50%. Индекс селективности вычисляли как отношение ТД к ЭД. Для сравнения использовали кислотную форму 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. Данные экспериментов приведены в табл. 1-3.
Таким образом, новые вещества – замещенные соли 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина ингибируют репродукцию ВИЧ-1 и ВИЧ-2 в культурах лимфоцитов человека Н9, МТ-4 и PBL примерно с той же активностью, с которой это наблюдалось и для кислотной формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. Токсичность заявляемых замещенных аммониевых солей 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина также находится в пределах токсичности кислотной формы 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина. В то же время новые соединения позволяют сделать процесс получения лекарственных форм на их основе более технологичным.
Формула изобретения Замещенные аммониевые соли 5′-Н-фосфоната 3′-азидо-3′-дезокситимидина общей формулы 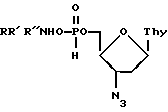 где RR’R”N представляют собой L-аланин, этаноламин, триэтаноламин, 6-аминокапроновую кислоту, пиридоксиламин или диметиламиноэтанол, являющиеся селективными ингибиторами продукции вируса иммунодефицита человека ВИЧ-1 и ВИЧ-2. РИСУНКИ
|
||||||||||||||||||||||||||
