Патент на изобретение №2206565
|
||||||||||||||||||||||||||
(54) ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ ЭТИЛ(R)-1-(1-ФЕНИЛЭТИЛ)-1H-ИМИДАЗОЛ-5-КАРБОКСИЛАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ
(57) Реферат: Изобретение относится к новому высокомеченному тритием этил(R)-1-(1-фенилэтил)-1Н-имидазол-5-карбоксилату формулы I. Также описан способ получения этого соединения, заключающийся в предварительном нанесении его исходного немеченого аналога на инертный носитель, смешении полученного комплекса с катализатором и проведении реакции изотопного обмена в атмосфере трития при нагревании. Полученное соединение может быть использовано в химии и медицине для исследования физиологически активных соединений. Технический результат: расширение ассортимента меченых аналогов физиологически активных соединений. 2 с. и 1 з.п.ф-лы. 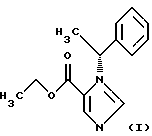
Изобретение относится к области органической химии и может найти применение в аналитической химии, биоорганической химии, биохимии и прикладной медицине. Известен этил (R)-1-(1-фенилэтил)-1Н-имидазол-5-карбоксилат формулы I: 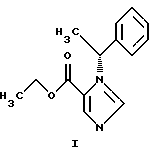 Данное соединение, содержащее аминобензильную группу, обладает физиологической активностью – снотворным действием и его препарат известен под наименованием “этомидат” (1999 Merck & Co., Inc., Whitehouse Station, NJ, USA., N 3927) [1]. Ряд методов изучения физиологически активных соединений требуют наличия их меченых аналогов. Однако меченный тритием аналог этомидата не описан. Ни в технической, ни в патентной литературе не описано получение равномерно меченных высокомеченных тритием органических соединений, содержащих аминобензильную группу, непосредственным введением тритиевой метки в немеченый аналог. Поэтому задача поиска условий получения высокомеченных тритием соединений, содержащих аминобензильную группу, непосредственным введением метки в их немеченые аналоги, актуальна. Техническим результатом, достигаемым настоящим изобретением, является получение нового соединения – высокомеченного тритием этомидата непосредственным введением метки в его немеченый аналог. Данный технический результат достигается тем, что получен новый высокоченный тритием [3H ]-этил(R)-1-(1-фенилэтил)-1Н-имидазол-5-карбоксилат формулы: 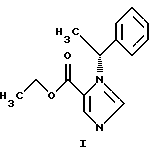 Указанный технический результат достигается также тем, что способ получения высокомеченного тритием [3H]-этил(R)-1-(1-фенилэтил)-1Н-имидазол-5-карбоксилата формулы I: 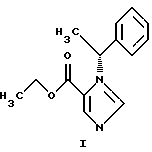 заключается в предварительном нанесении его исходного немеченого аналога на инертный носитель, смешении полученного комплекса с катализатором и проведении реакции изотопного обмена в атмосфере трития при нагревании. Рекомендуется в качестве инертного носителя использовать волокнистый углерод, в качестве катализатора – 5% Pd/BaSO4, а реакцию изотопного обмена проводить при 160oС. На примере этомидата собственными исследованиями было показано, что при проведении реакции изотопного обмена не происходит гидрогенолиз аминобензильной группы в содержащих ее органических соединениях, если проводить реакцию не непосредственно на катализаторе, а сначала исходный немеченый аналог нанести на инертный носитель, затем смешать его с катализатором и нагреть в атмосфере газообразного трития. Ниже приведены примеры реализации изобретения. Пример 1 В раствор 25 мг этомидата в 0.75 мл метанола добавили 250 мг волокнистого углерода и упарили на роторе. К остатку добавили 90 мг 5%Pd/BaSO4, 0.5 мл воды, упарили на роторе и лиофилизировали в течение 12 ч. Затем в ампулу поместили часть высушенной смеси, содержащей 20 мг этомидата, вакуумировали до давления 0,1 Па, заполняли газообразным тритием до давления 270 гПа и выдерживали при температуре 160oС 7.5 мин. Избыточный тритий удаляли вакуумированием. После охлаждения продукты реакции растворяли в метаноле (6  1 мл), катализатор отфильтровывали, а фильтраты упаривали несколько раз в виде раствора в метаноле (3 1 мл), катализатор отфильтровывали, а фильтраты упаривали несколько раз в виде раствора в метаноле (3 3 мл) для удаления лабильного трития.
Очистку меченого препарата осуществляли методом ВЭЖХ на колонке Kromasil 100C18 4 3 мл) для удаления лабильного трития.
Очистку меченого препарата осуществляли методом ВЭЖХ на колонке Kromasil 100C18 4 150 мм, 7 мкм, v – 1 мл/мин, в системе – метанол-вода-трифторуксусная кислота (50:50:0.1), время удерживания – 5.35 мин и в системе – ацетонитрил-вода-трифторуксусная кислота (30:70:0.1), время удерживания – 6.44 мин. Выход – 18-20%, молярная активность – 23,3 Ки/ммоль.
Пример 2 150 мм, 7 мкм, v – 1 мл/мин, в системе – метанол-вода-трифторуксусная кислота (50:50:0.1), время удерживания – 5.35 мин и в системе – ацетонитрил-вода-трифторуксусная кислота (30:70:0.1), время удерживания – 6.44 мин. Выход – 18-20%, молярная активность – 23,3 Ки/ммоль.
Пример 2В качестве инертного носителя изучили углерод фирмы “Норит”, окись алюминия, карбонат кальция и волокнистый углерод производства Воскресенского химкомбината. Лучшие радиохимические характеристики высокомеченного тритием этомидата были получены при использовании волокнистого углерода, графитовые нановолокна которого состоят из графитовых слоев шириной 30-500 ангстрем, уложенных в высокоупорядоченные структуры, что приводит к большей адсорбции водорода по сравнению, например, с активированным углем фирмы “Норит”. Таким образом, способом согласно изобретению впервые получено равномерно меченное высокомеченное тритием соединение, содержащее аминобензильную группу, непосредственно из его немеченого аналога. Формула изобретения
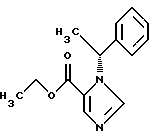 2. Способ получения высокомеченного тритием [3H]-этил(R)-1-(1-фенилэтил)-1H-имидазол-5-карбоксилата формулы I 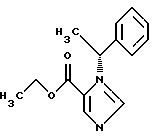 заключающийся в предварительном нанесении его исходного немеченого аналога на инертный носитель, смешении полученного комплекса с катализатором и проведении реакции изотопного обмена в атмосфере трития при нагревании. 3. Способ по п.2, отличающийся тем, что в качестве инертного носителя используют волокнистый углерод, в качестве катализатора – 5% Pd/BaSO4, а реакцию изотопного обмена проводят при 160oС. |
||||||||||||||||||||||||||
