Патент на изобретение №2206563
|
||||||||||||||||||||||||||
(54) УНДЕЦИЛОКСИБЕНЗОИЛАМИНОЗАМЕЩЕННЫЕ ФТАЛОДИНИТРИЛЫ
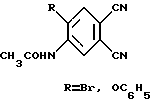
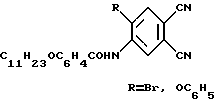
(57) Реферат: Изобретение касается новых ундецилоксибензоиламинозамещенных фталодинитрилов общей формулы I, где R = Br, ОС6Н5, которые могут быть использованы как промежуточные продукты в синтезе новых октазамещенных металлофталоцианинов, в частности ундецилоксибензоиламинозамещенных фталоцианинов кобальта, применяемых в качестве красителей, жидкокристаллических соединений, одномерных проводников, катализаторов различных процессов, материалов чувствительных элементов датчиков газов, фоточувствительных материалов для светорегистрирующих устройств. Способ получения соединений заключается в ацилировании 5-амино-4-бромфталодинитрила хлорангидридом п-ундецилоксибензойной кислоты при нагревании. 1 ил. 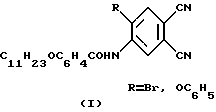
Область техники Изобретение относится к новым дизамещенным фталодинитрилам, которые могут найти применение как промежуточные продукты в синтезе новых октазамещенных металлофталоцианинов, применяемых в качестве красителей, жидкокристаллических соединений, катализаторов различных процессов, одномерных проводников, материалов чувствительных элементов датчиков газов, фоточувствительных материалов для светорегистрирующих устройств. Уровень техники Задачей изобретения является поиск новых соединений, которые являются промежуточными продуктами для синтеза новых октазамещенных фталоцианинов, обладающих фоточувствительностью, что обеспечивает возможность их использования в светорегистрирующих устройствах, а также проявляющих жидкокристаллические свойства. Поставленная задача решена синтезом ундецилоксибензоиламинозамещенных фталодинитрилов общей формулы 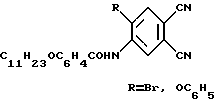 Структура этих соединений доказана данными элементного анализа, ИК- и ПМР спектроскопии. Так, в ИК-спектрах заявляемых соединений (см. чертеж) можно выделить ряд общих полос поглощения, являющихся характеристическими для фталодинитрилов [Сидоров А.Н., Котляр И.П. Оптика и спектроскопия, 1961, т.11, 2, с.175-184] . В области 2920-2848 см-1 обнаруживаются полосы, соответствующие колебаниям связей С-Н метиленовых и метильных групп. Также отмечается поглощение при 3416 и 1724-1688 см-1, характерное для валентных колебаний связей N-H и С=O соответственно [Дайер Д. Р. Приложения абсорбционной спектроскопии органических соединений. – М.: Химия, 1970, с.31-68]. Кроме того, в ИК-спектрах фталодинитрилов отмечаются полосы поглощения при 2232 и 1256 см-1, обусловленные колебаниями связей C  N и С-O соответственно.
Сведения, подтверждающие возможность осуществления изобретения N и С-O соответственно.
Сведения, подтверждающие возможность осуществления изобретенияЗаявляемые соединения получены ацилированием 5-амино-4-бром-(фенокси)фталодинитрилов хлорангидридом п-ундецилоксибензойной кислоты. Пример 1. Синтез 5-(4-ундецилокси)бензоиламино-4-бромфталодинитрила  Смесь 0,1 г 5-амино-4-бромфталодинитрила и 0,15 г хлорангидрида п-ундецилоксибензойной кислоты нагревали до 110-150oС и выдерживали при этой температуре 1 ч. Выделение соединения осуществляли разбавлением реакционной массы 5 мл 5%-ного водного раствора соды. Осадок отфильтровывали, промывали водой до нейтральной среды и сушили при 60oС, Очистку проводили с помощью перекристаллизации из бензола. Соединение – порошок желтого цвета, не растворяется в воде, растворяется в бензоле, ацетоне, хлороформе, ДМФА. Выход: 0,16 г (71%), т. пл. 80-82oС, ИК-спектр,  , см-1: 3416 [ , см-1: 3416 [ (NH)]; 2920, 2848 [ (NH)]; 2920, 2848 [ (CH)]; 2232 [ (CH)]; 2232 [ (CN)]; 1724, 1688 [ (CN)]; 1724, 1688 [ (C=O)]; 1304 [ (C=O)]; 1304 [ (C-N)], 1256 [ (C-N)], 1256 [ (С-O)] . ПМР (CDCl3), (С-O)] . ПМР (CDCl3),  , м.д.: 10,04 (s, 1H, NH); 9,19 (s, 1H, H-2); 8,74 (s, 1H, H-1); 8,07 (m, 2H, H-4, J=43 Hz); 7,03 (m, 2H, H-5, J=27 Hz); 4,07 (t, 2H, ОСН2, J= 17 Hz); 1,27 (s, 18H, CH2); 0,90 (t, 3Н, СН3, J=12 Hz). Найдено, %: Вr 16,3; N 8,3; С 63,1; Н 5,9. С26Н30N3О2Вr.
Вычислено, %: Вr 16,1, N 8,5, С 62,9; Н 6,1.
Пример 2. Синтез 5-(4-ундецилокси)бензоиламино-4-феноксифталодинитрила , м.д.: 10,04 (s, 1H, NH); 9,19 (s, 1H, H-2); 8,74 (s, 1H, H-1); 8,07 (m, 2H, H-4, J=43 Hz); 7,03 (m, 2H, H-5, J=27 Hz); 4,07 (t, 2H, ОСН2, J= 17 Hz); 1,27 (s, 18H, CH2); 0,90 (t, 3Н, СН3, J=12 Hz). Найдено, %: Вr 16,3; N 8,3; С 63,1; Н 5,9. С26Н30N3О2Вr.
Вычислено, %: Вr 16,1, N 8,5, С 62,9; Н 6,1.
Пример 2. Синтез 5-(4-ундецилокси)бензоиламино-4-феноксифталодинитрила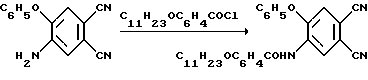 Смесь 0,1 г 5-амино-4-феноксифталодинитрила и 0,15 г хлорангидрида п-ундецилоксибензойной кислоты нагревали до 110-150oC и выдерживали при этой температуре 1 ч. Выделение соединения осуществляли разбавлением реакционной массы 5 мл 5%-ного водного раствора соды. Осадок отфильтровывали, промывали водой до нейтральной среды и сушили при 60oС. Очистку проводили с помощью перекристаллизации из бензола. Соединение – порошок желтого цвета, не растворяется в воде, растворяется в бензоле, ацетоне, хлороформе, ДМФА. Выход: 0,14 г (65%), т. пл. 88-90oС. ИК-спектр,  , см-1: 3456 [ , см-1: 3456 [ (NH)]; 2920, 2848 [ (NH)]; 2920, 2848 [ (CH)]; 2232 [ (CH)]; 2232 [ (CN)]; 1724, 1688 [ (CN)]; 1724, 1688 [ (C=O)]; 1304 [ (C=O)]; 1304 [ (C-N)], 1256 [ (C-N)], 1256 [ (С-O)]. Найдено, %: N 8,1; С 75,7; Н 6,6. С32Н35N3О3. Вычислено, %: N 8,4; С 75,4; Н 6,9.
Таким образом, заявляемые ундецилоксибензоиламинозамещенные фталодинитрилы являются органическими веществами класса производных дизамещенных фталодинитрилов.
Пример 3. Синтез тетра-5-(4-ундецилокси)бензоиламинотетра-4-бромфталоцианина кобальта из 5-(4-ундецилокси)бензоиламино-4-бромфталодинитрила.
Смесь 0,25 г 5-(4-ундецилокси)бензоиламино-4-бромфталодинитрила и 0,03 г ацетата кобальта тщательно растирали и нагревали в кварцевой ампуле при 200-210oС, выдерживали при этой температуре 1 час. Плав растворяли в 10 мл хлороформа и хроматографировали на колонке, заполненной силикагелем. Элюент хлороформ: этанол 10:1. Собирали первую зону ярко-сине-зеленого цвета и упаривали досуха.
Темно-сине-зеленое вещество, хорошо растворяется в бензоле, хлороформе, концентрированной серной кислоте, мало растворимо в ДМФА, не растворимо в ацетоне.
Выход: 0,09 г (36%). ИК-спектр, (С-O)]. Найдено, %: N 8,1; С 75,7; Н 6,6. С32Н35N3О3. Вычислено, %: N 8,4; С 75,4; Н 6,9.
Таким образом, заявляемые ундецилоксибензоиламинозамещенные фталодинитрилы являются органическими веществами класса производных дизамещенных фталодинитрилов.
Пример 3. Синтез тетра-5-(4-ундецилокси)бензоиламинотетра-4-бромфталоцианина кобальта из 5-(4-ундецилокси)бензоиламино-4-бромфталодинитрила.
Смесь 0,25 г 5-(4-ундецилокси)бензоиламино-4-бромфталодинитрила и 0,03 г ацетата кобальта тщательно растирали и нагревали в кварцевой ампуле при 200-210oС, выдерживали при этой температуре 1 час. Плав растворяли в 10 мл хлороформа и хроматографировали на колонке, заполненной силикагелем. Элюент хлороформ: этанол 10:1. Собирали первую зону ярко-сине-зеленого цвета и упаривали досуха.
Темно-сине-зеленое вещество, хорошо растворяется в бензоле, хлороформе, концентрированной серной кислоте, мало растворимо в ДМФА, не растворимо в ацетоне.
Выход: 0,09 г (36%). ИК-спектр,  , см-1: 3416 [ , см-1: 3416 [ (NH)]; 2920, 2848 [ (NH)]; 2920, 2848 [ (CH)] ; 1724, 1688 [ (CH)] ; 1724, 1688 [ (C=O)]; 1304 [ (C=O)]; 1304 [ (C-N)], 1256 [ (C-N)], 1256 [ (С-O)]. ЭСП, (С-O)]. ЭСП,  max, нм: 695, 634 (СНСl3); 772 (H2SO4). Найдено, %: С 61,0; Н 5,8; N 8,3; Br 15,3. C104H120Br4N12O8Co. Вычислено, %: С 61,1; Н 5,9; N 8,2; Br 15,6.
Пример 4. Синтез тетра-5-(4-ундецилокси)бензоиламинотетра-4-феноксифталоцианина кобальта 5-(4-ундецилокси)бензоиламино-4-феноксифталодинитрила.
Смесь 0,25 г 5-(4-ундецилокси)бензоиламино-4-феноксифталодинитрила и 0,03 г ацетата кобальта тщательно растирали и нагревали в кварцевой ампуле при 200-210oС, выдерживали при этой температуре 1 час. Плав растворяли в 10 мл хлороформа и хроматографировали на колонке, заполненной силикагелем. Элюент хлороформ: этанол 10:1. Собирали первую зону ярко-сине-зеленого цвета и упаривали досуха.
Темно-сине-зеленое вещество, хорошо растворяется в бензоле, хлороформе, ДМФА, концентрированной серной кислоте.
Выход: 0,1 г (33%). ИК-спектр, max, нм: 695, 634 (СНСl3); 772 (H2SO4). Найдено, %: С 61,0; Н 5,8; N 8,3; Br 15,3. C104H120Br4N12O8Co. Вычислено, %: С 61,1; Н 5,9; N 8,2; Br 15,6.
Пример 4. Синтез тетра-5-(4-ундецилокси)бензоиламинотетра-4-феноксифталоцианина кобальта 5-(4-ундецилокси)бензоиламино-4-феноксифталодинитрила.
Смесь 0,25 г 5-(4-ундецилокси)бензоиламино-4-феноксифталодинитрила и 0,03 г ацетата кобальта тщательно растирали и нагревали в кварцевой ампуле при 200-210oС, выдерживали при этой температуре 1 час. Плав растворяли в 10 мл хлороформа и хроматографировали на колонке, заполненной силикагелем. Элюент хлороформ: этанол 10:1. Собирали первую зону ярко-сине-зеленого цвета и упаривали досуха.
Темно-сине-зеленое вещество, хорошо растворяется в бензоле, хлороформе, ДМФА, концентрированной серной кислоте.
Выход: 0,1 г (33%). ИК-спектр,  , см-1: 3416 [ , см-1: 3416 [ (NH)]; 2920, 2848 [ (NH)]; 2920, 2848 [ (CH)] ; 1724, 1688 [ (CH)] ; 1724, 1688 [ (С=О)]; 1304 [ (С=О)]; 1304 [ (C-N)], 1256 [ (C-N)], 1256 [ (С-О)]. ЭСП, (С-О)]. ЭСП,  max, нм: 681, 615 (ДМФА); 678, 634 (СНСl3); 794 (H2SO4). Найдено, %: С 73,6; Н 6,4; N 8,4. C128H140N12O12Co. Вычислено, %: С 73,3; Н 6,7; N 8,0.
Исследование жидкокристаллических свойств max, нм: 681, 615 (ДМФА); 678, 634 (СНСl3); 794 (H2SO4). Найдено, %: С 73,6; Н 6,4; N 8,4. C128H140N12O12Co. Вычислено, %: С 73,3; Н 6,7; N 8,0.
Исследование жидкокристаллических свойствПоляризационно-микроскопическими исследованиями с использованием микроскопа МИН-8 поляроиды скрещены, установлено, что полученные октазамещенные фталоцианина кобальта проявляют текстуры, характерные для лиотропного и термотропного мезоморфизма. Тетра-5-(4-ундецилокси)бензоиламинотетра-4-бромфталоцианин кобальта обладает термотропным монотропным мезоморфизмом, формируя М-фазу при 100oС, которая сохраняется до комнатной температуры с текстурой, характерной для М-хромонической фазы, с последующей кристаллизацией, а также лиотропным мезоморфизмом в бинарной системе с толуолом и хлороформом. В настоящее время нет значительного коммерческого применения дискотических жидких кристаллов, к которым относятся заявляемые соединения. Тем не менее, уникальные свойства этих материалов предполагают в недалеком будущем хорошую перспективу их применения. Так, металлофталоцианиновые мезогены могут быть использованы в качестве молекулярных полупроводников [Pure Appl. Chem. -1989. – Vol.61. – P. 1625-1629; J. Am. Chem. Soc. – 1982. – Vol.104. – P.5245-5247; J. Am. Chem. Soc. – 1989. – Vol.111. – P.3024-3029], фотопроводников [Nature. – 1994. – Vol. 371. – P. 141-143], газовых сенсоров [Sensors and Actuators В – 1993. – Vol. 13-14. – Р. 276; Sensors and Actuators В – 1993. – Vol.13-14. – P.416], а также в фотокопировальных устройствах [Chromonics Handbook of Liquid Crystals. Vol.2B. / Ed. D.Demus et.al. Willey – VCH, 1998. – P.981-1007]. Исследования фоточувствительных свойств Из насыщенного раствора соединения нанесены на поверхность пьезоэлемента кварцевого резонатора с резонансной частотой 300 кГц, который освещался белым светом лампы накаливания 100 Вт, а также через фильтры инфракрасной ближней области пропускания с длиной волны 1,8 и 2,0 мкм. При этом регистрировалось эквивалентное активное сопротивление кварцевого резонатора, определяемое потерей механической энергии колебаний пьезоэлемента. Наблюдалось резкое изменение эквивалентного сопротивления кварцевого резонатора с нанесенными комплексами при облучении как белым светом, так и через ИК-фильтры, причем изменение сопротивления для тетра-5-(4-ундецилокси)бензоиламинотетра-4-бромфталоцианина кобальта составляет 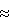 15%, а для тетра-5-(4-ундецилокси)бензоиламинотетра-4-феноксифталоцианина кобальта 15%, а для тетра-5-(4-ундецилокси)бензоиламинотетра-4-феноксифталоцианина кобальта 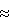 30%. Причиной изменения эквивалентного электрического сопротивления кварцевого резонатора при его фотооблучении является изменение внутреннего трения (вязкости) нанесенных на поверхность пьезоэлемента исследуемых комплексов.
На основе полученных результатов можно сделать вывод о наличии у синтезированных октазамещенных фталоцианина кобальта фоточувствительных свойств и о возможности их использования в светорегистрирующих устройствах, в том числе и в ИК-области. 30%. Причиной изменения эквивалентного электрического сопротивления кварцевого резонатора при его фотооблучении является изменение внутреннего трения (вязкости) нанесенных на поверхность пьезоэлемента исследуемых комплексов.
На основе полученных результатов можно сделать вывод о наличии у синтезированных октазамещенных фталоцианина кобальта фоточувствительных свойств и о возможности их использования в светорегистрирующих устройствах, в том числе и в ИК-области.
Формула изобретения
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 17.08.2003
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||