Патент на изобретение №2206506
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДА КАЛЬЦИЯ И НИТРАТА КАЛИЯ ИЗ ХЛОРИДА КАЛИЯ И НИТРАТА КАЛЬЦИЯ
(57) Реферат: Изобретение относится к производству минеральных солей, в частности хлористого кальция, и может быть использовано на действующих химических производствах, в частности, перерабатывающих фосфатные руды азотно-кислотным методом. Сущность способа заключается в том, что в процессе конверсии хлорида калия и нитрата кальция охлаждением выделяют нитрат калия, оставшийся маточник упаривают и охлаждают с выделением двойной соли KNO3  CaCl2 CaCl2 2H2O, которую после отделения от маточника направляют в начало процесса, при этом в исходной смеси берут избыток нитрата кальция относительно стехиометрического количества его, при этом мольное соотношение составляет Са(NO3)2: KCl 2H2O, которую после отделения от маточника направляют в начало процесса, при этом в исходной смеси берут избыток нитрата кальция относительно стехиометрического количества его, при этом мольное соотношение составляет Са(NO3)2: KCl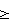 1,2: 2. Способ обеспечивает полную конверсию хлорида калия и нитрата кальция. 1 табл. 1,2: 2. Способ обеспечивает полную конверсию хлорида калия и нитрата кальция. 1 табл.
Изобретение относится к области производства минеральных солей, в частности хлористого кальция, и может быть использовано на действующих химических производствах, в частности, перерабатывающих фосфатные руды азотно-кислотным методом. Известен ряд способов получения хлорида кальция, в частности способы его получения из дистиллерной жидкости содового производства [Позин М.Е. Технология минеральных солей. Ч.1. – М.: Химия, 1974, с.738]. Способ заключается в последовательном выпаривании дистиллерной жидкости от концентрации ~10% CaCl2 до 67% и кристаллизации готового продукта. Данный способ не может быть использован для получения хлорида кальция из нитрата кальция – побочного продукта переработки природных фосфатов азотнокислым методом. Наиболее близким к предлагаемому изобретению является способ получения хлорида кальция из хлорида калия и нитрата кальция в водной среде [Швейцария, патент 416585, приоритет от 28.03.1963, публикация 31.01.1967]. Этот способ заключается в смешении с водой нитрата кальция и хлорида калия, взятых в мольном соотношении 1:2, охлаждении полученной смеси предпочтительно до температуры -10  -20oС, отделении выделившегося нитрата калия, упаривании полученного маточного раствора (I), охлаждении его до комнатной температуры, отделении выделившейся двойной соли KNO3 -20oС, отделении выделившегося нитрата калия, упаривании полученного маточного раствора (I), охлаждении его до комнатной температуры, отделении выделившейся двойной соли KNO3 СаСl2 СаСl2 2Н2O, охлаждении полученного маточника (II) до температуры -5 2Н2O, охлаждении полученного маточника (II) до температуры -5 -15oС, и отделении выделившегося в осадок СаСl2 -15oС, и отделении выделившегося в осадок СаСl2 6Н2O. Выделившаяся на предыдущей стадии двойная соль KNO3 6Н2O. Выделившаяся на предыдущей стадии двойная соль KNO3 CaCl2 CaCl2 2H2O возвращается в процесс.
Недостатком этого способа является, по результатам проведенной нами экспериментальной проверки, то, что при соблюдении заявленных в нем стехиометрического соотношения исходных реагентов Ca(NO3)2:KCl как 1:2 и рекомендуемых условий конверсия Са(NО3)2+2КСl=CaCl2+2KNO3 протекает не полностью: в твердой фазе обнаруживается значительное количество хлорида калия. Кроме того, указанный способ требует для проведения конверсии хлорида калия и нитрата кальция обеспечения довольно низких температур -10 2H2O возвращается в процесс.
Недостатком этого способа является, по результатам проведенной нами экспериментальной проверки, то, что при соблюдении заявленных в нем стехиометрического соотношения исходных реагентов Ca(NO3)2:KCl как 1:2 и рекомендуемых условий конверсия Са(NО3)2+2КСl=CaCl2+2KNO3 протекает не полностью: в твердой фазе обнаруживается значительное количество хлорида калия. Кроме того, указанный способ требует для проведения конверсии хлорида калия и нитрата кальция обеспечения довольно низких температур -10 -20oC.
Задачей предлагаемого изобретения является создание условий, в которых указанная конверсия протекала бы полностью и при более высоких температурах, что позволило бы снизить затраты на охлаждение реакционной массы.
Поставленная задача решается путем изменения соотношения исходных реагентов Ca(NO3)2: KCl, причем в исходной смеси берут избыток нитрата кальция относительно стехиометрического количества его, при этом мольное соотношение составляет Ca(NO3)2:KCl -20oC.
Задачей предлагаемого изобретения является создание условий, в которых указанная конверсия протекала бы полностью и при более высоких температурах, что позволило бы снизить затраты на охлаждение реакционной массы.
Поставленная задача решается путем изменения соотношения исходных реагентов Ca(NO3)2: KCl, причем в исходной смеси берут избыток нитрата кальция относительно стехиометрического количества его, при этом мольное соотношение составляет Ca(NO3)2:KCl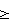 1,2:2.
Сущность предлагаемого изобретения состоит в том, что при предлагаемом соотношении исходных реагентов нитрат кальция вводится в процесс в избытке по сравнению с его стехиометрическим количеством, что обеспечивает полное протекание реакции конверсии как при температуре -10oС, так и при более высокой температуре (0oС).
Осуществление изобретения обеспечивает полную конверсию хлорида калия и нитрата кальция по сравнению с прототипом.
Пример: В 25 кг воды вносят 21,2 кг Ca(NO3)2 1,2:2.
Сущность предлагаемого изобретения состоит в том, что при предлагаемом соотношении исходных реагентов нитрат кальция вводится в процесс в избытке по сравнению с его стехиометрическим количеством, что обеспечивает полное протекание реакции конверсии как при температуре -10oС, так и при более высокой температуре (0oС).
Осуществление изобретения обеспечивает полную конверсию хлорида калия и нитрата кальция по сравнению с прототипом.
Пример: В 25 кг воды вносят 21,2 кг Ca(NO3)2 4Н2O и 7,5 кг KCl. Добавляют к этому раствору 12,6 кг двойной соли KNO3 4Н2O и 7,5 кг KCl. Добавляют к этому раствору 12,6 кг двойной соли KNO3 CaCl2 CaCl2 2Н2O. Мольное соотношение Ca(NO3)2:KCl в полученной смеси составляет 1,2:2. Смесь охлаждают до температуры 0oC выдерживают при этой температуре в течение 2 часов. Выделившийся осадок в количестве 9,6 кг содержит 83,5% KNO3, а также примеси хлорида и нитрата кальция за счет маточного раствора. По данным химического и кристаллооптического анализа KCl в осадке отсутствует, таким образом, реакция конверсии в этих условиях прошла полностью.
Маточный раствор в количестве 53 кг, полученный после отделения KNO3, упаривают на 25 кг и концентрат охлаждают до комнатной температуры (20oС). При этом выкристаллизовывается 12,6 кг двойной соли KNO3 2Н2O. Мольное соотношение Ca(NO3)2:KCl в полученной смеси составляет 1,2:2. Смесь охлаждают до температуры 0oC выдерживают при этой температуре в течение 2 часов. Выделившийся осадок в количестве 9,6 кг содержит 83,5% KNO3, а также примеси хлорида и нитрата кальция за счет маточного раствора. По данным химического и кристаллооптического анализа KCl в осадке отсутствует, таким образом, реакция конверсии в этих условиях прошла полностью.
Маточный раствор в количестве 53 кг, полученный после отделения KNO3, упаривают на 25 кг и концентрат охлаждают до комнатной температуры (20oС). При этом выкристаллизовывается 12,6 кг двойной соли KNO3 CaCl2 CaCl2 2Н2O, которая отделяется и возвращается в процесс. Оставшийся маточник в количестве 15 кг, содержащий CaCl2, охлаждается до температуры -10oС, при этом СaСl2 2Н2O, которая отделяется и возвращается в процесс. Оставшийся маточник в количестве 15 кг, содержащий CaCl2, охлаждается до температуры -10oС, при этом СaСl2 6Н2О выкристаллизовывается в количестве 6 кг, и образуется маточник, который возвращается в процесс.
Примеры, содержащие данные о протекании реакции конверсии при различных исходных соотношениях Са(NО3)2:KCl, сведены в таблицу.
Как следует из таблицы, твердая фаза, образовавшаяся в результате конверсии Ca(NO3)2 и КСl, взятых в мольном соотношении 1:2 (по прототипу), а также при соотношении 1,1: 2, содержит кроме KNO3 (основной продукт) примесь исходного КСl, то есть конверсия протекает не полностью. При соотношении исходных солей 1,2:2 и выше KCl в твердой фазе не обнаруживается как при -10oС, так и при 0oС. Таким образом, при соотношении Ca(NO3)2:КСl 6Н2О выкристаллизовывается в количестве 6 кг, и образуется маточник, который возвращается в процесс.
Примеры, содержащие данные о протекании реакции конверсии при различных исходных соотношениях Са(NО3)2:KCl, сведены в таблицу.
Как следует из таблицы, твердая фаза, образовавшаяся в результате конверсии Ca(NO3)2 и КСl, взятых в мольном соотношении 1:2 (по прототипу), а также при соотношении 1,1: 2, содержит кроме KNO3 (основной продукт) примесь исходного КСl, то есть конверсия протекает не полностью. При соотношении исходных солей 1,2:2 и выше KCl в твердой фазе не обнаруживается как при -10oС, так и при 0oС. Таким образом, при соотношении Ca(NO3)2:КСl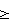 1,2:2 конверсия протекает полностью. 1,2:2 конверсия протекает полностью.
Формула изобретения
 CaCl2 CaCl2 2H2O, которую после отделения от маточника направляют в начало процесса, отличающийся тем, что в исходной смеси берут избыток нитрата кальция относительно стехиометрического количества его, при этом мольное соотношение составляет Са(NO3)2:KCl 2H2O, которую после отделения от маточника направляют в начало процесса, отличающийся тем, что в исходной смеси берут избыток нитрата кальция относительно стехиометрического количества его, при этом мольное соотношение составляет Са(NO3)2:KCl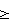 1,2:2. 1,2:2.
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 17.05.2004
Извещение опубликовано: 10.03.2006 БИ: 07/2006
|
||||||||||||||||||||||||||
