Патент на изобретение №2205411
|
||||||||||||||||||||||||||
(54) СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ РЕЗИСТЕНТНОСТЬЮ ФАКТОРА V К АКТИВИРОВАННОМУ ПРОТЕИНУ С
(57) Реферат: Изобретение относится к области медицины, в частности к гематологии. Способ обеспечивает повышение точности диагностики тромбофилии, обусловленной резистентностью фактора V к активированному протеину С. Проводят исследование в активированном парциальном тромбопластиновом тесте с применением активатора протеина С и оценкой времени свертывания. При этом определяют время свертывания смеси исследуемой плазмы с плазмой больного с резистентностью к активированному протеину С после добавления к этой смеси активатора протеина С и после добавления дистиллированной воды, рассчитывают показатель R, как отношение времени свертывания смеси с добавлением активатора протеина С к времени свертывания смеси с добавлением дистиллированной воды, и при значении этого показателя меньше 2,1 диагностируют тромбофилию. 3 табл. Изобретение относится к области медицины, в частности исследованию крови, и может быть использовано для лабораторной диагностики тромбофилии, обусловленой резистентностью к активированному протеину С (АПС). Наиболее близким по достигаемому положительному результату (прототипом) является способ диагностики тромбофилии, обусловленной резистентностью к АПС [Баркаган З. С. , Цывкина Л.П., Мамаев А.Н. Способ диагностики тромбофилии, обусловленной резистентностъю фактора V к активированному протеину С. Патент 2129282] , заключающийся в том, что для активации протеина С добавляют Protac  в стандартную оксалатную плазму, лишенную фактора V и фосфолипидных мембран тромбоцитов, а диагностику осуществляют определением нормализованного отношения (NR), как отношения показателя RБ для плазмы исследуемого больного, представляющего собой отношение времени свертывания плазмы больного, плазмы лишенной фактора V и содержащей активированный протеин С к времени свертывания разведенной плазмы больного, плазмы, лишенной фактора V, к показателю RК для нормальной плазмы, представляющей собой такое же отношение времени свертывания для этой плазмы, и при значении NR<0,8 результаты теста считают положительными. Однако существенным недостатком способа является зависимость показаний способа от концентрации факторов V, что существенно затрудняет интерпретацию результатов исследования, так как только в норме концентрация фактора V варьирует от 70 до 150%. При ряде патологических состояний (патология печени и др.) происходит снижение концентрации коагуляционного фактора V ниже 70%, а при сниженной концентрации фактора V в плазме результаты, полученные способом прототипом, неверны. Кроме того, в способе-прототипе применяют реактив импортного производства – Protac в стандартную оксалатную плазму, лишенную фактора V и фосфолипидных мембран тромбоцитов, а диагностику осуществляют определением нормализованного отношения (NR), как отношения показателя RБ для плазмы исследуемого больного, представляющего собой отношение времени свертывания плазмы больного, плазмы лишенной фактора V и содержащей активированный протеин С к времени свертывания разведенной плазмы больного, плазмы, лишенной фактора V, к показателю RК для нормальной плазмы, представляющей собой такое же отношение времени свертывания для этой плазмы, и при значении NR<0,8 результаты теста считают положительными. Однако существенным недостатком способа является зависимость показаний способа от концентрации факторов V, что существенно затрудняет интерпретацию результатов исследования, так как только в норме концентрация фактора V варьирует от 70 до 150%. При ряде патологических состояний (патология печени и др.) происходит снижение концентрации коагуляционного фактора V ниже 70%, а при сниженной концентрации фактора V в плазме результаты, полученные способом прототипом, неверны. Кроме того, в способе-прототипе применяют реактив импортного производства – Protac . Малая доступность этого реагента существенно затрудняет его широкое применение. Другим недостатком является то, что в способе прототипе два инкубационных этапа (первый раз трехминутная инкубация применяется для приготовления реагента, содержащего АПС, второй раз трехминутная инкубация применяется для активации внутреннего пути свертывания, путем добавления каолин-кефалиновой смеси).
Авторы предлагают способ, где применяется (см. ход определения заявляемого способа) плазма больного с резистентностью фактора V к АПС, т.е. в этой плазме нарушена только способность к разрушению активированным протеином С, но коагуляционные свойства фактора V в такой плазме нормальные, поэтому показания заявляемого способа не зависят от концентрации фактора V. Кроме того, заявляемый способ не требует применения импортных реагентов, он требует меньших временных затрат, чем выполнение способа-прототипа, так как имеет один инкубационный этап.
Положительным результатом предложенного способа является повышение точности диагностики путем исключения влияния на результаты теста концентрации коагуляционного фактора V, а также сокращение времени исследования.
Положительный результат достигается тем, что для устранения влияния концентрации фактора V на показания теста определяют время свертывания смеси исследуемой плазмы с плазмой больного с резистентностью к активированному протеину С, а диагностику осуществляют определением показателя R, как отношение времени свертывания смеси с добавлением активатора протеина С к времени свертывания смеси с добавлением дистиллированной воды, и при значении показателя R<2,1 результаты теста считают положительными.
Способ осуществляют следующим образом.
Реактивы и оборудование: . Малая доступность этого реагента существенно затрудняет его широкое применение. Другим недостатком является то, что в способе прототипе два инкубационных этапа (первый раз трехминутная инкубация применяется для приготовления реагента, содержащего АПС, второй раз трехминутная инкубация применяется для активации внутреннего пути свертывания, путем добавления каолин-кефалиновой смеси).
Авторы предлагают способ, где применяется (см. ход определения заявляемого способа) плазма больного с резистентностью фактора V к АПС, т.е. в этой плазме нарушена только способность к разрушению активированным протеином С, но коагуляционные свойства фактора V в такой плазме нормальные, поэтому показания заявляемого способа не зависят от концентрации фактора V. Кроме того, заявляемый способ не требует применения импортных реагентов, он требует меньших временных затрат, чем выполнение способа-прототипа, так как имеет один инкубационный этап.
Положительным результатом предложенного способа является повышение точности диагностики путем исключения влияния на результаты теста концентрации коагуляционного фактора V, а также сокращение времени исследования.
Положительный результат достигается тем, что для устранения влияния концентрации фактора V на показания теста определяют время свертывания смеси исследуемой плазмы с плазмой больного с резистентностью к активированному протеину С, а диагностику осуществляют определением показателя R, как отношение времени свертывания смеси с добавлением активатора протеина С к времени свертывания смеси с добавлением дистиллированной воды, и при значении показателя R<2,1 результаты теста считают положительными.
Способ осуществляют следующим образом.
Реактивы и оборудование:1) 3,8% (0.1М) раствор цитрата натрия. Получают растворением 3,8 г тринатрия-цитрата в 100 мл дистиллированной воды; 2) трис-HCl Буфер, рН 7,4 (производитель “Технология-Стандарт”, Россия); 3) каолин, (легкая фракция), концентрация 0,025 мг/мл, хранится при +2.. .8oС, (реагент готов к употреблению) перед применением встряхивается до получения гомогенной суспензии, (производитель “Технология-Стандарт”, Россия); 4) кефалин, флакон содержит 30 мг лиофильно высушенного кефалина, полученного из тканевого тромбопластина человека, (производитель “Технология-Стандарт”, Россия); 5) тромбоцитин, 1 мг лиофильно высушенного препарата отмытых тромбоцитов здорового человека, (производитель “Технология-Стандарт”, Россия); 6) хлорид кальция 0,025 М раствор, (производитель “Технология-Стандарт”, Россия); 7) активатор протеина С из яда Agkistrodon saxatilis, (производитель “Технология-Стандарт”, Россия); 8) диагностический набор “Фактор V-PC-тест”, (производитель “Технология-Стандарт”, Россия); 9) центрифуга ОПН-8, (Россия). Приготовление реагентов и исследуемых образцов плазмы. Приготовление каолин-кефалинового реагента: Смешивают 0,1 мл эмульсии кефалина с 3 мл взвеси каолина (0,25 мг/мл). Приготовление раствора тромбоцитина: Во флакон с сухим тромбоцитином вносят 1,0 мл дистиллированной воды, получают маточный раствор, который хранят при температуре +2…+8oС в течение 2 недель. Для получения рабочего раствора тромбоцитина 0,05 мл маточного раствора необходимо смешать с 5,0 мл трис-буфера. Рабочий раствор тромбоцитина используется в день исследования. Приготовление рабочего раствора активатора протеина С: Для приготовления рабочего раствора активатора протеина С необходимо развести активатор протеина С в 1 мл дистиллированной воды. Приготовление исследуемой плазмы: Кровь получают из локтевой вены силико-нированной иглой в пластиковую пробирку, содержащую 3,8% раствор цитрата натрия (соотношение крови и цитрата 9:1). Кровь центрифугируют 5 мин при 1000 об/мин (200g). Полученную богатую тромбоцитами плазму повторно центрифугируют в течение 20 мин при 3500 об/мин (1200g). Таким способом полученную бедную тромбоцитами плазму (БТП) используют для проведения исследования. Приготовление плазмы больного с тяжелой формой резистентности к АПС: Используя диагностический набор “Фактор V-PC-тест”, тестируют плазму больных с рецидивирующими тромботическими нарушениями. Для выполнения заявляемого способа отбирают образец плазмы, показатель нормализованного отношения (НО) которой меньше 0,55 (см. раздел “Оценка полученных результатов” диагностического набора “Фактор V-PC-тест”, производитель “Технология-Стандарт”, Россия). БТП больного с резистентностью к АПС разливают по 1 мл в пенициллиновые флаконы и замораживают при -20oС. В день исследования плазму больного с тяжелой формой резистентности к АПС размораживают и используют для выполнения заявляемого способа. Ход определения. Предложенный способ основан на применении активированного протеина С для свертывания в активированного парциальном тромбопластиновом тесте. 1) В первую пробирку с 0,05 мл плазмы больного с резистентностью к АПС, добавляют 0,05 мл исследуемой БТП, 0,1 мл каолин-кефалинового реагента, 0,05 мл активатора протеина С, 0,03 мл рабочего раствора тромбоцитина, инкубируют смесь на водяной бане 3 мин при температуре +37o С, после чего к ней добавляют 0,1 мл раствора хлорида кальция. Регистрируют время свертывания (t2) при непрерывном помешивании. 2) Во вторую пробирку с 0,05 мл плазмы больного с резистентностью к АПС добавляют 0,05 мл исследуемой БТП, 0,1 мл каолин-кефалинового реагента, 0,05 мл дистиллированой воды, 0,03 мл рабочего раствора тромбоцитина, инкубируют смесь на водяной бане 3 мин при температуре +37o С, после чего к ней добавляют 0,1 мл раствора хлорида кальция. Регистрируют время свертывания при непрерывном помешивании (t1). Оценка полученных результатов. Определяют отношение R для плазмы исследуемого больного по формуле 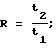 где R – математическое отношение времени свертывания в плазме после добавления активатора протеина С к времени свертывания в плазме после добавления дистиллированной воды (Показатель, характеризующий степень удлинения времени свертывания в тесте после добавления активатора протеина С); t1 – время свертывания после добавления дистиллированной воды; t2 – время свертывания после добавления активатора протеина С. В норме показатель R равен или больше 2.1. У больных с резистентностью к АПС этот показатель R снижен. При обследовании плазмы здоровых людей установлено, что R у здоровых был равен 2,7; SD=0,30; m=0,10; n=53, а пределы нормальных колебаний (X  2SD) составили 2,1-3,3.
Результаты теста считаются положительными, если R<2.1. 2SD) составили 2,1-3,3.
Результаты теста считаются положительными, если R<2.1.
Специфичность и воспроизводимость способа. Заявляемый способ высоко специфичен, его показания зависят только от резистентности фактора V к АПС и не зависят от концентрации фактора V, от влияния волчаночного антикоагулянта. Кроме того, его выполнение не требует применения импортных реагентов, он требует меньших временных затрат, чем выполнение способа-прототипа. Для оценки воспроизводимости способа использовали определение коэффициента вариации (в %) при многократном исследовании одних и тех же образцов нормальной плазмы и плазмы больных с резистентностью к протеину С. Заявляемый способ показал хорошую воспроизводимость. Коэффициент вариации (KB) не превышал 6%. Апробация предлагаемого способа в условиях измененной концентрации коагуляционного фактора V1. Для уточнения влияния концентрации фактора V на показания предлагаемого способа и способа-прототипа, использовали смеси двух плазм (плазму дефицитную по фактору V и нормальную плазму, где концентрация V фактора равна 100%). Смешивали эти плазмы так, чтобы концентрация фактора V в тестируемой смеси была равна 25%, 75%, 50% и 100%. Показания сравниваемых способов, при снижении уровня фактора V, представлены в таблице 3. Из таблицы 3 видно, что концентрация фактора V не оказывает влияния на показания предлагаемого способа, в отличие от способа-прототипа. При снижении концентрации фактора V показания способа-прототипа не воспроизводимы, а результаты предлагаемого способа имеют низкий коэффициент вариации, т.е. хорошо воспроизводимы. Примеры практического использования способа. 1. Больной К.С., 40 лет. Обратился к гематологу Алтайского гематологического центра по поводу рецидивирующих тромботических нарушений. Заболевание началось в возрасте 30 лет (1990 г.), с возникновения тромбоза глубоких вен правой голени. Лечился в терапевтическом отделении городской больницы 3 (г.Барнаул) в ноябре 1995 года по поводу тромбоэмболии легочной артерии, осложненной инфарктной пневмонией и синдромом дыхательной недостаточности III степени. Поверхностный тромбофлебит правого предплечья развился в январе 1996 года. К моменту обследования у больного имеется умеренный отек и болезненность правой голени. Назначены: низкомолекулярный гепарин, дезагреганты, препараты никотиновой кислоты. Исследование системы гемостаза (см. табл.1). В приведенном клиническом примере, используя предлагаемый способ, установлен диагноз: тромбофилия, обусловленная резистентностью фактора V к АПС 2. Больной B. C., 51 год. Больной поступил в терапевтическое отделение больницы 12 г.Барнаула 22.08.98 года с жалобами на тяжесть в правом подреберье, одышку при физической нагрузке, желтушность кожных покровов, сильную слабость, головные боли, головокружение, плохую память. Считает себя больным с 1983 года, когда через год после перенесенного вирусного гепатита вновь возникли желтуха, боли в правом подреберье, слабость. С 1983 года установлен диагноз хронический активный гепатит. После этого неоднократно лечился в условиях стационара. Цирроз печени у больного в течение последних 5 лет. Курсами 1-2 раза в год применяет гепатопротекторы. Из анамнеза жизни установлено, что больной перенес инфаркт миокарда в 1990 году и острое нарушение мозгового кровообращения по ишемическому типу с левосторонним гемипарезом в 1993 году, а сестра больного в возрасте 37 лет умерла от тромбоэмболии легочной артерии на фоне тромбоза поверхностных и глубоких вен левой нижней конечности. Общее состояние средней степени тяжести. Больной в сознании, ориентирован, речь с элементами дизартрии. На вопросы отвечает правильно. Тонус и сила мышц слева умеренно снижены. Патологические рефлексы и менингеальные знаки отсутствуют Нарушена чувствительность слева. Кожные покровы и слизистые желтушны. Дыхание везикулярное, хрипов нет, ЧДД-17 в мин. Тоны сердца приглушены, ритм правильный, ЧСС 86 в мин, АД 120/70. Живот увеличен в размерах, в горизонтальном положении “распластан”, при пальпации печени ее край плотный, острый, выступает из-под края реберной дуги на 2 сантиметра, пальпируется увеличенная селезенка. Данные лабораторных методов обследования. Нb – 135 г/л; РОЭ – 47 мм/ч; Лейкоциты – 4.3  10%; 10%;Лейкоцитарная формула: Б – 1% Э – 1% П – 1% С – 57% Л – 32% М – 8%; Биохимический анализ крови: Креатинин 74 мкмоль/л; мочевина 5.9 ммоль/л; общий билирубин 102 мкмоль/л, прямой 62 мкмоль/л, непрямой 40 мкмоль/л; глюкоза 4,6 ммоль/л: АЛТ 1,4; ACT 0,7; СРБ+; общий белок – 52,1 г/л, альбумины – 45%,  1 – 5,0%, 1 – 5,0%,  2 – 12,0%, 2 – 12,0%,  – 14,0%, – 14,0%,  – 24,0%.
По данным биопсии печени микронодулярный цирроз.
На электрокардиограмме ЧСС 82 в мин, электрическая ось расположена горизонтально, рубцовые изменения на заднедиафрагмальной стенке левого желудочка.
Проведено исследование системы гемостаза (см. табл. 2) для исключения тромбофилии вследствие резистентности к АПС, так как у больного и у родственников в анамнезе тромботические нарушения.
Установлен диагноз: Микронодулярный цирроз печени, гепатоцеллюлярная недостаточность, синдром портальной гипертензии, тромбоцитопения на фоне гиперспленизма, ИБС. Постинфарктный кардиосклероз (1990). Состояние после ОНМК (1993).
В этом клиническом примере показано, что на показания теста не оказывает влияния низкая концентрация фактора V. Исключена тромбофилия, обусловленная резистентностью фактора V к активированному протеину С. – 24,0%.
По данным биопсии печени микронодулярный цирроз.
На электрокардиограмме ЧСС 82 в мин, электрическая ось расположена горизонтально, рубцовые изменения на заднедиафрагмальной стенке левого желудочка.
Проведено исследование системы гемостаза (см. табл. 2) для исключения тромбофилии вследствие резистентности к АПС, так как у больного и у родственников в анамнезе тромботические нарушения.
Установлен диагноз: Микронодулярный цирроз печени, гепатоцеллюлярная недостаточность, синдром портальной гипертензии, тромбоцитопения на фоне гиперспленизма, ИБС. Постинфарктный кардиосклероз (1990). Состояние после ОНМК (1993).
В этом клиническом примере показано, что на показания теста не оказывает влияния низкая концентрация фактора V. Исключена тромбофилия, обусловленная резистентностью фактора V к активированному протеину С.
Формула изобретения
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.05.2003
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||
