Патент на изобретение №2203285
|
||||||||||||||||||||||||||
(54) САПОНИН ГЛИЦИРРЕТОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ
(57) Реферат: Изобретение относится к новым химическим соединениям, в частности к сапонину глицирретовой кислоты – 6′,6”-ди-  -D-галактопиранозилкарбоксилат 3-О-[2′-O-( -D-галактопиранозилкарбоксилат 3-О-[2′-O-( -D- глюкуронопиранозил)- -D- глюкуронопиранозил)- -D-глюкуронопиранозид) метилового эфира глицирретовой кислоты формулы IIб, проявляющему противоязвенную активность. Соединение IIб является малотоксичным веществом, обладающим выраженной противоязвенной активностью, превосходящей эффект известного противоязвенного препарата карбеноксолона в 2 раза при пероральном введении в 2 раза меньшей дозе. 1 табл. -D-глюкуронопиранозид) метилового эфира глицирретовой кислоты формулы IIб, проявляющему противоязвенную активность. Соединение IIб является малотоксичным веществом, обладающим выраженной противоязвенной активностью, превосходящей эффект известного противоязвенного препарата карбеноксолона в 2 раза при пероральном введении в 2 раза меньшей дозе. 1 табл.
Изобретение относится к новым химическим соединениям, конкретно к новому аналогу тритерпенового гликозида – глицирризиновой кислоты (ГК) (I) – сапонину глицирретовой кислоты: 6′,6”- Ди-  -D-галактопиранозилкарбоксилат 3-О-[2′-О-( -D-галактопиранозилкарбоксилат 3-О-[2′-О-( -D-глюкуронопиранозил)- -D-глюкуронопиранозил)- -D-глюкуронопиранозид) метилового эфира глицирретовой кислоты формулы (IIб), -D-глюкуронопиранозид) метилового эфира глицирретовой кислоты формулы (IIб),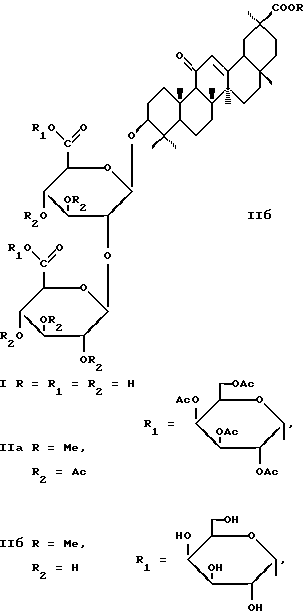 проявляющему противоязвенную (ПЯ) активность. Указанное соединение и его свойства в литературе не описаны. Задача, на решение которой направлено заявленное техническое решение, заключается в поиске новых модифицированных аналогов ГК, обладающих высокой ПЯ активностью. В заявленном техническом решении синтезировано новое химическое соединение – сапонин глицирретовой кислоты формулы (IIб), проявляющий противоязвенную активность. Острая токсичность сапонина (IIб) определялась на белых беспородных мышах массой 15-20 г при введении в желудок по методу Кербера (Елизарова О.Н. Определение пороговых доз промышленных ядов при пероральном введении. М.: Медицина, 1971. С. 47-48). Данное соединение в дозе до 1000 мг/кг токсических явлений не вызывало и может быть отнесено к III классу малоопасных веществ. 50 Результаты опытов представлены в таблице. Как видно из данных таблицы, сапонин (IIб) обладает выраженным противоязвенным действием в исследованных дозах, причем противоязвенный эффект соединения (IIб) превосходит эффект карбеноксолона (50 мг/кг) ~в 2 раза при введении в дозе 25 мг/кг, т.е. в 2 раза меньшей дозе. Синтез сапонина (IIб) проводили путем конденсации 2,3,4,6-тетра-О-ацетил-  -D-галактопиранозилбромида с 30-метиловым эфиром пента-О-ацетил-ГК (I) в присутствии свежеприготовленного Ag2CO3 (реактива Фетизона) в безводных условиях в дихлорэтане. Ацетат сапонина (IIа) выделен в гомогенном по ТСХ состоянии колоночной хроматографией на силикагеле с выходом 66%. Дезацетилирование сапонина (IIа) 0,5% раствором КОН в смеси метанола-хлористого метилена привело к тритерпеновому олигогликозиду (сапонину) (IIб), содержащему 2 остатка -D-галактопиранозилбромида с 30-метиловым эфиром пента-О-ацетил-ГК (I) в присутствии свежеприготовленного Ag2CO3 (реактива Фетизона) в безводных условиях в дихлорэтане. Ацетат сапонина (IIа) выделен в гомогенном по ТСХ состоянии колоночной хроматографией на силикагеле с выходом 66%. Дезацетилирование сапонина (IIа) 0,5% раствором КОН в смеси метанола-хлористого метилена привело к тритерпеновому олигогликозиду (сапонину) (IIб), содержащему 2 остатка  -D-галактопиранозы, связанных с диглюкуронидной частью ГК сложноэфирными связями и являющемуся модифицированным аналогом ГК с удлиненной углеводной цепью. Структура сапонина (IIб) была подтверждена спектральными методами.
Сущность технического решения поясняется следующими примерами.
Пример 1. Получение сапонина (IIб) -D-галактопиранозы, связанных с диглюкуронидной частью ГК сложноэфирными связями и являющемуся модифицированным аналогом ГК с удлиненной углеводной цепью. Структура сапонина (IIб) была подтверждена спектральными методами.
Сущность технического решения поясняется следующими примерами.
Пример 1. Получение сапонина (IIб)1. 30-Метиловый эфир перацетата 6′,6”-ди-О-  -D-галактопиранозилкарбоксилат 3-О-[2′-О-( -D-галактопиранозилкарбоксилат 3-О-[2′-О-( -D-глюкуронопиранозил)- -D-глюкуронопиранозил)- -D-глюкуронопиранозида) глицирретовой кислоты (IIа). Смесь 1,04 г (1 ммоль) пента-О-ацетата 30-метилового эфира ГК (I), 1 г молекулярных сит 4 А0, 1,4 г свежеприготовленного реактива Фетизона* и 2 ммоль перацетата l- -D-глюкуронопиранозида) глицирретовой кислоты (IIа). Смесь 1,04 г (1 ммоль) пента-О-ацетата 30-метилового эфира ГК (I), 1 г молекулярных сит 4 А0, 1,4 г свежеприготовленного реактива Фетизона* и 2 ммоль перацетата l- -бpoм-D-галактопиранозы в 50 мл сухого дихлорэтана кипятили 6 ч без доступа влаги в темноте. Осадок серебряных солей отфильтровали, промыли 20 мл дихлорэтана, фильтрат упарили в вакууме при ~50oС. Сухой остаток хроматографировали на колонке с силикагелем, элюируя смесью бензола-ацетона, 25: 1 (v/v) с контролем по ТСХ в системе хлороформ-спирт, 25: 1 (v/v). Фракции с целевым продуктом (IIa) (Rf 0,22) объединили, упарили и перекристаллизовали дважды из водного этанола. Выход 0,8 г (66%). Белый порошок. [ -бpoм-D-галактопиранозы в 50 мл сухого дихлорэтана кипятили 6 ч без доступа влаги в темноте. Осадок серебряных солей отфильтровали, промыли 20 мл дихлорэтана, фильтрат упарили в вакууме при ~50oС. Сухой остаток хроматографировали на колонке с силикагелем, элюируя смесью бензола-ацетона, 25: 1 (v/v) с контролем по ТСХ в системе хлороформ-спирт, 25: 1 (v/v). Фракции с целевым продуктом (IIa) (Rf 0,22) объединили, упарили и перекристаллизовали дважды из водного этанола. Выход 0,8 г (66%). Белый порошок. [ ]20D +62o (с 0,04; МеОН). ИК-спектр, ]20D +62o (с 0,04; МеОН). ИК-спектр,  , см-1: 1760 (ОАс); 1670 (С11=О). УФ-спектр, , см-1: 1760 (ОАс); 1670 (С11=О). УФ-спектр,  EtOHmax (lg EtOHmax (lg  ): 246 нм (4,1). Найдено, %: С 54,78; Н 6,44. С81Н110О39 ): 246 нм (4,1). Найдено, %: С 54,78; Н 6,44. С81Н110О39 3Н2О. Вычислено,%: С 55,22; Н 6,29. Спектр ЯМР 1Н (СDСl3, 3Н2О. Вычислено,%: С 55,22; Н 6,29. Спектр ЯМР 1Н (СDСl3,  , м.д.): 0,74; 0,80; 1,00; 1,12; 1,15; 1,22; 1,34 (все с, 21 Н, 7 СН3); 2,0-2,2 (все с, 39 Н, 13 Ac); 3,68 (с, 3Н, ОСН3); 3,9-4,1 (м, Н-5′, Н-5” ГК; 2 Н-5 Galp; 4 Н-6 Galp); 4,46 (д, J=6,7 Гц; 1 H, H-1′ ГК); 4,96 (д, 1 Н, J=6,8 Гц; Н-1” ГК); 5,0-5,3 (м, 2 Н-3 Galp; 2 Н-4 Galp; Н-3′, Н-3” ГК); 5,42 (д, 1Н, J=3,1 Гц; Н-1 , м.д.): 0,74; 0,80; 1,00; 1,12; 1,15; 1,22; 1,34 (все с, 21 Н, 7 СН3); 2,0-2,2 (все с, 39 Н, 13 Ac); 3,68 (с, 3Н, ОСН3); 3,9-4,1 (м, Н-5′, Н-5” ГК; 2 Н-5 Galp; 4 Н-6 Galp); 4,46 (д, J=6,7 Гц; 1 H, H-1′ ГК); 4,96 (д, 1 Н, J=6,8 Гц; Н-1” ГК); 5,0-5,3 (м, 2 Н-3 Galp; 2 Н-4 Galp; Н-3′, Н-3” ГК); 5,42 (д, 1Н, J=3,1 Гц; Н-1 / Galp); 5,50 (д, 1 Н, J=3,2 Гц; Н-1 / Galp); 5,50 (д, 1 Н, J=3,2 Гц; Н-1 Galp); 5,60 (с, 1Н, =C12-Н). Спектр ЯМР 13С (CDCl3, Galp); 5,60 (с, 1Н, =C12-Н). Спектр ЯМР 13С (CDCl3,  , м.д.): 103,50 (С1′ ГК); 102,74 (Cl” ГК); 170,87 (С6′ ГК); 170,76 (С6” ГК); 94,16 (C1 , м.д.): 103,50 (С1′ ГК); 102,74 (Cl” ГК); 170,87 (С6′ ГК); 170,76 (С6” ГК); 94,16 (C1  -D-Galp); 91,92 (Cl -D-Galp); 91,92 (Cl  -D-Galp); 61,80 и 61,63 (2 С6 Galp). Другие сигналы углеводной части: 77,26; 73,15; 72,99; 72,86; 72,04; 71,89; 71,68; 71,42; 70,41; 69,50; 68,37; 68,23; 67,66; 67,29; 67,09; 66,25. Агликоновая часть: 39,19 (Cl); 90,06 (C3); 55,22 (С4); 61,15 (С9); 200,05 (C11); 128,58 (С12); 170,44 (С13); 45,38 (С14); 48,42 (С18); 43,18(С20); 176,97 (C30); 51,80 (С31); СН3СО: 170,27; 170,16; 170,08; 169,72; 169,23; 169,14; 169,00; 167,07 (СО); 20,96; 20,83; 20,66 (СН3).
2. 30-Метиловый эфир 6′,6”- ди- -D-Galp); 61,80 и 61,63 (2 С6 Galp). Другие сигналы углеводной части: 77,26; 73,15; 72,99; 72,86; 72,04; 71,89; 71,68; 71,42; 70,41; 69,50; 68,37; 68,23; 67,66; 67,29; 67,09; 66,25. Агликоновая часть: 39,19 (Cl); 90,06 (C3); 55,22 (С4); 61,15 (С9); 200,05 (C11); 128,58 (С12); 170,44 (С13); 45,38 (С14); 48,42 (С18); 43,18(С20); 176,97 (C30); 51,80 (С31); СН3СО: 170,27; 170,16; 170,08; 169,72; 169,23; 169,14; 169,00; 167,07 (СО); 20,96; 20,83; 20,66 (СН3).
2. 30-Метиловый эфир 6′,6”- ди- -D-галактопиранозилкарбоксилат 3-O-[2′-O-( -D-галактопиранозилкарбоксилат 3-O-[2′-O-( -D-глюкуронопиразил)- -D-глюкуронопиразил)- -D-глюкуронопиранозида) глицирретовой кислоты (IIб). 0,5 г перацетата (IIа) перемешивали в 20 мл 0,5% раствора КОН в МеОН-СН2Сl2 при 20-22 0С 1 ч, обработали катионитом КУ-2-8 (H+-форма) до рН ~5 и упарили в вакууме при ~30oС. Остаток переосадили из сухого метанола эфиром. Выход 0,39 г (78%). Гигроскопичное аморфное вещество желтоватого цвета. [ -D-глюкуронопиранозида) глицирретовой кислоты (IIб). 0,5 г перацетата (IIа) перемешивали в 20 мл 0,5% раствора КОН в МеОН-СН2Сl2 при 20-22 0С 1 ч, обработали катионитом КУ-2-8 (H+-форма) до рН ~5 и упарили в вакууме при ~30oС. Остаток переосадили из сухого метанола эфиром. Выход 0,39 г (78%). Гигроскопичное аморфное вещество желтоватого цвета. [ ]20D +45 ]20D +45 20 (с 0,04; ЕtOН). ИК-спектр, 20 (с 0,04; ЕtOН). ИК-спектр,  , см-1: 3600-3200 (ОН); 1725 (ОСН3); 1660 (C11= O). УФ-спектр, , см-1: 3600-3200 (ОН); 1725 (ОСН3); 1660 (C11= O). УФ-спектр,  EtOHmax (lg EtOHmax (lg  ): 244 нм (4,1). Найдено,%: С 53,85; Н 6,80. С55-Н84O26 ): 244 нм (4,1). Найдено,%: С 53,85; Н 6,80. С55-Н84O26 3Н2O. Вычислено, %: С 54,35; Н 6,94.
Спектр ЯМР 1H(DMF-d7, 3Н2O. Вычислено, %: С 54,35; Н 6,94.
Спектр ЯМР 1H(DMF-d7,  , м.д.): 0,75; 0,78; 0,97; 1,08; 1,14; 1,26; 1,40 (все с, 21Н, 7 СН3); 2,40 (с, 1Н, Н-9); 3,65 (с, 1Н, ОСН3); 4,36 (д., 1Н, Н-1′ ГК); 4,48 (д. 1Н, Н-1” ГК); 4,70 (уш. с, 1Н, Н-1 , м.д.): 0,75; 0,78; 0,97; 1,08; 1,14; 1,26; 1,40 (все с, 21Н, 7 СН3); 2,40 (с, 1Н, Н-9); 3,65 (с, 1Н, ОСН3); 4,36 (д., 1Н, Н-1′ ГК); 4,48 (д. 1Н, Н-1” ГК); 4,70 (уш. с, 1Н, Н-1  -D-Galp); 5,10 (уш. с., 1Н, Н-1 -D-Galp); 5,10 (уш. с., 1Н, Н-1  -D-Galp); 5,50 (с, 1Н, -С12-Н). Спектр ЯМР 13С (DMF-d7, -D-Galp); 5,50 (с, 1Н, -С12-Н). Спектр ЯМР 13С (DMF-d7,  , м.д. ): 104,54 (С1′ ГК); 103,24 (С 1” ГК); 172,50 (С6′ ГК); 173,0 (С6” ГК); 98,62 (Cl , м.д. ): 104,54 (С1′ ГК); 103,24 (С 1” ГК); 172,50 (С6′ ГК); 173,0 (С6” ГК); 98,62 (Cl  -D-Galp); 93,79 (Cl -D-Galp); 93,79 (Cl  -D-Galp). Другие сигналы: 77,78; 77,15; 76,10; 75,80; 74,76; 74,00; 73,49; 72,95; 72,29; 72,00; 71,80; 71,40; 70,75; 70,14; 69,51; 68,50 (С2-С5 2Galp; C3′, C3”, С4′, С4”, С5′, С5” ГК); 64,02 и 63,50 (2 С6 Galp). Агликоновая часть: 39,80 (Cl); 89,26 (C3); 55,12 (С5); 61,83 (С9); 200,00 (С11); 128,25(С12); 167,65 (С13); 45,73 (С14); 48,97 (С18); 43,70 (С20); 177,24(С30); 51,95 (С31).
Пример 2. Изучение противоязвенного действия сапонина (IIб).
Противоязвенную активность сапонина (IIб) изучали на белых беспородных крысах массой 180-210 г на модели экспериментальных язв желудка, вызванных ацетилсалициловой кислотой. За сутки до моделирования язв животных лишали пищи и воды, содержали в помещении вивария при температуре не выше +16oС. Исследуемое соединение вводили через зонд в желудок в дозах 25 и 100 мг/кг. Через 1 ч внутрижелудочно вводили ацетилсалициловую кислоту в дозе 150 мг/кг двукратно с интервалом в 6 ч. Через 1 сутки животных забивали под эфирным наркозом, извлекали желудок и визуально учитывали все поражения слизистой оболочки. О противоязвенной активности препаратов судили по уменьшению количества деструкции слизистой оболочки желудка крыс. В качестве референспрепаратов использовали известное противоязвенное средство карбеноксолон. Результаты опытов приведены в таблице.
Установлено, что противоязвенное действие соединения (IIб) в дозе 25 мг/кг превосходит действие карбеноксолона в дозе 50 мг/кг в 2 раза. Данное соединение является менее токсичным веществом, чем карбеноксолон.
Источники информации
2. Елизарова О. Н. Определение пороговых доз промышленных ядов при пероральном введении. М.: Медицина, 1971. С. 47-48. -D-Galp). Другие сигналы: 77,78; 77,15; 76,10; 75,80; 74,76; 74,00; 73,49; 72,95; 72,29; 72,00; 71,80; 71,40; 70,75; 70,14; 69,51; 68,50 (С2-С5 2Galp; C3′, C3”, С4′, С4”, С5′, С5” ГК); 64,02 и 63,50 (2 С6 Galp). Агликоновая часть: 39,80 (Cl); 89,26 (C3); 55,12 (С5); 61,83 (С9); 200,00 (С11); 128,25(С12); 167,65 (С13); 45,73 (С14); 48,97 (С18); 43,70 (С20); 177,24(С30); 51,95 (С31).
Пример 2. Изучение противоязвенного действия сапонина (IIб).
Противоязвенную активность сапонина (IIб) изучали на белых беспородных крысах массой 180-210 г на модели экспериментальных язв желудка, вызванных ацетилсалициловой кислотой. За сутки до моделирования язв животных лишали пищи и воды, содержали в помещении вивария при температуре не выше +16oС. Исследуемое соединение вводили через зонд в желудок в дозах 25 и 100 мг/кг. Через 1 ч внутрижелудочно вводили ацетилсалициловую кислоту в дозе 150 мг/кг двукратно с интервалом в 6 ч. Через 1 сутки животных забивали под эфирным наркозом, извлекали желудок и визуально учитывали все поражения слизистой оболочки. О противоязвенной активности препаратов судили по уменьшению количества деструкции слизистой оболочки желудка крыс. В качестве референспрепаратов использовали известное противоязвенное средство карбеноксолон. Результаты опытов приведены в таблице.
Установлено, что противоязвенное действие соединения (IIб) в дозе 25 мг/кг превосходит действие карбеноксолона в дозе 50 мг/кг в 2 раза. Данное соединение является менее токсичным веществом, чем карбеноксолон.
Источники информации
2. Елизарова О. Н. Определение пороговых доз промышленных ядов при пероральном введении. М.: Медицина, 1971. С. 47-48.
Формула изобретения
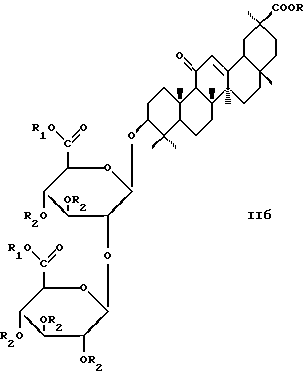 R=Me, R2=H 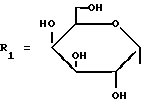 проявляющий противоязвенную активность. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 31.03.2004
Извещение опубликовано: 10.03.2006 БИ: 07/2006
|
||||||||||||||||||||||||||
