Патент на изобретение №2201248
|
||||||||||||||||||||||||||
(54) СТАБИЛЬНЫЙ ВОДНЫЙ ПЕПТИДНЫЙ ПРЕПАРАТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ГОРМОНЗАВИСИМОГО ЗАБОЛЕВАНИЯ У СУБЪЕКТА
(57) Реферат: Изобретение касается стабильных жидких водных препаратов пептидных соединений в высоких концентрациях (данные стабильные препараты содержат по меньшей мере приблизительно 15% пептида в воде), а также способ получения указанных препаратов и способ лечения гормонзависимых заболеваний указанными препаратами, в частности рака простаты. Изобретение позволяет хранить препараты при повышенных температурах (37oС), в течение длительного времени и применять в имплантируемых доставляющих устройствах для пролонгированной доставки лекарственного вещества. 3 с. и 24 з.п.ф-лы, 9 табл., 8 ил. Область техники, к которой относится изобретение Данное изобретение относится к стабильным водным препаратам пептидных соединений в высоких концентрациях. Уровень техники Лютеинизирующий гормонвысвобождающий гормон (LHRH), известный также как гонадотропин-высвобождающий гормон (GnRH), является декапептидом структуры: pGlu-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-NН2. Он секретируется гипоталамусом и связывается рецепторами гипофиза, высвобождая лютеинизирующий гормон (LH) и фолликулстимулирующий гормон (FSH). LH и FSH стимулируют синтез стероидных гормонов половыми железами. Известны многочисленные аналоги LHRH, включая пептиды, близкие LHRH, которые действуют как агонисты и пептиды, которые действуют как антагонисты (Zoladex (золадекс) (имплантат госерелина ацетата), справочник Physician’s Desk Reference, 50-е изд., с. 2858-2861 (1996); Патент США 3914412, выданный 21 октября 1975 г.; Патент США 4547370, выданный 15 октября 1985 г.; Патент США 4661472, выданный 28 апреля 1987 г.; Патент США 4689396, выданный 25 августа 1987 г. ; Патент США 4851385, выданный 25 июля 1989 г.; Патент США 5198533, выданный 30 марта 1993 г.; Патент США 5480868, выданный 02 января 1996 г.; WО 92/20711, опубликованная 26 ноября 1992 г.; WО 95/00168, опубликованная 05 января 1995 г.; WО 95/04540, опубликованная 16 февраля 1995 г.; Статья “Stability of Gonadorelin and Triptorelin in Aqueous Solution”, V.J.Helm, B. W.Muller, Pharmaceutical Research, 7/12, с. 1253-1256(1990); Статья “New Degradation Product of Des-Gly10-NH2-LH-RH-Ethilamide (Fertirelin) in Aqueous Solution”, J. Okada, T. Seo, F.Kasahara, K.Takeda, S.Kondo, J. of Pharmaceutical Sciences, 80/2, с. 167-170 (1991); Статья “Characterizaton of the Solution Degradation Product of Histrelin, a Gonadotropin Releasing Hormone (LHRH) Agonist”, A.R.Oyler, R.E.Naldi, J.R.Lloyd, D.A.Graden, C.J.Shaw, M.L. Cotter, J. of Pharmaceutical Sciences, 80/3, с. 271-275 (1991); Статья “Parenteral Peptide Formulations: Chemical and Physical Properties of Native Luteinizing Hormone-Releasing Hormone (LHRH) and Hydrophobic Analogues in Aqueous Solution”, M. F.Powell, L.M.Sanders, A.Rogerson, V. Si, Pharmaceutical Research, 8/10, с. 1258-1263(1991)). Описание каждой публикации, патента или патентной заявки введено в заявку в виде ссылки во всей полноте в той же мере, как если бы содержание каждой отдельной публикации, патента или патентной заявки было специально и индивидуально введено посредством ссылки. Известно, что аналоги LHRH используют для лечения гормонзависимых заболеваний, таких как рак простаты, доброкачественная простатомегалия, эндометриоз, миома матки, фиброма матки, преждевременное половое созревание или рак молочной железы, а также в качестве противозачаточных средств (Патент США 5480868, выданный 02 января 1996 г.). Назначение лекарств с непрерывным их высвобождением является предпочтительным как для агонистов близких LHRH соединений, которые снижают число доступных рецепторов после повторного приема лекарства таким образом, что подавляется образование стероидных гормонов, так и для антагонистов близких LHRH соединений, которые должны вводиться непрерывно для постоянного ингибирования эндогенного LHRH (Патент США 5480868, выданный 02 января 1996 г.). Непрерывная (продолжительная) парентеральная доставка лекарств, особенно пептидных лекарств, имеет множество преимуществ. Применение имплантируемых устройств для непрерывной доставки широкого круга лекарств или других полезных агентов хорошо известно в уровне техники. Типичные устройства описаны, например, в Патентах США 5034229, 5057318 и 5110569. Описание каждого из данных патентов введено здесь в виде ссылки. В общем случае биодоступность пептидов, включая близкие LHRH соединения, при пероральном введении является низкой (Статья “Degradation of the LHRH Analog Nafarelin Acetate in Aqueous Solution”, D.M.Johnson, R.A.Pritchard, W.F.Taylor, D.Conley, G.Zuniga, K.G.McGreevy, Intl. J. of Pharmaceutics, 31, с. 125-129 (1986); Статья “Percutaneous Absorption Enhancement of Leuprolide”, M. Y.Fu Lu, D.Lee, G.S.Rao, Pharmaceutical Research, 9/12, с. 1575-1576 (1992).). Имеющиеся в настоящее время в продаже водные препараты LHRH, его аналогов и близких соединений, которые используют для парентеральных инъекций, обычно содержат относительно низкие концентрации близких LHRH соединений (0,05 до 5 мг/мл) и могут также содержать наполнители, такие как маннит или лактозу (Lutrepulse (латрепалс) (гонадорелина ацетат для внутривенных инъекций), Справочник Physician’s Desk Reference, 50-e изд. , с. 980-982 (1996); Factrel (фактрел) (гонадорелин HCl для подкожных и внутривенных инъекций), Справочник Physician’s Desk Reference, 50-e изд., с. 2877-2878 (1996); Lupron (лапрон) (лейпролида ацетат для подкожных инъекций), Справочник Physician’s Desk Reference, 50-e изд., с. 2555-2556 (1996)). Такие препараты близких LHRH соединений должны либо храниться охлажденными, либо они могут храниться при комнатной температуре в течение коротких периодов времени. Доступные депо-препараты близких LHRH соединений, которые назначают для непрерывного высвобождения в течение 1 – 3 месяцев, включают препарат, содержащий 15% близкого LHRH соединения, диспергированного в матриксе сополимера D, L-мoлoчнoй и гликолевой кислот, представляющий собой цилиндр для подкожного введения (Zoladex (золадекс) (имплантат госерелина ацетата), справочник Physician’s Desk Reference, 50-e изд., с. 2858-2861 (1996)) и препарат, состоящий из микрочастиц, содержащих ядро из близкого LHRH соединения и желатина, которые окружены оболочкой из сополимера D,L-мoлoчнoй и гликолевой кислот. Данные микрочастицы суспендированы в разбавителе для подкожной или внутримышечной инъекции (Lupron depot (лапрон депо) (лейпролида ацетат для депо-суспензии), Справочник Physician’s Desk Reference, 50-e изд., с. 2556-2562 (1996); Статья “Preparation of Three-Month Depot Injectable Microspheres of Leuprorelin Acetate Using Biodegradable Polymers”, Pharmaceutical Research, 11/8, с. 1143-1147 (1994)). Эти продукты могут храниться при комнатной или более низкой температуре. Известно, что водные препараты близких LHRH соединений отличаются как химической, так и физической нестабильностью, а также разлагаются после облучения (Статья “Stability of Gonadorelin and Triptorelin in Aqueous Solution”, V.J. Helm, B.W. Muller, Pharmaceutical Research, 7/12, с. 1253-1256(1990); Статья “New Degradation Product of Des-Gly10-NH2-LH-RH-Ethilamide (Fertirelin) in Aqueous Solution”, J.Okada, T.Seo, F.Kasahara, K. Takeda, S.Kondo, J. of Pharmaceutical Sciences, 80/2, с. 167-170 (1991); Статья “Characterizaton of the Solution Degradation Product of Histrelin, a Gonadotropin Releasing Hormone (LHRH) Agonist”, A.R.Oyler, R.E.Naldi, J.R. Lloyd, D. A. Graden, C. J.Shaw, M.L.Cotter, J. of Pharmaceutical Sciences, 80/3, с. 271-275 (1991); Статья “Parenteral Peptide Formulations: Chemical and Physical Properties of Native Luteinizing Hormone-Releasing Hormone (LHRH) and Hydrophobia Analogues in Aqueous Solution”, M.F.Powell, L.M. Sanders, A. Rogerson, V. Si, Pharmaceutical Research, 8/10, с. 1258-1263 (1991); Статья “Degradation of the LHRH Analog Nafarelin Acetate in Aqueous Solution”, D.M.Johnson, R.A.Pritchard, W.F.Taylor, D.Conley, G.Zuniga, K.G. McGreevy, Intl. J. of Pharmaceutics, 31, с. 125-129 (1986); Статья Pharmaceutical Manipulation of Leuprorelin Acetate to Improve Clinical Performance”, H.Toguchi, J. of Intl. Medical Research, 18, с. 35-41 (1990); Статья “Long-Term Stability of Aqueous Solutions of Luteinizing Hormone-Releasing Hormone Assessed by an In-Vitro Bioassay and Liquid Chromatography”, Y.F. Shi, R. J.Sherins, D.Brightwell, J.F.Gallelli, D.C.Chatterji, J. of Pharmaceutical Sciences, 73/6, с. 819-821 (1984); Статья “Peptide Liquid Crystals: Inverse Correlation of Kinetic Formation and Thermodynamic Stability in Aqueous Solution”, M.F.Powell, J.FIeitman, L.M.Sanders, V.C. Si, Pharmaceutical Research, 11/9, с. 1352-1354 (1994); Статья “Solution Behavior of Leuprolide Acetate, an LHRH Agonist, as Determined by Circular Dichroism Spectroscopy”, M.E.Powers, A.Adejei, M.Y.Fu Lu, M.C.Manning, Intl. J. of Pharmaceutics, 108, с. 49-55 (1994)). Препараты, которые, как было показано, являлись стабильными (t90 приблизительно пять лет) были очень низкоконцентрированными (25 мкг/мл) водными забуференными (10 мМ буфер, ионная сила 0,15) растворами, которые хранили при температурах, не превышающих комнатную температуру (25oС) (Статья “Parenteral Peptide Formulations: Chemical and Physical Properties of Native Luteimzing Hormone-Releasing Hormone (LHRH) and Hydrophobic Analogues in Aqueous Solution”, M. F.Powell, L.M.Sanders, A.Rogerson, V. Si, Pharmaceutical Research, 8/10, с. 1258-1263 (1991)). Существует потребность в стабильных высококонцентрированных водных препаратах пептидов. Данное изобретение представляет стабильные водные препараты, которые являются растворами пептидных соединений в воде в концентрациях, по меньшей мере, приблизительно 10%. Данные стабильные высококонцентрированные препараты могут храниться при повышенных температурах (например, 37oС) в течение длительного времени, и они особенно полезны для использования в имплантируемых доставляющих устройствах для продолжительной доставки (например, 1 – 12 месяцев или дольше) лекарственного вещества. Водные препараты могут необязательно включать буфер, наполнители, этанол (ЕtOН), поверхностно-активное вещество или консервант. В одном аспекте изобретение представляет стабильные водные препараты пептидных соединений, при этом указанные препараты содержат, по меньшей мере, приблизительно 10% (маc./маc.) пептидного соединения и воду. В другом аспекте изобретение представляет способы приготовления стабильного водного препарата пептидного соединения, которые предусматривают растворение, по меньшей мере, приблизительно 10% (маc./маc.) пептидного соединения в воде. В еще одном аспекте изобретение представляет способы лечения субъекта, страдающего от состояния, которое может быть облегчено назначением приема пептидного соединения, при этом указанные способы предусматривают введение указанному субъекту эффективного количества стабильного водного препарата, содержащего, по меньшей мере, приблизительно 10% (маc./маc.) пептидного соединения и воду. Фигура 1 иллюстрирует стабильность 40% раствора лейпролида ацетата в воде через два месяца хранения при 80oС, определенную с помощью обращенно-фазовой HPLC (ВЭЖХ, высокоэффективной жидкостной хроматографии) (RP-HPLC). На Фигуре 2 представлен тот же самый образец, что на Фигуре 1, исследуемый хроматографией с использованием молекулярных сит (SEC) или гель-фильтрацией. На данной фигуре показано, что имеется очень небольшая агрегация, которая представлена димерными и тримерными продуктами при отсутствии агрегации более высокого порядка. На Фигуре 3 представлен график Аррениуса, показывающий потерю лейпролида в 40% растворах лейпролида ацетата в воде. Фигура 4 иллюстрирует химическую и физическую стабильность 40% раствора лейпролида ацетата в воде приблизительно через три месяца хранения при 80oС. Фигура 5 иллюстрирует потерю лейпролида ацетата, соответствующую кинетике псевдопервого порядка 40% раствора в воде спустя период от трех до шести месяцев хранения при 37, 50, 65 и 80oС. Фигура 6 иллюстрирует химическую и физическую стабильность 40% раствора лейпролида ацетата в воде через девять месяцев хранения при 37oС. Фигура 7 иллюстрирует стабильность 30% раствора госерелина в ацетатном буфере и манните через 14 дней хранения при 80oС. Фигура 8 иллюстрирует, что оба водных препарата лейпролида (370 мг/мл) в форме геля и негеля сохраняли стабильность в течение более чем шести месяцев при 37oС. Данное изобретение касается неожиданного открытия того, что растворение пептидных соединений в высоких концентрациях (т.е. по меньшей мере, приблизительно 10%) в воде приводит к образованию стабильных водных препаратов. Ранее известные водные препараты пептидных соединений, представляющие собой разбавленные забуференные водные растворы, содержащие наполнители, такие как ЭДТА (этилендиаминтетрауксусная кислота) или аскорбиновая кислота, которые должны храниться при низких температурах (4-25oС), образуют продукты разложения посредством таких способов разложения, как катализируемый кислотой/щелочью гидролиз, дезамидирование, рацемизация и окисление. Напротив, предложенные в данной заявке препараты стабилизируют пептидные соединения в высоких концентрациях при повышенных температурах (например, от 37 до 80oС), таким образом делая возможной доставку пептидов в имплантируемых доставляющих устройствах, что другим образом не могло бы быть осуществлено. Стандартные пептидные и белковые препараты состоят из разбавленных водных растворов. Два важнейших для пептидного препарата аспекта включают солюбилизацию (растворение) и стабилизацию молекулы лекарственного вещества. Стабильность пептида обычно достигается варьированием одного или более из следующих параметров: рН, тип буфера, ионная сила, наполнители (ЭДТА, аскорбиновая кислота и т.п.). Напротив, в данном изобретении высококонцентрированные препараты пептидов в воде дают стабильные растворы. Изобретение заключается в использовании высоких концентраций пептида в водном растворе для стабилизации пептидных препаратов в отношении как химического, так и физического разложения. А. Определения: Использованные в контексте заявки, данные термины имеют следующие значения: Термин “химическая стабильность” означает, что процент продуктов разложения, образующихся химическими путями, такими как окисление или гидролиз, является приемлемым. В частности, препарат считают химически стабильным, если не более чем приблизительно 20% продуктов распада образуются через два месяца хранения при 37oС. Термин “физическая стабильность” означает, что процент агрегатов (например, димеров, тримеров и более крупных форм) является приемлемым. В частности, препарат считают физически стабильным, если не более чем приблизительно 15% агрегатов образуется через два месяца хранения при 37oС. Термин “стабильный препарат” означает, что через два месяца хранения при 37oС (или в эквивалентных условиях при повышенной температуре) остается, по меньшей мере, приблизительно 65% химически и физически стабильного пептидного соединения. В частности, предпочтительными препаратами являются препараты, которые сохраняют, по меньшей мере, приблизительно 80% химически и физически стабильного пептида в данных условиях. Особенно предпочтительными стабильными препаратами являются препараты, которые не разлагаются после стерилизующего облучения (например,  -, -, -лучами или электронным пучком).
Термины “пептид” и/или “пептидное соединение” означают полимеры из не более чем 50 остатков аминокислот, связанных амидными (CONH) связями. Аналоги, производные, агонисты, антагонисты и фармацевтически приемлемые соли любого из указанных материалов включаются в данные термины. Термины включают также пептиды и/или пептидные соединения, которые содержат D-аминокислоты, модифицированные, дериватизированные или не существующие в естественных условиях аминокислоты в D- или L-конфигурации и/или пептомиметические единицы, являющиеся частью их структуры.
Термин “близкое LHRH соединение” означает лютеинизирующий гормонвысвобождающий гормон (LHRH) и его аналоги и фармацевтически приемлемые соли. Окта-, нона- и декапептидные агонисты и антагонисты LHRH включены в понятие близкие LHRH соединения, равно как природный LHRH. В частности, предпочтительные близкие LHRH соединения включают LHRH, лейпролид, госерелин, нафарелин и другие известные активные агонисты и антагонисты (Zoladex (золадекс) (имплантат госерелина ацетата), справочник Physician’s Desk Reference, 50-е изд. , с. 2858-2861 (1996); Патент США 3914412, выданный 21 октября 1975 г.; Патент США 4547370, выданный 15 октября 1985 г.; Патент США 4661472, выданный 28 апреля 1987 г.; Патент США 4689396, выданный 25 августа 1987 г.; Патент США 4851385, выданный 25 июля 1989 г.; Патент США 5198533, выданный 30 марта 1993 г. ; Патент США 5480868, выданный 02 января 1996 г.; WО 92/20711, опубликованный 26 ноября 1992 г.; WО 5/00168, опубликованный 05 января 1995 г. ; WО95/04540, опубликованный 16 февраля 1995 г.; Статья “Stability of Gonadorelin and Triptorelin in Aqueous Solution”, V.J.Helm, B. W.Muller, Pharmaceutical Research, 7/12, с. 1253-1256(1990); Статья “New Degradation Product of Des-Gly10-NH2-LH-RH-Ethilamide (Fertirelin) in Aqueous Solution”, J.Okada, T.Seo, F.Kasahara, K.Takeda, S.Kondo, J. of Pharmaceutical Sciences, 80/2, с. 167-170 (1991); Статья “Characterizaton of the Solution Degradation Product of Histrelin, a Gonadotropin Releasing Hormone (LHRH) Agonist”, A.R.Oyler, R.E.Naldi, J.R.Lloyd, D.A.Graden, C.J.Shaw, M.L. Cotter, J. of Pharmaceutical Sciences, 80/3, с. 271-275 (1991); Статья “Parenteral Peptide Formulations: Chemical and Physical Properties of Native Luteinizing Hormone-Releasing Hormone (LHRH) and Hydrophobic Analogues in Aqueous Solution”, M.F.Powell, L.M.Sanders, A.Rogerson, V. Si, Pharmaceutical Research, 8/10, с. 1258-1263(1991); Статья “Degradation of the LHRH Analog Nafarelin Acetate in Aqueous Solution”, D.M.Johnson, R.A.Pritchard, W.F.Taylor, D.Conley, G.Zuniga, K.G.McGreevy, Intl. J. of Pharmaceutics, 31, с. 125-129 (1986); Статья “Percutaneous Absorption Enhancement of Leuprolide”, M. Y.Fu Lu, D.Lee, G.S.Rao, Pharmaceutical Research, 9/12, с. 1575-1576 (1992); Lutrepulse (латрепалс) (гонадорелина ацетат для внутривенных инъекций), Справочник Physician’s Desk Reference, 50-е изд., с. 980-982 (1996); Factrel (фактрел) (гонадорелин HCl для подкожных и внутривенных инъекций), Справочник Physician’s Desk Reference, 50-е изд. , с. 2877-2878 (1996); Lupron (лапрон) (лейпролида ацетат для подкожных инъекций), Справочник Physician’s Desk Reference, 50-е изд., с. 2555-2556 (1996); Lupron depot (лапрон депо) (лейпролида ацетат для депо-суспензии), Справочник Physician’s Desk Reference, 50-е изд., с. 2556-2562 (1996)).
Термин “высокая концентрация” означает, по меньшей мере, приблизительно от 10% (маc. /маc. ) и до максимальной растворимости данного близкого LHRH соединения.
Термин “наполнитель” означает более или менее инертную субстанцию в препарате, которую добавляют как разбавитель или носитель или для придания формы или консистенции. Наполнители отличаются от растворителей, таких как ЕtOН, который используют для растворения лекарственных веществ в препаратах, от неионных поверхностно-активных веществ, таких как Твин 20 (Tween 20), которые используют для солюбилизации лекарственных веществ в препаратах, и от консервантов, таких как бензиловые спирты и метил- или пропилпарабены, которые используют для предотвращения или ингибирования роста микробов.
Термин “буферная емкость” означает способность раствора, обусловленную присутствием смеси пары кислоты/щелочи в растворе, уменьшать какие-либо изменения рН, которые в противном случае произошли бы в растворе при добавлении к нему кислоты или щелочи.
Термин “полярный непротонный растворитель” означает полярный растворитель, который не содержит кислотный водород и не действует как донор водородной связи. Примерами полярных непротонных растворителей являются диметилсульфоксид (ДМСО), диметилформамид (ДМФ), гексаметилфосфотриамид (триамид гексаметилфосфорной кислоты) (ГМФА) и н-метилпирролидон.
Б. Приготовление препаратов -лучами или электронным пучком).
Термины “пептид” и/или “пептидное соединение” означают полимеры из не более чем 50 остатков аминокислот, связанных амидными (CONH) связями. Аналоги, производные, агонисты, антагонисты и фармацевтически приемлемые соли любого из указанных материалов включаются в данные термины. Термины включают также пептиды и/или пептидные соединения, которые содержат D-аминокислоты, модифицированные, дериватизированные или не существующие в естественных условиях аминокислоты в D- или L-конфигурации и/или пептомиметические единицы, являющиеся частью их структуры.
Термин “близкое LHRH соединение” означает лютеинизирующий гормонвысвобождающий гормон (LHRH) и его аналоги и фармацевтически приемлемые соли. Окта-, нона- и декапептидные агонисты и антагонисты LHRH включены в понятие близкие LHRH соединения, равно как природный LHRH. В частности, предпочтительные близкие LHRH соединения включают LHRH, лейпролид, госерелин, нафарелин и другие известные активные агонисты и антагонисты (Zoladex (золадекс) (имплантат госерелина ацетата), справочник Physician’s Desk Reference, 50-е изд. , с. 2858-2861 (1996); Патент США 3914412, выданный 21 октября 1975 г.; Патент США 4547370, выданный 15 октября 1985 г.; Патент США 4661472, выданный 28 апреля 1987 г.; Патент США 4689396, выданный 25 августа 1987 г.; Патент США 4851385, выданный 25 июля 1989 г.; Патент США 5198533, выданный 30 марта 1993 г. ; Патент США 5480868, выданный 02 января 1996 г.; WО 92/20711, опубликованный 26 ноября 1992 г.; WО 5/00168, опубликованный 05 января 1995 г. ; WО95/04540, опубликованный 16 февраля 1995 г.; Статья “Stability of Gonadorelin and Triptorelin in Aqueous Solution”, V.J.Helm, B. W.Muller, Pharmaceutical Research, 7/12, с. 1253-1256(1990); Статья “New Degradation Product of Des-Gly10-NH2-LH-RH-Ethilamide (Fertirelin) in Aqueous Solution”, J.Okada, T.Seo, F.Kasahara, K.Takeda, S.Kondo, J. of Pharmaceutical Sciences, 80/2, с. 167-170 (1991); Статья “Characterizaton of the Solution Degradation Product of Histrelin, a Gonadotropin Releasing Hormone (LHRH) Agonist”, A.R.Oyler, R.E.Naldi, J.R.Lloyd, D.A.Graden, C.J.Shaw, M.L. Cotter, J. of Pharmaceutical Sciences, 80/3, с. 271-275 (1991); Статья “Parenteral Peptide Formulations: Chemical and Physical Properties of Native Luteinizing Hormone-Releasing Hormone (LHRH) and Hydrophobic Analogues in Aqueous Solution”, M.F.Powell, L.M.Sanders, A.Rogerson, V. Si, Pharmaceutical Research, 8/10, с. 1258-1263(1991); Статья “Degradation of the LHRH Analog Nafarelin Acetate in Aqueous Solution”, D.M.Johnson, R.A.Pritchard, W.F.Taylor, D.Conley, G.Zuniga, K.G.McGreevy, Intl. J. of Pharmaceutics, 31, с. 125-129 (1986); Статья “Percutaneous Absorption Enhancement of Leuprolide”, M. Y.Fu Lu, D.Lee, G.S.Rao, Pharmaceutical Research, 9/12, с. 1575-1576 (1992); Lutrepulse (латрепалс) (гонадорелина ацетат для внутривенных инъекций), Справочник Physician’s Desk Reference, 50-е изд., с. 980-982 (1996); Factrel (фактрел) (гонадорелин HCl для подкожных и внутривенных инъекций), Справочник Physician’s Desk Reference, 50-е изд. , с. 2877-2878 (1996); Lupron (лапрон) (лейпролида ацетат для подкожных инъекций), Справочник Physician’s Desk Reference, 50-е изд., с. 2555-2556 (1996); Lupron depot (лапрон депо) (лейпролида ацетат для депо-суспензии), Справочник Physician’s Desk Reference, 50-е изд., с. 2556-2562 (1996)).
Термин “высокая концентрация” означает, по меньшей мере, приблизительно от 10% (маc. /маc. ) и до максимальной растворимости данного близкого LHRH соединения.
Термин “наполнитель” означает более или менее инертную субстанцию в препарате, которую добавляют как разбавитель или носитель или для придания формы или консистенции. Наполнители отличаются от растворителей, таких как ЕtOН, который используют для растворения лекарственных веществ в препаратах, от неионных поверхностно-активных веществ, таких как Твин 20 (Tween 20), которые используют для солюбилизации лекарственных веществ в препаратах, и от консервантов, таких как бензиловые спирты и метил- или пропилпарабены, которые используют для предотвращения или ингибирования роста микробов.
Термин “буферная емкость” означает способность раствора, обусловленную присутствием смеси пары кислоты/щелочи в растворе, уменьшать какие-либо изменения рН, которые в противном случае произошли бы в растворе при добавлении к нему кислоты или щелочи.
Термин “полярный непротонный растворитель” означает полярный растворитель, который не содержит кислотный водород и не действует как донор водородной связи. Примерами полярных непротонных растворителей являются диметилсульфоксид (ДМСО), диметилформамид (ДМФ), гексаметилфосфотриамид (триамид гексаметилфосфорной кислоты) (ГМФА) и н-метилпирролидон.
Б. Приготовление препаратовДанное изобретение касается высококонцентрированных жидких водных препаратов пептидных соединений, которые стабильны в течение увеличенных периодов времени при повышенных температурах. Стандартные разведенные водные препараты пептидов или белков нуждаются в манипуляциях с типом буфера, ионной силой, рН и наполнителями (например, ЭДТА и аскорбиновой кислоты) для того, чтобы достигнуть стабильности. Напротив, в заявленных препаратах стабильность пептидных соединений достигается путем применения высоких концентраций (по меньшей мере, приблизительно 10% маc./маc.) соединения, растворенного в воде. Примеры пептидов и пептидных соединений, препараты которых могут быть получены с использованием данного изобретения, включают такие пептиды, которые обладают биологической активностью или могут быть использованы для лечения заболевания или другого патологического состояния. Они включают, но не ограничиваются адренокортикотропным гормоном, ангиотензинами I и II, натрийуретическим пептидом предсердия, бомбезином, брадикинином, кальцитонином, церебеллином, динорфином А,  – и – и  -эндорфином, эндотелином, энкефалином, эпидермальным ростовым фактором, фертирелином, фолликулярный гонадотропин высвобождающим пептидом, галанином, глюкагоном, гонадорелином, гонадотропином, госерелином, ростовой фактор высвобождающим пептидом, гистрелином, инсулином, лейпролидом, LHRH, мотилином, нафарелином, нейротензином, окситоцином, соматостатином, веществом Р, фактором некроза опухоли, трипторелином и вазопрессином. Могут быть также использованы аналоги, производные, антагонисты, агонисты и их фармацевтически приемлемые соли.
В зависимости от конкретного пептидного соединения, из которого готовят препарат, следует принимать во внимание такие факторы, как ионная сила и рН. Например, мы обнаружили, что предпочтительные водные препараты лейпролида ацетата имеют низкую ионную силу и значение рН между приблизительно 4 и приблизительно 6.
Пептидные соединения, применяемые в препаратах и способах, соответствующих данному изобретению, могут быть использованы в форме соли, предпочтительно фармацевтически приемлемой соли. Используемые соли известны специалистам и включают соли неорганических кислот, органических кислот, неорганических оснований и органических оснований. Предпочтительными солями являются ацетаты.
Для использования в данном изобретении предпочтительными являются гидрофильные и легко растворимые в воде пептидные соединения. Специалист может легко установить, какие соединения будут использованы, на основе их растворимости в воде, т.е. растворимость соединений в воде должна составлять, по меньшей мере, приблизительно 10% (маc./маc.). Предпочтительно, чтобы это было также фармацевтически эффективным количеством. В частности, предпочтительными пептидными соединениями являются близкие LHRH соединения, включая лейпролид и лейпролида ацетат.
Количественное соотношение пептида может изменяться в зависимости от соединения, состояния, которое лечат, растворимости соединения, ожидаемой дозы и длительности введения (См., например, монографии The Pharmacological Basis of Therapeutics, Gilman и соавт., 7-ое изд. (1985) и Pharmaceutical Sciences, Remington, 18-е изд. (1990), описания которых приведены здесь в виде ссылки). Концентрация пептидного соединения может изменяться в интервале от, по меньшей мере, приблизительно 10% (маc./маc.) до максимальной растворимости соединения. Предпочтительным интервалом является от приблизительно 20 до приблизительно 60% (маc. /маc.). В действительности более предпочтительным интервалом является от приблизительно 30 до приблизительно 50% (маc./маc.) и наиболее предпочтительным интервалом является от приблизительно 35 до приблизительно 45% (маc./маc.).
В большинстве случаев стабильные препараты, соответствующие данному изобретению, могут быть приготовлены простым растворением терапевтически эффективного количества желаемого пептидного соединения в воде, хотя при этом возможно доведение рН.
Специалистам известно, что буферы, наполнители, растворители, такие как ЕЮН, солюбилизаторы, такие как неионные поверхностно-активные вещества, и консерванты могут быть с успехом добавлены в фармацевтические пептидные препараты (См. , например, монографию Pharmaceutical Sciences, Remington, 18-е изд. (1990)). Такие агенты могут добавляться в заявленные препараты в необязательном порядке.
В. Способы -эндорфином, эндотелином, энкефалином, эпидермальным ростовым фактором, фертирелином, фолликулярный гонадотропин высвобождающим пептидом, галанином, глюкагоном, гонадорелином, гонадотропином, госерелином, ростовой фактор высвобождающим пептидом, гистрелином, инсулином, лейпролидом, LHRH, мотилином, нафарелином, нейротензином, окситоцином, соматостатином, веществом Р, фактором некроза опухоли, трипторелином и вазопрессином. Могут быть также использованы аналоги, производные, антагонисты, агонисты и их фармацевтически приемлемые соли.
В зависимости от конкретного пептидного соединения, из которого готовят препарат, следует принимать во внимание такие факторы, как ионная сила и рН. Например, мы обнаружили, что предпочтительные водные препараты лейпролида ацетата имеют низкую ионную силу и значение рН между приблизительно 4 и приблизительно 6.
Пептидные соединения, применяемые в препаратах и способах, соответствующих данному изобретению, могут быть использованы в форме соли, предпочтительно фармацевтически приемлемой соли. Используемые соли известны специалистам и включают соли неорганических кислот, органических кислот, неорганических оснований и органических оснований. Предпочтительными солями являются ацетаты.
Для использования в данном изобретении предпочтительными являются гидрофильные и легко растворимые в воде пептидные соединения. Специалист может легко установить, какие соединения будут использованы, на основе их растворимости в воде, т.е. растворимость соединений в воде должна составлять, по меньшей мере, приблизительно 10% (маc./маc.). Предпочтительно, чтобы это было также фармацевтически эффективным количеством. В частности, предпочтительными пептидными соединениями являются близкие LHRH соединения, включая лейпролид и лейпролида ацетат.
Количественное соотношение пептида может изменяться в зависимости от соединения, состояния, которое лечат, растворимости соединения, ожидаемой дозы и длительности введения (См., например, монографии The Pharmacological Basis of Therapeutics, Gilman и соавт., 7-ое изд. (1985) и Pharmaceutical Sciences, Remington, 18-е изд. (1990), описания которых приведены здесь в виде ссылки). Концентрация пептидного соединения может изменяться в интервале от, по меньшей мере, приблизительно 10% (маc./маc.) до максимальной растворимости соединения. Предпочтительным интервалом является от приблизительно 20 до приблизительно 60% (маc. /маc.). В действительности более предпочтительным интервалом является от приблизительно 30 до приблизительно 50% (маc./маc.) и наиболее предпочтительным интервалом является от приблизительно 35 до приблизительно 45% (маc./маc.).
В большинстве случаев стабильные препараты, соответствующие данному изобретению, могут быть приготовлены простым растворением терапевтически эффективного количества желаемого пептидного соединения в воде, хотя при этом возможно доведение рН.
Специалистам известно, что буферы, наполнители, растворители, такие как ЕЮН, солюбилизаторы, такие как неионные поверхностно-активные вещества, и консерванты могут быть с успехом добавлены в фармацевтические пептидные препараты (См. , например, монографию Pharmaceutical Sciences, Remington, 18-е изд. (1990)). Такие агенты могут добавляться в заявленные препараты в необязательном порядке.
В. СпособыНами было показано, что стабильные водные препараты пептидных соединений могут быть приготовлены путем растворения пептидного соединения, из которого готовят препарат, в высокой концентрации (по меньшей мере 10% в воде. Мы протестировали данные препараты пептидных соединений, в частности препараты близкого LHRH соединения лейпролида, на стабильность, помещая их в условия ускоренного старения при повышенной температуре и измеряя химическую и физическую стабильность препаратов. Результаты данных исследований (представленные, например, в Таблице III и на Фигурах 1, 2 и 6) показывают, что эти препараты были стабильными в условиях, которые приближаются или превышают условия хранения в течение одного года при 37oС. Мы также протестировали препараты пептидных соединений, приготовленные, как описано в контексте заявки, на стабильность после  – облучения 2,5 Мрад. Результаты, представленные в Таблице IV, показывают, что данные препараты оставались химически и физически стабильными после такого облучения. Было обнаружено, что препараты, подвергнутые облучению пучком электронов, также оставались стабильными.
Как показано в Таблице I, мы исследовали широкий круг пептидных препаратов, в частности лейпролида, госерелина, LHRH, ангиотензина I, брадикинина, кальцитонина, инсулина, трипсиногена и вазопрессина, на стабильность путем растворения (или попытки растворения) их в воде с последующим помещением их в условия ускоренного старения при повышенных температурах. Была определена стабильность препаратов. Результаты представлены в Таблице I, как период полураспада при 37oС, принимая, что Еa = 22,2 ккал/моль. Многие протестированные пептиды были растворимы в воде и сохраняли стабильность в условиях тестирования. Растворимость конкретного пептида в воде и стабильность полученного раствора легко определяют с помощью рутинных способов, известных специалистам.
Показан линейный характер разложения препаратов 40% лейпролида в воде, которые хранили в течение шести месяцев при 37oС, который определяли по общей потере пептида в растворе. Анализ данных результатов дает значения энергии активации (Еа) 22,2 ккал/моль и t90 13,8 месяца, показывая стабильность данных препаратов при повышенных температурах.
Мы также неожиданно обнаружили, что определенные пептидные препараты, соответствующие данному изобретению, являются бактериостатическими (т.е. ингибируют рост бактерий), бактерицидными (т.е. вызывают гибель бактерий) и спороцидными (т.е. убивают споры). В частности, препараты, содержащие 50-400 мг/мл лейпролида, проявляли бактеристатическую, бактерицидную и спороцидную активность. На стабильность образцов не влияло внесение бактерий, что указывает на то, что ферменты, выделяющиеся из убитых или лизированных бактерий, не оказывают вредного воздействия на стабильность продукта. Это служит доказательством того, что на данные препараты не влияет активность ферментов.
Известно, что некоторые пептиды, например кальцитонин и лейпролид, являются физически нестабильными, проявляя агрегацию, образование геля и фибриллярность, когда из них готовят водный раствор. Например, повышение концентрации пептида, введение солей или осторожное перемешивание могут привести к образованию геля лейпролида. Улучшение физической стабильности позволяет производить более простое парентеральное введение, включая введение с использованием имплантируемых систем для доставки лекарственных веществ.
Было неожиданно обнаружено, что добавление полярных непротонных растворителей, таких как ДМСО, к водным препаратам определенных пептидов, таких как лейпролид, госерелин и кальцитонин, препятствует образованию геля в препарате. Это, вероятно, происходит потому, что неводные полярные непротонные растворители вызывают у пептидов формирование случайной закрученной/ – облучения 2,5 Мрад. Результаты, представленные в Таблице IV, показывают, что данные препараты оставались химически и физически стабильными после такого облучения. Было обнаружено, что препараты, подвергнутые облучению пучком электронов, также оставались стабильными.
Как показано в Таблице I, мы исследовали широкий круг пептидных препаратов, в частности лейпролида, госерелина, LHRH, ангиотензина I, брадикинина, кальцитонина, инсулина, трипсиногена и вазопрессина, на стабильность путем растворения (или попытки растворения) их в воде с последующим помещением их в условия ускоренного старения при повышенных температурах. Была определена стабильность препаратов. Результаты представлены в Таблице I, как период полураспада при 37oС, принимая, что Еa = 22,2 ккал/моль. Многие протестированные пептиды были растворимы в воде и сохраняли стабильность в условиях тестирования. Растворимость конкретного пептида в воде и стабильность полученного раствора легко определяют с помощью рутинных способов, известных специалистам.
Показан линейный характер разложения препаратов 40% лейпролида в воде, которые хранили в течение шести месяцев при 37oС, который определяли по общей потере пептида в растворе. Анализ данных результатов дает значения энергии активации (Еа) 22,2 ккал/моль и t90 13,8 месяца, показывая стабильность данных препаратов при повышенных температурах.
Мы также неожиданно обнаружили, что определенные пептидные препараты, соответствующие данному изобретению, являются бактериостатическими (т.е. ингибируют рост бактерий), бактерицидными (т.е. вызывают гибель бактерий) и спороцидными (т.е. убивают споры). В частности, препараты, содержащие 50-400 мг/мл лейпролида, проявляли бактеристатическую, бактерицидную и спороцидную активность. На стабильность образцов не влияло внесение бактерий, что указывает на то, что ферменты, выделяющиеся из убитых или лизированных бактерий, не оказывают вредного воздействия на стабильность продукта. Это служит доказательством того, что на данные препараты не влияет активность ферментов.
Известно, что некоторые пептиды, например кальцитонин и лейпролид, являются физически нестабильными, проявляя агрегацию, образование геля и фибриллярность, когда из них готовят водный раствор. Например, повышение концентрации пептида, введение солей или осторожное перемешивание могут привести к образованию геля лейпролида. Улучшение физической стабильности позволяет производить более простое парентеральное введение, включая введение с использованием имплантируемых систем для доставки лекарственных веществ.
Было неожиданно обнаружено, что добавление полярных непротонных растворителей, таких как ДМСО, к водным препаратам определенных пептидов, таких как лейпролид, госерелин и кальцитонин, препятствует образованию геля в препарате. Это, вероятно, происходит потому, что неводные полярные непротонные растворители вызывают у пептидов формирование случайной закрученной/ -спиральной конформации, которая не переукладывается в структуру -спиральной конформации, которая не переукладывается в структуру  -листа, и вследствие этого гель не образуется. Таким образом, данные растворители обладают антижелирующим эффектом.
Кроме того, исследования водных препаратов лейпролида (370 мг/мл) в форме геля и негеля при хранении при 37oС в течение 6 недель показали близкий профиль химической стабильности по данным RP-HPLC. Результаты представлены на Фигуре 8. Аналогичным образом стабильность водных препаратов лейпролида в форме жидкости и геля (полученного при взбалтывании) (370 мг/мл) исследовали in vitro при 37oС и in vivo на крысах соответственно. Результаты, представленные в Таблице II, показывают, что оба препарата в форме геля и жидкости оставались стабильными в течение более 18 недель.
Главный аспект изобретения состоит в том, что водные растворы, содержащие высокие концентрации пептидных соединений, являются стабильными при высоких температурах в течение длительных периодов времени. Таким образом, данные препараты имеют преимущество в том, что они могут транспортироваться и/или храниться в течение длительных периодов времени при комнатной или более высокой температуре. Они также пригодны для применения в имплантируемых доставляющих устройствах.
Описание примеров изобретения -листа, и вследствие этого гель не образуется. Таким образом, данные растворители обладают антижелирующим эффектом.
Кроме того, исследования водных препаратов лейпролида (370 мг/мл) в форме геля и негеля при хранении при 37oС в течение 6 недель показали близкий профиль химической стабильности по данным RP-HPLC. Результаты представлены на Фигуре 8. Аналогичным образом стабильность водных препаратов лейпролида в форме жидкости и геля (полученного при взбалтывании) (370 мг/мл) исследовали in vitro при 37oС и in vivo на крысах соответственно. Результаты, представленные в Таблице II, показывают, что оба препарата в форме геля и жидкости оставались стабильными в течение более 18 недель.
Главный аспект изобретения состоит в том, что водные растворы, содержащие высокие концентрации пептидных соединений, являются стабильными при высоких температурах в течение длительных периодов времени. Таким образом, данные препараты имеют преимущество в том, что они могут транспортироваться и/или храниться в течение длительных периодов времени при комнатной или более высокой температуре. Они также пригодны для применения в имплантируемых доставляющих устройствах.
Описание примеров изобретенияДля осуществления исследований, изложенных ниже в Примерах, используют следующие методы. 1. Приготовление растворов лейпролида ацетата. Лейпролида ацетат (полученный, например, от Mallinckrodt, St. Louis, Missouri) взвешивают, добавляют во взвешенное количество растворителя (стерильная дистиллированная вода, этанол/вода или вода с неионным поверхностно-активным веществом) в соответствующей концентрации (мас./мас.), затем осторожно перемешивают для растворения. Если не указано иначе, содержание лейпролида в виде свободного основания, вычисленное по сертификату анализа величины активности, равно 37% свободного основания. Это составляет 40% лейпролида ацетата за исключением указанных случаев. 2. Приготовление емкостей Емкости имплантируемых устройств для доставки лекарственных веществ (как описано в Патентной заявке США Serial 08/595761, введенной здесь в виде ссылки) наполняют соответствующим раствором лейпролида ацетата. Наполненные устройства затем проходят тест на стабильность. Препарат вносят в титановые или полимерные емкости с полимерными пробками, закрывающими каждый конец. Наполненную емкость затем запечатывают в пакет из полимерной фольги и помещают в сушильный шкаф для тестирования на стабильность. Следует отметить, что препараты в емкостях данных устройств полностью изолированы от внешней среды. 3. Обращенно-фазовая ВЭЖХ (RP-HPLC) Все исследуемые на стабильность образцы анализируют на концентрацию лейпролида и % площади пика, полученные при обращенно-фазовой ВЭЖХ с градиентом элюции с использованием охлаждаемого автоматического пробоотборника (4oС) для уменьшения разложения образца. Конкретные условия хроматографии приведены ниже в Таблице III. Стандарты лейпролида (в воде) различных (от 4 до 6) уровней концентраций, обычно в интервале 0,1 – 1,2 мг/мл, пропускают через колонку параллельно с образцами, исследуемыми на стабильность. Образцы, исследуемые на стабильность, проводят между наборами стандартов, не более чем по 40 образцов между наборами стандартов. Все пики, полученные между свободным (“мертвым”) объемом и 45 минутами элюирования, объединяют. Объединенные площади пиков стандартов лейпролида наносят на график как функцию концентрации. Затем вычисляют концентрации лейпролида для образцов, исследуемых на стабильность, используя линейную регрессию. Процент площадей пика для пика лейпролида, сумму всех пиков, элюированных до лейпролида (отмеченных как “другие”) и сумму всех пиков, элюируемых после лейпролида (отмеченных как “агрегаты”) также записывают и наносят на график как функцию точек времени выхода образца. 4. Хроматография с использованием молекулярных сит (гель-фильтрация) (SEC). Отобранные образцы, исследуемые на стабильность, анализируют по % площади пика и молекулярным массам, используя SEC-анализ с изократным раствором и с охлаждаемым автоматическим пробоотборником (4oС). Используемые условия хроматографии представлены в Таблице IV. Для вычисления молекулярных масс требуется определить свободный объем и общий объем колонки для гель-фильтрации. Для определения свободного объема и общего объема соответственно используют высокомолекулярный стандарт BioRad и 0,1% ацетон. Время удерживания первого пика в стандарте BioRad и пика ацетона записывают и переводят в единицы объема, используя приведенные ниже уравнения. Поскольку данные величины являются постоянными для определенной колонки, используемой для SEC и системы ВЭЖХ, то свободный и общий объемы определяют заново в случае внесения изменений в колонку для SEC или системы ВЭЖХ. Затем наносят стандартный образец, после которого проводят образцы, исследуемые на стабильность. Смесь стандартов содержит приблизительно 0,2 мг/мл следующих пептидов: бурсин (мол. масса = 449), пептид WLFR (мол. масса = 619), ангиотензин (мол. масса = 1181), GRF (мол. масса = 5108) и цитохром С (мол. масса = 12394). Данные стандарты выбирают потому, что молекулярная масса лейпролида заключена между их значениями и все они имеют основную рI (изоэлектрическую точку) (9,8 – 11,0), близкую pI лейпролида. Процент (%) площадей пиков записывают для всех пиков. Молекулярные массы разделенных образцов вычисляют, используя приведенные ниже уравнения. Vs = скорость потока (мл/мин)  время удерживания пика образца (мин) время удерживания пика образца (мин)Vo = скорость потока (мл/мин)  время удерживания пика свободного объема (мин) время удерживания пика свободного объема (мин)Vt = скорость потока (мл/мин)  время удерживания пика общего объема (мин) время удерживания пика общего объема (мин)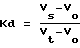 где Vs = объем стандарта или образца Vo = свободный объем Vt = общий объем Vs вычисляют для пика каждого стандартного пептида. Затем вычисляют Kd для каждого стандартного пептида, используя определенные ранее значения Vt и Vo. Линию линейной регрессии из графика logMW vs. относительно Kd-1 используют для определения молекулярной массы для каждого пика в образце, исследуемом на стабильность. Записывают также % площадей пиков для образцов, исследуемых на стабильность. 5. Оборудование и материалы Для RP-HPLC и SEC используют следующее оборудование и материалы: Систему ВЭЖХ Waters Millennium, состоящую из автоматического пробоотборника 717, насоса 626, контроллера 6000S, детектора с фотодиодной матрицей 900 и рефрактометрического детектора 414 (Waters Chromatography, Milford, MA) Флаконы для ВЭЖХ; кассеты с 48 положениями и 96 положениями (Waters Chromatography, Milford, MA) Колонку для ВЭЖХ HaiSil С18, 120 А, 5 мкм 4,6  250 мм (Higgins Analytical, Mountain View, CA) 250 мм (Higgins Analytical, Mountain View, CA)Колонку для SEC Pharmacia Peptide, HR 10/30 (Pharmacia Biotech, Piscataway, NJ). 6. Чистота Исследуемые на стабильность образцы анализируют, используя RP-HPLC. Площадь под кривой для пика лейпролида, деленная на сумму площадей под кривой для всех пиков, дает % чистоты. [Следует отметить, что данные по % концентрации, представленные данными по % чистоты (Примеры 5, 6 и 7), неубедительны. Способы анализа, используемые для определения % концентрации, являются ненадежными]. Следующие примеры предложены для иллюстрации данного изобретения и никоим образом не должны быть истолкованы как ограничивающие объем изобретения. Пример 1 Ускоренные исследования стабильности препаратов лейпролида ацетата Препараты 40% (маc./маc.) лейпролида ацетата (эквивалент приблизительно 37% лейпролида в виде свободного основания) в стерильной дистиллированной воде, этаноле/воде (70/30) или воде с 10% Tween 20 готовят, как описано выше, и используют для наполнения емкостей имплантируемых устройств для доставки лекарственных веществ так же, как описано выше. Некоторые емкости делают из полимерных материалов, тогда как некоторые – из титана. Заполненные устройства подвергают ускоренному старению путем хранения их при повышенных температурах (80-88oС) в течение семи дней в термостате (Precision Scientific или Thelco). Это эквивалентно приблизительно 1,5 годам при 37oС или приблизительно четырем годам при комнатной температуре (25oС), принимая энергию активации (Еa) за 22,2 ккал/моль. Образцы анализируют с помощью RP-HPLC или SEC, как описано выше, с целью определения химической и физической стабильности выдержанных (состаренных) препаратов. Результаты, представленные в Таблице V, показывают, что данные водные препараты способны поддерживать стабильность близкого LHRH соединения лейпролида. В каждом из случаев сохраняется, по меньшей мере, 65% лейпролида. Однако в процессе исследования большое количество препарата с ЕtOH улетучивается из емкости, указывая на то, что длительное хранение при повышенных температурах препаратов с высокими концентрациями летучего растворителя, подобного ЕtOH, может быть проблематичным. Было показано, что препарат, который содержит неионное поверхностно-активное вещество Tween 20, не более стабилен, чем водные растворы без данного солюбилизатора. Пример 2 Исследования стабильности облученных препаратов лейпролида ацетата Препараты 40% (мас./мас.), как получено, лейпролида ацетата (эквивалент 37% лейпролида в виде свободного основания) в воде готовят, как описано выше и используют для наполнения емкостей устройств для доставки лекарственных веществ так же, как описано выше. Некоторые емкости делают из полимерных материалов, тогда как некоторые – из титана. Наполненные емкости подвергают  -облучению 2,5 мегарад. Образцы партиями отправляют в Sterigenics (Tustin, California) и облучают -облучению 2,5 мегарад. Образцы партиями отправляют в Sterigenics (Tustin, California) и облучают  -лучами (Кобальт 60). Затем образцы подвергают ускоренному старению, как в Примере 1. Образцы, отмеченные “cold” (“на холоду”) транспортируют и облучают на сухом льду. Образцы берут на 0-й день и 7-й день и анализируют, используя RP-HPLC и SEC, как описано выше, с целью определения химической и физической стабильности облученных препаратов.
Результаты, представленные в Таблице VI, демонстрируют, что данные препараты лейпролида ацетата стабильны после облучения. В каждом случае сохраняется, по меньшей мере, 65% лейпролида при низких уровнях образования агрегатов.
Пример 3 -лучами (Кобальт 60). Затем образцы подвергают ускоренному старению, как в Примере 1. Образцы, отмеченные “cold” (“на холоду”) транспортируют и облучают на сухом льду. Образцы берут на 0-й день и 7-й день и анализируют, используя RP-HPLC и SEC, как описано выше, с целью определения химической и физической стабильности облученных препаратов.
Результаты, представленные в Таблице VI, демонстрируют, что данные препараты лейпролида ацетата стабильны после облучения. В каждом случае сохраняется, по меньшей мере, 65% лейпролида при низких уровнях образования агрегатов.
Пример 3Ускоренные исследования длительной стабильности лейпролида ацетата в воде Готовят растворы 40% (мас. /мас.) лейпролида ацетата в воде, вносят в емкости, хранят в течение двух месяцев при 80oС и анализируют, как описано выше. Результаты, представленные на Фигурах 1 (RP-HPLC) и 2 (SEC), показывают, что через два месяца выделяют 81,1% лейпролида при всего лишь 14,6% химического разложения и 5,1% физической агрегации. Растворы лейпролида ацетата (40% (мас./мас.) в воде) готовят, вносят, хранят и анализируют, как указано выше. Фигура 4 является графиком лейпролида и продуктов его химического и физического разложения, выделенных через три месяца. Сумму данных трех элементов представляют также как массовый баланс. Результаты показывают, что можно учитывать весь пептидный материал либо как интактный лейпролид, либо как продукты разложения, указывающие, что в исследованиях стабильности не упускается неизвестный процесс или продукт разложения. Растворы лейпролида ацетата (40% (мас./мас.) в воде) готовят, вносят, хранят при 37, 50, 65 или 80oС и анализируют с использованием RP-HPLC, как показано выше. На Фигуре 5 представляют потерю лейпролида в данных растворах через период от трех до шести месяцев и указывают, что разложение лейпролида соответствует кинетике псевдопервого порядка. Более того, как будет объяснено ниже, на Фигуре 3 представляют, что разложение лейпролида в воде соответствует линейной кинетике Аррениуса. Вследствие этого ускоренные исследования стабильности являются обоснованным способом оценки стабильности лейпролида и экстраполируются с понижением на температурные условия 37oС. Растворы 40% лейпролида ацетата (мас./мас.) в воде готовят, вносят в емкости, хранят при 37, 50, 65 или 80oС и анализируют с использованием RP-HPLC, как представлено выше. Результаты вычисляют, как описано в монографии Physical Pharmacy: Physical Chemical Principles in the Pharmaceutical Sciences, 3-е изд. , Martin et al., Глава 14 (1983) и показывают, что Еа данных растворов составляет 22,2 ккал/мол при t90, равном 13,8 месяца. Данные показаны в Таблице VII, и график Аррениуса этих данных представлен на Фигуре 3. Пример 4 Исследования длительной стабильности лейпролида ацетата в воде Химическая стабильность растворов 40% лейпролида ацетата, приготовленных и проанализированных, как описано выше, представлена на Фигуре 6. Через девять месяцев хранения при 37oС присутствует более чем 85% (88,3%) лейпролида при менее чем 10% (8,4%) продуктов химической деградации (показанные как “ранние” на фигуре на основе профиля RP-HPLC) и менее чем 5% (3,5%) физических агрегатов (показанные, как “поздние” на фигуре на основе профиля RP-HPLC, но при хорошей корреляции с данными SEC). Пример 5 Ускоренные исследования стабильности госерелина Препараты 30% госерелина (мас./мас.) в ацетатном буфере (рН 5,0; 0,0282 М) с 3% маннита хранят в стеклянных ампулах в течение 14 дней при 80oС и анализируют на чистоту, как описано выше. Результаты, представленные на Фигуре 7, показывают, что через 9 дней сохраняется приблизительно 65% госерелина. Пример 6 Исследование стабильности препаратов госерелина Препараты 40 – 45% (мас./мас.) госерелина либо в ацетатном буфере с 3% маннита, либо в ацетатном буфере с солью (0,9% NaCl) готовят, как описано выше, и помещают в полимерные контейнеры. Контейнеры хранят при 37oС в течение одного месяца в термостате. Образцы анализируют, используя RP-HPLC для определения химической стабильности состаренных препаратов. Представленные в Таблице VIII результаты демонстрируют, что данные водные препараты способны поддерживать стабильность близкого LHRH соединения госерелина. В каждом случае сохраняется, по меньшей мере, 98% госерелина. Пример 7 Исследования стабильности препаратов нафарелина Препараты 15% (мас. /мас. ) нафарелина в ацетатном буфере с 3% маннита готовят, как описано выше, и помещают в полимерные контейнеры. Контейнеры хранят при 37oС в течение одного месяца в термостате. Образцы анализируют, используя RP-HPLC для определения химической стабильности состаренных препаратов. Представленные в Таблице IX результаты демонстрируют, что данные водные препараты способны поддерживать стабильность близкого LHRH соединения нафарелина, поскольку сохраняется, по меньшей мере, 98% нафарелина. Модификация вышеописанных способов реализации различных вариантов осуществления данного изобретения будет очевидной для специалистов, которые следуют указаниям данного изобретения, как представлено в контексте заявки. Вышеописанные примеры не являются ограничивающими, но только представляют данное изобретение, объем которого определен следующей формулой изобретения. Формула изобретения
 -лучами или пучком электронов.
13. Способ по п. 12, отличающийся тем, что растворяют по меньшей мере приблизительно 30 мас. % близкого LHRH пептидного соединения.
14. Способ по п. 12, отличающийся тем, что указанное близкое LHRH пептидное соединение выбрано из группы, состоящей из лейпролида, LHRH, нафарелина и госерелина.
15. Способ по п. 12, отличающийся тем, что он дополнительно включает добавление по меньшей мере одного компонента, который выбирают из группы, состоящей из буфера, наполнителя, растворителя, солюбилизатора и консерванта.
16. Способ по п. 12, отличающийся тем, что в качестве близкого LHRH соединения используют лейпролида ацетат, который растворяют в количестве приблизительно от 30 мас. % до приблизительно 50 мас. % в стерильной дистиллированной воде.
17. Способ по п. 12, отличающийся тем, что он дополнительно включает добавление по меньшей мере одного неводного полярного непротонного растворителя.
18. Способ по п. 17, отличающийся тем, что указанный неводный полярный непротонный растворитель представлен диметилсульфоксидом или диметилформамидом.
19. Способ лечения гормонзависимого заболевания у субъекта, включающий введение близкого LHRH пептидного соединения, отличающийся тем, что указанному субъекту вводят эффективное количество препарата по п. 1.
20. Способ по п. 19, отличающийся тем, что указанное введение осуществляют парентерально.
21. Способ по п. 19, отличающийся тем, что указанное введение осуществляют длительно непрерывно.
22. Способ по п. 20, отличающийся тем, что указанное введение осуществляют посредством имплантируемого устройства для доставки лекарственного вещества.
23. Способ по п. 19, отличающийся тем, что указанное гормонзависимое заболевание представлено раком простаты, причем в качестве близкого LHRH пептидного соединения используют лейпролид.
24. Способ по п. 19 или 23, отличающийся тем, что осуществляют ежедневное введение по меньшей мере приблизительно 80 мкг лейпролида.
25. Способ по п. 24, отличающийся тем, что указанное ежедневное введение осуществляют в течение периода, выбранного из группы, состоящей из 3, 6 и 12 месяцев.
26. Способ по п. 25, отличающийся тем, что указанное ежедневное введение осуществляют посредством устройства для доставки лекарственного вещества.
27. Способ по п. 19, отличающийся тем, что указанное гормонзависимое заболевание представлено раком простаты, причем в качестве близкого LHRH пептидного соединения используют антагонист LHRH. -лучами или пучком электронов.
13. Способ по п. 12, отличающийся тем, что растворяют по меньшей мере приблизительно 30 мас. % близкого LHRH пептидного соединения.
14. Способ по п. 12, отличающийся тем, что указанное близкое LHRH пептидное соединение выбрано из группы, состоящей из лейпролида, LHRH, нафарелина и госерелина.
15. Способ по п. 12, отличающийся тем, что он дополнительно включает добавление по меньшей мере одного компонента, который выбирают из группы, состоящей из буфера, наполнителя, растворителя, солюбилизатора и консерванта.
16. Способ по п. 12, отличающийся тем, что в качестве близкого LHRH соединения используют лейпролида ацетат, который растворяют в количестве приблизительно от 30 мас. % до приблизительно 50 мас. % в стерильной дистиллированной воде.
17. Способ по п. 12, отличающийся тем, что он дополнительно включает добавление по меньшей мере одного неводного полярного непротонного растворителя.
18. Способ по п. 17, отличающийся тем, что указанный неводный полярный непротонный растворитель представлен диметилсульфоксидом или диметилформамидом.
19. Способ лечения гормонзависимого заболевания у субъекта, включающий введение близкого LHRH пептидного соединения, отличающийся тем, что указанному субъекту вводят эффективное количество препарата по п. 1.
20. Способ по п. 19, отличающийся тем, что указанное введение осуществляют парентерально.
21. Способ по п. 19, отличающийся тем, что указанное введение осуществляют длительно непрерывно.
22. Способ по п. 20, отличающийся тем, что указанное введение осуществляют посредством имплантируемого устройства для доставки лекарственного вещества.
23. Способ по п. 19, отличающийся тем, что указанное гормонзависимое заболевание представлено раком простаты, причем в качестве близкого LHRH пептидного соединения используют лейпролид.
24. Способ по п. 19 или 23, отличающийся тем, что осуществляют ежедневное введение по меньшей мере приблизительно 80 мкг лейпролида.
25. Способ по п. 24, отличающийся тем, что указанное ежедневное введение осуществляют в течение периода, выбранного из группы, состоящей из 3, 6 и 12 месяцев.
26. Способ по п. 25, отличающийся тем, что указанное ежедневное введение осуществляют посредством устройства для доставки лекарственного вещества.
27. Способ по п. 19, отличающийся тем, что указанное гормонзависимое заболевание представлено раком простаты, причем в качестве близкого LHRH пептидного соединения используют антагонист LHRH.
РИСУНКИ
|
||||||||||||||||||||||||||
