Патент на изобретение №2200157
|
||||||||||||||||||||||||||
(54) ПИРИДИНКАРБОКСАМИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ
(57) Реферат: Изобретение относится к новым пиридинкарбоксамидинам формулы (I) 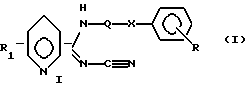 или их таутомерным формам, где присоединение к пиридину осуществляется в положении 2, 3 или 4; R1 обозначает водород; Q обозначает С1-С9-двухвалентный насыщенный углеводородный радикал; Х обозначает метилен или кислород; R обозначает водород, галоген, нитро, метилендиокси, алкил или алкокси, содержащие от 1 до 4 атомов углерода, или их фармацевтически приемлемым нетоксичным смолям и N-оксидам. Соединения формулы (I) ингибируют нежелательную пролиферацию клеток, например клеток кожи и раковых клеток, и могут найти применение в медицине. 3 с. и 3 з.п.ф-лы, 3 табл. Изобретение относится к новому классу соединений, проявляющему высокую активность в ингибировании нежелательной пролиферации клеток, например клеток кожи и раковых клеток, фармацевтическим препаратам, содержащим эти соединения, к единичным дозированным формам таких препаратов и их применению в лечении и профилактике заболеваний, характеризуемых аномальной дифференциацией и/или пролиферацией клеток, таких как, например, псориаз и рак. Соединения по данному изобретению представлены общей формулой I: 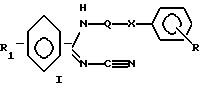 или их таутомерные формы, присоединение к пиридину осуществляется в положении 2, 3 или 4, в указанной формуле 1 обозначает один или более заместителей, которые могут быть одинаковыми или различными и которые выбирают из группы, включающей водород, галоген, амино, трифторметил, нитро, циано, карбокси или алкил, алкокси или алкоксикарбонил, с содержанием С от 1 до 4; Q обозначает С4-С9-двухвалентный углеводородный радикал, который может быть линейным, разветвленным, насыщенным или ненасыщенным; X обозначает метилен, кислород, серу или азот, a R обозначает водород или один или более заместителей, которые могут быть одинаковыми или различными и которые выбирают из группы, включающей гидрокси, амино, галоген, трифторметил, циано, нитро, карбокси, карбамоил, метилендиокси или алкил, алкокси, алкилтио, алкиламино или алкоксикарбонил, с содержанием С от 1 до 4. Если настоящие соединения содержат один или более асимметричных атомов углерода, эти соединения могут образовывать оптические изомеры или диастереоизомеры. Данное изобретение включает также такие изомеры и их смеси. Соединения могут быть использованы в форме их солей, образованных с фармацевтически приемлемыми неорганическими или органическими кислотами, такими как хлористоводородная, бромистоводородная, йодистоводородная кислота, фосфорная кислота, серная кислота, азотная кислота, 4-толуолсульфокислота, метансульфокислота, муравьиная кислота, уксусная кислота, пропионовая кислота, лимонная кислота, винная кислота, янтарная кислота, бензойная кислота и малеиновая кислота. Даже если настоящие соединения хорошо абсорбируются после парентерального введения, в некоторых случаях может быть выгодно получать соответствующие биообратимые производные соединений по изобретению, т.е. получать так называемые пролекарства, предпочтительно производные, физико-химические свойства которых приводят к улучшенной растворимости при физиологическом значении рН и/или абсорбции и/или биологической доступности рассматриваемого соединения. Такими производными являются, например, пиридил-N-оксидные производные соединений по изобретению; такие соединения получают окислением атома азота пиридила с помощью пригодного окисляющего агента, например, 3-хлорпербензойной кислоты, в инертном растворителе, например дихлорметане. Могут также быть использованы другие пригодные способы улучшения физико-химических свойств и/или растворимости рассматриваемых соединений. N-алкил-N’-циано-N”-пиридилгуанидины, описанные в патенте Великобритании 1489879, являются сильными активаторами калиевых каналов с ярко выраженным действием в качестве предкапиллярных вазодилататоров, снижающих общее периферическое сопротивление сосудов у животных и человека и, таким образом, пригодных в качестве гипотензивных средств. Подобная биологическая активность описана для ряда близко родственных N-алкил-N’-циано-пиридин-карбоксамидинов (Nakajima, Т. et al., Chem. Pharm. Bull., 42, 2475-2490 (1994) и патент США 5223508). Как установлено в международном патенте PCT/DK 93/00291, поданном 13 сентября 1993, публикации WO 94/06770, введение арилоксисодержащих радикалов в алифатические группы из вышеуказанного патента Великобритании приводит к получению структур, имеющих более специфические фармакологические действия на выделенные ткани и клетки, при отсутствии воздействия или незначительном воздействии на 86Rb-отток из калиевых каналов, по сравнению с воздействием, оказываемым соединениями, защищенными в вышеуказанном патенте Великобритании. Соединения по данному изобретению ингибируют пролиферацию различных опухолевых клеточных линий в культурах при той же концентрации, что и самые лучшие соединения, известные из уровня техники (смотри таблицу 1). Однако соединения по данному изобретению значительно удлиняют время выживания несущих опухоли крыс по сравнению с соединениями, известными из уровня техники, что, таким образом, делает их потенциально полезными в противоопухолевой химиотерапии. Ингибирование пролиферации опухолевых клеток изучено с использованием различных типов человеческих раковых клеточных линий. Исследовали клеточные линии, такие как мелкоклеточная карцинома легкого (NYH) и карцинома молочной железы (MCF-7) с использованием следующей основной методики. Клетки выращивают in vitro в течение 24 часов в присутствии испытуемого соединения. ДНК-синтез оценивают путем включения [3Н]-тимидина и рассчитывают средние ингибирующие концентрации (IС50) соединений. Результаты показаны в таблице 1. Результаты показывают, что соединения по данному изобретению способны ингибировать пролиферацию опухолевых клеток in vitro при таких же или сопоставимых концентрациях с концентрациями соединений известного уровня техники (смотри таблицу 1). Пролонгирование времени выживания несущих опухоли крыс изучают на LEW/Mol-инбредных самках крыс, инокулированных клетками саркомы Yoshida’a в количестве 2  107 клеток. Несущим опухоли крысам (6 животных на группу) ежедневно перорально один раз в день вводили определенную дозу лекарства, начиная с 3 дня после перекоса опухолевых клеток и до момента гибели или до увеличения веса тела на 10% вследствие пролиферации опухоли. Для расчета ILS (увеличение длительности жизни) используют график зависимости среднего числа дней выживания крыс, получавших лекарство, от среднего числа дней выживания крыс, не получавших лекарство. ILS = ((среднее значение для получавших лекарство крыс / среднее значение для контроля) – 1) 107 клеток. Несущим опухоли крысам (6 животных на группу) ежедневно перорально один раз в день вводили определенную дозу лекарства, начиная с 3 дня после перекоса опухолевых клеток и до момента гибели или до увеличения веса тела на 10% вследствие пролиферации опухоли. Для расчета ILS (увеличение длительности жизни) используют график зависимости среднего числа дней выживания крыс, получавших лекарство, от среднего числа дней выживания крыс, не получавших лекарство. ILS = ((среднее значение для получавших лекарство крыс / среднее значение для контроля) – 1)  100%. Результаты приведены в таблице 2.
Эти результаты показывают, что соединения по изобретению способны продлевать время выживания крыс с опухолью саркомы Yoshida’a при более низких концентрациях и с более высоким ILS, чем соединение примера 18 PCT/DK 93/00291.
Соединения по изобретению хорошо переносимы и нетоксичны и имеют описанные полезные активности при отсутствии или при минимальном воздействии на общее кровяное давление. В основном они могут быть введены пероральным, внутривенным, внутрибрюшинным, интраназальным или трансдермальным способами.
Настоящее изобретение относится также к способам получения целевых соединений общей формулы I. Соединения формулы I обычно могут быть получены стандартными способами, подробно описанными в соответствующей области. Способы представлены на реакционной схеме 1.
Рассматриваемые соединения предназначены для применения в фармацевтических композициях, полезных для лечения вышеуказанных болезней.
Необходимое для терапевтического воздействия количество соединения формулы (I) (далее называемого активным ингредиентом) будет, конечно, меняться как в зависимости от конкретного соединения, способа введения, так и от нуждающегося в лечении млекопитающего. Пригодная доза соединения формулы (I) для системного лечения составляет от 0,1 до 400 мг на килограмм веса тела, особенно предпочтительна доза от 1,0 до 100 мг на килограмм веса тела, например 5-20 мг/кг; вводимая однократно или за большее число раз в день.
Суточная доза (для взрослых) может составлять от 1 мг до 10000 мг, предпочтительно, 70-5000 мг, а в ветеринарной практике соответственно суточные дозы составляют от 0,1 до 400 мг/кг веса тела.
Хотя можно вводить активный ингредиент как таковой в виде чистого химического соединения, предпочтительно вводить его в виде фармацевтической композиции. Удобно, чтобы активный ингредиент составлял от 0,1 до 90% от веса композиции. Обычно единичные дозированные формы композиции содержат от 0,5 мг до 1 г активного ингредиента. Для местного введения активный ингредиент предпочтительно составляет от 1 до 20% от веса композиции, но активный ингредиент может составлять около 50 вес.%. Композиции, пригодные для назального или трансбуккального введения, могут содержать от 0,1 до 20 вес.%, например около 2 вес.% активного ингредиента.
Термин “однократная доза” включает единичную дозу, которая может быть введена пациенту и которую легко обрабатывать и упаковывать, остающуюся как физически, так и химически стабильной единичной дозой и включающую либо активный материал как таковой, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Композиции по данному изобретению как для ветеринарного, так и медицинского применения включают активный ингредиент в сочетании с фармацевтически приемлемым носителем и, необязательно, другим терапевтическим ингредиентом (ингредиентами). Носитель (носители) должны быть приемлемы в том смысле, что должны быть совместимы с другими ингредиентами композиций и не оказывать вредного воздействия на реципиента.
Композиции включают носители в форме, пригодной для перорального, ректального, парентерального (включая подкожное, внутримышечное, внутривенное и внутрибрюшинное) введения.
Композиции могут быть удобно представлены в форме единичной дозированной формы и могут быть приготовлены любым способом, хорошо известным в области фармации. Все способы включают стадию введения активного ингредиента в сочетании с носителем, содержащим один или более вспомогательных ингредиентов. В основном композиции получают путем равномерного и однородного смешивания активного ингредиента с жидким носителем, или тонко измельченным твердым носителем, или с обоими, а затем при необходимости придают продукту форму желаемой композиции.
Пригодные для перорального введения композиции по данному изобретению могут быть в форме дискретных единиц, таких как капсулы, пастилки, таблетки или лепешки, каждая из которых содержит заранее рассчитанное количество активного ингредиента; в форме порошка или гранул; в форме раствора или суспензии в водной или неводной жидкости; или в форме эмульсии типа масло-в-воде или вода-в-масле. Активный ингредиент может также быть введен в форме болюса, электуария или пасты.
Композиции для ректального введения могут быть в форме суппозитория, включающего активный ингредиент и носитель, такой как масло какао, или в форме клизмы.
Пригодные для парентерального введения композиции обычно включают препарат в стерильном масле или водный препарат активного ингредиента, который предпочтительно изотоничен с кровью реципиента.
В дополнение к вышеуказанным ингредиентам композиции по изобретению могут включать один или более ингредиентов, таких как разбавители, буферы, корригенты, связывающие вещества, поверхностно-активные вещества, загустители, смазывающие вещества, консерванты, например метилгидроксибензоат, (включая антиоксиданты), эмульгирующие вещества и тому подобные.
Кроме того, композиции могут дополнительно содержать другие терапевтически активные соединения, обычно используемые для лечения вышеуказанных патологических состояний, например противоопухолевые агенты, что может приводить к синергическим действиям на опухолевые клетки.
Далее изобретение дополнительно описано с помощью следующих общих методик и примеров.
Примеры соединений I перечислены в таблице 3.
Все температуры плавления не скорректированы. Для спектра 13С-ядерного магнитного резонанса (ЯМР) (300 МГц) все значения химических сдвигов ( 100%. Результаты приведены в таблице 2.
Эти результаты показывают, что соединения по изобретению способны продлевать время выживания крыс с опухолью саркомы Yoshida’a при более низких концентрациях и с более высоким ILS, чем соединение примера 18 PCT/DK 93/00291.
Соединения по изобретению хорошо переносимы и нетоксичны и имеют описанные полезные активности при отсутствии или при минимальном воздействии на общее кровяное давление. В основном они могут быть введены пероральным, внутривенным, внутрибрюшинным, интраназальным или трансдермальным способами.
Настоящее изобретение относится также к способам получения целевых соединений общей формулы I. Соединения формулы I обычно могут быть получены стандартными способами, подробно описанными в соответствующей области. Способы представлены на реакционной схеме 1.
Рассматриваемые соединения предназначены для применения в фармацевтических композициях, полезных для лечения вышеуказанных болезней.
Необходимое для терапевтического воздействия количество соединения формулы (I) (далее называемого активным ингредиентом) будет, конечно, меняться как в зависимости от конкретного соединения, способа введения, так и от нуждающегося в лечении млекопитающего. Пригодная доза соединения формулы (I) для системного лечения составляет от 0,1 до 400 мг на килограмм веса тела, особенно предпочтительна доза от 1,0 до 100 мг на килограмм веса тела, например 5-20 мг/кг; вводимая однократно или за большее число раз в день.
Суточная доза (для взрослых) может составлять от 1 мг до 10000 мг, предпочтительно, 70-5000 мг, а в ветеринарной практике соответственно суточные дозы составляют от 0,1 до 400 мг/кг веса тела.
Хотя можно вводить активный ингредиент как таковой в виде чистого химического соединения, предпочтительно вводить его в виде фармацевтической композиции. Удобно, чтобы активный ингредиент составлял от 0,1 до 90% от веса композиции. Обычно единичные дозированные формы композиции содержат от 0,5 мг до 1 г активного ингредиента. Для местного введения активный ингредиент предпочтительно составляет от 1 до 20% от веса композиции, но активный ингредиент может составлять около 50 вес.%. Композиции, пригодные для назального или трансбуккального введения, могут содержать от 0,1 до 20 вес.%, например около 2 вес.% активного ингредиента.
Термин “однократная доза” включает единичную дозу, которая может быть введена пациенту и которую легко обрабатывать и упаковывать, остающуюся как физически, так и химически стабильной единичной дозой и включающую либо активный материал как таковой, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Композиции по данному изобретению как для ветеринарного, так и медицинского применения включают активный ингредиент в сочетании с фармацевтически приемлемым носителем и, необязательно, другим терапевтическим ингредиентом (ингредиентами). Носитель (носители) должны быть приемлемы в том смысле, что должны быть совместимы с другими ингредиентами композиций и не оказывать вредного воздействия на реципиента.
Композиции включают носители в форме, пригодной для перорального, ректального, парентерального (включая подкожное, внутримышечное, внутривенное и внутрибрюшинное) введения.
Композиции могут быть удобно представлены в форме единичной дозированной формы и могут быть приготовлены любым способом, хорошо известным в области фармации. Все способы включают стадию введения активного ингредиента в сочетании с носителем, содержащим один или более вспомогательных ингредиентов. В основном композиции получают путем равномерного и однородного смешивания активного ингредиента с жидким носителем, или тонко измельченным твердым носителем, или с обоими, а затем при необходимости придают продукту форму желаемой композиции.
Пригодные для перорального введения композиции по данному изобретению могут быть в форме дискретных единиц, таких как капсулы, пастилки, таблетки или лепешки, каждая из которых содержит заранее рассчитанное количество активного ингредиента; в форме порошка или гранул; в форме раствора или суспензии в водной или неводной жидкости; или в форме эмульсии типа масло-в-воде или вода-в-масле. Активный ингредиент может также быть введен в форме болюса, электуария или пасты.
Композиции для ректального введения могут быть в форме суппозитория, включающего активный ингредиент и носитель, такой как масло какао, или в форме клизмы.
Пригодные для парентерального введения композиции обычно включают препарат в стерильном масле или водный препарат активного ингредиента, который предпочтительно изотоничен с кровью реципиента.
В дополнение к вышеуказанным ингредиентам композиции по изобретению могут включать один или более ингредиентов, таких как разбавители, буферы, корригенты, связывающие вещества, поверхностно-активные вещества, загустители, смазывающие вещества, консерванты, например метилгидроксибензоат, (включая антиоксиданты), эмульгирующие вещества и тому подобные.
Кроме того, композиции могут дополнительно содержать другие терапевтически активные соединения, обычно используемые для лечения вышеуказанных патологических состояний, например противоопухолевые агенты, что может приводить к синергическим действиям на опухолевые клетки.
Далее изобретение дополнительно описано с помощью следующих общих методик и примеров.
Примеры соединений I перечислены в таблице 3.
Все температуры плавления не скорректированы. Для спектра 13С-ядерного магнитного резонанса (ЯМР) (300 МГц) все значения химических сдвигов ( ), если не указано особо, приведены для растворов в дейтерированном хлороформе (CDCl3) и гексадейтеродиметилсульфоксиде (ДМСО-d6) относительно тетраметилсилана ( ), если не указано особо, приведены для растворов в дейтерированном хлороформе (CDCl3) и гексадейтеродиметилсульфоксиде (ДМСО-d6) относительно тетраметилсилана ( 0,00) или хлороформа ( 0,00) или хлороформа ( 76,81 (13С-ЯМР)). Хроматографию осуществляют на силикагеле.
Общая методика 1: Сочетание соединений общей формулы II с соединениями общей формулы IIIa, IIIb, IIIc с образованием соединений общей формулы I 76,81 (13С-ЯМР)). Хроматографию осуществляют на силикагеле.
Общая методика 1: Сочетание соединений общей формулы II с соединениями общей формулы IIIa, IIIb, IIIc с образованием соединений общей формулы IСоединение общей формулы IIIa, IIIb или IIIc (5 ммоль) растворяют в метаноле (10 мл) и добавляют соединение общей формулы II (10 ммоль) в метаноле (10 мл). Реакционную смесь перемешивают при комнатной температуре обычно в течение 18 часов. Реакционную смесь упаривают в вакууме, получая сырой продукт. Сырой продукт дополнительно очищают, например, кристаллизацией или флэш-хроматографией, получая указанное в заглавии соединение. ПРИМЕР 1 N2-циано-N1-(6-(4-хлорфенокси)гексил)-3-пиридинкарбоксамидин (соединение 101) Общая методика 1. Исходное соединение II: 6-(4-хлорфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридин-карбоксиимидат. Очистка: хроматография с применением метанола/дихлорметана 1:20 в качестве элюента с последующим растиранием в диэтиловом эфире. Т.пл.: сублимируется при 69oС. 13С-ЯМР (CDCl3):  168,0, 157,6, 152,5, 147,5, 135,3, 129,3, 128,7, 125,4, 123,6, 117,1, 115,8, 68,0, 42,9, 29,0, 28,3, 26,6, 25,7.
ПРИМЕР 2 168,0, 157,6, 152,5, 147,5, 135,3, 129,3, 128,7, 125,4, 123,6, 117,1, 115,8, 68,0, 42,9, 29,0, 28,3, 26,6, 25,7.
ПРИМЕР 2N2-циано-N1-(6-(2-метоксифенокси)гексил)-3-пиридинкарбоксамидин (соединение 102) Общая методика 1. Исходное соединение II: 6-(2-метоксифенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридин-карбоксиимидат. Очистка: хроматография с применением метанола/дихлорметана 1:20 в качестве элюента с последующим растиранием в диэтиловом эфире. Т.пл.: 87-88oС. 13С-ЯМР (СDСl3):  167,9, 152,4, 149,3, 148,4, 147,6, 135,2, 128,7, 123,5, 121,1, 121,0, 117,2, 113,3, 112,0, 68,8, 55,9, 42,8, 28,9, 28,1, 26,5, 25,6.
ПРИМЕР 3 167,9, 152,4, 149,3, 148,4, 147,6, 135,2, 128,7, 123,5, 121,1, 121,0, 117,2, 113,3, 112,0, 68,8, 55,9, 42,8, 28,9, 28,1, 26,5, 25,6.
ПРИМЕР 3N2-цианo-N1-(6-(3,4-метилендиоксифенокси)гексил)-3-пиридинкарбоксамидин (соединение 103) Общая методика 1. Исходное соединение II: 6-(3,4-метилендиоксифенокси)-гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридин-карбоксиимидат. Очистка: хроматография с применением метанола/дихлорметана 1:20 в качестве элюента с последующей кристаллизацией из метанола. Т.пл.: 130-131oС. 13С-ЯМР (ДМСО-d6):  167,7, 154,0, 151,9, 147,8, 147,7, 140,9, 135,4, 128,6, 123,4, 117,3, 107,9, 105,5, 100,8, 97,6, 68,0, 41,9, 28,5, 27,5, 26,0, 25,1, 167,7, 154,0, 151,9, 147,8, 147,7, 140,9, 135,4, 128,6, 123,4, 117,3, 107,9, 105,5, 100,8, 97,6, 68,0, 41,9, 28,5, 27,5, 26,0, 25,1,ПРИМЕР 4 N2-циaнo-N1-(6-(2,4,6-трихлорфенокси)гексил)-3-пиридинкарбоксамидин (соединение 104) Общая методика 1. Исходное соединение II: 6-(2,4,6-трихлорфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением этилацетата в качестве элюента с последующей кристаллизацией из хлороформа/диэтилового эфира. 13С-ЯМР (ДМСО-d6):  167,7, 152,0, 150,2, 147,7, 135,5, 129,3, 128,8, 128,6, 123,4, 117,3, 73,5, 41,9, 29,3, 27,5, 26,0, 24,9.
ПРИМЕР 5 167,7, 152,0, 150,2, 147,7, 135,5, 129,3, 128,8, 128,6, 123,4, 117,3, 73,5, 41,9, 29,3, 27,5, 26,0, 24,9.
ПРИМЕР 5N2-циано-N1-(6-(4-фторфенокси)гексил)-3-пиридинкарбоксамидин (соединение 105) Общая методика. 1. Исходное соединение II: 6-(4-фторфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением дихлорметана/метанола/аммиака (водн.) 95:5:1 в качестве элюента. Т.пл.: 99-101oС. 13С-ЯМР (ДМСО-d6):  167,8, 157,9, 154,9, 154,7, 153,2, 152,3, 152,0, 147,8, 135,5, 128,6, 123,4, 117,3, 115,8, 115,6, 115,5, 115,5, 67,8, 41,9, 28,5, 27,5, 26,0, 25,1.
ПРИМЕР 6 167,8, 157,9, 154,9, 154,7, 153,2, 152,3, 152,0, 147,8, 135,5, 128,6, 123,4, 117,3, 115,8, 115,6, 115,5, 115,5, 67,8, 41,9, 28,5, 27,5, 26,0, 25,1.
ПРИМЕР 6N2-циано-N1-(6-(3,5-диметоксифенокси)гексил)-3-пиридинкарбoксамидин (соединение 106) Общая методика 1. Исходное соединение II: 6-(3,5-диметоксифенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридин-карбоксиимидат. Очистка: хроматография с применением дихлорметана/ метанола/аммиака (водн.) 95:5:1 в качестве элюента. 13С-ЯМР (ДМСО-d6):  167,7, 161,1, 160,5, 152,0, 147,7, 135,4, 128,6, 123,4, 117,3, 93,1, 92,7, 67,3, 55,0, 41,9, 28,5, 27,5, 26,0, 25,1.
ПРИМЕР 7 167,7, 161,1, 160,5, 152,0, 147,7, 135,4, 128,6, 123,4, 117,3, 93,1, 92,7, 67,3, 55,0, 41,9, 28,5, 27,5, 26,0, 25,1.
ПРИМЕР 7N2-циано-N1-(6-(3-хлорфенокси)гексил)-3-пиридинкарбоксамидин (соединение 107) Общая методика 1. Исходное соединение II: 6-(3-хлорфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением дихлорметана/ метанола/аммиака (водн. ) 95: 5: 1 в качестве элюента с последующим растиранием в диэтиловом эфире. Т.пл.: 77-79oС. 13С-ЯМР (ДМСО-d6):  167,7, 159,6, 152,0, 147,8, 135,5, 133,7, 130,7, 128,6, 123,4, 120,2, 117,3, 114,3, 113,5, 67,7, 41,9, 28,3, 27,5, 26,0, 25,1.
ПРИМЕР 8 167,7, 159,6, 152,0, 147,8, 135,5, 133,7, 130,7, 128,6, 123,4, 120,2, 117,3, 114,3, 113,5, 67,7, 41,9, 28,3, 27,5, 26,0, 25,1.
ПРИМЕР 8N2-циано-N1-(6-(2-нитрофенокси)гексил)-3-пиридинкарбоксамидин (соединение 108) Общая методика 1. Исходное соединение II: 6-(2-нитрофенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением дихлорметана/метанола/аммиака (водн. ) 95: 5: 1 в качестве элюента с последующим растиранием в диэтиловом эфире. Т.пл.: 103-106oС. 13С-ЯМР (ДМСО-d6):  167,9, 152,1, 151,3, 147,9, 139,7, 135,6, 134,4, 128,8, 124,9, 123,5, 120,4, 117,4, 115,1, 69,1, 42,1, 28,3, 27,7, 26,0, 25,0.
ПРИМЕР 9 167,9, 152,1, 151,3, 147,9, 139,7, 135,6, 134,4, 128,8, 124,9, 123,5, 120,4, 117,4, 115,1, 69,1, 42,1, 28,3, 27,7, 26,0, 25,0.
ПРИМЕР 9N2-циано-N1-(6-(2-хлорфенокси)гексил)-3-пиридинкарбоксамидин (соединение 109) Общая методика 1. Исходное соединение II: 6-(2-хлорфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением дихлорметана/ метанола/аммиака (водн. ) 95: 5: 1 в качестве элюента с последующим растиранием в хлороформе/диэтиловом эфире 1:4. Т.пл.: 108-109oС. 13С-ЯМР (ДМСО-d6):  167,9, 154,0, 152,1, 147,9, 135,6, 129,9, 128,7, 128,3, 123,5, 121,4, 121,3, 117,4, 113,9, 68,4, 42,0, 28,4, 27,7, 26,1, 25,2.
ПРИМЕР 10 167,9, 154,0, 152,1, 147,9, 135,6, 129,9, 128,7, 128,3, 123,5, 121,4, 121,3, 117,4, 113,9, 68,4, 42,0, 28,4, 27,7, 26,1, 25,2.
ПРИМЕР 10N2-циано-N1-(6-(2,3-дихлорфенокси)гексил)-3-пиридинкарбоксамидин (соединение 110) Общая методика 1. Исходное соединение II: 6-(2,3-дихлорфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: кристаллизация из метанола. Т.пл.: 141-142oС. 13С-ЯМР (ДМСО-d6):  167,7, 155,5, 152,0, 147,8, 135,5, 132,2, 128,6, 128,4, 123,4, 121,8, 120,0, 117,3, 112,2, 69,0, 41,9, 28,3, 27,5, 25,9, 25,0.
ПРИМЕР 11 167,7, 155,5, 152,0, 147,8, 135,5, 132,2, 128,6, 128,4, 123,4, 121,8, 120,0, 117,3, 112,2, 69,0, 41,9, 28,3, 27,5, 25,9, 25,0.
ПРИМЕР 11N2-циано-N1-(6-(4-хлор-3-метилфенокси(гексил)-3-пиридинкарбоксамидин (соединение 111) Общая методика 1. Исходное соединение II: 6-(4-хлор-3-метилфенокси)гексиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением дихлорметана/ метанола/аммиака (водн. ) 95: 5: 1 в качестве элюента с последующим растиранием в диэтиловом эфире. Т.пл.: 91-92oС. 13С-ЯМР (CDCI3):  167,9, 157,5, 152,4, 147,6, 136,9, 135,2, 129,5, 128,6, 125,6, 123,5, 117,2, 117,0, 113,0, 67,9, 42,8, 29,1, 28,3, 26,6, 25,7, 20,3.
ПРИМЕР 12 167,9, 157,5, 152,4, 147,6, 136,9, 135,2, 129,5, 128,6, 125,6, 123,5, 117,2, 117,0, 113,0, 67,9, 42,8, 29,1, 28,3, 26,6, 25,7, 20,3.
ПРИМЕР 12N2-циaнo-Nl-(9-фенилнонил)-3-пиридинкарбоксамидин (соединение 112) Общая методика 1. Исходное соединение II: 9-фенилнониламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридин-карбоксиимидат. Очистка: хроматография с применением дихлорметана/ метанола/аммиака (водн.) 90:10:1 в качестве элюента с последующим растиранием в пентане. Т.пл.: 54-57oС. 13С-ЯМР (СDСl3):  167,9, 152,5, 147,5, 142,8, 135,3, 128,7, 128,4, 128,2, 125,6, 123,5, 117,1, 43,0, 36,0, 31,5, 29,4, 29,3, 29,2, 28,4, 26,9.
ПРИМЕР 13 167,9, 152,5, 147,5, 142,8, 135,3, 128,7, 128,4, 128,2, 125,6, 123,5, 117,1, 43,0, 36,0, 31,5, 29,4, 29,3, 29,2, 28,4, 26,9.
ПРИМЕР 13N2-циано-N1-(4-феноксибутил)-3-пиридинкарбоксамидин (соединение 113) Общая методика 1. Исходное соединение II: 4-феноксибутиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением дихлорметана/ метанола/аммиака (водн.) 90:10:1 в качестве элюента. 13С-ЯМР (CDCl3):  168,0, 158,6, 152,5, 147,6, 135,2, 129,6, 128,7, 123,5, 121,0, 117,2, 114,5, 67,2, 42,6, 26,6, 25,3.
ПРИМЕР 14 168,0, 158,6, 152,5, 147,6, 135,2, 129,6, 128,7, 123,5, 121,0, 117,2, 114,5, 67,2, 42,6, 26,6, 25,3.
ПРИМЕР 14N2-циано-N1-(7-(4-хлорфенокси)гептил)-3-пиридинкарбоксамидин (соединение 114) Общая методика 1. Исходное соединение II: 7-(4-хлорфенокси)гептиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением метанола/дихлорметана 1:20 в качестве элюента. 13С-ЯМР (ДMCO-d6):  167,7, 157,4, 152,0, 147,7, 135,4, 129,1, 128,6, 123,9, 123,4, 117,3, 116,1, 67,7, 42,0, 28,4, 28,3, 27,5, 26,2, 25,3.
ПРИМЕР 15 167,7, 157,4, 152,0, 147,7, 135,4, 129,1, 128,6, 123,9, 123,4, 117,3, 116,1, 67,7, 42,0, 28,4, 28,3, 27,5, 26,2, 25,3.
ПРИМЕР 15N2-циано-N1-(5-(4-хлорфенокси)пентил)-3-пиридинкарбоксамидин (соединение 115) Общая методика 1. Исходное соединение II: 5-(4-хлорфенокси)пентиламин. Исходное соединение IIIb: изопропил-N-циано-3-пиридинкарбоксиимидат. Очистка: хроматография с применением метанола/дихлорметана 1:20 в качестве элюента. 13С-ЯМР (ДМСО-d6):  167,8, 157,4, 152,0, 147,7, 135,4, 129,1, 128,6, 124,0, 123,4, 117,3, 116,1, 67,6, 41,8, 28,1, 27,3, 22,8.
ПРИМЕР 16 167,8, 157,4, 152,0, 147,7, 135,4, 129,1, 128,6, 124,0, 123,4, 117,3, 116,1, 67,6, 41,8, 28,1, 27,3, 22,8.
ПРИМЕР 16N2-цианo-N1-(6-(4-хлорфенокси)гексил)-2-пиридинкарбоксамидин (соединение 116) Общая методика 1. Исходное соединение II: 6-(4-хлорфенокси)гексиламин. Исходное соединение IIIa: метил-N-циано-2-пиридинкарбоксиимидат. Очистка: растирание в метаноле и диэтиловом эфире. Т.пл.: 80-81oС. 13С-ЯМР (CDCI3):  160,7, 157,7, 148,5, 147,3, 137,9, 129,3, 126,9, 125,4, 123,1, 116,8, 115,8, 68,0, 42,2, 29,3, 29,0, 26,5, 25,7.
ПРИМЕР 17 160,7, 157,7, 148,5, 147,3, 137,9, 129,3, 126,9, 125,4, 123,1, 116,8, 115,8, 68,0, 42,2, 29,3, 29,0, 26,5, 25,7.
ПРИМЕР 17N2-циано-N1-(6-(4-хлорфенокси)гексил)-4-пиридинкарбоксамидин (соединение 117) Общая методика 1. Исходное соединение II: 6-(4-хлорфенокси)гексиламин. Исходное соединение IIIc: изопропил-N-циано-4-пиридинкарбоксиимидат. Очистка: растирание в метаноле и диэтиловом эфире. Т.пл.: 117-118oС. 13С-ЯМР (ДМСО-d6):  168,0, 157,5, 150,2, 139,6, 129,1, 124,0, 121,6, 116,9, 116,1, 67,7, 41,8, 28,4, 27,5, 26,0, 25,1.
ПРИМЕР 18 168,0, 157,5, 150,2, 139,6, 129,1, 124,0, 121,6, 116,9, 116,1, 67,7, 41,8, 28,4, 27,5, 26,0, 25,1.
ПРИМЕР 18Капсулы 1 капсула содержит, мг: N2-Циано-N1-(6-(4-хлорфенокси)гексил)-3- пиридинкарбоксамидин (активное соединение) – 100 Полиэтиленгликоль – 962 Желатиновая капсула 00 желатин – 122 ПРИМЕР 19 Таблетка Промышленное получение 10000 таблеток, КГ I N2-Циано-N1-(6-(4-хлорфенокси)гексил)-3- пиpидинкapбoкcaмидин (активное соединение) – 10000 Натрий-кросскармеллоза – 0,300 II Гидроксипропилметилцеллюлоза с низкой вязкостью – 0,200 Сорбимакрогольолеат – 0,010 Очищенная вода – q.s. III Натрий-кроскармеллоза – 0,200 Коллоидная безводная двуокись кремния – 0,050 Стеарат магния – 0,050 I перемешивают до получения однородной массы в смесителе, обеспечивающем высокую степень измельчения, смачивают II и гранулируют с получением влажной массы. Влажные гранулы сушат в сушилке с псевдоожиженным слоем при температуре воздуха на входе 60oС до содержания воды в высушенном грануляте 0,3-0,4 (= в равновесии с воздухом 30-40% R.H. (относительной влажности)). Высушенный гранулят пропускают через сито с размером отверстий 850 мм. Далее пропущенный через сито гранулят смешивают с III в конусном смесителе. Готовый гранулят прессуют в таблетки массой 1071 мг и с достаточной твердостью. Формула изобретения
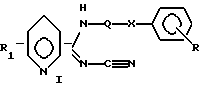 или их таутомерные формы, где присоединение к пиридину осуществляется в положении 2, 3 или 4, где R1 обозначает водород; Q обозначает С1-С9-двухвалентный насыщенный углеводородный радикал; Х обозначает метилен или кислород; R обозначает водород, галоген, нитро, метилендиокси, алкил или алкокси, содержащие от 1 до 4 атомов углерода, или их фармацевтически приемлемые нетоксичные соли и N-оксиды. 2. Соединение формулы I по п. 1, в котором присоединение к пиридину осуществляется в положении 3, где R1, Q, Х и R имеют определенные в п. 1 значения. 3. Соединение по п. 1, которое выбирают из группы включающей: N2-циано-N1-(6-(4-хлорфенокси)гексил)-3-пиридинкарбоксамидин; N2-циано-N1-(6-(2-метоксифенокси)гексил)-3-пиридинкарбоксамидин; N2-циaнo-Nl-(6-(3,4-метилендиоксифенокси)гексил)-3-пиридинкарбоксамидин N2-циaнo-Nl-(6-(2-нитрофенокси) гексил-3-пиридинкарбоксамидин, или их соли и чистые энантиомерные формы. 4. Фармацевтическая композиция, ингибирующая нежелательную пролиферацию клеток, содержащая соединение по любому из пп. 1-3 вместе с необходимыми вспомогательными агентами. 5. Способ получения соединения формулы I по п. 1, включающий взаимодействие соединения общей формулы IIIa, IIIb или IIIс: 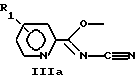 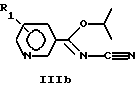 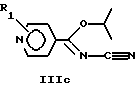 с соединением общей формулы II 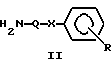 где R1 и R имеют указанные в п. 1 значения, в метаноле или другом подходящем растворителе при комнатной или повышенной температуре. 6. Соединение по п. 1, ингибирующее нежелательную пролиферацию клеток. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 16.05.2004
Извещение опубликовано: 10.05.2005 БИ: 13/2005
|
||||||||||||||||||||||||||
