Патент на изобретение №2197480
|
||||||||||||||||||||||||||
(54) СПОСОБ АЦИЛИРОВАНИЯ
(57) Реферат: Изобретение относится к способу получения 3-ацилированных индолов формулы I 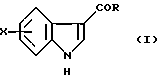 где R – С1-С6-алкил, С1-С6-алкокси, С3-С7-циклоалкил, арил, необязательно замещенный одним или более гидрокси-, С1-С4-алкилом, С1-С4-алкокси, фтором, фтор(С1-С4)-алкилом и фтор(С1-С4)-алкокси; Х – водород или один или более заместителей, независимо выбранных из CN, Г, NO2, С1-С6-алкила, С1-С6-алкокси, С3-С7-циклоалкила, арила, который необязательно замещен одним или более циано-, Г, NO2, С1-С4-алкилом, С1-С4-алкокси, фтор(С1-С4)алкилом и фтор(С1-С4)алкокси; или R – N-карбоксибензил-2-пирролидинил, а Х – 5-Br. Способ включает отдельное и одновременное добавление к перемешиваемому раствору индола формулы II 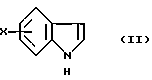 где Х определен ранее, (i) раствора, содержащего хлорангидрид кислоты RCOCl, где R определен ранее, и (ii) раствора, содержащего алкил- или арилмагнийгалогенид, таким образом, что а) растворы (i) и (ii) добавляют с достаточным разделением для предотвращения их взаимодействия друг с другом и b) растворы (i) и (ii) добавляют при эквивалентных скоростях молярного добавления. Способ предусматривает дальнейшее превращение соединения с N-карбоксибензил-2-пирролидинильной группы до соединения формулы III 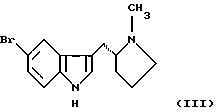 его превращения по реакции Хека в соединение IV 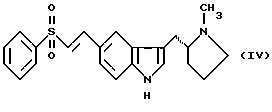 с последующим каталитическим гидрированием до соединения формулы V 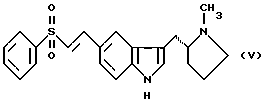 Полученное соединение V, известное как 5-НТ1, – агонист, используют при лечении мигрени. 10 з.п. ф-лы. Изобретение относится к ацилированию индолов, в частности, к получению 3-ацилированных индолов, которые могут быть подвергнуты дополнительной обработке с целью получения индолов, имеющих альтернативный заместитель в 3-положении. До настоящего времени 3-ацилирование индолов обычно осуществляли способом, описанным, например, в международной патентной заявке PCT/US91/07194, то есть путем взаимодействия магниевой соли индола с хлорангидридом кислоты 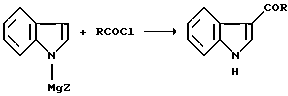 где Z является галогеном, и R представляет собой, например, замещенный пирролидинил, азетидинил или пиперидинил. Магниевую соль получают взаимодействием соответствующего индола с алкил- или арилмагнийгалогенидом, предпочтительно этилмагнийбромидом, в инертном растворителе, например диэтиловом эфире или тетрагидрофуране, при температуре в интервале от -30oС до 65oС, предпочтительно примерно 25oС. Хлорангидрид кислоты получают взаимодействием соответствующей кислоты, например, с оксалил или тионилхлоридом в инертном растворителе, например, хлористом метилене, диэтиловом эфире или тетрагидрофуране, при температуре в интервале от -10oС до 25oС. В кислотах с N-содержащим гетероциклическим фрагментом его можно защитить от полученного хлорангидрида кислоты путем N-замещения подходящей защитной группой, например карбоксибензильной (КБЗ). Затем раствор хлорангидрида кислоты медленно добавляют к перемешиваемому раствору магниевой соли при температуре в интервале от -30oС до 50oС, предпочтительно примерно 25oС, получая в результате целевой 3-ацилированный индол. Этот способ получения 3-ацилированных индолов, фактически требующий независимого получения каждого исходного вещества, является как время-, так и трудоемким и не годится для легкого применения в промышленном масштабе. Поэтому была разработана новая методология получения 3-ацилированных индолов, в которой отсутствует необходимость независимого получения вышеупомянутых исходных веществ. Согласно настоящему изобретению, 3-ацилированные индолы можно получать с хорошим выходом путем добавления растворов хлорангидрида кислоты (N-защищенной, при необходимости) и алкил- или арилмагнийгалогенида отдельно и одновременно к раствору индола при согласованных (синхронизированных) скоростях молярного добавления. Таким образом, задача, решаемая настоящим изобретением, состоит в обеспечении быстрого и эффективного по стоимости способа получения 3-ацилированных индолов, в котором избегают неудовлетворительного конвергентного синтеза предшествующего уровня техники, в частности, необходимости получать и выделять магниевую соль индола. В качестве дополнительной меры экономии стоимости в способе настоящего изобретения требуется только один молярный эквивалент дорогостоящего исходного вещества индола. Это противопоставляется двум эквивалентам, необходимым в способе предшествующего уровня техники, и эффективно удваивает выход ацилированного вещества, основанного на индольном исходном веществе. В соответствии с настоящим изобретением раскрывается способ получения 3-ацилированных индолов, включающий получение хлорангидрила кислоты, как описано, и затем добавление растворов (i) хлорангидрида кислоты и (ii) алкил- или арилмагнийгалогенида отдельно и одновременно к перемешиваемому раствору индола таким образом, чтобы (а) два потока входящих реагентов не вступали в непосредственный контакт, т.е. их добавляют отдельно на некотором расстоянии, чтобы предотвратить их взаимодействие друг с другом, а не с индолом, и (b) два реагента добавляют при “согласованных” скоростях молярного добавления. В частности, изобретение предлагает способ получения соединения формулы (I): 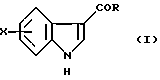 в которой R представляет C1-С6алкил, C1-С6алкокси, С3-С7циклоалкил или арил, необязательно замещенный одним или более гидрокси, С1-С4алкилом, С1-С4алкокси, фтором, фтор(С1-С4)алкилом и фтор(C1-C4)алкокси, и Х представляет собой водород или один или более заместителей, независимо выбранных из циано, галогена, нитро, С1-С6алкила, C1-С6алкокси, С3-С7циклоалкила и арила, необязательно замещенного одним или более циано, галогеном, нитро, С1-С4алкилом, С1-С4алкокси, фтор(С1-С4)алкилом и фтор(C1-C4)алкокси; включающий отдельное и одновременное добавление к перемешиваемому раствору индола формулы (II): 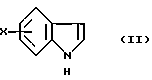 в которой Х имеет значения, определенные выше; (i) раствора, содержащего хлорангидрид кислоты формулы RCOC1, в которой R имеет значение, определенное ранее; и (ii) раствора, содержащего алкил- или арилмагнийгалогенид, таким образом, что (a) растворы (i) и (ii) добавляют с достаточным разделением для предотвращения их взаимодействия друг с другом; и (b) растворы (i) и (ii) добавляют при эквивалентных скоростях молярного добавления. Согласно особенно предпочтительным признакам изобретения, индол формулы (II) представляет собой индол как таковой, или 5-галогениндол, и галогенид магния является алкил- или арилмагнийбромидом, предпочтительно этилмагнийбромидом. Способ данного изобретения иллюстрируется следующими примерами. Пример 1 Получение 3-(N-КБЗ-2-пирродинилкарбокси)-5-броминдола В свежевысушенный реакционный сосуд, снабженный подвесной мешалкой и поддерживаемый в атмосфере азота, добавляют 5-броминдол (3,85 кг, 19,6 моль), затем хлористый метилен (12,3 л). Полученную смесь перемешивают при температуре окружающей среды до получения гомогенного раствора, после чего охлаждают до 10-12oС. Затем одновременно, в течение 2-3 часов с противоположных сторон сосуда добавляют растворы КБЗ-пролиноилхлорида в хлористом метилене (20 моль, 1,02 экв. ) и 1М этилмагнийбромида в МТВЕ (метилтретбутиловом эфире) (37,7 кг, 39,2 моль, 2 экв.), поддерживая при этом температуру 10-15oС. Эти добавления должны осуществляться таким образом, чтобы два потока не смешивались и чтобы скорости молярного добавления каждого реагента были постоянно синхронизированы. Полученную суспензию добавляют к энергично перемешиваемой смеси концентрированной НС1 (3 л), деминерализованной воды (28 л) и ТГФ (тетрагидрофурана) (29 л) в течение 30 минут, поддерживая температуру ниже 25oС. Полученную двухфазную смесь перемешивают 30 минут, оставляют отстаиваться в течение 20 минут, затем фазы разделяют, сохраняя верхний органический слой. Этот органический слой промывают насыщенным водным раствором NаНСО3 (28 л) в течение 20 минут при 20-25oС, оставляют отстаиваться в течение 20 минут, затем фазы разделяют, сохраняя верхний органический слой. После этого растворители удаляют при пониженном давлении, поддерживая температуру ниже 50oС; кристаллизация наблюдалась во время поздних стадий. К полученной суспензии добавляют этилацетат (15,5 л) и гексан (15,5 л), охлаждают полученную смесь до 0oС и гранулируют при этой температуре в течение 1 часа. После этого продукт выделяют фильтрованием, промывают смесью 1:1 гексан: этилацетат (10 л), затем сушат в течение ночи в вакууме при 35oС, получая 6,85 кг (82%) (R)-3-(N-карбоксибензоил-2-пирролидинилкарбокси)-5-бром-1Н-индол в виде тонких белых кристаллов. Вычислено,%: С 59,03%, Н 4,48%, N 6,56% Найдено,%: С 59,01%, Н 4,50%, N 6,58% Пример 2 Получение 3-(N-КБЗ-2-пирролидинилкарбокси)индола К раствору 25 ммоль индола в хлористом метилене (25 мл) одновременно добавляют в течение 1 часа раствор КБЗ-пролиноилхлорида (25 ммоль) в 25 мл МТВЕ и 50 мл 1М раствора этилмагнийбромида в МТВЕ. Два потока добавляют с противоположных сторон сосуда при эффективном перемешивании и при поддерживании температуры при 10-15oС. По завершении добавления реакцию гасят добавлением 1,0 М водным НС1 (50 мл). После перемешивания, отстаивания и разделения фаз органическую фазу промывают соляным раствором (50 мл) и затем уменьшают в объеме на 75%, вызывая кристаллизацию продукта. Продукт отфильтровывают, промывают этилацетатом (~10 мл) и сушат в вакууме при 45oС. Выход 81%. Пример 3 Получение 3-бензоил-5-броминдола 3-Бензоил-5-броминдол получают с 94% выходом, используя методику, описанную в примере 2. Пример 4 Получение 3-бензоилиндола 3-Бензоилиндол получают с 91% выходом, используя методику, описанную в примере 2. Специалисту будет понятно, что 3-ацилированные индолы, полученные в соответствии со способом изобретения, можно дополнительно обрабатывать для получения индолов, имеющих в 3-положении альтернативный заместитель. Таким образом, особым вариантом изобретения является случай, когда R= N-КБЗ-2-пирролидинил, и Х=бром, полученный таким образом 3-(N-КБЗ-2-пирролидинилкарбокси)-5-броминдол формулы (I) 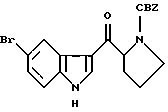 можно затем восстановить с использованием, например, литийалюмогидрида в тетрагидрофуране, получая 3-(N-метил-2(R)-пирролидинилметил)-5-броминдол (III) 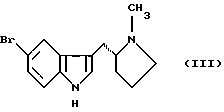 который, в свою очередь, можно превратить, используя подходящую реакцию Хека (Heck) в 3-(N-метил-2(R)-пирролидинилметил)-5-(2-фенилсульфонилэтенил)-lH-индол (IV) 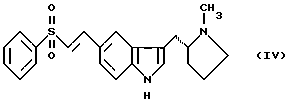 который, в свою очередь, можно подвергнуть каталитическому гидрированию, получая 3-(N-метил-2(R)-пирролидинилметил)-5-(2-фенилсульфонилэтил)-lH-индол (V) 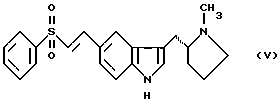 соединение, которое является известным как 5-HT1 агонистом, используемым при лечении мигрени. Формула изобретения
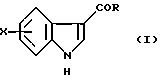 в которой R – C1-6 алкил, C1-6 алкокси, С3-7циклоалкил или арил, необязательно замещенный одним или более гидрокси-, С1-4 алкилом, С1-4 алкокси, фтором, фтор(С1-4)алкилом и фтор(С1-4)алкокси; Х – водород или один или более заместителей, независимо выбранных из циано, галогена, нитро, C1-6 алкила, C1-6 алкокси, С3-7 циклоалкила и арила, необязательно замещенного одним или более циано, галогеном, нитро, С1-4 алкилом, С1-4 алкокси, фтор(С1-4)алкилом и фтор(С1-4)алкокси; или R – N-карбоксибензил-2-пирролидинил и Х – 5-бром, включающий отдельное и одновременное добавление к перемешиваемому раствору индола формулы (II) 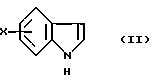 в которой Х имеет значение, определенное ранее, (i) раствора, содержащего хлорангидрид кислоты формулы RCOCl, в которой R имеет значение определенное ранее, и (ii) раствора, содержащего алкил- или арилмагнийгалогенид, таким образом, что (a) растворы (i) и (ii) добавляют с достаточным разделением для предотвращения их взаимодействия друг с другом (b) растворы (i) и (ii) добавляют при эквивалентных скоростях молярного добавления. 2. Способ по п. 1, в котором индол формулы (II) представляет собой индол как таковой или 5-галогениндол. 3. Способ по п. 1 или 2, в котором галогенид магния является алкил- или арилмагнийбромидом. 4. Способ по любому из пп. 1-3, в котором галогенид магния является этилмагнийбромидом. 5. Способ по любому из пп. 1-4, в котором полученное таким образом соединение формулы (I) представляет собой 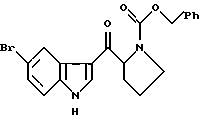 6. Способ по п. 5, в котором полученное таким образом соединение затем восстанавливают с получением соединения формулы (III) 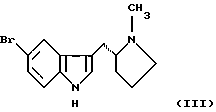 7. Способ по п. 6, в котором указанное восстановление осуществляют с использованием литийалюмогидрида в тетрагидрофуране. 8. Способ по пп. 6 и 7, в котором полученное таким образом соединение формулы (III) затем превращают в соединение формулы (IV) 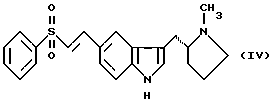 9. Способ по п. 8, в котором указанное превращение осуществляют с использование подходящей реакции Хека. 10. Способ по пп. 8 и 9, в котором полученное таким образом соединение формулы (IV) затем превращают в соединение формулы (V) 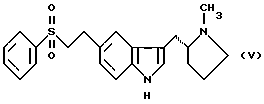 11. Способ по п. 10, в котором указанное превращение осуществляют путем каталитического гидрирования. MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 30.09.2009
Извещение опубликовано: 20.09.2010 БИ: 26/2010
|
||||||||||||||||||||||||||
