Патент на изобретение №2196136
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 6-АРИЛ-5-АРИЛАЗО-3,4-ДИГИДРО-3,4-ПИРИДАЗИНДИОНОВ
(57) Реферат: Изобретение относится к способу получения 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионов общей формулы I, где Аr1 обозначает фенил или п-хлорфенил, Аr2 обозначает фенил. В соответствии с изобретением указанные соединения получают путем взаимодействия 1-арил-3-ароил-4,5-дигидро-4,5-пиразолдионов формулы II, где Аr1 и Аr2 имеют вышеуказанные обозначения, с арилсульфонилгидразинами при комнатной температуре с последующим выделением целевых продуктов обычными методами. Технический результат – получение 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионов, которые являются потенциально биологически активными веществами. 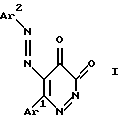 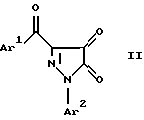
Изобретение относится к области органической химии, а именно к способу получения неописанных ранее 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионов, которые могут найти применение в качестве исходных веществ для синтеза конденсированных систем с пиридазиновым циклом и как потенциально биологически активного вещества. Этот способ-аналог взят нами за прототип (см. схему синтеза 1). Реакция проводится при кипячении исходных веществ в ледяной уксусной кислоте в течение 2 ч. Однако данный способ-прототип не позволяет ввести в положение 5 пиридазиндионового цикла арилазогруппу вследствие отсутствия в доступных заявителю источниках соответствующих производных фурандиона, а также не позволяет получить производные пиридазиндиона, не содержащие заместителей в 1 и 2 положениях. Задачей создания изобретения является разработка способа получения 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионов. Указанная задача достигается взаимодействием 1-арил-3-ароил-4,5-дигидро-4,5-пиридазиндионов с арилсульфонилгидразинами при комнатной температуре. Реакция идет по схеме 2. Изменение условий проведения реакции – повышение температуры реакционной массы – приводит к осмолению последней и понижает выход целевого продукта. Примеры осуществления заявляемого способа Пример 1. 6-Фенил-5-фенилазо-3,4-дигидро-3,4-пиридазиндион. К раствору 0,56 г (0,002 моль) 3-бензоил-1-фенил-4,5-дигидро-4,5-пиразолдиона в 15 мл абсолютного диоксана добавляют раствор 0,37 г (0,002 моль) п-тозилгидразина в 5 мл абсолютного диоксана, перемешивают в течение 0,5 ч при 25oС, диоксан испаряют, остаток перекристаллизовывают из этанола. Выход 0,50 г (86%). Т. пл. 136-137oС (этанол). Найдено, %: С 66,43; Н 3,60; N 19,48. C16H10N402. Вычислено, %: С 66,20; Н 3,47; N 19,30. В ИК спектре полученного соединения, снятом в вазелиновом масле, наблюдаются полосы валентных колебаний кетонной и амидной карбонильных групп гетероцикла в области 1695 и 1685 см-1 и связи N=N и C=N в области 1640 см-1. В спектре ПМР, снятом в ДМСО-d6, наблюдается только мультиплет ароматических протонов с центром при 7,81 м.д. В масс-спектре присутствует пик молекулярного иона с m/z 290 и интенсивностью 18%. Пример 2. 6-Фенил-5-фенилазо-3,4-дигидро-3,4-пиридазиндион. К раствору 0,28 г (0,001 моль) 3-бензоил-1-фенил-4,5-дигидро-4,5-пиразолдиона в 15 мл абсолютного диоксана добавляют раствор 0,21 г (0,001 моль) п-хлорфенилсульфонилгидразина в 5 мл абсолютного диоксана. Далее реакцию проводят, как описано в примере 1. Выход 0,26 г (89%). Вещество, полученное в данном примере с использованием п-хлорфенилсульфонилгидразина, идентично веществу, полученному в примере 1 с использованием п-тозилгидразина. Пример 3. 6-(п-Хлорфенил)- 5-фенилазо-3,4-дигидро-3,4-пиридазиндион. К раствору 0,62 г (0,002 моль) 3-п-хлорбензоил-1-фенил-4,5-дигидро-4,5-пиразолдиона в 15 мл абсолютного диоксана добавляют раствор 0,37 г (0,002 моль) п-тозилгидразина в 5 мл абсолютного диоксана, перемешивают в течение 0,5 часа при комнатной температуре, растворитель испаряют, остаток перекристаллизовывают из этанола. Выход 0,34 г (52%). Т.пл. 138-139oС (этанол). Найдено, %: С 59,71; Н 3,01; С1 10,67; N 17,13. С16H9ClN4O2. Вычислено, %: С 58,18; Н 2,79; С1 10,92; N 17,25. В ИК спектре соединения (вазелиновое масло) наблюдаются полосы валентных колебаний кетонной и амидной карбонильной групп гетероцикла в области 1690 см-1 и связи N=N и C=N в области 1640 см-1. В спектре ПМР, снятом в ДМСО-d6, присутствует группа сигналов бензольных колец с центром при 7,50 м.д. В масс-спектре наблюдаются пики молекулярного иона с m/z 324 и 326 (относительная интенсивность 12 и 4%, что отвечает изотопному соотношению атомов хлора). Пример 4. 6-Фенил-5-фенилазо-3,4-дигидро-3,4-пиридазиндион. К раствору 0,28 г (0,001 моль) 3-бензоил-1-фенил-4,5-дигидро-4,5-пиразолдиона в 15 мл абсолютного диоксана добавляют раствор 0,21 г (0,001 моль) п-хлорфенилсульфонилгидразина в 5 мл абсолютного диоксана, перемешивают в течение 0,5 ч при 50oС, растворитель испаряют, остаток перекристаллизовывают из этанола. Получают 0,17 г (58%) соединения. В патентной и технической литературе не были выявлены способы получения 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионов, имеющие сходные признаки с заявляемым способом, а именно не использовались аналогичные исходные вещества, на основании чего можно сделать вывод о соответствии технического решения критериям “новизна” и “изобретательский уровень”. Предлагаемый способ прост в осуществлении, одностадиен, позволяет получить неописанные ранее 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионы. Формула изобретения
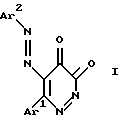 где Аr1 обозначает фенил или п-хлорфенил; Аr2 обозначает фенил, отличающийся тем, что 1-арил-3-ароил-4,5-дигидро-4,5-пиразолдионы формулы II 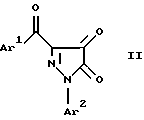 где Аr1 и Аr2 имеют вышеуказанные обозначения, подвергают взаимодействию с арилсульфонилгидразинами при комнатной температуре с последующим выделением целевых продуктов обычными методами. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 13.10.2002
Номер и год публикации бюллетеня: 18-2004
Извещение опубликовано: 27.06.2004
|
||||||||||||||||||||||||||
