Патент на изобретение №2195445
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ЦИС-1-{2-[4-(6-МЕТОКСИ-2-ФЕНИЛ-1,2,3,4-ТЕТРАГИДРОНАФТАЛИН-1-ИЛ)ФЕНОКСИ]ЭТИ Л}ПИРРОЛИДИНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ
(57) Реферат: Изобретение относится к улучшенному способу получения цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил] этил} пирролидина, который является промежуточным веществом для получения (-)цис-6-фенил-5-[4-(2-пирролидин-1-ил-этокси)фенил-5,6,7,8-тетрагидронафталин-2-ола, который используется в лечении остеопороза, а также к промежуточным соединениям для этого способа. Способ получения цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси]этил}пирролидина, включает следующие стадии: 1) бромирование 2-бром-5-метокситолуола с получением 1-бром-2-бромметил-4-метоксибензола; 2) алкилирование этилового эфира бензоилацетата продуктом стадии 1 с последующим декарбоксилированием с получением 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-она; 3) взаимодействие продукта стадии 2 с этиленгликолем с получением 2-[2-(2-бром-5-метоксифенил)этил]-2-фенил) [1,3] диоксолана; 4) обработка продукта стадии 3 н-бутиллитием и взаимодействие продукта реакции с 4-бензилоксибензонитрилом с получением (4-бензилоксифенил)-{4-метокси-2-[2- (2-фенил[1,3]-диоксолан-2-ил)этил]фенил}метанона, который гидролизуют, получая 3-[2-(4-бензилоксибензоил)-5-метоксифенил]-1-фенил-пропан-1-он; 5) обработка продукта стадии 4 хлоридом титана(III) и парой цинк – медь с получением 4-(4-бензилоксифенил)-7-мет-окси-3-фенил-1,2-дигидронафталина; 6) гидрирование продукта стадии 5 и обработка трифенилфосфином, DEAD и 1-(2-гидроксиэтил)пирролидином с получением 1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси] -этил} пирролидина. Соединения, выбранные из группы, включающей: 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-он; 2-[2-(2-бром-5-метоксифенил)этил] -2-фенил[1,3] диоксолан; 3-[2-(4-бензилоксибензоил)-5-метоксифенил]-1-фенилпропан-1-он; 4-(4-бензилоксифенил) -7-метокси-3-фенил-1,2-дигидронафталин. 2 с.п. ф-лы. Изобретение предлагает улучшенный способ получения цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси] этил} пирролидина, который является промежуточным веществом для получения (-)цис-6-фенил-5-[4-(2-пирролидин-1-ил-этокси)фенил] -5,6,7,8-тетрагидронафталин-2-ола, пригодного для лечения остеопороза. Получение (-)цис-б-фенил-5-[4-(2-пирролидин-1-ил-этокси)фенил] -5,6,7,8-тетрагидронафталин-2-ола описано в патенте США 5552412, который включен здесь в качестве ссылки. Это соединение является агонистом эстрогена и пригодно в лечении состояний, вызванных дефицитом эстрогена. Патент США 5552412 также описывает синтез цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси] этил} пирролидина путем гидрирования нафоксидина. Lednicer et al. , J. Med. Chem., 12, 881 (1969) описывает антагонисты эстрогена, имеющие структуру 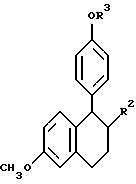 где R2 представляет собой фенил или циклопентил и R3 представляет собой Н, 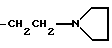 или -CH2CHOHCH2OH. Bencze et al. , J.Med.Chem., 10, 138 (1967) получил ряд тетрагидронафталинов, предназначенных для достижения разделения эстрогенной активности, активности, направленной против способности к воспроизводству потомства, и гипохолестеринемической активности. Эти структуры общей формулы 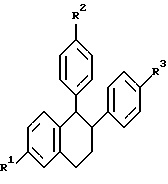 где R1 представляет собой Н или ОСН3; R2 представляет собой Н, ОН, ОСН3, OPO(OC2H5)2, OCH2CH2N (C2H5)2, ОСН2СООН или ОСН(СН3)СООН. Патент США 3234090 предлагает соединения, которые обладают эстрогенными и противогрибковыми свойствами, формулы 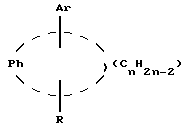 в которой Ph представляет собой 1,2-фениленовый радикал, Аr представляет собой моноциклическую карбоциклическую арильную группу, замещенную третичным аминонизшим алкилокси, в которой третичный амино отделен от окси по крайней мере двумя атомами углерода, R представляет собой водород, алифатический радикал, карбоциклический арильный радикал, карбоциклический арилалифатический радикал, гетероциклический арильный радикал или гетероциклический арильный алифатический радикал, группа формулы -(СnН2n-2)- обозначает алкиленовый радикал с неразветвленной цепью, имеющий от трех до пяти атомов углерода и несущий группы Аr и R, их соли, N-оксиды, соли N-оксидов или их четвертичные аммониевые соединения, а также методику получения подобных соединений. Патент США 3277106 относится к основным эфирам с эстрогенными, гипохолестеринемическими и направленными на снижение способности к воспроизведению потомства эффектами, которые имеют формулу 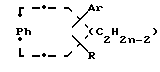 в которой Ph представляет собой 1,2-фениленовый радикал, Аr представляет собой моноциклический арильный радикал, замещенный по крайней мере одной аминонизшей алкилоксигруппой, в которой атом азота отделен от атома кислорода по крайней мере двумя атомами углерода, R представляет собой арильный радикал и фрагмент -(CnH2n-2)- обозначает низший алкилен, образуя с Ph шести- или семичленное кольцо, в котором два из атомов углерода несут группы Аr и R к их солям, N-оксидам, солям N-оксидов и их четвертичным аммониевым соединениям. Lednicer et al. в J.Med.Chem., 10, 78 (1967) и патенте США 3274213 относится к соединениям формулы 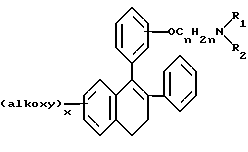 где R1 и R2 выбраны из класса, состоящего из низшего алкила и низшего алкила, связанных вместе с образованием 5-7-членного насыщенного гетероциклического радикала. Данное изобретение предлагает промежуточные соединения, которые пригодны для получения (-)цис-6-фенил-5-[4-(2-пирролидин-1-ил-этокси)фенил-5,6,7,8-тетрагидронафталин-2-ола. Эти соединения включают: 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-он; 2-[2-(2-бром-5-метоксифенил)этил] -2-фенил[1,3]-диоксолан; 3-[2-(4-бензилоксибензоил)-5-метоксифенил]-1-фенилпропан-1-он; и 4-(4-бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталин и (4-бензилоксифенил)-{4-метокси-2-[2-(2-фенил[1,3]диоксолан-2-ил)этил]фенил}метанон. Данное изобретение также предлагает способ получения цис-1-{4-[6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси] этил}пирролидина, который включает следующие стадии: 1) 2-бром-5-метокситолуол бромируют для получения 1-бром-2-бромметил-4-метоксибензола; 2) Продукт стадии 1 используют для алкилирования этилового эфира бензоилацетата с последующим декарбоксилированием с получением 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-она (соединение г). 3) Продукт стадии 2 (г) взаимодействует с этиленгликолем с получением 2-[2-(2-бром-5-метоксифенил)этил] -2-фенил)этил] -2-фенил[1,3] диоксолана (соединение а). 4) Продукт стадии 3 (а) подвергается реакции обмена металл-галоген с н-бутиллитием и взаимодействует с 4-бензилоксибензонитрилом с получением 2-[2-(2-(4-бензилоксибензоил)-5-метоксифенил)этил] -2-фенил[1,3] диоксолана (соединение е), который подвергают кислотному гидролизу, отщепляя 1,3-диоксолан с получением 3-[2-(4-бензилоксибензоил)-5-метоксифенил]-1-фенилпропан-1-она; 5) Продукт стадии 4 обрабатывают хлоридом титана (III) и парой цинк-медь для получения 4-(4-бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталина 6) Продукт стадии 5 подвергают гидрированию и обрабатывают трифенилфосфином, DEAD и 1-(2-гидроксиэтил)пирролидином, получая 1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидро-нафталин-1-ил]этил}пирролидин. Данное изобретение также предлагает способ взаимодействия 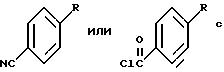 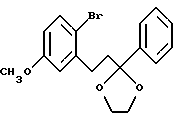 с получением 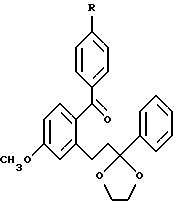 где R представляет собой защищенный фенил или 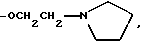 который включает взаимодействие 2-[2-(2-бром-5-метоксифенил)этил]-2-фенил[1,3]диоксолана с бутиллитием с последующей реакцией с 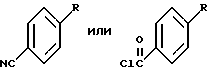 Изобретение предлагает новый способ синтеза цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси] этил}пирролидина (см. схему в конце текста). В описании используются следующие сокращения: NDS – N-бромсукцинимид; AIBN – 2,2′-азобисизобутиронитрил; TMSCI – триметилхлорсилан; TNF – тетрагидрофуран; PPTS – пиридин-паратолуолсульфонат; DEAD – диэтилазодикарбоксилат; DME – диметоксиэтан. Термин “защищенный фенол” включает бензилоксигруппы, необязательно замещенные алкокси, нитро или галогеном и другими приемлемыми защитными группами для спиртов. Синтез начинается с бромирования 2-бром-5-метокситолуола (а) с получением бензилбромида 1-бром-2-бромметил-4-мет-оксибензола (b). Алкилирование этилбензоилацетата (с) этим бензилбромидом с последующим декарбоксилированием приводит к получению 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-она кетона (d), который защищают, переводя в кеталь 2-[2-бром-5-метоксифенил]-2-фенил[1,3] диоксолана. Металл-галоген обменная реакция кеталя 2-[2-бром-5-метоксифенил)-2-фенил[1,3] -диоксолана дает производное ариллития, которое легко присоединяется к 4-бензилоксибензоату или 4-бензоксибензонитрилу (f) и дает дикетон 3-[2-(4-бензилоксибензоил)-5-метоксифенил]-1-фенилпропан-1-она после обработки кислотой. Дикетон подвергают титан-медиированной конденсации по типу McMurry для получения 4-(4-бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталина (i), который имеет углеродный скелет цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)-фенокси] этил} пирролидина со всеми функциональными группами уже в ней. Гидрирование с палладиевым катализатором в одном сосуде приводит к восстановлению олефиновой двойной связи и снятию защиты бензилового эфира. Введение N-этил-пирролидино в качестве боковой цепи достигается в условиях реакции Mitsunobu с получением 1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси]этил}пирролидина (j), ключевого предшественника цис-1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси]этил}пирролидина. Это соединение превращается в цис-6-фенил-5-[4-(2-пирролидин-1-ил-этокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол реакцией с НВr, как описано в патенте США 5552412. ПРИМЕР 1. 1-Бром-2-бромметил-4-метоксибензол Ссылка: Synthetic Communications, 1984, 1205-1211. К раствору 2-бром-5-метокситолуола (50 г, 0,25 моль) в дихлорэтане (375 мл) добавляют N-бромсукцинимид (48,8 г, 0,275 моль) и AIBN (1,36 г) и реакционную смесь кипятят с обратным холодильником в течение 4 часов. Охлажденный раствор фильтруют и растворитель выпаривают, получая 44,8 г неочищенного 1-бром-2-бромметил-4-метоксибензола (выход 64%). Это соединение используют на следующей стадии без дальнейшей очистки. ПРИМЕР 2. 3-(2-Бром-5-метоксифенил)-1-фенилпропан-1-он Ссылка: JACS, 1977, 2786. К раствору этоксида натрия (5,72 г, 84 ммоль) в 50 мл безводного этанола при перемешивании добавляют 14,8 г (77 ммоль) этилбензоилацетата. Затем реакционную смесь осторожно нагревают до кипения с обратным холодильником и в течение 20 минут добавляют 19,6 г (70 ммоль) 1-бром~2-бромметил-4-метоксибензола в 20 мл этанола. Реакционную смесь кипятят с обратным холодильником в течение 2 часов. Реакционную смесь охлаждают, фильтруют и концентрируют. Концентрированную смесь подвергают кислотному гидролизу и декарбоксилированию путем кипячения с обратным холодильником в течение ночи в растворе, содержащем 40 мл ледяной уксусной кислоты, 5 мл концентрированной серной кислоты и 10 мл воды. Затем реакционную смесь нейтрализуют 10% NaOH и экстрагируют метиленхлоридом. Экстракты концентрируют, получая 19,43 г сырого 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-она (выход 87%). Это соединение затем используют на следующей стадии без дальнейшей очистки. 1Н HMR (CDCl3, 400 МHz)  7.96 (m, 2Н), 7.50(m, 4Н), 6.81 (s, 1H), 6.61(m, 1Н), 3.70[s,3H), 3.13(t,J=8Hz,2H), 3.37(t, J=8Hz,2H). GC-MS:319.
ПРИМЕР 3. 2-[2-(2-Бром-5-метоксифенил)этил]-2-фенил-[1,3]диоксолан 7.96 (m, 2Н), 7.50(m, 4Н), 6.81 (s, 1H), 6.61(m, 1Н), 3.70[s,3H), 3.13(t,J=8Hz,2H), 3.37(t, J=8Hz,2H). GC-MS:319.
ПРИМЕР 3. 2-[2-(2-Бром-5-метоксифенил)этил]-2-фенил-[1,3]диоксоланСсылка: Synthesis, 1983, 203. К раствору неочищенного 3-(2-бром-5-метоксифенил)-1-фенилпропан-1-она (19,43 г, 61 моль) в сухом этиленгликоле (300 мл) в атмосфере N2 добавляют хлортриметилсилан (31 мл, 0,25 моль). Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. Добавляют 5% водный раствор МаНСО3 (300 мл). Смесь экстрагируют диизопропиловым эфиром и экстракты промывают насыщенным солевым раствором. Объединенные эфирные экстракты сушат Na2SO4 и растворитель удаляют при пониженном давлении, получая 21,52 г сырого 2-[2-(2-бром-5-метоксифенил) этил]-2-фенил [1,3]диоксолана (выход 97%). 1H NMR (CDCl3, 400 MHz)  7.48(m, 2Н), 7.32 (m, 4H), 6.70 (s, 1H), 6.60(m, 1H), 4.05(t,J=16,2Н), 3.80 (t,J=1,6Hz, 2H), 3.71 (s, 3Н), 2.75(t,J= 3,2Hz, 2H), 2.16(t,J=3,2Нz,2Н). GC-MS: 364 7.48(m, 2Н), 7.32 (m, 4H), 6.70 (s, 1H), 6.60(m, 1H), 4.05(t,J=16,2Н), 3.80 (t,J=1,6Hz, 2H), 3.71 (s, 3Н), 2.75(t,J= 3,2Hz, 2H), 2.16(t,J=3,2Нz,2Н). GC-MS: 364ПРИМЕР 4. 4-Бензилоксибензонитрил Ссылка: Tetrahedron Lett.,1986, 279-282 К раствору 4-цианофенола (25 г, 0,21 моль) и К2СО3 (138 г, 1 моль) в DMF (300 мл) добавляют бензилхлорид (27,91 г, 0,22 моль) одной порцией. Полученную в результате смесь перемешивают при комнатной температуре в течение ночи. Суспензию фильтруют и фильтрат выливают в ледяную воду. Полученное в результате твердое вещество собирают, получая 43,5 г продукта (выход 99%). ПРИМЕР 5. 3-[2-(4-Бензилоксибензоил)- 5-метоксифенил]-l-фенилпропан-1-он Раствор 2-[2-(2-бром-5-метоксифенил)этил] -2-фенил[1,3]-диоксолана (0,9 г, 2,5 ммоль) в 10 мл THF охлаждают до -78oС и по каплям добавляют н-BuLi (2,5М в гексане, 1 мл). Раствор перемешивают при -78oС в течение 2 часов и добавляют 4-бензилоксибензонитрил (0,575 г, 2,75 ммоль) в 2 мл THF. Смеси дают нагреться до комнатной температуры и кипятят с обратным холодильником в течение ночи. Затем раствор гасят насыщенным раствором NH4Cl и растворитель выпаривают. Остаток растворяют в 20 мл влажного ацетона, 5 мл Н2O, содержащей PPTS (118 мг, 0,75 ммоль) и кипятят с обратным холодильником в течение ночи. Обычная обработка и колоночная очистка дают 0,8 г неоптимального веса 3-[2-(4-бензилоксибензоил)-5-метоксифенил]-1-фенилпропан-1-она. 1Н NMR(CDCl3, 400 MHz)  7.92 (d, J=6.8Hz,2Н), 7.79(d, J=6.8Hz,2H), 7.40 (m, 9Н), 7.0(m, 2H), 6.92 (s, 1H), 6.77 (m, 2H), 5.12 (s, 2H), 3.83 (S, 3H), 3.13 [t, J=8Hz, 2H), 3.37 (t, J=8Hz, 2H). GC-MS 450.
ПРИМЕР 6. 4-(4-Бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталин 7.92 (d, J=6.8Hz,2Н), 7.79(d, J=6.8Hz,2H), 7.40 (m, 9Н), 7.0(m, 2H), 6.92 (s, 1H), 6.77 (m, 2H), 5.12 (s, 2H), 3.83 (S, 3H), 3.13 [t, J=8Hz, 2H), 3.37 (t, J=8Hz, 2H). GC-MS 450.
ПРИМЕР 6. 4-(4-Бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталинСсылка: LOC, 1977, 2656. TiCl3 (2,62 г, 13 ммоль) и пару Zn-Cu (2,02 г, 30,8 ммоль) помещают в 200-миллилитровую круглодонную колбу в атмосфере 2, добавляют безводный диметоксиэтан (40 мл) и смесь кипятят с обратным холодильником в течение 1 часа. Примечание: пару Zn-Cu получают путем добавления цинкового порошка (9,8 г, 150 ммоль) к 40 мл деоксигенированной воды, продувая взвесь газоообразным N2 в течение 15 минут и затем добавляя CuSO4 (0,75 г, 4,7 ммоль). Черную суспензию фильтруют в атмосфере N2, промывают деоксигенированной водой, ацетоном, эфиром и затем хранят в атмосфере N2. К взвеси, которую кипятят с обратным холодильником, добавляют 3-[2-(4-бензилоксибензоил)-5-метоксифенил] -1-фенилпропан-1-он (540 мг, 1,2 ммоль) в 80 мл DME и полученную в результате смесь кипятят с обратным холодильником в течение 15 минут. Суспензию фильтруют и растворитель выпаривают, получая 0,45 г 4-(4-бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталина (выход 90%, структура подтверждена рентгенографически. 1Н NMR (CDCl1, 400 MHz)  7.38 (m, 17H), 5.01 (s, 2H), 3.80(s, 3H), 2.95 (t, J=8Hz, 2H), 2.78(t,J=8Hz, 2H).
ПРИМЕР 7. 1-{ 2-[4-(6-Метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)этил}пирролидин 7.38 (m, 17H), 5.01 (s, 2H), 3.80(s, 3H), 2.95 (t, J=8Hz, 2H), 2.78(t,J=8Hz, 2H).
ПРИМЕР 7. 1-{ 2-[4-(6-Метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)этил}пирролидин4-(4-Бензилоксифенил)-7-метокси-3-фенил-1,2-дигидронафталин (0,45 г, 1,08 ммоль) растворяют в смеси EtOH (15 мл) в аппарате Парра. Добавляют Pd(OH)2 (0,3 г) в 2 мл Н2O и смесь встряхивают в атмосфере Н2 (50 ф/дм2) при комнатной температуре. Раствор фильтруют и обрабатывают эквивалентным количеством трифенилфосфина, DEAD и 1-(2-гидроксиэтил)пирролидина. Обычная обработка дает 1-{2-[4-(6-метокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил этил)пирролидин. Формула изобретения
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 24.05.2007
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
