Патент на изобретение №2193566
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ МОНОЭФИРА ЯНТАРНОЙ КИСЛОТЫ ИЗ 17-ОКСИСТЕРОИДА И ЯНТАРНОГО АНГИДРИДА
(57) Реферат: Изобретение относится к области органической химии, к способу получения моноэфира из 17-оксистероида и янтарного ангидрида. Способ включает ацилирование 17-оксистероида с использованием янтарного ангидрида в среде апротонного биполярного растворителя при 20-110oC в присутствии каталитического количества или избытка основания. В качестве реакционной среды используют диметилформамид, диметилацетамид, диметилсульфоксид и другие аналогичные растворители. В качестве катализатора используют различные основания: прокаленный поташ, тиэтиламин. Избыток основания отрицательно не сказывается на выходе целевого продукта, выход целевого продукта достигает 91%. Процесс проводят в мягких условиях. Изобретение относится к области органической химии – способу получения моноэфира янтарной кислоты и 17-оксистероида. Известен способ получения моноэфира янтарной кислоты путем ацилирования 17-оксистероида, например тренболона (эстра-4,9,11-триен-17  -гидрокси-3-он) (I), основанный на нагревании его с янтарным ангидридом в среде пиридина: -гидрокси-3-он) (I), основанный на нагревании его с янтарным ангидридом в среде пиридина: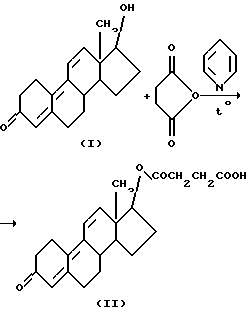 Однако условия проведения реакции, нагревание в пиридине при 75oС в течение 3 ч, для высоко лабильного сопряженного триенона, каковым является тренболон (I), весьма жестки, и выход целевого продукта-моноэфира янтарной кислоты (II) не превышает 56,6% [1]. Следует отметить, что пиридин относится к числу высоко токсичных соединений и обладает недостаточно высокой растворяющей способностью. Помимо этого, при выделении целевого продукта, в случае использования пиридина возникает необходимость нейтрализации его сильной минеральной кислотой, что создает дополнительное неудобство. Целью изобретения является разработка нового способа получения моноэфира янтарной кислоты из 17-оксистероида и янтарного ангидрида в более мягких и экологичных условиях, упрощение выделения и повышение выхода целевого продукта, расширение ассортимента применяемых растворителей. Указанная цель достигается тем, что ацилирование 17-оксистероида с янтарным ангидридом осуществляют в среде апротонного биполярного растворителя при 20-110oС в присутствии каталитического количества или избытка основания. Предлагаемый способ ацилирования тренболона (I) имеет общий характер и может быть применен при ацилировании других 17-оксистероидов, например, 19-нортестостерона (III). 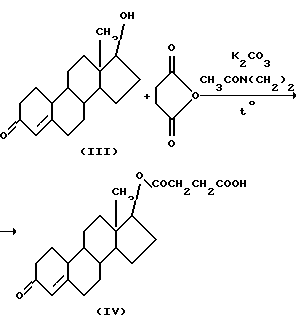 В качестве реакционной среды в предлагаемом способе можно использовать диметилформамид, диметилацетамид, диметилсульфоксид и аналогичные растворители. Реакция 17-оксистероидов с янтарным ангидридом при нагревании в среде апротонных биполярных растворителей идет и без применения катализатора, однако выход соответствующих моноэфиров янтарной кислоты (II, IV) невелик (2-3%). В качестве катализатора можно использовать различные основания (прокаленный поташ, триэтиламин). Органические основания лучше применять при более низких температурах проведения реакции (20-60oС), неорганические – повышенных температурах (60-100oС). Ацилирование успешно идет с применением каталитического количества основания. Избыток основания отрицательно не сказывается на выходе целевого продукта. Моноэфиры янтарной кислоты (II, IV), синтезированные ацилированием соответствующих 17-оксистероидов (I, III) янтарным ангидридом, имеют важное значение для получения антигенов, широко применяемых для определения следовых количеств этих стероидов, обладающих анаболическим действием [2, 3]. Ход реакции и чистоту получаемых продуктов контролируют методом тонкослойной хроматографии на пластинах с силикагелем “Силуфол UV-254”. В качестве подвижной фазы при хроматографировании используют смесь хлороформа и ацетона в соотношении 10: 1. Пластины просматривают в УФ-свете или опрыскивают 0,1%-ным спиртовым раствором бромфенолового синего. При проведении реакции применяют свежепрокаленный углекислый калий и сухие растворители, перегнанные в вакууме. УФ-спектры снимают на приборе СФ-16 в этаноле, ИК-спектр – на приборе UR-20 в вазелиновом масле. Изобретение иллюстрируется следующими примерами. Пример 1. Смесь 135 мг (0,5 ммоль) тренболона (эстра-4,9,11-триен-17  -гидрокси-3-он) (I), 200 мг (2 ммоль) янтарного ангидрида, 1,2 см3 диметилсульфоксида и 20 мг (0,15 ммоль) углекислого калия нагревают 4 ч при 80oС. Реакционную смесь охлаждают до 20oС и обрабатывают при охлаждении льдом 10 см3 2%-ной соляной кислоты. Выпавший осадок отделяют фильтрованием и растирают на стеклянном фильтре трижды с 3 см3 воды. Осадок сушат на воздухе. Выход моноэфира янтарной кислоты (II) 170 мг (92%), Т.пл. 152-153oС, Rf эфира (II) – 0,23, Rf тренболона (I)- 0,3, -гидрокси-3-он) (I), 200 мг (2 ммоль) янтарного ангидрида, 1,2 см3 диметилсульфоксида и 20 мг (0,15 ммоль) углекислого калия нагревают 4 ч при 80oС. Реакционную смесь охлаждают до 20oС и обрабатывают при охлаждении льдом 10 см3 2%-ной соляной кислоты. Выпавший осадок отделяют фильтрованием и растирают на стеклянном фильтре трижды с 3 см3 воды. Осадок сушат на воздухе. Выход моноэфира янтарной кислоты (II) 170 мг (92%), Т.пл. 152-153oС, Rf эфира (II) – 0,23, Rf тренболона (I)- 0,3,  max 320 нм ( max 320 нм ( 20 500).
После перекристаллизации из метанола Т.пл.155-156oС. По литературным данным температура плавления моноэфира янтарной кислоты (II)- 155-157oС [I].
Целевой продукт в примерах 2-6 выделяют так же, как и в примере 1.
Пример 2. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 20 500).
После перекристаллизации из метанола Т.пл.155-156oС. По литературным данным температура плавления моноэфира янтарной кислоты (II)- 155-157oС [I].
Целевой продукт в примерах 2-6 выделяют так же, как и в примере 1.
Пример 2. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,12 см3 диметилацетамида и 2 мг (0,015 ммоль) углекислого калия нагревают 3 ч при 75oС. Выход эфира (II)- 89%.
Пример 3. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,12 см3 диметилацетамида и 2 мг (0,015 ммоль) углекислого калия нагревают 3 ч при 75oС. Выход эфира (II)- 89%.
Пример 3. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,12 см3 диметилсульфоксида и 8 мг (0,07 ммоль) углекислого калия размешивают при 20oС трое суток. Выход эфира (II)- 32%.
Пример 4. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,12 см3 диметилсульфоксида и 8 мг (0,07 ммоль) углекислого калия размешивают при 20oС трое суток. Выход эфира (II)- 32%.
Пример 4. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,06 см3 диметилацетамида и 0,06 см3 триэтиламина выдерживают одну неделю при комнатной температуре. Выход эфира (II)- 91%.
Пример 5. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,06 см3 диметилацетамида и 0,06 см3 триэтиламина выдерживают одну неделю при комнатной температуре. Выход эфира (II)- 91%.
Пример 5. Смесь 13,5 мг (0,05 ммоль) тренболона (эстра-4,9,11-триен-17 -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,06 см3 диметилацетамида и 0,003 см3 (0,02 ммоль) триэтиламина нагревают в закрытой пробирке при 60oС четыре часа. Выход эфира (II)- 65%.
Пример 6. Смесь 27,4 (0,1 ммоль) 19-нортестостерона (III), 15 мг (0,15 ммоль) янтарного ангидрида, 0,1 см3 диметилацетамида и 8 мг (0,07 ммоль) углекислого калия нагревают 10-15 мин при 110oС. Выход эфира (IV)- 90%, -гидрокси-3-он) (I), 20 мг (0,2 ммоль) янтарного ангидрида, 0,06 см3 диметилацетамида и 0,003 см3 (0,02 ммоль) триэтиламина нагревают в закрытой пробирке при 60oС четыре часа. Выход эфира (II)- 65%.
Пример 6. Смесь 27,4 (0,1 ммоль) 19-нортестостерона (III), 15 мг (0,15 ммоль) янтарного ангидрида, 0,1 см3 диметилацетамида и 8 мг (0,07 ммоль) углекислого калия нагревают 10-15 мин при 110oС. Выход эфира (IV)- 90%,  max 239 нм (16,5). ИК-спектр: 1728 (C=O-OR), 1645 (-СОСН=С), 1605 (C=С). max 239 нм (16,5). ИК-спектр: 1728 (C=O-OR), 1645 (-СОСН=С), 1605 (C=С).
Формула изобретения
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 13.03.2009
Извещение опубликовано: 7.05.2010 БИ: 15/2010
|
||||||||||||||||||||||||||
