Патент на изобретение №2193526
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ КРИОЛИТА
(57) Реферат: Изобретение относится к области производства регенерационного криолита на алюминиевых заводах. Способ получения криолита включает смешение фторсодобикарбонатного раствора и алюминатного раствора в непрерывном режиме, кристаллизацию, обезвоживание и сушку криолита. Алюминатный раствор подают на смешение в зависимости от концентраций во фторсодобикарбонатном растворе гидрокарбоната натрия и фторида натрия, их соотношения, от расхода этого раствора и от концентрации оксида алюминия в алюминатном растворе. Данное изобретение позволяет повысить выход и качество продукта. 3 табл. Изобретение относится к области производства регенерационного криолита на алюминиевых заводах. Получение регенерационного криолита на алюминиевых заводах основано на смешении газоочистных фторсодобикарбонатных растворов с раствором алюмината натрия. Известен способ получения криолита из фторсодержащих содобикарбонатных растворов газоочистных сооружений путем осаждения раствором алюмината натрия при повышенной температуре, в котором процесс ведут при избытке фторида на 10-50% относительно стехиометрического количества, причем процесс ведут до остаточной концентрации бикарбоната натрия 5-10 г/л и при 30-95oС (А.с. СССР 415955, С 01 F 7/54, 1979г. [1]). Недостаток известного способа – низкое извлечение фтора (67-70%), невысокая производительность процесса. Известен способ получения криолита, включающий обработку газоочистного фторсодобикарбонатного раствора карбонатсодержащим соединением и алюминатным раствором с последующим отделением выделенного продукта, в котором обработку фторсодобикарбонатного раствора карбонатсодержащим соединением ведут до массового отношения карбоната натрия к бикарбонату натрия 0,1-0,9 (А.с. СССР 1090661, C 01 F 7/54, 1984г. [2]). По технической сущности, наличию сходных признаков данное решение принято в качестве ближайшего аналога. Недостатки известного решения: низкий выход фтора в криолит, необходимость предварительной подготовки (обработка СО2-содержащим газом) газоочистного фторсодобикарбонатного раствора, регулирование процесса осуществляется только по одному технологическому параметру, что для достижения высоких технико-экономических показателей недостаточно. Не осуществляется дозирование алюминатного раствора, важнейшего параметра процесса получения регенерационного криолита. Точность дозирования алюминатного раствора оказывает существенное влияние на процесс получения криолита. При избытке (передозировке) алюминатного раствора: – ухудшается химический состав криолита (снижается содержание фтора) вследствие образования тонкодисперсных фракций гидроалюмокарбоната натрия и гидроокиси алюминия; – за счет образования данных примесей ухудшаются физические свойства криолита: снижается скорость осветления и фильтрации криолитовой пульпы; увеличиваются потери криолита с верхним сливом криолитового сгустителя, что, в свою очередь, приводит к интенсивному зарастанию трубопроводов и газоочистных аппаратов криолитом. Недостаток (недодозировка) алюминатного раствора не позволяет связать в криолит максимально возможное количество фторида натрия из газоочистных растворов, что приводит: – к недополучению криолита; – к повышению концентрации фторида натрия в растворах, подаваемых на газоочистку, как следствие этого – к повышению концентрации фторида натрия в растворах, поступающих с газоочистки на кристаллизацию (варку) криолита, что также приводит к ухудшению физических свойств криолита (крупность, скорость отстаивания и фильтрации). Задачей предлагаемого изобретения является повышение выхода и качества продукта, повышение технико-экономических показателей процесса производства регенерационного криолита за счет более эффективного использования реагентов и снижения их безвозвратных потерь. Техническим результатом предлагаемой технологии является оптимизация дозировки алюминатного раствора, подаваемого на кристаллизацию криолита, с учетом соотношения концентрации гидрокарбоната натрия к фториду натрия во фторсодобикарбонатном растворе, величины концентраций этих компонентов во фторсодобикарбонатном растворе и в маточном растворе, величины концентрации оксида алюминия в алюминатном растворе. Указанный технический результат достигается тем, что в способе получения криолита, включающем смешение фторсодобикарбонатного раствора и алюминатного раствора, кристаллизацию, обезвоживание и сушку криолита, процесс ведут в непрерывном режиме, алюминатный раствор подают на смешение в зависимости от концентраций во фторсодобикарбонатном растворе гидрокарбоната натрия и фторида натрия, их соотношения, от расхода этого раствора, от концентрации оксида алюминия в алюминатном растворе и поддерживают расход алюминатного раствора, дмз/чac: при 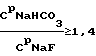 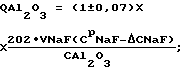 если CМNaF  5, то 5, то  CNaF=7; CNaF=7;5  CNaF=6; CNaF=6;6  CМNaF CМNaF 8, 8,  CNaF=4; CNaF=4;CМNaF>8,  CNaF=2; CNaF=2;при 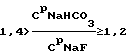 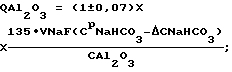 если СМNaНСО3<6, то  CNaHCO3=8; CNaHCO3=8;6  СМNаНСО3 СМNаНСО3 8, 8,  CNaHCO3=6; CNaHCO3=6;8<СМNаНСО3  10, 10,  СNаНСО3=4; СNаНСО3=4;СМNаНСО3>10,  СNаНСО3=3; СNаНСО3=3;при 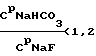 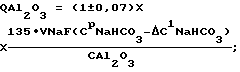 если СМNaНСО3  6, то 6, то  C1NaHCO3=6; C1NaHCO3=6;6<СМNаНСО3  8, 8,  C1NaHCO3=4; C1NaHCO3=4;8<СМNаНСО3  10, 10,  С1NаНСО3=2; С1NаНСО3=2;СМNаНСО3>10,  С1NаНСО3=0; С1NаНСО3=0;где QАl2О3 – расход подаваемого на кристаллизацию криолита алюминатного раствора, дм3/час; VNaF – расход фторсодобикарбонатного раствора, подаваемого на кристаллизацию, м3/час; СpNaF – концентрация фторида натрия во фторсодобикарбонатном растворе, подаваемом на кристаллизацию, г/дм3; СpNaНСО3 – концентрация гидрокарбоната натрия во фторсодобикарбонатном растворе, подаваемом на кристаллизацию, г/дм5; САl2О3 – концентрация оксида алюминия в алюминатном растворе, подаваемом на кристаллизацию, г/дм3; СМNaF – остаточная концентрация фторида натрия в маточном растворе, г/дм3; СМNаНСО3 – остаточная концентрация гидрокарбоната натрия в маточном растворе, г/дм3;  СNaF – концентрация фторида натрия, принимаемая в зависимости от его остаточной концентрации в маточном растворе, г/дм; СNaF – концентрация фторида натрия, принимаемая в зависимости от его остаточной концентрации в маточном растворе, г/дм; CNaHO3, CNaHO3,  C1NaHCO3 – концентрации гидрокарбоната натрия, принимаемые в зависимости от его остаточной концентрации в маточном растворе, г/дм3; C1NaHCO3 – концентрации гидрокарбоната натрия, принимаемые в зависимости от его остаточной концентрации в маточном растворе, г/дм3;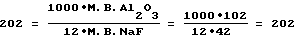 – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования; – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования;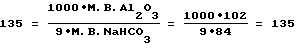 – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования; – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования;1000 – переводной коэффициент из м3 в дм3. Множитель (1+0,07) представляет собой доверительный интервал значений, в который с надежностью 95% укладываются результаты всех экспериментов. Наличие данного интервала обусловлено неточностями при замере и регулировке технологических параметров процесса варки криолита, погрешностями анализов растворов, а также колебанием модуля алюминатного раствора. Предлагаемое решение характеризуется следующими отличительными от ближайшего аналога признаками: – процесс ведут в непрерывном режиме; – расход алюминатного раствора поддерживают в зависимости от концентраций во фторсодобикарбонатном растворе гидрокарбоната натрия и фторида натрия, расхода этого раствора и от концентрации оксида алюминия в алюминатном растворе; – в зависимости от соотношений концентраций во фторсодобикарбонатном растворе гидрокарбоната натрия и фторида натрия расход алюминатного раствора определяется по формулам с учетом остаточных концентраций в маточном растворе либо по гидрокарбонату натрия, либо по фториду натрия. Использование указанной совокупности отличительных признаков обеспечивает оперативное реагирование на скачки концентраций в газоочистном и маточном растворах, стабилизирует работу узла варки криолита в условиях нестационарного процесса за счет быстрого приведения системы к оптимальным технологическим параметрам. Таким образом, предлагаемое техническое решение соответствует критерию патентоспособности изобретения “новизна”. Сравнение предлагаемого технического решения с ближайшим аналогом и другими известными решениями в данной области, выявленными в процессе поиска, показывает следующее: – известен способ получения криолита, включающий обработку газоочистного фторсодобикарбонатного раствора карбонатсодержащим соединением и алюминатным раствором с последующим отделением выделенного продукта, в котором обработку фторсодобикарбонатного раствора карбонатсодержащим соединением ведут до массового отношения карбоната натрия к бикарбонату натрия 0,1-0,9 [2]; – известен способ получения криолита из фторсодержащих содобикарбонатных растворов газоочистных сооружений путем осаждения раствором алюмината натрия, при этом процесс ведут при избытке фторида на 10-50% относительно стехиометрического количества, до остаточной концентрации бикарбоната натрия 5-10 г/л [1]; – известен способ получения криолита, включающий обработку фторсодержащих газов щелочным раствором и его варку с получением пульпы криолита, отделение криолита от щелочного раствора и подачу раствора на обработку отходящих фторсодержащих газов, в котором часть щелочного насыщенного раствора после обработки газов смешивают с пульпой криолита при соотношении (0,1-4):1 (А.с. СССР 925866, C 01 F 7/54, 1982г. [3]). Предлагаемое решение характеризуется известными признаками: – получение криолита смешением фторсодобикарбонатного раствора с алюминатным раствором, кристаллизацией, обезвоживанием и сушкой [1, 2, 3]; – ведение процесса до остаточной концентрации бикарбоната натрия 5-10 г/л [1] (частично в заявляемых интервалах). Предлагаемое решение характеризуется также не известными ранее признаками: – расход алюминиевого раствора установлен в зависимости от величины остаточных концентраций в маточном растворе фторида натрия и гидрокарбоната натрия в различных пределах; – расход алюминатного раствора установлен в зависимости от соотношения гидрокарбоната натрия к фториду натрия в фторсодобикарбонатном растворе в различных пределах. Таким образом, предлагаемое техническое решение характеризуется существенными отличительными признаками, позволяющими при их использовании получить более высокие технико-экономические показатели: – стабилизация процесса; – оперативная оптимизация технологических параметров процесса варки криолита; – повышение извлечения алюминия и фтора во вторичный криолит, что свидетельствует о его соответствии критерию патентоспособности изобретения “изобретательский уровень”. Примеры. Во всех примерах на постоянном уровне выдерживались следующие технологические параметры. 1. Количество фторсодобикарбонатного раствора на варку криолита 110 м3/час. 2. Концентрация Аl2О3 в алюминатном растворе 290г/дм3. 3. Содержание фтора в получаемом криолите 44%. 4. Извлечение фтора в криолит определяли по отношению количества фтора, фактически переведенного в криолит (по разности концентраций NaF в исходном и маточном растворах), к количеству фтора, которое может быть переведено в криолит при концентрации NaF в маточном растворе, равной 6 г/дм3. 5. В примерах сравниваются два варианта: Вариант 1 – существующая дозировка алюминатного раствора; Вариант 2 – предлагаемый способ дозировки. 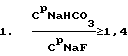 В табл.1.1 рассмотрены случаи, когда концентрация NaF в маточном растворе СМNaF  5; 5<СМNaF<6; 6 5; 5<СМNaF<6; 6 СМNaF СМNaF 8.
В табл. 1.2 рассмотрены случаи, когда СМNaF>8; 5<СМNaF<6; 6 8.
В табл. 1.2 рассмотрены случаи, когда СМNaF>8; 5<СМNaF<6; 6 СМNaF СМNaF 8.
Из табл. 1-3 видно, что предлагаемый способ расчета дозировки алюминатного раствора позволяет получить лучшие технико-экономические показатели варки криолита за счет более быстрого достижения и поддержания оптимальной концентрации NaF в маточном растворе.
Проведены опытно-промышленные испытания предлагаемой технологии на Красноярском и на Иркутском алюминиевых заводах, подтвердившие ее эффективность.
Следует также отметить, что область применения предлагаемого способа не ограничивается получением криолита из газоочистных фторсодобикарбонатных растворов алюминиевых заводов. Данный способ применим и к тем случаям, когда кристаллизация криолита ведется из фторсодобикарбонатных растворов, полученных любым другим способом, например: 8.
Из табл. 1-3 видно, что предлагаемый способ расчета дозировки алюминатного раствора позволяет получить лучшие технико-экономические показатели варки криолита за счет более быстрого достижения и поддержания оптимальной концентрации NaF в маточном растворе.
Проведены опытно-промышленные испытания предлагаемой технологии на Красноярском и на Иркутском алюминиевых заводах, подтвердившие ее эффективность.
Следует также отметить, что область применения предлагаемого способа не ограничивается получением криолита из газоочистных фторсодобикарбонатных растворов алюминиевых заводов. Данный способ применим и к тем случаям, когда кристаллизация криолита ведется из фторсодобикарбонатных растворов, полученных любым другим способом, например:– смешением растворов фторида натрия и бикарбоната натрия; – разложением кремнефторида натрия содой, протекающим по реакции Na2SiF6+4Na2СО3+2H2O=6NaF+4NaHCO3+SiO2 Фторсодобикарбонатный раствор при этом может иметь следующий состав, г/дм3: NaF – 10-40; Nа2СО3 – 3-12; NаНСО3 – 12-50. Применение предлагаемой технологии к различным технологическим схемам получениям криолита дают аналогичные положительные результаты. ИСТОЧНИКИ ИНФОРМАЦИИ 1. А.с. СССР 415955, C 01 F 7/54, 1979г. 2. А.с. СССР 1090661, C 01 F 7/54, 1984г. 3. А.с. СССР 925866, C 01 F 7/54, 1982г. Формула изобретения
при 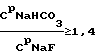 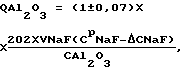 если СМNaF  5, то 5, то  CNaF= 7; CNaF= 7;5<СМNaF<6,  CNaF= 6; CNaF= 6;6  СМNaF СМNaF 8, 8,  CNaF= 4; CNaF= 4;СМNaF>8,  CNaF= 2; CNaF= 2;при 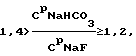 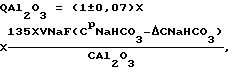 если СМNaHCO3<6, то  CNaHCO3= 8, CNaHCO3= 8,6  СМNaHCO3 СМNaHCO3 8, 8,  CNaHCO3= 6; CNaHCO3= 6;8<СМNaHCO3  10, 10,  CNaHCO3= 4; CNaHCO3= 4;СМNaHCO3>10,  CNaHCO3= 3; CNaHCO3= 3;при 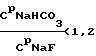 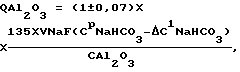 если СМNaHCO3  6, то 6, то  C1NaHCO3= 6; C1NaHCO3= 6;6<СМNaHCO3  8, 8,  C1NaHCO3= 4; C1NaHCO3= 4;8<СМNaHCO3  10, 10,  C1NaHCO3= 2; C1NaHCO3= 2;СМNaHCO3>10,  C1NaHCO3= 0; C1NaHCO3= 0;где QAl2O3 – расход подаваемого на кристаллизацию криолита алюминатного раствора, дм3/ч; V NaF – расход фторсодобикарбонатного раствора, подаваемого на кристаллизацию, м3/ч; СрNaF – концентрация фторида натрия во фторсодобикарбонатном растворе, подаваемом на кристаллизацию, г/дм3; СрNaНСО3 – концентрация гидрокарбоната натрия во фторсодобикарбонатном растворе, подаваемом на кристаллизацию, г/дм3; СAl2O3 – концентрация оксида алюминия в алюминатном растворе, подаваемом на кристаллизацию, г/дм3; СМNaF – остаточная концентрация фторида натрия в маточном растворе, г/дм3; СМNaНСО3 – остаточная концентрация гидрокарбоната натрия в маточном растворе, г/дм3;  C NaF – концентрация фторида натрия, принимаемая в зависимости от его остаточной концентрации в маточном растворе, г/дм3; C NaF – концентрация фторида натрия, принимаемая в зависимости от его остаточной концентрации в маточном растворе, г/дм3; CNaHCO3, CNaHCO3,  C1NaHCO3 – концентрации гидрокарбоната натрия, принимаемые в зависимости от его остаточной концентрации в маточном растворе, г/дм3; C1NaHCO3 – концентрации гидрокарбоната натрия, принимаемые в зависимости от его остаточной концентрации в маточном растворе, г/дм3;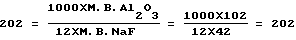 – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования; – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования;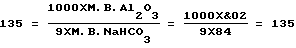 – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования; – коэффициент учета молекулярных весов реагентов, участвующих в реакции криолитообразования;1000 – переводной коэффициент из м3 в дм3; (1  0,07) – доверительный интервал значений, в который с надежностью 95% укладываются результаты всех экспериментов. 0,07) – доверительный интервал значений, в который с надежностью 95% укладываются результаты всех экспериментов.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 12.07.2008
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
