Патент на изобретение №2192423
|
||||||||||||||||||||||||||
(54) СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ЭТИЛ-3,6-ДИАЛКИЛЦИКЛОГЕПТАОКСАЛАНОВ И 1-ЭТИЛ-3,5-ДИАЛКИЛЦИКЛОГЕПТАОКСАЛАНОВ
(57) Реферат: Описывается способ совместного получения 1-этил-3,6-диалкилциклогептаоксаланов формулы 1 и 1-этил-3,5- диалкилциклогептаоксаланов формулы (2), где R= н-C4H9, н-C6H13; R’=н-C3H17, i-C3H7, н-C5H11, отличающийся тем, что  -олефины формулы -олефины формулы 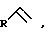 , где R, как определено выше, подвергают взаимодействию с триэтилалюминием (AlEt3) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2) в мольном соотношении , где R, как определено выше, подвергают взаимодействию с триэтилалюминием (AlEt3) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2) в мольном соотношении 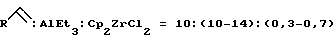 в атмосфере аргона в течение 8 часов с последующим добавлением гексана, охлаждением реакционной массы до -10oС и добавлением катализатора однохлористой меди (CuCl) и альдегида формулы R’-CHO, где R’, как определено выше, в мольном соотношении CuCl:R’CHO= (0,8-1,2): (10-14) и перемешиванием реакционной массы в течение 6-10 ч при комнатной температуре и нормальном давлении. Получаемые соединения могут найти применение в тонком органическом и металлоорганическом синтезе, а также в качестве сокатализаторов в процессах олиго- и полимеризации олефинов и диенов. 1 табл. в атмосфере аргона в течение 8 часов с последующим добавлением гексана, охлаждением реакционной массы до -10oС и добавлением катализатора однохлористой меди (CuCl) и альдегида формулы R’-CHO, где R’, как определено выше, в мольном соотношении CuCl:R’CHO= (0,8-1,2): (10-14) и перемешиванием реакционной массы в течение 6-10 ч при комнатной температуре и нормальном давлении. Получаемые соединения могут найти применение в тонком органическом и металлоорганическом синтезе, а также в качестве сокатализаторов в процессах олиго- и полимеризации олефинов и диенов. 1 табл.
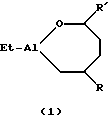 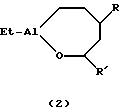
Предлагаемое изобретение относится к способам получения новых алюминийорганических соединений (АОС), конкретно к способу получения 1-этил-3,6-диалкилциклогептаоксаланов и 1-этил-3,5-диалкилциклогептаоксаланов общей формулы (1) и (2): 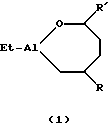 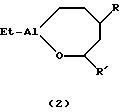 где R=н-C4H9, н-С6Н13; R’=н-С3Н7, i-С3Н7, н-С5Н11 Предлагаемые соединения могут найти применение в тонком органическом и металлоорганическом синтезе, а также в качестве сокатализаторов в процессах олиго- и полимеризации олефинов и диенов. Известен способ ([1] , Л.И. Захаркин, Л.А. Савина. Изв. АН СССР, Сер. хим. , 1960, 6, 1039-1043) получения внутрикомплексных алюминийорганических соединений (3) взаимодействием i-Bu2AlH с  -функциональнопроизводными -функциональнопроизводными  -олефинов по схеме 1 (см. в конце описания).
Известный способ не позволяет получать 1-этилдиалкилциклогептаоксаланы (1) и (2).
Известен способ ([2] , Л.И. Захаркин, Л.А. Савина, Изв. АН СССР, ОХП, 1962, 5, 824-827) получения 1-изобутилциклопентаоксаланов (4) взаимодействием аллилового спирта с триизобутилалюминием при -5 – -10oС с последующим прибавлением i-Bu2A1H и нагреванием в течение 6 часов до 125-130oС по схеме 2.
Известный способ не позволяет получать 1-этилциклогептаоксаланы (1) и (2).
Таким образом, в литературе отсутствуют сведения по совместному получению 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2).
Предлагается новый способ синтеза 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2).
Сущность способа заключается во взаимодействии в атмосфере инертного газа -олефинов по схеме 1 (см. в конце описания).
Известный способ не позволяет получать 1-этилдиалкилциклогептаоксаланы (1) и (2).
Известен способ ([2] , Л.И. Захаркин, Л.А. Савина, Изв. АН СССР, ОХП, 1962, 5, 824-827) получения 1-изобутилциклопентаоксаланов (4) взаимодействием аллилового спирта с триизобутилалюминием при -5 – -10oС с последующим прибавлением i-Bu2A1H и нагреванием в течение 6 часов до 125-130oС по схеме 2.
Известный способ не позволяет получать 1-этилциклогептаоксаланы (1) и (2).
Таким образом, в литературе отсутствуют сведения по совместному получению 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2).
Предлагается новый способ синтеза 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2).
Сущность способа заключается во взаимодействии в атмосфере инертного газа  -олефинов общей формулы -олефинов общей формулы 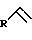 , где R=н-C4H9, н-С6Н13, с триэтилалюминием (AlEt3) в присутствии катализатора цирконацендихлорида (Cp2ZrC12), взятыми в мольном соотношении , где R=н-C4H9, н-С6Н13, с триэтилалюминием (AlEt3) в присутствии катализатора цирконацендихлорида (Cp2ZrC12), взятыми в мольном соотношении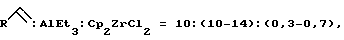 предпочтительно 10:12:0,5, при комнатной температуре (20-22oС) в течение 8 часов с последующим охлаждением реакционной массы до -10oС и добавлением катализатора однохлористой меди (CuС1) и альдегида общей формулы 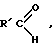 где R’= н-С3Н7, i-С3Н7, н-С5Н11, взятыми в мольном соотношении CuCl: R’CHO= (0,8-1,2): (10-14) предпочтительно 1:12, с последующим перемешиванием при комнатной температуре в течение 6-10 часов, предпочтительно 8 часов. Общий выход 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2) составляет 62-78%, соотношение (1):(2)~1,5:1. Реакция протекает по схеме 3. Проведение указанной реакции в присутствии медного катализатора больше 12 мол.% по отношению к исходному  -олефину не приводит к существенному увеличению выхода целевых продуктов. Использование катализатора менее 0,8 мол.% снижает выход АОС (1) и (2), что связано, возможно, со снижением каталитически активных центров в реакционной массе.
Проведение реакции при более высокой температуре (например, 40oС) не приводит к увеличению выхода целевых продуктов. При меньшей температуре (например, 0oС) снижается скорость реакции.
Существенные отличия предлагаемого способа.
В предлагаемом способе используются в качестве исходных соединений -олефину не приводит к существенному увеличению выхода целевых продуктов. Использование катализатора менее 0,8 мол.% снижает выход АОС (1) и (2), что связано, возможно, со снижением каталитически активных центров в реакционной массе.
Проведение реакции при более высокой температуре (например, 40oС) не приводит к увеличению выхода целевых продуктов. При меньшей температуре (например, 0oС) снижается скорость реакции.
Существенные отличия предлагаемого способа.
В предлагаемом способе используются в качестве исходных соединений  -олефины, Еt3А1, альдегиды, катализаторы Cp2ZrC12 и CuCl, которые обуславливают образование 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2). В известном способе применяются в качестве исходных соединений аллиловый спирт, i-Вu3Al и i-Bu2AlH.
Предлагаемый способ обладает следующими преимуществами.
1. Способ позволяет получать 1-этил-3,6-диалкилциклогептаоксаланы (1) и 1-этил-3,5-диалкилциклогептаоксаланы (2), синтез которых в литературе не описан.
Способ поясняется следующими примерами.
Пример 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке в атмосфере аргона, помещают 10 ммоль октена-1, 12 ммоль Еt3А1, 0,5 ммоль Cp2ZrCl2 и перемешивают 8 часов, затем добавляют 6 мл гексана, охлаждают до -10oС, добавляют 1 ммоль CuC1 и 12 ммоль масляного альдегида. Температуру доводят до комнатной и перемешивают 8 часов.
Получают 1-этил-3-пропил-6-гексилциклогептаоксалан (1) и 1-этил-3-пропил-5-гексилциклогептаоксалан (2) с общим выходом 72% и соотношением (1): (2)~1,5:1.
Общий выход и соотношение целевых продуктов определяли по продуктам гидролиза. При гидролизе полученных 1-этил-3-пропил-6-гексилциклогептаоксалана (1) и 1-этил-3-пропил-5-гексилциклогептаоксалана (2) образуются 7-метилтридеканол-4 (5) и 6-этилдодеканол-4 (6), идентифицированные спектральными методами. (Далее см. схему 4).
Спектр ЯМР 13С ( -олефины, Еt3А1, альдегиды, катализаторы Cp2ZrC12 и CuCl, которые обуславливают образование 1-этил-3,6-диалкилциклогептаоксаланов (1) и 1-этил-3,5-диалкилциклогептаоксаланов (2). В известном способе применяются в качестве исходных соединений аллиловый спирт, i-Вu3Al и i-Bu2AlH.
Предлагаемый способ обладает следующими преимуществами.
1. Способ позволяет получать 1-этил-3,6-диалкилциклогептаоксаланы (1) и 1-этил-3,5-диалкилциклогептаоксаланы (2), синтез которых в литературе не описан.
Способ поясняется следующими примерами.
Пример 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке в атмосфере аргона, помещают 10 ммоль октена-1, 12 ммоль Еt3А1, 0,5 ммоль Cp2ZrCl2 и перемешивают 8 часов, затем добавляют 6 мл гексана, охлаждают до -10oС, добавляют 1 ммоль CuC1 и 12 ммоль масляного альдегида. Температуру доводят до комнатной и перемешивают 8 часов.
Получают 1-этил-3-пропил-6-гексилциклогептаоксалан (1) и 1-этил-3-пропил-5-гексилциклогептаоксалан (2) с общим выходом 72% и соотношением (1): (2)~1,5:1.
Общий выход и соотношение целевых продуктов определяли по продуктам гидролиза. При гидролизе полученных 1-этил-3-пропил-6-гексилциклогептаоксалана (1) и 1-этил-3-пропил-5-гексилциклогептаоксалана (2) образуются 7-метилтридеканол-4 (5) и 6-этилдодеканол-4 (6), идентифицированные спектральными методами. (Далее см. схему 4).
Спектр ЯМР 13С ( , м.д.) 7-метилтридеканола-4 (5): 14,09 к (С1), 18,80 т (С2), 34,95 т (С3), 72,04 д (С4), 39,63 т (С5), 27,09 т (С6), 32,90 д (С7), 27,02 т (С8), 32,81 т (С9), 26,65 т (С10), 31,92 т (С11), 22,66 т (С12), 14,06 к (С13), 19,68 к (С14).
Спектр ЯМР 13С ( , м.д.) 7-метилтридеканола-4 (5): 14,09 к (С1), 18,80 т (С2), 34,95 т (С3), 72,04 д (С4), 39,63 т (С5), 27,09 т (С6), 32,90 д (С7), 27,02 т (С8), 32,81 т (С9), 26,65 т (С10), 31,92 т (С11), 22,66 т (С12), 14,06 к (С13), 19,68 к (С14).
Спектр ЯМР 13С ( , м.д.): 6-этилдодеканола-4 (6): 14,10 к (С1), 18,83 т (С2), 32,95 т (С3), 69,70 д (С4), 41,81 т (С5), 35,53 д (С6), 40,39 т (С7), 26,64 т (С8), 29,89 т (С9), 31,91 т (С10), 22,66 т (С11), 14,06 к (С12), 25,54 т (С13), 10,84 к (С14).
Другие примеры, подтверждающие способ, приведены в таблице 1.
Реакции проводили при комнатной температуре (20-22oС) в гексане. Соотношение продуктов (1) и (2) составляло во всех опытах ~1.5:1. , м.д.): 6-этилдодеканола-4 (6): 14,10 к (С1), 18,83 т (С2), 32,95 т (С3), 69,70 д (С4), 41,81 т (С5), 35,53 д (С6), 40,39 т (С7), 26,64 т (С8), 29,89 т (С9), 31,91 т (С10), 22,66 т (С11), 14,06 к (С12), 25,54 т (С13), 10,84 к (С14).
Другие примеры, подтверждающие способ, приведены в таблице 1.
Реакции проводили при комнатной температуре (20-22oС) в гексане. Соотношение продуктов (1) и (2) составляло во всех опытах ~1.5:1.
Формула изобретения
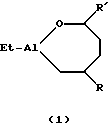 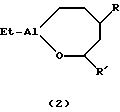 где R= н-C4H9, н-C6H13; R’= н-C3H7, i-C3H7, н-C5H11, отличающийся тем, что  -олефины формулы -олефины формулы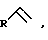 где R – как определено выше подвергают взаимодействию с триэтилалюминием (AlEt3) в присутствии катализатора цирконацендихлорида (Cp2ZrCl2) в мольном соотношении 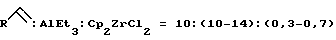 в атмосфере аргона в течение 8 ч с последующим добавлением гексана, охлаждением реакционной массы до -10oС и добавлением катализатора однохлористой меди (CuCl) и альдегида формулы в атмосфере аргона в течение 8 ч с последующим добавлением гексана, охлаждением реакционной массы до -10oС и добавлением катализатора однохлористой меди (CuCl) и альдегида формулыR’-CHO, где R’ – как определено выше, в мольном соотношении CuCl : R’CHO= (0,8-1,2): (10-14) и перемешиванием реакционной массы в течение 6-10 ч при комнатной температуре и нормальном давлении. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 27.02.2003
Номер и год публикации бюллетеня: 18-2004
Извещение опубликовано: 27.06.2004
|
||||||||||||||||||||||||||
