Патент на изобретение №2189596
|
||||||||||||||||||||||||||
(54) СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФОРМАЛЬДЕГИДА, АЦЕТАЛЬДЕГИДА, ПРОПИОНОВОГО И МАСЛЯНОГО АЛЬДЕГИДОВ В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ
(57) Реферат: Изобретение относится к области медицины, в частности к медицинским, токсикологическим исследованиям. Способ обеспечивает расширение спектра определяемых компонентов из одной пробы мочи, повышение чувствительности и точности определения. Обрабатывают анализируемую пробу солянокислым раствором 2,4-динитрофенилгидразина и гексаном, гексановый экстракт высушивают, высушенный остаток растворяют в потоке элюента, состоящего из смеси ацетонитрила и воды при их объемном соотношении 60 : 40, и определяют содержание альдегида по калибровочному графику, при этом перед введением гексана в пробу последнюю подкисляют концентрированной соляной кислотой до рН=1-2, а растворение высушенного остатка производят в элюенте, дополнительно содержащем по объему 2,0-2,5% ледяной уксусной кислоты и 1,0-1,5% диэтиламина. 2 з.п.ф-лы, 3 табл. Изобретение относится к области медицины, в частности к медицинским, токсикологическим исследованиям, и может быть использовано при диагностике экологически обусловленной патологии, вызванной альдегидами, в лабораториях биохимии, специализированных учреждениях и клинико-диагностических лабораториях медицинских учреждений. Большая часть современных методов определения альдегидов представлена колориметрическими методами определения формальдегида и ацетальдегида в различных субстратах, например, при взаимодействии с хромотроповой или фуксинсернистой кислотой. При наличии формальдегида или ацетальдегида в пробе появляется характерное окрашивание, по интенсивности которого определяют содержание альдегида в пробе. Чувствительность указанных известных методов составляет 0,03 мкг в пробе (см., например, В.Ф.Крамаренко “Токсикологическая химия”, Киев, Изд-во “Выща школа”, 1989 г., с. 127; И.Д.Гадаскина и др. “Превращение и определение промышленных органических ядов в организме”., Л., Изд-во “Медицина”, 971 г., с. 153). Недостатком указанных известных способов является неспецифичность определения альдегидов, т. к. реакция взаимодействия с вышеуказанными кислотами, положенная в основу известных способов, характерна и для других альдегидов и кетонов и позволяет определять лишь их сумму. Известен также способ определения ацетальдегида в биосредах (крови и моче) методом газохроматографического анализа равновесной паровой фазы. Согласно этому способу биологическую жидкость нагревают до образования равновесной паровой фазы и анализируют газовую фазу на газовом хроматографе. Например, описан метод раздельного количественного определения этанола и этаналя в одной пробе биологического материала газохроматографическим методом в паровой фазе в интервале 0,01-5,0 мкг/мл. Чувствительность метода составляет 0,01 мкг/мл, погрешность –  5 отн.%, при анализе этаналя в концентрациях менее 0,01 мкг/мл ошибка может достигать 5 отн.%, при анализе этаналя в концентрациях менее 0,01 мкг/мл ошибка может достигать  35-40 отн.% (см., например, Баньковский А.А., Садовник М.Н., Сатановский В.И. Лабораторное дело. – 1980. – 2. – С. 89-91.).
Недостатком указанного известного способа является низкая чувствительность и недостаточная точность определения низких концентраций альдегидов.
Также известен способ количественного определения формальдегида в биосреде путем совместной обработки пробы биосреды солянокислым раствором 2,4-динитрофенилгидразина и толуолом в течение 0,5 ч с последующим газохроматографическим определением образовавшегося 2,4-динитрофенилгидразона в толуольном экстракте методом абсолютной калибровки (см. авт, свид. СССР 1097955, кл. G 01 N 33/50, от 1982 г.).
Однако указанный известный способ длителен по времени и не позволяет с достаточной степенью чувствительности определять количество альдегида.
Недостатком указанного известного способа является низкая чувствительность определения.
Технической задачей предлагаемого способа является расширение спектра определяемых компонентов из одной пробы мочи, обеспечение селективности, повышение чувствительности и точности определения.
Указанная техническая задача достигается способом количественного определения формальдегида, ацетальдегида, пропионового и масляного альдегидов в моче методом жидкостной хроматографии, согласно которому производят последовательную обработку анализируемой пробы солянокислым раствором 2,4-динитрофенилгидразина и гексаном, выделение гексанового экстракта, его высушивание, растворение высушенного остатка в элюенте, состоящем из смеси ацетонитрила и воды при их объемном соотношении 60:40, и определение содержания альдегида по калибровочному графику, при этом перед введением гексана в пробу последнюю подкисляют концентрированной хлористоводородной кислотой до рН 1-2, а растворение высушенного остатка производят в элюенте, дополнительно содержащем по объему 2,0 – 2,5% ледяной уксусной кислоты и 1,0 – 1,5 % диэтиламина.
Кроме того, количественное определение по предлагаемому способу проводят методом абсолютной калибровки по стандартным растворам альдегидов в моче, предварительно обработанным аналогично анализируемым пробам.
Экспериментальным путем было обнаружено, что добавление к пробе мочи солянокислого раствора 2,4-динитрофенилгидразина (2,4-ДНФГ), в частности 0,20%-ного раствора 2,4-динитрофенилгидразина, в 2 М хлористоводородной кислоте (HCL), и последующее подкисление пробы концентрированной хлористоводородной кислотой до рН=1-2 позволяет более полно проводить реакцию превращения альдегидов в 2,4-динитрофенилгидразонпроизводные.
Данные о степени превращения формальдегида, ацетальдегида, пропионового и масляного альдегидов в соответствующие 2,4-динитрофенилгидразон производные этих альдегидов в различных условиях приведены в таблице 1.
Данные, приведенные в таблице 1, показывают, что оптимальный эффект превращения альдегидов в соответствующие 2,4-динитрофенилгидразон производные наблюдается при использовании 2,5 мл 0,20%-ного раствора 2,4-динитрофенилгидразина в 2 М хлористоводородной кислоте и 0,2 мл концентрированной хлористоводородной кислоты в качестве реагентов при проведении реакции дериватизации, т. к. только при создании в пробе мочи рН=1-2 (за счет прибавления концентрированной хлористоводородной кислоты), обеспечивается наиболее полная степень превращения альдегидов в 2,4-динитрофенилгидразон производные.
Для обеспечения селективности и расширения спектра определяемых компонентов из одной пробы путем достижения эффективного хроматографического разделения смеси 2,4-динитрофенилгидразонов формальдегида, ацетальдегида, пропионового и масляного альдегидов на обращенно-фазном сорбенте к известному элюенту, содержащему ацетонитрил и воду в соотношении 60:40 по объему, добавляют модификаторы, в качестве которых используют ледяную уксусную кислоту и диэтиламин. Уксусная кислота добавляется в элюент в предложенном объемном соотношении 2,0-2,5% до установления реакции среды рН=2,0 с целью смещения равновесия “диссоциированная форма-молекулярная форма” в сторону образования мономерных молекул 2,4-динитрофенилгидразонов. Диэтиламин добавляют в объемном соотношении 1,0-1,5% для образования на поверхности адсорбента ассоциата “адсорбат-компонент элюента”. Тем самым достигается симметричная форма и сужение основания хроматографических пиков 2,4-динитрофенилгидразонов альдегидов и обеспечивается высокая эффективность разделения исследуемых веществ (коэффициент разделения Kp 35-40 отн.% (см., например, Баньковский А.А., Садовник М.Н., Сатановский В.И. Лабораторное дело. – 1980. – 2. – С. 89-91.).
Недостатком указанного известного способа является низкая чувствительность и недостаточная точность определения низких концентраций альдегидов.
Также известен способ количественного определения формальдегида в биосреде путем совместной обработки пробы биосреды солянокислым раствором 2,4-динитрофенилгидразина и толуолом в течение 0,5 ч с последующим газохроматографическим определением образовавшегося 2,4-динитрофенилгидразона в толуольном экстракте методом абсолютной калибровки (см. авт, свид. СССР 1097955, кл. G 01 N 33/50, от 1982 г.).
Однако указанный известный способ длителен по времени и не позволяет с достаточной степенью чувствительности определять количество альдегида.
Недостатком указанного известного способа является низкая чувствительность определения.
Технической задачей предлагаемого способа является расширение спектра определяемых компонентов из одной пробы мочи, обеспечение селективности, повышение чувствительности и точности определения.
Указанная техническая задача достигается способом количественного определения формальдегида, ацетальдегида, пропионового и масляного альдегидов в моче методом жидкостной хроматографии, согласно которому производят последовательную обработку анализируемой пробы солянокислым раствором 2,4-динитрофенилгидразина и гексаном, выделение гексанового экстракта, его высушивание, растворение высушенного остатка в элюенте, состоящем из смеси ацетонитрила и воды при их объемном соотношении 60:40, и определение содержания альдегида по калибровочному графику, при этом перед введением гексана в пробу последнюю подкисляют концентрированной хлористоводородной кислотой до рН 1-2, а растворение высушенного остатка производят в элюенте, дополнительно содержащем по объему 2,0 – 2,5% ледяной уксусной кислоты и 1,0 – 1,5 % диэтиламина.
Кроме того, количественное определение по предлагаемому способу проводят методом абсолютной калибровки по стандартным растворам альдегидов в моче, предварительно обработанным аналогично анализируемым пробам.
Экспериментальным путем было обнаружено, что добавление к пробе мочи солянокислого раствора 2,4-динитрофенилгидразина (2,4-ДНФГ), в частности 0,20%-ного раствора 2,4-динитрофенилгидразина, в 2 М хлористоводородной кислоте (HCL), и последующее подкисление пробы концентрированной хлористоводородной кислотой до рН=1-2 позволяет более полно проводить реакцию превращения альдегидов в 2,4-динитрофенилгидразонпроизводные.
Данные о степени превращения формальдегида, ацетальдегида, пропионового и масляного альдегидов в соответствующие 2,4-динитрофенилгидразон производные этих альдегидов в различных условиях приведены в таблице 1.
Данные, приведенные в таблице 1, показывают, что оптимальный эффект превращения альдегидов в соответствующие 2,4-динитрофенилгидразон производные наблюдается при использовании 2,5 мл 0,20%-ного раствора 2,4-динитрофенилгидразина в 2 М хлористоводородной кислоте и 0,2 мл концентрированной хлористоводородной кислоты в качестве реагентов при проведении реакции дериватизации, т. к. только при создании в пробе мочи рН=1-2 (за счет прибавления концентрированной хлористоводородной кислоты), обеспечивается наиболее полная степень превращения альдегидов в 2,4-динитрофенилгидразон производные.
Для обеспечения селективности и расширения спектра определяемых компонентов из одной пробы путем достижения эффективного хроматографического разделения смеси 2,4-динитрофенилгидразонов формальдегида, ацетальдегида, пропионового и масляного альдегидов на обращенно-фазном сорбенте к известному элюенту, содержащему ацетонитрил и воду в соотношении 60:40 по объему, добавляют модификаторы, в качестве которых используют ледяную уксусную кислоту и диэтиламин. Уксусная кислота добавляется в элюент в предложенном объемном соотношении 2,0-2,5% до установления реакции среды рН=2,0 с целью смещения равновесия “диссоциированная форма-молекулярная форма” в сторону образования мономерных молекул 2,4-динитрофенилгидразонов. Диэтиламин добавляют в объемном соотношении 1,0-1,5% для образования на поверхности адсорбента ассоциата “адсорбат-компонент элюента”. Тем самым достигается симметричная форма и сужение основания хроматографических пиков 2,4-динитрофенилгидразонов альдегидов и обеспечивается высокая эффективность разделения исследуемых веществ (коэффициент разделения Kp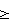 1), что, в свою очередь, повышает чувствительность определения.
Эффективность разделения альдегидов, рассчитанная из хроматограмм, и чувствительность определения смеси 2,4-динитрофенилгидразонов формальдегида, ацетальдегида, пропионового и масляного альдегидов представлены в таблице 2.
Данные, приведенные в таблице 2, показывают, что только при 1), что, в свою очередь, повышает чувствительность определения.
Эффективность разделения альдегидов, рассчитанная из хроматограмм, и чувствительность определения смеси 2,4-динитрофенилгидразонов формальдегида, ацетальдегида, пропионового и масляного альдегидов представлены в таблице 2.
Данные, приведенные в таблице 2, показывают, что только придобавлении в элюирующую жидкость модификаторов в количестве 2,0-2,5 об.% уксусной кислоты и 1,0-1,5 об. % диэтиламина обеспечивается эффективное разделение 2,4-динитрофенилгидразонов альдегидов и увеличение чувствительности определения альдегидов из одной пробы. При осуществлении предлагаемого способа проводят следующие операции в нижеуказанной последовательности: – берут пробу мочи, содержащую формальдегид, ацетальдегид, пропионовый и масляный альдегид; – добавляют солянокислый раствор 2,4-динитрофенилгидразина; – вводят концентрированную хлористоводородную кислоту до рН 1-2; – затем в пробу мочи добавляют гексан и смесь встряхивают в течение 10 минут для проведения экстракции образующихся 2,4-динитрофенилгидразонов альдегидов; – после расслоения жидкостей отбирают верхний (гексановый) слой и центрифугируют; – отбирают аликвотную часть экстракта и высушивают под ИК-лампой; – высушенный остаток растворяют в элюенте, содержащем ацетонитрил и воду в объемном соотношении 60:40, а также добавленных к этому количеству 2,0-2,5 об. % ледяной уксусной и 1.0-1,5 об.% диэтиламина, и подвергают хроматографическому анализу; – количество альдегидов определяют с использованием калибровочного графика, который строят методом абсолютной калибровки. Пример 1. Брали 50 см3 мочи, содержащей формальдегид, ацетальдегид, пропионовый и масляный альдегид. В эту пробу добавляли 2,5 мл 0,2%-ного раствора 2,4-динитрофенилгидразина в 2 М хлористоводородной кислоте и 0,2 мл концентрированной хлористоводородной кислоты. Затем добавляли гексан в количестве 5 мл. Полученную смесь встряхивали в течение 10 минут для лучшего осуществления экстракции гексаном образующихся 2,4-динитрофенилгидразонов альдегидов. Полученный экстракт центрифугировали для лучшего разделения фаз в течение 20 мин со скроростью 1500 об/мин. Отбирали 2,0 мл гексанового экстракта, высушивали его под ИК-лампой досуха, остаток растворяли в элюенте и анализировали на жидкостном хроматографе “Милихром-4” в ультрафиолетовом свете при длине волны 360 нм на колонке 8 см х 3 мм, заполненной Диасорб C16. При этом элюент, содержащий растворители: ацетонитрил: вода=60:40 (по объему)+2,5 об. % ледяной уксусной кислоты +1,0 об.% диэтиламина, прогоняли через колонку со скоростью 100 мкл/мин. Затем, используя ранее построенные калибровочные графики, проводили количественное определение формальдегида, ацетальдегида, пропионового и масляного альдегидов в моче. Для построения калибровочных графиков использовали пробы мочи, отобранные у контрольной группы детей, проживающих в экологически благополучной местности, и содержащие заданные концентрации формальдегида, ацетальдегида, пропионового и масляного альдегидов. Определение проводили аналогично примеру 1 за исключением того, что при построении калибровочных графиков полученный остаток, растворенный в элюенте, – стандартный раствор каждой пробы, анализировали на хроматографе не менее 5 раз. В результате проведенных лабораторных исследований было установлено, что чувствительность определения формальдегида, ацетальдегида и пропионового альдегида в моче предлагаемым способом составляет 0,001 мкг/см3, масляного альдегида – 0,0009 мкг/см3. Также в ходе лабораторных испытаний устанавливали точность (относительную погрешность) определения предлагаемым способом концентраций формальдегида, ацетальдегида, пропионового и масляного альдегидов в моче при их совместном присутствии. Полученные данные приведены в таблице 3. Данные, приведенные в таблице 3, показывают, что погрешность определения формальдегида предлагаемым способом составляет 7,24%, ацетальдегида – 9,67%, пропионового альдегида – 7,91%, масляного альдегида – 9,81%. Таким образом, предлагаемым способом можно с высокой степенью точности и чувствительности определять формальдегид, ацетальдегид, пропионовый и масляный альдегиды в моче при их совместном присутствии в пробе. Применение предлагаемого способа позволяет повысить чувствительность определения по формальдегиду в 89 раз по сравнению с прототипом. Формула изобретения
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.05.2003
Извещение опубликовано: 20.04.2005 БИ: 11/2005
|
||||||||||||||||||||||||||
