Патент на изобретение №2188203
|
||||||||||||||||||||||||||
(54) 2′,3′-ДИДЕГИДРО-2′,3′-ДИДЕЗОКСИТИМИДИН-5′[(ЭТОКСИКАРБОНИЛ)(ЭТИЛ)ФОСФОНАТ]- ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА
(57) Реферат: Изобретение относится к области молекулярной биологии, вирусологии и медицины, а именно к новому 2 ,3 -дидезокси-2 ,3 -дидегидротимидина (d4T) – 2′,3′-дидегидро-2′,3′-дидезоксимитидин -5′[(этоксикарбонил) (этил)фосфонату] в качестве ингибитора ВИЧ. Антивирусная активность нового соединения в отношении ВИЧ превышает таковую для d4T. 1 ил., 1 табл. Изобретение относится к области молекулярной биологии, вирусологии и медицины, а именно к применению новых производных нуклеозидов для подавления репродукции вируса иммунодефицита человека. В настоящее время известен целый ряд соединений, обладающих противовирусной активностью в отношении ВИЧ, в том числе и используемых в медицинской практике. К ним относятся такие производные нуклеозидов, как 3 -азидо-3 -дезокситимидин (AZT), 2’3′-дидезоксицитидин, 2’3′-дидезоксиинозин, 2’3′-дидезокси-2’3′-дидегидротимидин и 2’3′-дидезокси-3′-тиотимидин [1-4]. Механизм действия указанных соединений состоит в проникновении в инфицированные клетки, где они подвергаются трифосфорилированию и специфично блокируют синтез ДНК, катализируемый обратной транскриптазой ВИЧ. Однако по сравнению с природными нуклеозидами процесс фосфорилирования модифицированных нуклеозидов клеточными ферментами происходит значительно менее эффективно, что дает время проникшему в клетки вирусу интегрироваться в геном в форме провирусной ДНК. Кроме этого, необходимость создания новых модифицированных производных нуклеозидов диктуется достаточно высокой токсичностью применяемых препаратов (AZT) и появлением резистентных штаммов даже в случае комбинированного лечения [5,6]. Технической задачей изобретения является создание новых нуклеозидных производных, высокоэффективных в отношении ВИЧ, устойчивых к действию ферментов дефосфорилирования, способных проникать внутрь клетки и обладающих избирательной активностью в подавлении синтеза ДНК, катализируемого обратной транскриптазой ВИЧ. Задача решена тем, что согласно изобретению заявляется новое соединение – производное 2’3′-дидезокси-2’3′-дидегидротимидина (d4T) [прототип; 4]-2′, 3′-дидегидро-2′, 3′-дидезокситимидин-5′[(этоксикарбонил) (этил)фосфонат], с химической формулой: 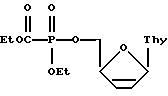 Ингибирование репродукции ВИЧ включает культивирование первично инфицированных лимфоидных клеток МТ-4 в присутствии исследуемого препарата, конечная концентрация которого в культуральной среде составляет 0,001-100 мкг/мл, на протяжении одного пассажа – в течение 4 суток. Об ингибировании репродукции ВИЧ в культуре чувствительных клеток судят по снижению накопления вирусспецифического белка р24 (по данным иммуноферментного анализа), а также по увеличению жизнеспособности клеток в присутствии препарата по сравнению с контролем, определяемому на 4 сутки культивирования методом исключения трипанового синего. Из полученных экспериментальных данных, приведенных в таблице, видно, что исследуемый препарат, помимо спрособности защищать клетки от гибели (>50% в дозе 0,28 мкМ/мл), в высокой степени подавляет репродукцию вируса иммунодефицита 1 типа в культуре клеток МТ-4 (>50% в дозе 0,0027 мкМ/мл и >90% в дозе 0,28 мкМ/мл), что соответственно в 100 и 10 раз превышает аналогичные характеристики для d4T. Терапевтический индекс исследуемого соединения (отношение токсической дозы препарата к его эффективной дозе) в 200 раз больше, чем у d4T (таблица). Фиг. 1. Анти-ВИЧ действие 2′, 3′-дидегидро-2′, 3′-дидезокситимидин-5′[(этоксикарбонил) (этил)фосфоната]:  – токсичность препарата; % жизнеспособности клеток МТ-4 по отношению к контролю, – токсичность препарата; % жизнеспособности клеток МТ-4 по отношению к контролю, – защита клеток; % по отношению к контролю вируса, – защита клеток; % по отношению к контролю вируса, – ингибирование р24.
Ниже приведены конкретные примеры, раскрывающие сущность изобретения.
Пример 1. Синтез 2′,3′-дидегидро-2′,3′-дидезокситимидин-5′[(этоксикарбонил) (этил)фосфоната].
К раствору диэтил[(этокси)карбонил]фосфоната (190 мкл, 1 ммоль) в абсолютном CCl4 (10 мл) добавляют PCl5 (210 мг, 1 ммоль). Кипятят с обратным холодильником 3 часа. Упаривают растворитель, сухой остаток растворяют в диметилформамиде (4 мл). Полученный раствор охлаждают до -50oС и добавляют охлажденный до той же температуры раствор 2 ,3 -дидeгидpo-2 ,3 -дидезокситимидина (70 мг, 0.3 ммоль) в диметилформамиде (2 мл). Перемешивают ночь при комнатной температуре. Упаривают растворитель. Остаток хроматографируют на колонке с силикагелем (2 – ингибирование р24.
Ниже приведены конкретные примеры, раскрывающие сущность изобретения.
Пример 1. Синтез 2′,3′-дидегидро-2′,3′-дидезокситимидин-5′[(этоксикарбонил) (этил)фосфоната].
К раствору диэтил[(этокси)карбонил]фосфоната (190 мкл, 1 ммоль) в абсолютном CCl4 (10 мл) добавляют PCl5 (210 мг, 1 ммоль). Кипятят с обратным холодильником 3 часа. Упаривают растворитель, сухой остаток растворяют в диметилформамиде (4 мл). Полученный раствор охлаждают до -50oС и добавляют охлажденный до той же температуры раствор 2 ,3 -дидeгидpo-2 ,3 -дидезокситимидина (70 мг, 0.3 ммоль) в диметилформамиде (2 мл). Перемешивают ночь при комнатной температуре. Упаривают растворитель. Остаток хроматографируют на колонке с силикагелем (2 25 см), элюируя системой хлороформ-метанол 96:4. Выход 89%. УФ (H2O, 25 см), элюируя системой хлороформ-метанол 96:4. Выход 89%. УФ (H2O,  макс): 266 нм. 1Н ЯМР (CDCl3), макс): 266 нм. 1Н ЯМР (CDCl3),  м.д.: 8.50с (1Н, NH), 7.28с, 7,30с (1Н, Н6,),7.01с (1Н, Н1′), 6.32м (1Н, Н3′), 5.91м (1Н, Н2′), 5.00м (1Н, Н4′), 4.42м (2Н, Н5′), 4.31м (4Н, м.д.: 8.50с (1Н, NH), 7.28с, 7,30с (1Н, Н6,),7.01с (1Н, Н1′), 6.32м (1Н, Н3′), 5.91м (1Н, Н2′), 5.00м (1Н, Н4′), 4.42м (2Н, Н5′), 4.31м (4Н, 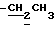 ), 1.88с (3Н, СН3), 1.37 м, 1.32м (6Н, ), 1.88с (3Н, СН3), 1.37 м, 1.32м (6Н,  ). 31Р ЯМР (CD3CN), ). 31Р ЯМР (CD3CN),  ppm: -5.96 с, -6.25 с.
Пример 2. Оценка цитотоксичности соединения. Цитотоксичность препарата оценивают путем добавления его разведений в среде RPMI-1640 к клеточной суспензии МТ-4, помещенной в лунки 96-луночного планшета (“Cel-Cult”, England), до конечных концентраций 0,001-100 мкг/мл (по три лунки на каждую дозу) с последующим культивированием при 37oС в течение 4 суток. Посевная концентрация составляет 0,5 ppm: -5.96 с, -6.25 с.
Пример 2. Оценка цитотоксичности соединения. Цитотоксичность препарата оценивают путем добавления его разведений в среде RPMI-1640 к клеточной суспензии МТ-4, помещенной в лунки 96-луночного планшета (“Cel-Cult”, England), до конечных концентраций 0,001-100 мкг/мл (по три лунки на каждую дозу) с последующим культивированием при 37oС в течение 4 суток. Посевная концентрация составляет 0,5 106 клеточных частиц в миллилитре. Контролем служат клетки без добавления препарата. Жизнеспособность клеток подсчитывают в камере Горяева с предварительным окрашиванием трипановым синим. Токсичность различных доз препарата определяют по жизнеспособности клеток относительно контроля (см. чертеж), по полученным результатам рассчитывают дозу, на 50% снижающую жизнеспособность клеток (CD50). Данные приведены в таблице. Следует отметить, что токсическое действие на клетки МТ-4, выражающееся в изменении их морфологии, снижении репродуктивности и жизнеспособности, оказывают только высокие концентрации препарата (>150 мкМ/мл), что более чем в два раза выше, чем у d4T и в 50000 раз превышает эффективные в отношении ВИЧ-1 дозы (таблица).
Пример 3. Изучение влияния исследуемого препарата на репродукцию ВИЧ-1 в культуре клеток МТ-4.
Исследование противовирусной активности препарата в отношении ВИЧ-1 проводят на перевиваемой линии чувствительных клеток МТ-4. Для заражения используют супернатант инфицированных клеток, хранившийся в жидком азоте, множественность заражения составляет 0,2-0,5 инфекционных единиц на клетку. Суспензию клеток МТ-4 с концентрацией 2,0 106 клеточных частиц в миллилитре. Контролем служат клетки без добавления препарата. Жизнеспособность клеток подсчитывают в камере Горяева с предварительным окрашиванием трипановым синим. Токсичность различных доз препарата определяют по жизнеспособности клеток относительно контроля (см. чертеж), по полученным результатам рассчитывают дозу, на 50% снижающую жизнеспособность клеток (CD50). Данные приведены в таблице. Следует отметить, что токсическое действие на клетки МТ-4, выражающееся в изменении их морфологии, снижении репродуктивности и жизнеспособности, оказывают только высокие концентрации препарата (>150 мкМ/мл), что более чем в два раза выше, чем у d4T и в 50000 раз превышает эффективные в отношении ВИЧ-1 дозы (таблица).
Пример 3. Изучение влияния исследуемого препарата на репродукцию ВИЧ-1 в культуре клеток МТ-4.
Исследование противовирусной активности препарата в отношении ВИЧ-1 проводят на перевиваемой линии чувствительных клеток МТ-4. Для заражения используют супернатант инфицированных клеток, хранившийся в жидком азоте, множественность заражения составляет 0,2-0,5 инфекционных единиц на клетку. Суспензию клеток МТ-4 с концентрацией 2,0 106 клеточных частиц в миллилитре и жизнеспособностью не менее 90% помещают в лунки 96-луночного планшета (“Cel-Cult”, England) непосредственно после внесения вируссодержащего материала и сразу же добавляют исследуемые препараты, разведенные в среде RPMI-1640 без сыворотки, до конечных концентраций 0,001-100 мкг/мл (по три лунки на каждую дозу). Контролями служат инфицированные ВИЧ-1 клетки МТ-4 без добавления препарата (вместо препарата вносят такое же количество среды RPMI-1640 без добавок) и неинфицированные клетки.
Планшет инкубируют в течение часа при 37oС для адсорбции вируса, затем клетки разводят до посевной концентрации (0,5 106 клеточных частиц в миллилитре и жизнеспособностью не менее 90% помещают в лунки 96-луночного планшета (“Cel-Cult”, England) непосредственно после внесения вируссодержащего материала и сразу же добавляют исследуемые препараты, разведенные в среде RPMI-1640 без сыворотки, до конечных концентраций 0,001-100 мкг/мл (по три лунки на каждую дозу). Контролями служат инфицированные ВИЧ-1 клетки МТ-4 без добавления препарата (вместо препарата вносят такое же количество среды RPMI-1640 без добавок) и неинфицированные клетки.
Планшет инкубируют в течение часа при 37oС для адсорбции вируса, затем клетки разводят до посевной концентрации (0,5 106 в миллилитре) питательной средой RPMI-1640 с добавлением 10% фетальной сыворотки КРС, предварительно инактивированной прогреванием при 56oС в течение 30 минут, 300 мг/мл L-глютамина и 100 мкг/мл гентамицина. Затем планшет помещают в термостат на 37oС в атмосфере 5% СО2. На 4 сутки культивирования подсчитывают концентрацию и жизнеспособность клеток методом исключения трипанового синего. В лунки планшета добавляют Твин-80 до конечной концентрации 0,1% и оставляют его на 24 часа при 4oС для инактивации ВИЧ. По полученным данным строят график зависимости прироста жизнеспособности клеток относительно контроля под действием возрастающих доз препарата (см. чертеж), т.е. определяют способность препарата защищать инфицированные клетки от цитопатогенного действия вируса (таблица). Затем проводят оценку анти-ВИЧ активности соединения с использованием количественного определения вирусспецифического белка р24 методом прямого иммуноферментного анализа, как описано в [10], и строят дозозависимую кривую, по которой рассчитывают концентрации, на 50 и 90% подавляющие прирост вирусного антигена (ID50 и ID90). Результаты представлены в таблице. На основании этих количественных показателей ингибирования можно судить об эффективности противовирусного действия препарата, заключающейся в высокой степени подавления размножения ВИЧ-1 в культуре клеток МТ-4 и превышающей эффективность d4T.
Относительную степень защиты инфицированных клеток от гибели различными дозами препарата рассчитывают по формуле: 106 в миллилитре) питательной средой RPMI-1640 с добавлением 10% фетальной сыворотки КРС, предварительно инактивированной прогреванием при 56oС в течение 30 минут, 300 мг/мл L-глютамина и 100 мкг/мл гентамицина. Затем планшет помещают в термостат на 37oС в атмосфере 5% СО2. На 4 сутки культивирования подсчитывают концентрацию и жизнеспособность клеток методом исключения трипанового синего. В лунки планшета добавляют Твин-80 до конечной концентрации 0,1% и оставляют его на 24 часа при 4oС для инактивации ВИЧ. По полученным данным строят график зависимости прироста жизнеспособности клеток относительно контроля под действием возрастающих доз препарата (см. чертеж), т.е. определяют способность препарата защищать инфицированные клетки от цитопатогенного действия вируса (таблица). Затем проводят оценку анти-ВИЧ активности соединения с использованием количественного определения вирусспецифического белка р24 методом прямого иммуноферментного анализа, как описано в [10], и строят дозозависимую кривую, по которой рассчитывают концентрации, на 50 и 90% подавляющие прирост вирусного антигена (ID50 и ID90). Результаты представлены в таблице. На основании этих количественных показателей ингибирования можно судить об эффективности противовирусного действия препарата, заключающейся в высокой степени подавления размножения ВИЧ-1 в культуре клеток МТ-4 и превышающей эффективность d4T.
Относительную степень защиты инфицированных клеток от гибели различными дозами препарата рассчитывают по формуле:Защита (%) = (А-O)/(В-O)*100, где А – % жизнеспособности инфицированных клеток в присутствии препарата на 4 сутки культивирования, В – % жизнеспособности в контроле клеток, О – % жизнеспособности инфицированных клеток без добавления препарата (контроль вируса). Относительную степень ингибирования репродукции вирусного белка считают по формуле: %ингибир.= (Рх-Ро)/(Р-Ро)*100, где Рх – концентрация белка р24 на 4 сутки культивирования в присутствии препарата, Ро – концентрация р24 после 1 часа инкубирования ВИЧ-1 с клетками без добавления препарата (“O” точка), Р – концентрация р24 на 4 сутки культивирования ВИЧ-1 в клетках без добавления препарата (контроль вируса). Терапевтический индекс, или индекс селективности (IS), определяют как отношение концентрации препарата, токсичной для 50% клеток (CD50), к концентрации, на 50% подавляющей прирост вирусного антигена (ID50): IS=CD50/ID50 Таким образом показано, что исследуемый препарат обладает способностью ингибировать репродукцию вируса иммунодефицита 1 типа в культуре клеток МТ-4, не оказывая токсического действия на клетки, причем противовирусная активность его превышает активность d4T. Это говорит о перспективности предлагаемого соединения для создания новых лекарственных форм, используемых в терапии СПИДа. Список литературы: 1. G.J.Veal, S.Agrawal. R.A. Byrn. Synergistic inhibition of HIV-1 by an antisense oligonucleotide and nucleoside analog reverse transcriptase inhibitors. Antiviral Research 1988, 38, 63-73. 2. H. Mitsuya, K. J. Weinhold, P.A.Furman, M.N.St.Clair, S. Nusinoff-Lehrman. , R. C. Gallo, D.Bolognesi, D.W.Barry, S. Broder. 3′-Azido-3′-deoxythymidine; an antiviral agent that inhibits the inefectivity and cytopathetic effect of human T-lymphotropic virus type III/lymphoadenopathy-associated virus in vitro. Proc. Nat. Acad. Sci. USA 1985, 82, 7096-7100. 3. V. M.Cardona, A.I.Ayi, A.M.Aubertin, R.Guedj. Synthesis and anti-HIV activity of some novel arylphosphate and H-phosphonate derivatives of 3′-azido-2′, 3′-dideoxythymidine and 2′, 3′-didehydro-2′,3′-dideoxythymidine. Antiviral Res 1999, 42(3), 189-196. 4. P.Herdewijn, J.Balzarini, M. A.Baba, E.De Clercq et al. 3′-Substituted 2′,3′-dideoxynucleoside analogues as potential anti-HIV (HTLV/LAV) agents. J. Med. Chem. 1987, 30, 1270-1278. 5. R.F.Schinazi, R.M.Lloyd, JR., C.S.Ramanathan and E.W.Taylor. Antiviral Drug Resistance Mutation in Human Immunodeficiency Virus T-type 1 Reverse Transcriptase Occur in Specific RNA Structural Regions. Antimicrobial Agents and Chemotherapy 1994, 38(2), 268-274. 6. V. I.Avramis, R.Kwock, M.M.Solorzano, and E.Gomperts. Evidense of In Vitro Development of Drug Resistanse to Azidothymidine in T-Lymphocytic Leukemia Cell Lines (Jurkat E6-1/AZT-100) and in Pediatric Patients with HIV-1 Infection. Journal of Acquired Immune Deficiency Syndromes 1993, 6, 1287-1296. 7. F. P. Svinarchuk, D.A.Konevetz, O.A.Pliasunova, A.G.Pokrovsky, V.V. Vlasov. Inhibition of HIV proliferation in MT-4 cells by antisense oligonucleotide conjugated to lipophilic groups. Biochimie 1993, 75, 49-54. 8. A.G. Pokrovskii, O.A.Pliasunova, V.M.Blinov, V.V.Vlasov, F.P. Svinarchuk, T.V.Abramova, V.V.Gorn and D.A. Konevetz. Inhibition of Human Immunodeficiency Virus by Sense and Antisense Oligodeoxynucleotides. Molecular Biology 1993, 27(5), N 1, 641-644. 9. Патент РФ 2144956, кл. С 12 N 7/04, опубл. 27.01.2000 г. БИ 3. Формула изобретения
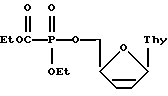 ингибитор репродукции вируса иммунодефицита человека. РИСУНКИ
|
||||||||||||||||||||||||||
