Патент на изобретение №2188015
|
||||||||||||||||||||||||||
(54) СПОСОБ ИНГИБИРОВАНИЯ НЕЙРОПЕПТИДА Y
(57) Реферат: Изобретение относится к области медицины, а именно к фармакологии. Для ингибирования рецепторов нейропептида Y, избыток которого вызывает различные физиологические расстройства, вводят эффективное количество соединения из группы 2-фенил-3-ароилбензтиофенов. Способ позволяет повысить эффективность ингибирования рецепторов нейропептида Y. 2 з.п. ф-лы, 1 табл. Нейропептид Y является пептидом, присутствующим в центральной и периферической нервных системах. Пептид существует совместно с норадреналином во многих нейронах и действует как нейротрансмиттер сам по себе или синергически вместе с ноадреналином. Волокна, содержащие нейропептид Y, окружают в большом количестве артерии в сердце, но найдены также вокруг артерий в дыхательных путях, желудочно-кишечном тракте и мочеполовых путях. Нейропептид Y присутствует также в головном мозге, оказывая влияние на кровяное давление, пищевое поведение и высвобождение различных гормонов. Изменения концентраций нейропептида Y в головном мозге причастны к этиологии психиатрических расстройств. Нейропептид Y был открыт и выделен и определены его последовательности примерно десять лет тому назад, когда его выделили из свиного мозга с определением последовательности в ходе общего скрининга с целью обнаружения амидированных пептидов с концевыми карбоксигруппами, и был назван нейропептидом Y из-за его выделения из нервной ткани и присутствия тирозина в виде аминокислоты как с концевыми аминогруппами, так и с концевыми карбоксигруппами. Нейропептид Y является представителем семейства панкреатических пептидов и находится в одном гомологическом ряду с панкреатическим полипептидом и пептидом YY. Нейропептид Y и другие представители этого семейства пептидов отличаются третичной структурой, состоящей из N-концевой полипропиленовой спирали и амфифильной  -спирали, соединенной с -спирали, соединенной с  -витком с образованием шпильковидной петли, которую иногда называют панкреатической полипептидной (РР) складкой. Спирали удерживаются вместе благодаря гидрофобным взаимодействиям. От шпильковидной петли выступает амидированная С-концевая часть.
После обнаружения нейропептида Y было установлено, что он является наиболее распространенным пептидом в центральной нервной системе, включая кору головного мозга, мозговой ствол, гиппокамп, гипоталамус, миндалевидное тело и таламус, а также присутствует в периферической нервной системе в симпатических нейронах и хромафинных клетках надпочечника.
Нейропептид Y, по-видимому, полностью удовлетворяет нейротрансмиттерным критериям, поскольку он хранится в симпатических гранулах, высвобождается при электрической стимуляции нерва и действует как специфические рецепторы. Очевидно, что нейропептид Y по праву является важным переносчиком, вероятно в мозге, где нейропептид Y, видимо, ингибирует активность аденилатциклазы и вызывает повышение внутриклеточных уровней кальция. Центральная инъекция нейропептида Y приводит к изменениям кровяного давления, увеличению питания, повышенному накоплению жира, повышенному содержанию сахара и инсулина в крови, снижению двигательной активности, пониженной температуре тела и каталепсии.
Нейропептид Y (а также его химические родственники) действует на зависимые от гуаниннуклеотидов рецепторы мембран, известные как G-протеинсвязанные рецепторы. Протеины G являются семейством мембранных протеинов, которые становятся активированными только после связывания гуанозин-трифосфата. Активированные протеины G в свою очередь активируют фермент-усилитель на внутренней поверхности мембраны, после чего фермент преобразует молекулы предшественника во вторые переносчики.
Нейропептид Y, по-видимому, взаимодействует с семейством близко родственных рецепторов. Эти рецепторы обычно классифицируют на несколько подтипов на основе способности различных тканей и рецепторов связывать различные фрагменты нейропептида Y и близко родственного пептида YY. Рецептор подтипа Y1, видимо, является основным рецептором сосудистого нейропептида Y. Рецепторы подтипов Y2 могут также появляться постсинаптически на гладкой мышце кровеносного сосуда. Пока еще не выделенным рецептором подтипа Y3 является, по-видимому, нейропептид Y специфический, не связывающий нейропептид YY. Этот рецептор, вероятно, присутствует в тканях надпочечника, мозгового вещества, сердца и ствола мозга, а также в других местах. [В отношении обзора, касающегося нейропептида и рецепторов нейропептида, смотри, например, C. Wahlestedt and D. Reis, Annual Review of Pharmacology and Toxicology, 33: 309-352 (1993)].
Ввиду большого количества заболеваний, связанных с избытком нейропептида Y, создание антагонистов рецепторов нейропептида Y обеспечит возможность контролирования этих болезненных состояний. Наиболее ранними антагонистами таких рецепторов были производные пептидов. Как было доказано, эти антагонисты имеют ограниченную фармацевтическую полезность из-за их метаболической нестойкости.
В соответствии с настоящим изобретением предлагается, по существу, класс мощных непептидных антагонистов рецепторов нейропептида Y. Благодаря их непептидной природе соединения по настоящему изобретению не имеют недостатков известных пептидных антагонистов рецепторов нейропептида Y в отношении метаболической нестойкости.
Настоящее изобретение охватывает способы лечения или предупреждения физиологического расстройства, связанного с избытком нейропептида Y, включающие введение млекопитающему, нуждающемуся в указанном лечении, эффективного количества соединения формулы 1 -витком с образованием шпильковидной петли, которую иногда называют панкреатической полипептидной (РР) складкой. Спирали удерживаются вместе благодаря гидрофобным взаимодействиям. От шпильковидной петли выступает амидированная С-концевая часть.
После обнаружения нейропептида Y было установлено, что он является наиболее распространенным пептидом в центральной нервной системе, включая кору головного мозга, мозговой ствол, гиппокамп, гипоталамус, миндалевидное тело и таламус, а также присутствует в периферической нервной системе в симпатических нейронах и хромафинных клетках надпочечника.
Нейропептид Y, по-видимому, полностью удовлетворяет нейротрансмиттерным критериям, поскольку он хранится в симпатических гранулах, высвобождается при электрической стимуляции нерва и действует как специфические рецепторы. Очевидно, что нейропептид Y по праву является важным переносчиком, вероятно в мозге, где нейропептид Y, видимо, ингибирует активность аденилатциклазы и вызывает повышение внутриклеточных уровней кальция. Центральная инъекция нейропептида Y приводит к изменениям кровяного давления, увеличению питания, повышенному накоплению жира, повышенному содержанию сахара и инсулина в крови, снижению двигательной активности, пониженной температуре тела и каталепсии.
Нейропептид Y (а также его химические родственники) действует на зависимые от гуаниннуклеотидов рецепторы мембран, известные как G-протеинсвязанные рецепторы. Протеины G являются семейством мембранных протеинов, которые становятся активированными только после связывания гуанозин-трифосфата. Активированные протеины G в свою очередь активируют фермент-усилитель на внутренней поверхности мембраны, после чего фермент преобразует молекулы предшественника во вторые переносчики.
Нейропептид Y, по-видимому, взаимодействует с семейством близко родственных рецепторов. Эти рецепторы обычно классифицируют на несколько подтипов на основе способности различных тканей и рецепторов связывать различные фрагменты нейропептида Y и близко родственного пептида YY. Рецептор подтипа Y1, видимо, является основным рецептором сосудистого нейропептида Y. Рецепторы подтипов Y2 могут также появляться постсинаптически на гладкой мышце кровеносного сосуда. Пока еще не выделенным рецептором подтипа Y3 является, по-видимому, нейропептид Y специфический, не связывающий нейропептид YY. Этот рецептор, вероятно, присутствует в тканях надпочечника, мозгового вещества, сердца и ствола мозга, а также в других местах. [В отношении обзора, касающегося нейропептида и рецепторов нейропептида, смотри, например, C. Wahlestedt and D. Reis, Annual Review of Pharmacology and Toxicology, 33: 309-352 (1993)].
Ввиду большого количества заболеваний, связанных с избытком нейропептида Y, создание антагонистов рецепторов нейропептида Y обеспечит возможность контролирования этих болезненных состояний. Наиболее ранними антагонистами таких рецепторов были производные пептидов. Как было доказано, эти антагонисты имеют ограниченную фармацевтическую полезность из-за их метаболической нестойкости.
В соответствии с настоящим изобретением предлагается, по существу, класс мощных непептидных антагонистов рецепторов нейропептида Y. Благодаря их непептидной природе соединения по настоящему изобретению не имеют недостатков известных пептидных антагонистов рецепторов нейропептида Y в отношении метаболической нестойкости.
Настоящее изобретение охватывает способы лечения или предупреждения физиологического расстройства, связанного с избытком нейропептида Y, включающие введение млекопитающему, нуждающемуся в указанном лечении, эффективного количества соединения формулы 1 где R1 и R3 независимо представляют водород, -СН3,  (C1-C6алкил) или (C1-C6алкил) или 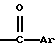 , где Аr представляет необязательно замещенный фенил; , где Аr представляет необязательно замещенный фенил;R2 выбран из группы, состоящей из пирролидино, гексаметиленимино и пиперидино; и его фармацевтически приемлемых солей и сольватов. Настоящее изобретение касается открытия того, что выбранная группа 2-фенил-3-ароилбензотиофенов формулы 1 полезна для ингибирования физиологического расстройства, связанного с избытком нейропептида Y. Терапевтическое и профилактическое лечения по настоящему изобретению осуществляют путем введения нуждающемуся в этом человеку дозы соединения формулы 1, или его фармацевтически приемлемой соли, или сольвата, эффективной для ингибирования физиологического расстройства, связанного с избытком нейропептида Y, или его симптомов. Термин “ингибирование” имеет обычное принятое значение, включающее исключение возможности, предупреждение, ограничение и замедление, прекращение или обеспечение обратного хода болезни или вызванного ею симптома. Как таковой предлагаемый способ охватывает по потребности лечение как терапевтическое, так и профилактическое. Предпочтительным соединением настоящего изобретения является ралоксифен, представляющий собой гидрохлорид (соль) соединения формулы 1, где R1 и R3 представляют водород и R2 представляет 1-пиперидинил. Как правило, по крайней мере одно соединение формулы 1 смешивают с обычными наполнителями, разбавителями или носителями и прессуют в таблетки или изготавливают в виде элексиров или растворов для удобного перорального введения или вводят внутримышечно или внутривенно. Соединения могут быть введены чрескожно или могут быть изготовлены в виде лекарственных форм отсроченного действия и тому подобное. Соединения, используемые в способах по настоящему изобретению, могут быть получены в соответствии с разработанными технологическими процессами, такими как подробно описанные в патентах США 4133814, 4418068 и 4380635, которые включены в данное описание в качестве ссылки. Обычно процесс начинают, взяв в качестве исходного соединения бензо [b] тиофен, имеющий 6-гидроксильную группу и группу 2-(4-гидроксифенил). Исходное соединение защищают, ацилируют и освобождают от защиты, получив в результате соединения формулы 1. Примеры получения таких соединений даны в указанных выше патентах США. Термин “необязательно замещенный фенил” охватывает фенил и фенил, замещенный один или два раза C1-C6 алкилом, С1-С4 алкокси, гидрокси, нитро, хлором, фтором или три(хлор или фтор)метилом. Соединения, используемые в способах по настоящему изобретению, образуют фармацевтически приемлемые кислотно- и основно-аддитивные соли с самыми разнообразными органическими и неорганическими кислотами и основаниями и включают физиологически приемлемые соли, которые часто используют в фармацевтической химии. Такие соли тоже являются частью настоящего изобретения. Типичные неорганические кислоты, используемые для получения таких солей, включают хлороводородную, бромоводородную, иодоводородную, азотную, серную, фосфорную, гипофосфорную и тому подобные кислоты. Могут быть также использованы соли, полученные из органических кислот, таких как алифатические моно-и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые кислоты и гидроксиалкановые дикислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты. Таким образом, фармацевтически приемлемые соли включают ацетат, фенилацетат, трифторацетат, акрилат, аскорбат, бензоат, хлорбензоат, динитробензоат, гидроксибензоат, метоксибензоат, метилбензоат, o-ацетоксибензоат, нафталин-2-бензоат, бромид, изобутират, фенилбутират,  -гидроксибутират, бутин-1,4-диоат, гексин-1,4-диоат, капрат, каприлат, хлорид, циннамат, цитрат, формиат, фумарат, гликоллат, гептаноат, гиппурат, лактат, малат, малеат, гидроксималеат, малонат, манделат, мезилат, никотинат, изоникотинат, нитрат, оксалат, фталат, терафталат, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, пропиолат, пропионат, фенилпропионат, салицилат, себакат, сукцинат, суберат, сульфат, бисульфат, пиросульфат, сульфит, бисульфит, сульфонат, бензолсульфонат, п-бромфенилсульфонат, хлорбензолсульфонат, этансульфонат, 2-гидроксиэтансульфонат, метансульфонат, нафталин-1-сульфонат, нафталин-2-сульфонат, п-толуолсульфонат, ксилолсульфонат, тартрат и тому подобное. Предпочтительной солью является гидрохлорид.
Фармацевтически приемлемые кислотно-аддитивные соли обычно получают взаимодействием соединения формулы 1 с эквимолярным или избыточным количеством кислоты. Реагенты обычно смешивают в совместном растворителе, таком как диэтиловый эфир или бензол. Соль обычно выпадает из раствора в осадок в пределах примерно от одного часа до 10 дней и может быть отделена путем фильтрования или путем отгонки растворителя обычным образом.
Основания, широко используемые для образования солей, включают гидроксид аммония и гидроксиды и карбонаты щелочных и щелочноземельных металлов, а также алифатические и первичные, вторичные и третичные амины, алифатические диамины. Основания, особенно пригодные для получения аддитивных солей, включают гидроксид аммония, карбонат калия, метиламин, диэтиламин, этилендиамин и циклогексиламин.
Фармацевтически приемлемые соли обычно имеют лучшие характеристики растворимости по сравнению с соединением, из которого их получают, и потому они больше подходят для изготовления лекарственных форм в виде жидкостей или эмульсий.
Фармацевтические препараты могут быть изготовлены известными в данной области техники способами. Например, соединения можно смешивать с обычными наполнителями, разбавителями или носителями и изготавливать в виде таблеток, капсул, суспензий, порошков и тому подобное. Примерами наполнителей, разбавителей и носителей, подходящих для изготовления таких лекарственных форм, являются: наполнители и сухие разбавители, такие как крахмал, сахара, маннит и производные кремния; связывающие вещества, такие как карбоксиметилцеллюлоза и другие производные целлюлозы, альгинаты, желатин и поливинилпирролидон; увлажняющие вещества, такие как глицерин; разрыхляющие вещества, такие как карбонат кальция и бикарбонат натрия; вещества для замедления процесса растворения, такие как парафин; ускорители всасывания, такие как четвертичные соединения аммония; поверхностно-активные вещества, такие как цетиловый спирт, глицеринмоностеарат; адсорбционные носители, такие как каолин и бентонит; и смазывающие вещества, такие как тальк, стеарат кальция, стеарат магния и твердые полиэтиленгликоли.
Соединения могут быть приготовлены в виде эликсиров или растворов для удобного перорального введения или в виде растворов, подходящих для парентерального введения, например внутримышечного, подкожного или внутривенного. Кроме того, соединения вполне пригодны для изготовления лекарственных форм отсроченного действия и тому подобное. Состав лекарственных форм может быть таким, чтобы он обеспечивал высвобождение активного компонента только или предпочтительно в конкретной части желудочно-кишечного тракта, возможно в течение некоторого периода времени. Могут быть изготовлены покрытия, оболочки и защитные матрицы, например, из полимерных веществ и восков.
Конкретная доза соединения формулы 1, необходимая для обеспечения ингибирования физиологического расстройства, связанного с избытком нейропептида Y, или его симптомов в соответствии с настоящим изобретением зависит от тяжести состояния, способа введения и других подобных факторов по усмотрению лечащего врача. Приемлемые эффективные суточные дозы обычно составляют от примерно 0,1 до примерно 1000 мг в сутки и более предпочтительно от примерно 50 до примерно 200 мг в сутки. Такие дозы вводят больному один-три раза в сутки или чаще в случае более эффективного лечения или предупреждения состояния или симптома(ов).
Обычно является предпочтительным вводить соединение формулы 1 в виде кислотно-аддитивной соли, как принято при введении лекарственных веществ, несущих основную группу, такую как пиперидиновое кольцо. Для таких целей годятся следующие пероральные лекарственные формы.
ПРЕПАРАТЫ -гидроксибутират, бутин-1,4-диоат, гексин-1,4-диоат, капрат, каприлат, хлорид, циннамат, цитрат, формиат, фумарат, гликоллат, гептаноат, гиппурат, лактат, малат, малеат, гидроксималеат, малонат, манделат, мезилат, никотинат, изоникотинат, нитрат, оксалат, фталат, терафталат, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, пропиолат, пропионат, фенилпропионат, салицилат, себакат, сукцинат, суберат, сульфат, бисульфат, пиросульфат, сульфит, бисульфит, сульфонат, бензолсульфонат, п-бромфенилсульфонат, хлорбензолсульфонат, этансульфонат, 2-гидроксиэтансульфонат, метансульфонат, нафталин-1-сульфонат, нафталин-2-сульфонат, п-толуолсульфонат, ксилолсульфонат, тартрат и тому подобное. Предпочтительной солью является гидрохлорид.
Фармацевтически приемлемые кислотно-аддитивные соли обычно получают взаимодействием соединения формулы 1 с эквимолярным или избыточным количеством кислоты. Реагенты обычно смешивают в совместном растворителе, таком как диэтиловый эфир или бензол. Соль обычно выпадает из раствора в осадок в пределах примерно от одного часа до 10 дней и может быть отделена путем фильтрования или путем отгонки растворителя обычным образом.
Основания, широко используемые для образования солей, включают гидроксид аммония и гидроксиды и карбонаты щелочных и щелочноземельных металлов, а также алифатические и первичные, вторичные и третичные амины, алифатические диамины. Основания, особенно пригодные для получения аддитивных солей, включают гидроксид аммония, карбонат калия, метиламин, диэтиламин, этилендиамин и циклогексиламин.
Фармацевтически приемлемые соли обычно имеют лучшие характеристики растворимости по сравнению с соединением, из которого их получают, и потому они больше подходят для изготовления лекарственных форм в виде жидкостей или эмульсий.
Фармацевтические препараты могут быть изготовлены известными в данной области техники способами. Например, соединения можно смешивать с обычными наполнителями, разбавителями или носителями и изготавливать в виде таблеток, капсул, суспензий, порошков и тому подобное. Примерами наполнителей, разбавителей и носителей, подходящих для изготовления таких лекарственных форм, являются: наполнители и сухие разбавители, такие как крахмал, сахара, маннит и производные кремния; связывающие вещества, такие как карбоксиметилцеллюлоза и другие производные целлюлозы, альгинаты, желатин и поливинилпирролидон; увлажняющие вещества, такие как глицерин; разрыхляющие вещества, такие как карбонат кальция и бикарбонат натрия; вещества для замедления процесса растворения, такие как парафин; ускорители всасывания, такие как четвертичные соединения аммония; поверхностно-активные вещества, такие как цетиловый спирт, глицеринмоностеарат; адсорбционные носители, такие как каолин и бентонит; и смазывающие вещества, такие как тальк, стеарат кальция, стеарат магния и твердые полиэтиленгликоли.
Соединения могут быть приготовлены в виде эликсиров или растворов для удобного перорального введения или в виде растворов, подходящих для парентерального введения, например внутримышечного, подкожного или внутривенного. Кроме того, соединения вполне пригодны для изготовления лекарственных форм отсроченного действия и тому подобное. Состав лекарственных форм может быть таким, чтобы он обеспечивал высвобождение активного компонента только или предпочтительно в конкретной части желудочно-кишечного тракта, возможно в течение некоторого периода времени. Могут быть изготовлены покрытия, оболочки и защитные матрицы, например, из полимерных веществ и восков.
Конкретная доза соединения формулы 1, необходимая для обеспечения ингибирования физиологического расстройства, связанного с избытком нейропептида Y, или его симптомов в соответствии с настоящим изобретением зависит от тяжести состояния, способа введения и других подобных факторов по усмотрению лечащего врача. Приемлемые эффективные суточные дозы обычно составляют от примерно 0,1 до примерно 1000 мг в сутки и более предпочтительно от примерно 50 до примерно 200 мг в сутки. Такие дозы вводят больному один-три раза в сутки или чаще в случае более эффективного лечения или предупреждения состояния или симптома(ов).
Обычно является предпочтительным вводить соединение формулы 1 в виде кислотно-аддитивной соли, как принято при введении лекарственных веществ, несущих основную группу, такую как пиперидиновое кольцо. Для таких целей годятся следующие пероральные лекарственные формы.
ПРЕПАРАТЫВ следующих ниже составах препаратов “Активный компонент” означает соединение формулы 1. Состав 1: Желатиновые капсулы Твердые желатиновые капсулы изготавливают, используя следующее: Ингредиент – Количество (мг/капсулу) Активный ингредиент – 0,1-1000 Крахмал, NF – 0-650 Крахмал в виде сыпучего порошка – 0-650 Силиконовая жидкость, 350 сантистоксов – 0-15 Ингредиенты смешивают, пропускают сквозь сито 45 меш стандарта США и заключают в твердые желатиновые капсулы. Примеры конкретных капсульных препаратов ралоксифена, которые были изготовлены, представлены ниже: Состав 2: Капсула с ралоксифеном Ингредиент – Количество (мг/капсулу) Ралоксифен – 1 Крахмал, NF – 112 Крахмал в виде сыпучего порошка – 225,3 Силиконовая жидкость, 350 сантистоксов – 1,7 Состав 3: Капсула с ралоксифеном Ингредиент – Количество (мг/капсулу) Ралоксифен – 5 Крахмал, NF – 108 Крахмал в виде сыпучего порошка – 225,3 Силиконовая жидкость, 350 сантистоксов – 1,7 Состав 4: Капсула с ралоксифеном Ингредиент – Количество (мг/капсулу) Ралоксифен – 10 Крахмал, NF – 103 Крахмал в виде сыпучего порошка – 225,3 Силиконовая жидкость, 350 сантистоксов – 1,7 Состав 5: Капсула с ралоксифеном Ингредиент – Количество (мг/капсулу) Ралоксифен – 50 Крахмал, NF – 150 Крахмал в виде сыпучего порошка – 397 Силиконовая жидкость, 350 сантистоксов – 3,0 Составы представленных выше конкретных препаратов можно в разумных пределах изменять. Препарат в форме таблеток изготавливают, используя следующие ингредиенты: Состав 6: Таблетки Ингредиент – Количество (мг/таблетку) Активный компонент – 0,1-1000 Целлюлоза, микрокристаллическая – 0-650 Диоксид кремния, тонкодисперсный – 0-650 Стеариновая кислота – 0-15 Компоненты смешивают и прессуют в таблетки. Альтернативно таблетки, содержащие каждая 0,1-1000 мг активного ингредиента, изготавливают следующим образом: Состав 7: Таблетки Компонент – Количество (мг/таблетку) Активный компонент – 0,1-1000 Крахмал – 45 Целлюлоза, микрокристаллическая – 35 Поливинилпирролидон (в виде 10%-ного раствора в воде) – 4 Натрий-карбоксиметилцеллюлоза – 4,5 Стеарат магния – 0,5 Тальк – 1 Активный ингредиент, крахмал и целлюлозу пропускают сквозь сито 45 меш по стандарту США и тщательно смешивают. Полученный порошок смешивают с раствором поливинилпирролидина, после чего смесь пропускают сквозь сито 14 меш (стандарт США). Полученные при этом гранулы высушивают при 50-60oС и пропускают сквозь сито 18 меш. Затем к гранулам добавляют натрий-карбоксиметилцеллюлозу, стеарат магния и тальк, ранее пропущенные сквозь сито 60 (стандарт США), и после перемешивания полученную смесь прессуют на таблеточной машине для получения таблеток. Суспензии, содержащие каждая 0,1-1000 мг активного ингредиента на 5 мл дозу, изготавливают следующим образом: Состав 8: Суспензии Компонент – Количество (мг/5 мл) Активный компонент – 0,1-1000 мг Натрий-карбоксиметилцеллюлоза – 50 мг Сироп – 1,25 мг Раствор бензойной кислоты – 0,10 мл Корригент – По усмотрению Красящее вещество – По усмотрению Очищенная вода – До 5 мл Активный ингредиент пропускают сквозь сито 45 меш (стандарт США) и, смешав с натрий-карбоксиметилцеллюлозой и сиропом, получают однородную пасту. Раствор бензойной кислоты, корригент и красящее вещество разбавляют некоторым количеством воды и добавляют в пасту с перемешиванием. Затем для получения требуемого объема добавляют достаточное количество воды. Соединения по настоящему изобретению связываются с рецепторами, специфическими для нейропептида Y, а также близко родственных пептидов. В отношении обзора рецепторов нейропептида Y смотри D.Gehlert, Life Sciences, 55:551-562 (1994). Рецепторы для нейропептида Y и пептида YY имеют значительное перекрытие, а панкреатический полипептид, по-видимому, имеет свой индивидуальный набор рецепторов. Многие (но не все) эффекты нейропептида Y можно воспроизвести, используя пептид YY. Первоначально были предложены два подтипа рецепторов для нейропептида Y на основе сродства 13-36 фрагмента нейропептида при использовании препарата симпатической нервной системы. Хотя они являются наилучшими обнаруженными рецепторами для нейропептида Y, но имеется много доказательств, что существуют дополнительные подтипы рецепторов. Наилучшим из обнаруженных является рецептор Y-3, который восприимчив к нейропептиду Y, но не к пептиду YY. Недавно был описан другой рецептор, который связывается с пептидом YY с высоким сродством и нейропептидом Y с более низким сродством. Фармакология “пищевой” реакции на нейропептид Y, по-видимому, связана с действием рецептора Y-1, но был предложен и отдельный “пищевой рецептор”. Рецептор Y-1 является единственным рецептором, успешно клонированным на сегодняшний день. Далее кратко изложена имеющаяся информация об известных подтипах рецепторов нейропептида Y и их возможной роли в физиологических процессах. Y- 1 Рецептор Y-1 Рецептор является наиболее характеризованным рецептором для нейропептида Y. Этот рецептор обычно считают постсинаптическим и он является медиатором многих известных действий нейропептида Y на периферии. Первоначально этот рецептор был описан как имеющий низкое сродство с С-концевыми фрагментами нейропептида Y, такими как 13-36 фрагмент, но он с одинаковым сродством взаимодействует с нейропептидом Y и пептидом YY, имеющими полную длину. С. Wahlestedt et al. , Regulatory Peptides, 13:307-318 (1986); C. Wahlestedt et al., Neuronal Messengers in Vascular Function, 231-241 (Nobin et al. , изд. 1987). Замещение аминокислоты в положении 34 пролином (Рrо34) дает в результате белок, специфический для Y-1 рецептора. Е.К. Potter et al. , European Journal of Pharmacology, 19315-19 (1991). Этот способ использовали для установления роли Y-1 рецептора в самых разнообразных функциях. Думается, что рецептор связывается с аденилатциклазой с проявлением ингибирующего действия в коре головного мозга, клетках гладких мышц кровеносных сосудов и SK-N-MS [cмотри B.J. McDermot et al.. Cardiovascular Research, 27: 893-905 (1993)]. Этому действию препятствует применение токсина коклюша, подтверждающего роль G-белоксвязанного рецептора. Y-1 Рецептор является медиатором мобилизации внутриклеточного кальция в клетках гладких мышц кровеносных сосудов свиньи и эритролейкозных клетках человека. Клонированный человеческий Y-1 рецептор можно связать либо с гидролизом фосфотидилинозитола, либо с ингибированием аденилатциклазы в зависимости от типа клетки, в которой осуществляется экспрессия рецептора. Н. Herzog et al. , Proceedings of the National Academy of Sciences (USA), 89:5794-5798 (1992). Как было сообщено, Y-1 рецептор связан либо с системой вторых переносчиков при исследовании с использованием тканевых препаратов, либо с линиями клеток, естественно экспрессирующими рецептор. Упомянутый выше D. Gehlert, стр. 553. Таким образом, Y-1 рецептор нельзя отличить только на основе связи с единственным вторым переносчиком. Y-2 Рецептор Как и Y-1 рецептор, этот подтип рецептора был первоначально описан с использованием препаратов кровеносных сосудов. Фармакологически Y-2 рецептор отличается от Y-1 проявлением сродства по отношению к С-концевым фрагментам нейропептида Y. Рецептор чаще всего дифференцируют, используя нейропептид Y (13-36), хотя 3-36 фрагмент нейропептида Y и пептида YY обеспечивает улучшенные сродство и избирательность. Y.Dumont et al. Society for Neuroscience Abstracts, 19: 726 (1993). Подобно Y-1 рецептору, этот рецептор связывают с ингибированием аденилатциклазы, хотя в некоторых препаратах он может не быть восприимчивым к токсину коклюша. Как было обнаружено, Y-2 рецептор снижает внутриклеточные уровни кальция в синапсе путем избирательного ингибирования кальциевых каналов N-типа. Как и Y-1 рецептор, рецептор Y-2 может проявлять различное связывание с вторым переносчиком. Y-2 Рецепторы обнаружены в самых разных зонах головного мозга, включающих гиппокамп, substania nigralateralis, таламус, гипоталамус и ствол. На периферии Y-2 обнаружен в периферической нервной системе, такой как симпатическая, парасимпатическая, и сенсорных нейронах. Во всех этих тканях Y-2 рецепторы являются медиаторами уменьшения высвобождения нейротрансмиттеров. Y-3 Рецептор Этот рецептор является самым новым и наименее изученным из обнаруженных подтипов рецепторов нейропептида Y. Нейропептид Y – это вполне эффективный агонист в этом семействе рецепторов, в то время как пептид YY малоэффективен. Это фармакологическое свойство используют для определения этого рецептора. Рецептор, имеющий фармакологию, как у Y-3 рецептора, был идентифицирован в области САЗ гиппокампа с использованием электрофизиологических методов. Этот рецептор может усиливать возбудительную реакцию указанных нейронов на N-метил-D-аспартат (NMDA). F.P. Monnet et al., European Journal of Pharmacology, 182:207-208 (1990). Наличие этого рецептора лучше всего устанавливается в стволе головного мозга крысы, в частности в ядре одиночного пути (nucleus tractus solitarius). Введение нейропептида Y в эту зону обеспечивает зависящее от дозы снижение кровяного давления и частоты сердечных сокращений. В эту зону головного мозга могут внести существенный вклад также и рецепторы Y-1 и Y-2. Нейропептид Y также ингибирует вызванное ацетилхолином высвобождение катехоламинов из мозгового вещества надпочечника, по-видимому, через Y-3 рецептор. С. Wahlestedt et al., Life Sciences, 50:PL7-PL14 (1992). Рецептор, предпочитающий пептид YY Был уже описан и четвертый рецептор, оказывающий умеренное предпочтение пептиду по сравнению с нейропептидом Y. Этот рецептор был первоначально выявлен в тонкой кишке крысы и описан как имеющий в 5-10 раз более высокое сродство по отношению к пептиду YY, чем к нейропептиду Y. M. Laburthe et al. , Endocrinology 118: 1910-1917 (1986). Затем этот рецептор был обнаружен в адипоците и линии клеток проксимальных почечных канальцев. Этот рецептор связан с возможностью ингибирующего действия с аденилатциклазой и восприимчив к коклюшному токсину. В кишке этот рецептор осуществляет мощное ингибирование секреции жидкости и электролита. Рецептор локализован в клетках крипты, где, по-видимому, имеет место кишечная секреция хлорида. Рецептор, предпочитающий пептид YY в адипоцитах является медиатором уменьшения липолиза посредством циклического аденозинмонофосфат(цАМФ, сАМР)зависимого механизма. “Пищевой рецептор” Одним из наиболее рано обнаруженных основных эффектов нейропептида Y было значительное увеличение приема пищи, которое наблюдалось после введения пептида в гипоталамус крыс. Реакция была наибольшей при вливании пептида в околоводную область гипоталамуса. B. G. Stoneley, et al., Research, 604: 304-317 (1993). Фармакология этой реакции подобна таковой у Y-1 рецептора, но фрагмент 2-36 нейропептида Y был значительно более мощным, чем нейропептид Y. Кроме того, интрацеребровентрикулярный нейропептид Y (2-36) в полной мере стимулирует питание, но не снижает температуру тела, как это делает нейропептид Y полной длины. F.B. Jolicour et al. Brain Research Bulletin, 26:309-311(1991). Биологическую активность соединений по настоящему изобретению оценивали путем первоначального скрининга, при котором быстро и точно измеряли связывание испытуемого соединения с известными клеточными рецепторами нейропептида Y. Испытания, пригодные для оценки антагонистов рецепторов нейропептида Y, хорошо известны в данной области медицины. Смотри, например, патент США 5284839, выданный 8 февраля 1994 г., который включен в данное описание в качестве ссылки. Смотри также M.W. Walker et al. Jornal Neurosciences, 8: 2438-2446 (1998). Испытание на связывание с нейропептидом Y Проверяли способность соединений настоящего изобретения связываться с нейропептидом Y методом, описанным у М.W. Walker et al., см. выше. В этом испытании использовали клеточную линию SK-N-MC. Эта клеточная линия была получена из лечебного учреждения Sloane-Kettering, Меmorial Hospital, Нью-Йорк. Эти клетки культивировали в колбах Т-150, используя минимальные незаменимые питательные среды Дульбекко (DMEM) с добавлением 5%-ной плодной сыворотки теленка. Клетки вручную извлекали из колб путем выскабливания, таблетировали и хранили при -70oС. Таблетки вновь суспендировали, используя стеклянный гомогенизатор, в 25 мМ буфера НЕРЕS (рН 7,4), содержавшего 2,5 мМ хлорида кальция, 1 мМ хлорида магния и 2 мг/л бацитрацина. Инкубацию осуществляли в конечном объеме 200 мкл, содержащем 0,1 нМ 1251-пептида YY (2200 Ci/ммоль) и 0,2-0,4 мг белка, в течение примерно двух часов при комнатной температуре. Неспецифическое связывание определяли в виде величины радиоактивности, оставшейся связанной с тканью после инкубации в присутствии 1 мкМ нейропептида Y. В нескольких экспериментах в инкубационную смесь включали различные концентрации соединений. Инкубацию заканчивали быстрым фильтрованием через стекловолоконные фильтры, предварительно пропитанные 0,3%-ным полиэтиленимином, использовав устройство для сбора культивированных клеток с 96 ячейками. Фильтры промывали 5 мл 50 мМ Трис (рН 7,4) при 4oС и быстро высушивали при 60oС. Затем обрабатывали фильтры наплавляемыми сцинтилляционными листами и считали радиоактивность, оставшуюся на фильтрах. Результаты анализировали, использовав различные комплекты программного обеспечения. Концентрацию белков измеряли с помощью стандартных реактивов для белкового анализа, использовав в качестве стандартов бычий сывороточный альбумин (см.таблицу). Так как соединения формулы 1 являются эффективными антагонистами рецепторов нейропептида Y, то эти соединения полезны для лечения самых разных клинических состояний, которые характеризуются наличием избытка нейропептида Y. Поэтому, в соответствии с настоящим изобретением предлагается способ лечения или предупреждения физиологического расстройства, связанного с избытком нейропептида Y, включающий в себя введение млекопитающему, нуждающемуся в таком лечении, эффективного количества соединения формулы 1 или его фармацевтически приемлемой (ого) соли, сольвата или пролекарства. Термин “физиологическое расстройство, связанное с избытком нейропептида ” охватывает те расстройства, которые связаны с несоответствующей стимуляцией рецепторов нейропептида Y независимо от действительного количества нейропептида Y, присутствующего в месте действия. Эти физиологические расстройства могут включать: расстройства или заболевания сердца, кровеносных сосудов или почечной системы, такие как вазоспазм, сердечная недостаточность, шок, гипертрофия сердца, повышенное кровяное давление, стенокардия, инфаркт миокарда, внезапная остановка сердца, аритмия, заболевание периферических кровеносных сосудов и анормальные почечные состояния, такие как нарушенный ток жидкости, анормальный массоперенос или почечная недостаточность; состояния, связанные с повышенной активностью симпатических нервов, например, во время или после хирургической операции на коронарных сосудах и манипуляций и хирургической операции в желудочно-кишечном тракте, болезни головного мозга и заболевания, связанные с центральной нервной системой, такие как инфаркт головного мозга, нейродегенерация, эпилепсия, удар и состояния, связанные с ударом, церебральный вазоспазм и кровоизлияние, депрессия, тревога, шизофрения и слабоумие; состояния, связанные с болью или восприятием повреждающих воздействий нервными центрами; заболевания, связанные с аномальной моторикой желудочно-кишечного тракта и аномальным выделением, такими как различные формы илеуса, недержание мочи и болезнь Крона; аномальное питье и расстройства приема пищи, такие как ожирение, анорексия, булемия, и метаболические расстройства; заболевания, связанные с сексуальной дисфункцией, и репродуктивные расстройства; состояния или расстройства, связанные с воспалением; респираторные заболевания, такие как астма и состояния, связанные с астмой, и сужение просвета бронхов; заболевания, связанные с анормальным выделением гормонов, таких как лютеинизирующий гормон, гормон роста, инсулин и пролактин. Формула изобретения
 где R1 и R2 независимо представляют водород, СН3,  (C1-С6 алкил) или (C1-С6 алкил) или  где Аr представляет необязательно замещенный фенил; R2 выбран из группы, состоящей из пирролидино, гексаметиленимино и пиперидино, или его фармацевтически приемлемой соли или сольвата. 2. Способ по п.1, отличающийся тем, что указанное соединение представляет собой его хлористоводородную соль. 3. Способ по п.1, отличающийся тем, что указанное соединение представляет собой  или его хлористоводородную соль. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 20.10.2002
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||
