Патент на изобретение №2186055
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-КАРБОКСИ-4-ГИДРОКСИБЕНЗАЛЬДЕГИДА, СПОСОБ ПОЛУЧЕНИЯ 4-ГИДРОКСИБЕНЗАЛЬДЕГИДА, СПОСОБЫ ПОЛУЧЕНИЯ ВАНИЛИНА И ЭТИЛВАНИЛИНА
(57) Реферат: Изобретение относится к способу получения производных 3-карбокси-4-гидроксибензилальдегидов из фенольных соединений, несущих формильную и/или гидроксиметильную группы в положении 2 и 4; описывается также получение 4-гидроксибензальдегида из 3-карбокси-4-гидроксибензальдегида и получение 3-метокси-4-гидроксибензальдегида и 3-этокси-4-гидроксибензальдегида, называемых соответственно “ванилин” и “этилванилин”. Способ получения 3-карбокси-4-гидроксибензальдегида осуществляют селективным окислением фенольного соединения, которое содержит формильную группу и/или гидроксиметильную группу в положении 2 и 4, при этом группа в положении 2 окисляется до карбоксильной, в случае необходимости, гидроксиметильная группа в положении 4 окисляется до формильной. Декарбоксилирование 3-карбокси-4-гидроксибензальдегида приводит к 4-гидроксибензальдегиду. 4 с. и 22 з.п.ф-лы. Объектом настоящего изобретения является способ получения 3-карбокси-4-гидроксибензальдегидов и их производных из фенольных соединений, которые являются носителями формильной и/или гидроксиметильной групп в положении 2 и 4. Другим объектом изобретения является получение 4-гидроксибензальдегидов из 3-карбокси-4-гидроксибензальдегидов. В частности, изобретение относится к получению 3-метокси-4-гидроксибензальдегида и 3-этокси-4-гидроксибензальдегида, называемых соответственно “ванилин” и “этилванилин”. В основном ванилин получают из натурального сырья, например из лигнина, но частично его получают химическим путем. В литературе описано очень много способов получения ванилина, и некоторые из них используют гваякол и 2-метоксифенол в качестве исходного сырья. Один из таких способов получения заключается в реакции гваякола с глиоксиловой кислотой и окислении на воздухе конденсата с последующим выделением ванилина из реакционной среды путем ее подкисления. Недостаток данного способа состоит в том, что приходится использовать глиоксиловую кислоту, которая является дорогостоящим продуктом. Другой способ получения ванилина основан на реакции Реймер-Тиемана и состоит во взаимодействии гваякола и хлороформа в присутствии гидроокиси калия. Недостатком этого способа является образование смолы. Согласно реакции Гаттермана ванилин синтезируют взаимодействием цианистоводородной кислоты и гваякола в присутствии соляной кислоты. Кроме того, что этот способ использует реактив, требующий осторожного обращения, недостаток его заключается еще и в том, что он не является селективным, так как ванилин сопровождается образованием изованилина и орто-ванилина. Основной трудностью в синтезе ванилина является селективная фиксация формильной группы на гваяколе в пара-положении к гидроксильной группе. Другая серьезная задача, которую необходимо разрешить, состоит в разработке способа, достаточно надежного для осуществления в промышленности. Настоящее изобретение предлагает новый способ, позволяющий устранить названные недостатки и удовлетворить требованиям, указанным выше. Первым объектом настоящего изобретения является способ получения 3-карбокси-4-гидроксибензальдегида, отличающийся тем, что подвергают фенольное соединение, являющееся носителем формильной группы и/или гидроксиметильной группы в положении 2 и 4, селективному окислению, чтобы группа, находящаяся в положении 2, окислилась до карбоксильной группы и, в случае необходимости, гидроксиметильная группа, находящаяся в положении 4, окислялась до формильной группы. Другим объектом изобретения является получение 4-гидроксибензальдегида путем декарбоксилирования 3-карбокси-4-гидроксибензальдегида. Способ согласно изобретению очень хорошо подходит для получения ванилина. В самом деле, он позволяет осуществлять селективное окисление 4,6-диформилгваякола или 4,6-ди(гидроксиметил)гваякола или 4-формил-6-гидроксиметилгваякола или 4-гидроксиметил-6-формилгваякола до 5-карбоксиванилина, затем удаляют карбоксильную группу, находящуюся в положении 5, и таким образом получают ванилин. Таким же образом способ применим к (2-этоксифенол)гваяколу, для получения этилванилина. Предлагаемый способ является селективным и очень выгодным с промышленной точки зрения, так как использует не очень дорогие реактивы. Исходным субстратом, используемым в способе по изобретению, является фенольное соединение, несущее формильную группу и/или гидроксиметильную группу в положении 2 и 4. Под “фенольным соединением” подразумевают любое ароматическое соединение, ароматическое ядро которого является носителем гидроксильной группы. В нижеследующем описании настоящего изобретения под определением “ароматический” подразумевают классическое понятие ароматичности, которое дано в литературе, например,автором Джерри Марш, в Advanced Organic Chemistry, 4-ое изд. John Wiley and Sons, 1992, стр. 40 и следующие. Это фенольное соединение является носителем в положении 2 и 4 групп гидроксиметильной и/или формильной. Фенольные соединения, преимущественно применяемые в способе по изобретению, отвечают общей формуле (II) 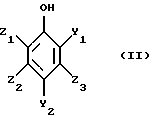 в которой Y1 и Y2 идентичные или разные, представляют одну из следующих групп: группу СНО, группу СН2ОН; Z1, Z2 и Z3, идентичные или разные, представляют атом водорода, радикал алкил, алкенил, алкокси, гидроксиалкил, алкоксиалкил, циклоалкил, арил, гидроксильную группу, группу нитро, атом галогена, трифторметильную группу. Соединения, которые особенно подходят для осуществления способа по изобретению, отвечают формуле (II), в которой Z1, Z2 и Z3, идентичные или разные, представляют один из атомов или групп: атом водорода, алкильный радикал, линейный или разветвленный, имеющий 1-12 атомов углерода, преимущественно 1-4 атома углерода, такой как метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, алкенильный радикал, линейный или разветвленный, имеющий 2-12 атомов углерода, преимущественно 2-4 атома углерода, такой как винил, аллил, алкоксирадикал, линейный или разветвленный, имеющий 1-12 атомов углерода, преимущественно 1-4 атома углерода,такой как радикалы метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, фенильный радикал, атом галогена, преимущественно атом фтора, хлора или брома. Настоящее изобретение не исключает присутствия на ароматическом цикле заместителей различного типа, если они не оказывают влияния на реакцию способа по изобретению. Настоящее изобретение относится преимущественно к соединениям формулы (II), в которой Z1 означает алкоксильный радикал, линейный или разветвленный, имеющий 1-6 атомов углерода, преимущественно 1-4 атома углерода; Z2 и Z3 означают атом водорода; Y1 и Y2 идентичные, означают формильную группу или гидроксиметильную группу. В качестве предпочитаемых примеров субстратов, используемых в способе по изобретению, можно назвать следующие: – 2,4-диформилфенол, – 1,2-дигидрокси-3,5-диформилбензол, – 1-гидрокси-2-метокси-4,6-диформилбензол [4,6-диформилгваякол], – 1-гидрокси-2-этокси-4,6-диформилбензол [4,6-диформилгветол], – 4,6-ди(гидроксиметил)гваякол, – 4,6-ди(гидроксиметил)гветол. Среди вышеуказанных субстратов наиболее предпочтительными для использования являются 4,6-диформилгваякол и 4,6-ди (гидроксиметил)гваякол. Согласно предложенному способу исходным является фенольное соединение, которое преимущественно является соединением, отвечающим формуле (II). Ниже дается реакционная схема способа по изобретению, чтобы сделать более легким понимание изобретения. 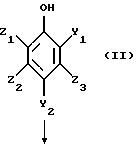 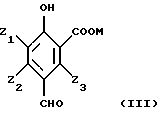 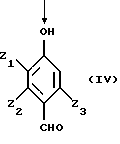 В названных формулах (II)-(IV): – М представляет атом водорода и/или катион металла группы (Iа) или (IIа) периодической системы или катион аммония, – Z1, Z2, Z3 имеют значения, данные выше. В настоящем тексте дается ссылка на периодическую систему элементов, опубликованную в Бюллетене химического общества Франции, 1, 1966 год. Согласно способу по изобретению осуществляют селективное окисление группы Y1 в положении 2 до карбоксильной группы в фенольном соединении, являющимся носителем групп формильной и/или гидроксиметильной в положении 2 и 4 и отвечающем преимущественно формуле (II), и, при необходимости, окисление гидроксиметильной группы в положении 4 до формильной группы. Окисление осуществляют молекулярным кислородом или его содержащим газом в присутствии катализатора. Предпочитаемый метод окисления состоит в окислении фенольного соединения формулы (II) в жидкой фазе с помощью молекулярного кислорода или газа, его содержащего, в водной среде, содержащей агент основного характера, в присутствии катализатора на основании металла М1, выбираемого среди металлов группы Iб и VIII периодической системы элементов, содержащего, в случае необходимости, в качестве активаторов кадмий, церий, висмут, свинец, серебро, теллур или олово. Согласно изобретению было совершенно неожиданно обнаружено, что если увеличивать температуру и проводить реакцию предпочтительно под давлением, и если увеличивать количество основания, присутствующего при окислении, то окисляются селективно группы формильная и/или гидроксиметильная в положении 2 до карбоксильной группы, при этом группа, находящаяся в положении 4, окисляется до альдегидной группы. Катализаторы, используемые в способе, содержат металл группы Iб и VIII периодической системы. В качестве примеров катализаторов на основе металлов группы VIII периодической системы, можно назвать катализаторы на основе никеля, рутения, родия, палладия, осмия, иридия, платины и их смесей. Из металлов группы Iб предпочитают использовать медь. Предпочтительно используют катализаторы на основе платины и/или палладия в любой имеющейся форме, например платиновая чернь, палладиевая чернь, окись платины, окись палладия, или в виде нанесенного на различные носители благородного металла, где носителем может быть сажа, карбонат кальция, активированная окись алюминия и двуокись кремния или эквивалентные вещества. Особенно подходят каталитические массы на основе сажи. Количество катализатора, используемого в способе, выраженное как масса металла М1 по отношению к массе фенольного соединения формулы (II), может изменяться от 0,01 до 10%, предпочтительно от 0,04 до 2%. Более подробно катализаторы описаны в патентах: США – А-367257, Франции А-2305420 и А-2350323. Активатор может быть выбран среди тех, которые перечислены в указанных выше патентах. Предпочтительно используют висмут, свинец или кадмий в виде свободных металлов или катионов. В последнем случае связанный с ним анион не имеет критического значения, поэтому можно использовать все производные этих металлов. Предпочтительно используют висмут и его производные. Можно использовать минеральное или органическое производное висмута, в котором степень окисления атома висмута выше нуля, например равно 2, 3, 4 или 5. Остаток, связанный с висмутом, не имеет решающего значения, если он соответствует указанному условию. Активатор может быть растворимым или нерастворимым в реакционной среде. В качестве иллюстрации соединениями, которые могут использоваться в качестве активаторов, являются: окиси висмута, гидроокиси висмута, соли минеральных водородных кислот, таких как хлорид, бромид, иодид, сульфид, селенид, теллур висмута; соли минеральных оксикислот, такие как сульфит, сульфат, нитрит, нитрат, фосфит, фосфат, пирофосфат, карбонат, перхлорат, антимониат, арсениат, селенит, селениат висмута; соли оксикислот с переходными металлами, такие как ванадат, ниобат, танталат, хромат, молибдат, вольфрамат, перманганат висмута. Другими подходящими соединениями также являются соли органических алифатических или ароматических кислот, например ацетат, пропионат, бензоат, салициалат, оксалат, тартрат, цитрат висмута; фенаты, такие как галлат и пирогаллат висмута. Эти соли и фенаты могут быть также солями висмутила. В качестве других минеральных или органических соединений можно использовать бинарные композиции висмута с такими элементами, как фосфор и мышьяк; гетерополикислоты, содержащие висмут, а также их соли; подходят также алифатические или ароматические висмутины. В качестве специфических примеров можно назвать: – в качестве оксидов: BiO, Bi2O3, Bi2O4, Bi2O5, – в качестве гидроксидов: Bi(OH)3, – в качестве солей минеральных водородных кислот: хлорид висмута ВiСl3, бромид висмута BiBr3, иодид висмута BiJ3, сульфид висмута Bi2S3, селенид висмута Bi2Se3, теллур висмута Вi2Те3, – в качестве солей минеральных оксикислот: основной сульфит висмута Вi2(SO3); Bi2O3  5Н2O; нейтральный сульфат висмута Bi2(SO4)3; сульфат висмутила (ВiO)НSО4; нитрит висмутила (ВiO)NO2 5Н2O; нейтральный сульфат висмута Bi2(SO4)3; сульфат висмутила (ВiO)НSО4; нитрит висмутила (ВiO)NO2 0,5 Н2O; нейтральный нитрат висмута Bi(NO3)3 0,5 Н2O; нейтральный нитрат висмута Bi(NO3)3 5H2O, двойной нитрат висмута и магния 2Bi(NO3)3 5H2O, двойной нитрат висмута и магния 2Bi(NO3)3 3Mg(NO3)2 3Mg(NO3)2 24H2O; нитрат висмутила (BiO)NO3; фосфит висмута Bi2(PO3H)3 24H2O; нитрат висмутила (BiO)NO3; фосфит висмута Bi2(PO3H)3 3Н2О; нейтральный фосфат висмута ВiРО4; пирофосфат висмута Bi4(P2O7)3; карбонат висмутила (ВiО)2СО3 3Н2О; нейтральный фосфат висмута ВiРО4; пирофосфат висмута Bi4(P2O7)3; карбонат висмутила (ВiО)2СО3 0,5 Н2O; нейтральный перхлорат висмута Вi(СlO4)3 0,5 Н2O; нейтральный перхлорат висмута Вi(СlO4)3 5Н2О; перхлорат висмутила (ВiO)СlO4; антимониат висмута ВiSbO4; нейтральный арсениат висмута Bi(AsO4)3; арсениат висмутила (ВiO)AsО4 5Н2О; перхлорат висмутила (ВiO)СlO4; антимониат висмута ВiSbO4; нейтральный арсениат висмута Bi(AsO4)3; арсениат висмутила (ВiO)AsО4 5Н2O; селенит висмута Вi2(SеO3)3, 5Н2O; селенит висмута Вi2(SеO3)3,– в качестве солей оксикислот с переходными металлами: ванадат висмута BiVO4; ниобат висмута BiNbO4; танталат висмута ВiТаО4; нейтральный хромат висмута Bi2(CrO4); дихромат висмутила [(ВiO)2]2Сr2О7; кислый хромат висмутила Н(ВiO)CrO4; двойной хромат висмутила и калия K(BiO)CrO4; молибдат висмута Bi2(МоО4)3; вольфрамат висмута Bi2(WO4)3; двойной молибдат висмута и натрия NаВi(МоO4)2; основной перманганат висмута Вi2О2(ОН)МnО4, – в качестве солей алифатических и ароматических органических кислот: ацетат висмута Bi(С2Н3О2)3; пропионат висмутила (ВiO)С3Н5О2; основной бензоат висмута С6Н5CO2Bi(ОН)2; силицилат висмутила С6Н4СО2(ВiО)(ОН); оксалат висмута (С2О4)3Bi2; тартрат висмута Bi2(С4Н4О6)3  6Н2O; лактат висмута (С6Н9О5)ОBi 6Н2O; лактат висмута (С6Н9О5)ОBi 7Н2O; цитрат висмута С6Н6O7Вi, 7Н2O; цитрат висмута С6Н6O7Вi,– в качестве фенатов: основной галлат висмута С7Н7О7В, основной пирогаллат висмута С6Н3(ОН)2(ОВi)(ОН). В качестве других минеральных и органических соединений подходит также: фосфид висмута BiP, арсенид висмута Bi3As4, висмутат натрия NаВiO3, висмут-тиоциановые кислоты Н2[Bi(ВNS)5], H3[Bi(CNS)6] и их соли натрия и калия, триметилвисмутин Вi(СН3)3, трифенилвисмутин Вi(С6Н5)3. Производными висмута, которые предпочитают использовать для осуществления способа по изобретению, являются: окиси висмута, гидроокиси висмута, соли висмута или висмутила минеральных водородных кислот, соли висмута или висмутила минеральных оксикислот, соли висмута или висмутила алифатических или ароматических органических кислот и фенаты висмута или висмутила. Группа активаторов, которые особенно хорошо подходят для осуществления изобретения, включает: окиси висмута Bi2O3 и Вi2O4, гидроокись висмута Вi(ОН)3, нейтральный сульфат висмута Вi2(SO4)3, хлорид висмута BiCl3, бромид висмута BiBr3, иодид висмута BiI3, нейтральный нитрат висмута Вi(NO3)3  5Н2O, нитрат висмутила ВiO(NО3), карбонат висмутила (ВiO)2СО3 5Н2O, нитрат висмутила ВiO(NО3), карбонат висмутила (ВiO)2СО3 0,5Н2O, ацетат висмута Вi(C2H3O2)3, салицилат висмутила C6H4CO2(BiO)(ОН).
Используемое количество активатора, выраженное через количество металла, содержащегося в активаторе, по отношению к массе металла М1, введенного в реакцию, может изменяться в широком диапазоне. Например, это количество может быть очень низким, например 0,1%, и может достигать массы введенного металла М1 и даже превышать его, не создавая при этом проблем.
Более предпочтительно это количество выбирают таким образом, чтобы в среде окисления находилось от 10 до 900 ррm веса активирующего металла по отношению к фенольному соединению формулы (II). Для этого могут использоваться количества активатора порядка 900-1500 ррм, но без значительного дополнительного преимущества.
Согласно способу по изобретению окисление проводят в водной среде, которая содержит в растворенном состоянии вещество основного характера, в частности гидроокись аммония, щелочные или щелочно-земельные основания, среди которых можно назвать такие гидроокиси, как гидроокись натрия, калия, лития и барит, щелочные алканоляты, такие как метилат, этилат, изопропилат и трет-бутилат натрия или калия, карбонаты или бикарбонаты натрия и калия и соли щелочных или щелочно-земельных оснований и слабых кислот.
Таким образом, соединения формулы (III) могут находиться полностью или частично в виде соли в зависимости от количества используемого основного вещества. Отсюда следует, что в формуле (III) М означает атом водорода и/или катион металла группы (Iа) или (IIа) или катион аммония.
Из-за экономических соображений используют гидроокись натрия или калия. Содержание используемого минерального основания может быть равно 0,5-10 молей, преимущественно 1-4 моля, а предпочтительно 2-4 моля минерального основания на моль фенольного соединения формулы (II).
Весовая концентрация фенольного соединения формулы (II) в жидкой фазе обычно равна 1-60%, преимущественно 2-30%.
Практически метод осуществления способа состоит в том, что подвергают контактированию с молекулярным кислородом или газом, его содержащим, например с воздухом, раствор, содержащий фенольное соединение формулы (II), агент основного характера, катализатор на основе металла М1, в случае необходимости активатор, в пропорциях, указанных выше.
Можно работать при атмосферном давлении, но предпочтительнее работать под давлением 1-20 бар.
Затем смесь перемешивают при желаемой температуре до тех пор, пока не будет израсходовано такое количество кислорода, которое необходимо для преобразования гидроксиметильной и/или формильной группы в группу карбоксильную, а в случае необходимости гидроксиметильной группы в группу формильную.
Температуру реакции варьируют в зависимости от термостабильности получаемых продуктов.
Согласно изобретению температуру выбирают преимущественно в температурном диапазоне от 30-200oС, преимущественно 40-160oС.
Температуру специалист выбирает в зависимости от реакционных условий (в частности, в зависимости от количества основания, природы металла М1, давления и перемешивания). Было определено, что чем ниже температура, тем больше требуется агента основного характера, которое используется в реакции.
В качестве примера можно указать предпочтительные условия в случаях предпочтительных металлов – платины и палладия. Для платины температуру выбирают 100-160oС, количество используемого основания преимущественно равно 1-3 моля на моль фенольного соединения формулы (II). В случае палладия температуру выбирают 30-200oС, преимущественно 30-100oС, и для этого интервала температур предпочтительное количество основания равно 2-4 моля на моль названного фенольного соединения.
В конце реакции, которая продолжается преимущественно от 30 минут до 6 часов, рекуперируют 2-гидроксибензойную кислоту, формилированную в положении 5, которая может быть частично или полностью превращена в соль, и отвечающую преимущественно формуле (III).
Затем, после охлаждения, если оно имеет место, отделяют с помощью фильтрации каталитическую массу от реакционной массы.
На последнем этапе способа осуществляют реакцию декарбоксилирования.
Для этого полученную среду подкисляют путем добавления протоновой кислоты минерального происхождения, преимущественно серной или соляной кислоты, или органической кислоты, такой как, например, трифторметансульфоновой кислоты или метансульфоновой, до получения рН, меньшего или равного 3.
Нагревают реакционную среду до температуры в интервале, например, от 120 до 350oС, преимущественно от 150 до 220oС. Способ осуществляют преимущественно под автогенным давлением реактивов.
В конце реакции охлаждают реакционную среду до температуры 20-80oС.
Получают двухфазную среду, состоящую из неорганической фазы, содержащей, с одной стороны, 4-гидроксибензальдегид, отвечающий предпочтительно формуле (IV), и возможно исходный субстрат формулы (П), а, с другой стороны, соленую водную фазу.
Разделяют органическую и водную фазы и рекуперируют 4-гидроксибензальдегид из органической фазы согласно классическим методам разделения, предпочтительно путем отгонки или путем экстракции с помощью соответствующего растворителя.
В соответствии со способом по изобретению получают 3-карбокси-4-гидроксибензальдегид путем селективного окисления фенольного соединения, являющегося носителем формильной и/или гидроксиметильной группы в положении 2 и 4.
Таким образом, исходные субстраты отвечают формулам (IIа), (IIb), (IIс) и (IId), показанным ниже. 0,5Н2O, ацетат висмута Вi(C2H3O2)3, салицилат висмутила C6H4CO2(BiO)(ОН).
Используемое количество активатора, выраженное через количество металла, содержащегося в активаторе, по отношению к массе металла М1, введенного в реакцию, может изменяться в широком диапазоне. Например, это количество может быть очень низким, например 0,1%, и может достигать массы введенного металла М1 и даже превышать его, не создавая при этом проблем.
Более предпочтительно это количество выбирают таким образом, чтобы в среде окисления находилось от 10 до 900 ррm веса активирующего металла по отношению к фенольному соединению формулы (II). Для этого могут использоваться количества активатора порядка 900-1500 ррм, но без значительного дополнительного преимущества.
Согласно способу по изобретению окисление проводят в водной среде, которая содержит в растворенном состоянии вещество основного характера, в частности гидроокись аммония, щелочные или щелочно-земельные основания, среди которых можно назвать такие гидроокиси, как гидроокись натрия, калия, лития и барит, щелочные алканоляты, такие как метилат, этилат, изопропилат и трет-бутилат натрия или калия, карбонаты или бикарбонаты натрия и калия и соли щелочных или щелочно-земельных оснований и слабых кислот.
Таким образом, соединения формулы (III) могут находиться полностью или частично в виде соли в зависимости от количества используемого основного вещества. Отсюда следует, что в формуле (III) М означает атом водорода и/или катион металла группы (Iа) или (IIа) или катион аммония.
Из-за экономических соображений используют гидроокись натрия или калия. Содержание используемого минерального основания может быть равно 0,5-10 молей, преимущественно 1-4 моля, а предпочтительно 2-4 моля минерального основания на моль фенольного соединения формулы (II).
Весовая концентрация фенольного соединения формулы (II) в жидкой фазе обычно равна 1-60%, преимущественно 2-30%.
Практически метод осуществления способа состоит в том, что подвергают контактированию с молекулярным кислородом или газом, его содержащим, например с воздухом, раствор, содержащий фенольное соединение формулы (II), агент основного характера, катализатор на основе металла М1, в случае необходимости активатор, в пропорциях, указанных выше.
Можно работать при атмосферном давлении, но предпочтительнее работать под давлением 1-20 бар.
Затем смесь перемешивают при желаемой температуре до тех пор, пока не будет израсходовано такое количество кислорода, которое необходимо для преобразования гидроксиметильной и/или формильной группы в группу карбоксильную, а в случае необходимости гидроксиметильной группы в группу формильную.
Температуру реакции варьируют в зависимости от термостабильности получаемых продуктов.
Согласно изобретению температуру выбирают преимущественно в температурном диапазоне от 30-200oС, преимущественно 40-160oС.
Температуру специалист выбирает в зависимости от реакционных условий (в частности, в зависимости от количества основания, природы металла М1, давления и перемешивания). Было определено, что чем ниже температура, тем больше требуется агента основного характера, которое используется в реакции.
В качестве примера можно указать предпочтительные условия в случаях предпочтительных металлов – платины и палладия. Для платины температуру выбирают 100-160oС, количество используемого основания преимущественно равно 1-3 моля на моль фенольного соединения формулы (II). В случае палладия температуру выбирают 30-200oС, преимущественно 30-100oС, и для этого интервала температур предпочтительное количество основания равно 2-4 моля на моль названного фенольного соединения.
В конце реакции, которая продолжается преимущественно от 30 минут до 6 часов, рекуперируют 2-гидроксибензойную кислоту, формилированную в положении 5, которая может быть частично или полностью превращена в соль, и отвечающую преимущественно формуле (III).
Затем, после охлаждения, если оно имеет место, отделяют с помощью фильтрации каталитическую массу от реакционной массы.
На последнем этапе способа осуществляют реакцию декарбоксилирования.
Для этого полученную среду подкисляют путем добавления протоновой кислоты минерального происхождения, преимущественно серной или соляной кислоты, или органической кислоты, такой как, например, трифторметансульфоновой кислоты или метансульфоновой, до получения рН, меньшего или равного 3.
Нагревают реакционную среду до температуры в интервале, например, от 120 до 350oС, преимущественно от 150 до 220oС. Способ осуществляют преимущественно под автогенным давлением реактивов.
В конце реакции охлаждают реакционную среду до температуры 20-80oС.
Получают двухфазную среду, состоящую из неорганической фазы, содержащей, с одной стороны, 4-гидроксибензальдегид, отвечающий предпочтительно формуле (IV), и возможно исходный субстрат формулы (П), а, с другой стороны, соленую водную фазу.
Разделяют органическую и водную фазы и рекуперируют 4-гидроксибензальдегид из органической фазы согласно классическим методам разделения, предпочтительно путем отгонки или путем экстракции с помощью соответствующего растворителя.
В соответствии со способом по изобретению получают 3-карбокси-4-гидроксибензальдегид путем селективного окисления фенольного соединения, являющегося носителем формильной и/или гидроксиметильной группы в положении 2 и 4.
Таким образом, исходные субстраты отвечают формулам (IIа), (IIb), (IIс) и (IId), показанным ниже.
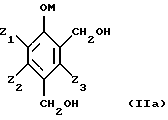 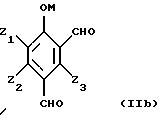 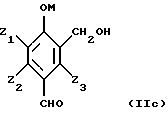 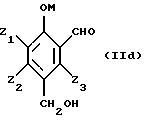 Названные соединения являются обычно известными продуктами, которые можно получить различными методами органического синтеза. Например, соединения формулы (IIb) могут быть получены путем окисления поли(гидроксиметил)фенолов формулы (IIа) молекулярным кислородом или газом, который его содержит, в жидкой щелочной фазе в присутствии катализатора на основе металла группы VIII периодической системы, предпочтительно платины и палладия, содержащего в случае необходимости в качестве активатора такие металлы,l как кадмий, церий, висмут, свинец, серебро, теллур или олово. Такие способы описаны в патентах: США – А-3673257, Франции – А-2305420 и А-2350323. Поли(гидроксиметил)фенолы являются продуктами, известными в большинстве своем, и могут быть получены путем гидроксиметилирования фенолов, замещенных или незамещенных, с помощью формальдегида или соединений, генерирующих формальдегид, например параформальдегида, в условиях самых разнообразных: H. G. РЕER, Rec. Trav. Chim. Голландия, 79. 825-835 (1960), GB-A-774696, GB-A-751845, EP-A-165, J.H. FREEMAN, J. Am. Chem. Soc. 74, 6 257-6 260 (1952) и 76 2080-2087(1954); H.G. PEER Rеc. Trаv. Chim. Голландия, 78 851-863 (1959), H. EULER и др. Arkiv 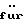 Chem. 13 1-7 (1939), P. CLAUS и др. Monath. Chem. 103, 1178-1293 (1972).
Способ гидроксиметилирования фенолов, который подходит, в частности, для синтеза поли(гидроксиметил)фенолов, используемых для получения соединений формулы (III), состоит в конденсации формальдегида или соединений, генерирующих формальдегид, с фенолом в водной фазе в присутствии щелочного или щелочно-земельного основания.
Оказалось, что с промышленной точки зрения для осуществления способа по изобретению выгодно использовать соединения формулы (IIb), полученные двухэтапным способом, включающим: Chem. 13 1-7 (1939), P. CLAUS и др. Monath. Chem. 103, 1178-1293 (1972).
Способ гидроксиметилирования фенолов, который подходит, в частности, для синтеза поли(гидроксиметил)фенолов, используемых для получения соединений формулы (III), состоит в конденсации формальдегида или соединений, генерирующих формальдегид, с фенолом в водной фазе в присутствии щелочного или щелочно-земельного основания.
Оказалось, что с промышленной точки зрения для осуществления способа по изобретению выгодно использовать соединения формулы (IIb), полученные двухэтапным способом, включающим:– гидроксиметилирование фенола в водной среде в присутствии щелочного или щелочно-земельного основания с помощью формальдегида или соединения, генерирующего формальдегид, с получением поли(гидроксиметил)фенола, – и окисление, без промежуточного выделения, поли(гидроксиметил)фенолов с помощью молекулярного кислорода или газа, его содержащего, в водной щелочной фазе в присутствии катализатора на основе металла группы 8 периодической системы, и, в случае необходимости, активирующего металла, такого, которые перечислены выше. Более конкретно, способ согласно изобретению включает получение соединений формулы (III) из поли(гидроксиметил)фенолов формулы (IIа), полученных способом, состоящим из двух этапов: – гидроксиметилирование фенола, не замещенного в положениях орто и пара по отношению к гидроксильной группе, общей формулы (I) 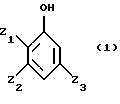 с получением поли(гидроксиметил)фенола, содержащего, по меньшей мере, одну гидроксиметильную группу в положении орто и пара по отношению к гидроксильной группе, общей формулы (IIа) 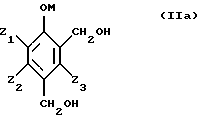 с помощью формальдегида или генератора формальдегида в водной фазе в присутствии щелочного или щелочно-земельного основания; – окисление в щелочной водной фазе полученных поли(гидроксиметил)фенолов формулы (Па) молекулярным кислородом или газом, его содержащим, в присутствии катализатора на основании металла группы VIII периодической системы, содержащего в случае необходимости, металл, используемый в качестве активаторов, без промежуточного выделения поли(гидроксиметил)фенолов. Среди фенолов формулы (I), которые могут служить исходными при синтезе соединений формулы (II), можно назвать фенол, пирокатехин, гваякол, гветол, 3-метоксифенол, 3-этоксифенол, 3-изопропоксифенол, 3-трет-бутоксифенол, м-крезол, о-крезол. Условия проведения этапов гидроксиметилирования и окисления поли(гидроксиметил)фенолов описаны в известном уровне техники, упомянутом выше. Можно использовать формальдегид или любой генератор формальдегида, такой, например, как триоксан или параформальдегид, используемый в форме линейных полиформальдегидов с любой степенью полимеризации, имеющей преимущественно число звеньев (СН2O), равное 8-100. Формальдегид может быть использован в виде водного раствора, концентрация которого не является критической. Она может изменяться в интервале от 20 до 50% веса: используют преимущественно промышленные растворы, концентрация которых равна приблизительно 30-40% веса. Количество формальдегида, выраженное в молях формальдегида на моль фенола, может изменяться в широких диапазонах. Молярное соотношение формальдегид/фенол может меняться в интервале 1-8, преимущественно 2 – 4. Количество основания, присутствующего в среде гидроксиметилирования, выраженное числом молей основания к фенольному гидроксилу гидроксиметилируемого фенола, может изменяться в широких диапазонах. Обычно это соотношение зависит от природы основания и может изменяться между 0,1 и 2, но преимущественно между 0,5 и 1,1. В качестве основания можно использовать основания, перечисленные выше для этапа окисления. Целесообразно применять водные растворы гидроокиси щелочных металлов. Обычно этап гидроксиметилирования проводят при температуре, равной 0-100oС, преимущественно равной 20-70oС. Предпочтительно проводить способ под автогенным давлением реактивов, чтобы избежать возможные потери параформальдегида, который может находиться в форме газа, при температурах, используемых для осуществления данного способа. Предпочитают проводить реакцию в контролируемой атмосфере инертных газов, таких как азот или аргон. Продолжительность реакции может быть различна. Очень часто она продолжается от 30 минут до 24 часов, преимущественно от 4 часов до 8 часов. С практической точки зрения реакция легко осуществляется в аппаратуре, куда загружается фенол и формальдегид, в случае необходимости, основание, затем реакционную смесь подвергают перемешиванию при желаемой температуре до тех пор, пока не окончится реакция. Порядок введения реактивов не является критическим и может быть различным. Окисление поли(гидроксиметил)фенолов до поли(формил)фенолов, являющихся промежуточными, с помощью молекулярного кислорода может быть проведено, так как это было изложено выше, т.е. непосредственно в щелочном водном растворе солей поли(гидроксиметил)фенолов, полученных на этапе гидроксиметилирования. В случае необходимости рН раствора доводят до величины 8-13 путем возможного добавления основания щелочного или щелочно-земельного металла. Оптимальная величина рН зависит от природы поли(гидроксиметил)фенолов. Температура реакции окисления составляет 10-100oС, преимущественно 20-60oС. Из фенольных соединений формулы (II) получают, согласно изобретению, 3-карбокси-4-гидроксибензальдегид, который после декарбоксилирования приводит к 4-гидроксибензальдегиду. Как указано выше, способ по изобретению особенно приемлем для получения ванилина и этилванилина. Ниже даются примеры выполнения изобретения. Эти примеры даны только для иллюстрации изобретения, но не ограничивают его. В примерах определяют степень конверсии и полученный выход. Степень соответствует соотношению между числом молей полученного продукта и числом молей введенного субстрата. ПРИМЕРЫ Пример 1. В этом примере осуществляют окисление 4,6-диформилгваякола. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, загружают 0,502 г 4,6-диформилгваякола с концентрацией 86% (2,41 ммоль), 3,3 мл водного раствора гидроокиси натрия с концентрацией 33,4 г/л (2,75 ммоль), 17 мл воды, 0,3 г катализатора, содержащего платину, нанесенную на уголь, с содержанием 2,5% вес. металла и 20 мг сульфата висмута [Bi2(SO4)3]. Подают воздух со скоростью 3 л/час и устанавливают давление 20 бар. Нагревают реакционную смесь при 120oС в течение 2 часов. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную среду анализируют высокоэффективной жидкостной хроматографией. Получены следующие результаты: – конверсия 4,6-диформилгваякола составляет 59%, – выход 5-карбоксиванилина составляет 59%. Пример 2. В нижеследующем примере осуществляют окисление 4-гидроксиметил-6-формилгваякола. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, загружают 0,507 г 4-гидроксиметил-6-формилгваякола (2,75 ммоль), 1,1 мл водного раствора гидроокиси натрия с концентрацией 7,69 моль/л (8,46 ммоль), 19 мл воды, 0,3 г катализатора, содержащего платину, нанесенную на уголь с содержанием 2,5% вес. металла, 0,0185 г сульфата висмута [Bi2(SO4)3]. Подают поток воздуха (3 л/час), поддерживая давление 20 бар. Нагревают в течение 7 часов при 45o С, затем в течение 5 часов 30 минут при 120oС. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную среду затем анализируют высокоэффективной жидкостной хроматографией. Полученные результаты являются следующими: – конверсия 4-гидроксиметил-6-формилгваякола является полной, – выход 5-карбоксиванилина составляет 52%, – выход 5-карбоксиванилиновой кислоты составляет 4,5%, – выход 4,6-диформилгваякола составляет 29%. Пример 3. В этом примере осуществляют окисление 4-гидроксиметил-6-формилгваякола. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, загружают 0,507 г 4-гидроксиметил-6-формилгваякола (2,75 ммоля), 1,1 мл водного раствора гидроокиси натрия с концентрацией 7,69 моль/л (8,46 ммоль), 19 мл воды, 0,3 г катализатора, содержащего платину на угле в количестве 2,5% вес. металла. Подают поток воздуха (3,0 л/час), поддерживая давление 20 бар. Нагревают в течение 4 часов 30 минут при 120oС. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную среду анализируют высокоэффективной жидкостной хроматографией. Полученные результаты являются следующими: – конверсия 4-гидроксиметил-6-формилгваякола составляет 98%, – выход 5-карбоксиванилина составляет 25%, – выход 4,6-диформилгваякола равен 59%. Пример 4. В этом примере осуществляют окисление 4,6-ди(гидроксиметил)гваякола. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, загружают 0,8832 г 4,6 ди-(гидроксиметил)гваякола концентрацией 75% (3,60 ммоль), 1,1 мл водного раствора гидроокиси натрия концентрацией 7,69 моль/л (8,46 ммоль), 19 мл воды, 0,44 г катализатора, содержащего палладий, осаженный на угле в количестве 3% вес. металла. Вводят поток воздуха (3 л/час), поддерживая давление 20 бар. Нагревают в течение 3 часов 40 минут при 120oС. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную смесь анализируют высокоэффективной жидкостной хроматографией. Полученные результаты являются следующими: – конверсия 4,6-ди(гидроксиметил)гваякола полная, – выход 5-карбоксиванилина составляет 32%, – выход 4,6-диформилгваякола составляет 14%, – выход 5-карбоксиванилиновой кислоты составляет 12%. Пример 5. В этом примере осуществляют окисление 4,6-ди(гидроксиметил)гваякола. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, загружают 0,8947 г 4,6-ди(гидроксиметил)гваякола концентрацией 75% (3,64 ммоль), 1,1 мл водного раствора гидроокиси натрия с содержанием 7,69 моль/л (8,46 ммоль), 19 мл воды, 0,46 г катализатора, содержащего платину, осаженную на угле в количестве 2,5% вес. металла. Подают поток воздуха (3 л/час), поддерживая давление 20 бар. Нагревают 3 часа 30 минут при 120oС. Охлаждают смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную среду анализируют путем высокоэффективной жидкостной хроматографии. Полученные результаты являются следующими: – конверсия 4,6-дигидроксиметилгваякола полная, – выход 5-карбоксиванилина составляет 41%, – выход 4,6-диформилгваякола составляет 31%, – выход 5-карбоксиванилиновой кислоты составляет 4,5%. Пример 6. В данном примере осуществляют получение ванилина согласно процедуре, заключающейся в окислении 4,6-ди(гидроксиметил)гваякола с последующим декарбоксилированием. Автоклав емкостью 50 мл, снабженный турбиной для перемешивания, загружают 0,8952 г 4,6-ди(гидроксиметил)гваякола с концентрацией 75% (3,64 ммоль), 1,1 мл водного раствора гидроокиси натрия с содержанием 7,69 моль/л (8,46 ммоль),19 мл воды, 0,44 г катализатора, содержащего платину, нанесенную на уголь в количестве 2,5% вес. металла. Подают поток воздуха (3 л/час), поддерживая давление до 20 бар. Нагревают в течение 3 часов 40 минут при 120oС. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционная среда является гомогенной. Подкисляют реакционную среду с помощью 10 мл 2 н. водного раствора серной кислоты. Нагревают реакционную смесь при автогенном давлении 25 мин при 200oС. Охлаждают реакционную среду, разбавляют ацетонитрилом и анализируют с помощью высокоэффективной жидкостной хроматографии. Выход полученного ванилина равен 41%. Пример 7. В этом примере осуществляют окисление 4,6-диформилгваякола. В автоклав емкостью 2000 мл, снабженный турбиной для перемешивания, загружают 120 г 4,6-диформилгваякола (0,67 моль), 270 г водного раствора гидроокиси натрия с концентрацией 30% вес. (2 моль), 1600 мл воды, 21 г катализатора, содержащего палладий, нанесенный на уголь в количестве 3% вес. металла, 1,4 гсульфата висмута [Bi2(SO4)3]. Подают воздух с расходом 600 л/ч, устанавливая давление 15 бар. Нагревают реакционную смесь при 100oС в течение 1 часа. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную смесь анализируют путем ВЭЖХ. Полученные результаты являются следующими: – конверсия 4,6-диформилгваякола составляет 84%, – выход 5-карбоксиванилина равен 82%. Пример 8. В этом примере также осуществляют окисление 4,6-диформилгваякола. В автоклав емкостью 2000 мл, снабженный турбиной для перемешивания, загружают 120 г 4,6-диформилгваякола (0,67 моль), 210 г водного раствора гидроокиси натрия с концентрацией 30% вес. (2 моль), 1650 мл воды, 20 г катализатора, содержащего платину на угле в количестве 3% вес. металла, 0,3 г сульфата висмута [Bi2(SO4)3]. Подают воздух с расходом 600 л/час, устанавливая давление 15 бар, Нагревают реакционную смесь при 140oС в течение 3 часов. Охлаждают реакционную смесь и доводят давление до атмосферного, затем фильтруют катализатор. Реакционную среду анализируют с помощью ВЭЖХ. Получают следующие результаты: – конверсия 4,6-диформилгваякола равна 89%, – выход 5-карбоксиванилина равен 81%. Примеры 9 и 10. Работают согласно условиям примера 1, но используют оксид висмута (пример 9) или нитрат висмута (пример 10) вместо сульфата висмута. Полученные результаты эквивалентны результатам примера 1, а именно степень конверсии 4,6-диформилгваякола составляет 60%, а выход 5-карбоксиванилина составляет 60%. Пример 11. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, вводят 0,88 г 80%-ного 4,6-ди(гидроксиметил)гветола (3,55 ммоль), 1,1 мл водного раствора гидроксида натрия с концентрацией 7,69 моль/л (8,46 ммоль), 19 мл воды и 0,44 г катализатора, содержащего платину, нанесенную на уголь в количестве 3% мас. В автоклав подают поток воздуха (3 л/час), поддерживая давление 20 бар. Нагревают в течение 3,5 часов при 120oС. Охлаждают реакционную смесь и давление доводят до атмосферного, затем катализатор фильтруют. Реакционную смесь затем анализируют с помощью жидкостной высокоэффективной хроматографии. Получены следующие результаты: – конверсия 4,6-ди(гидроксиметил)гветола полная, – выход 5-карбоксиэтилванилина 30%, – выход 4,6-диформилгветола 17%, – выход 5-карбоксиэтилванилиновой кислоты 10%. Пример 12. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, вводят 0,88 г 80%-ного 4,6-ди(гидроксиметил)гветола (3,55 ммоль), 1,1 мл водного раствора гидроксида натрия с концентрацией 7,69 моль/л (8,46 ммоль), 18 мл воды и 0,46 г катализатора, содержащего платину, нанесенную на уголь в количестве 2,5% мас. В автоклав подают поток воздуха (3 л/час), поддерживая давление 20 бар. Нагревают в течение 3,5 часов при 120oС. Охлаждают реакционную смесь и давление доводят до атмосферного, затем катализатор фильтруют. Реакционную среду анализируют с помощью высокоэффективной жидкостной хротатографии. Получают следующие результаты: – конверсия 4,6-дигидроксиметилгветола полная, – выход 5-карбоксиэтилванилина 38%, – выход 4,6-диформилгветола 35%, – выход 5-карбоксиэтилванилиновой кислоты 3%. Пример 13. В этом примере иллюстрируется получение ванилина по схеме, включающей окисление 4,6-ди(гидроксиметил)гветола с последующим декарбоксилированием. В автоклав емкостью 50 мл, снабженный турбиной для перемешивания, вводят 0,88 г 80%-ного 4,6-ди(гидроксиметил)гветола (3,55 моль), 1,1 мл водного раствора гидроксида натрия с концентрацией 7,69 моль/л (8,46 ммоль), 20 мл воды и 0,44 г катилизатора, содержащего платину, нанесенную на уголь в количестве 2,5% мас. Вводят в автоклав поток воздуха (3 л/час), поддерживая давление 20 бар. Нагревают в течение 3,5 часов при 120oС. Охлаждают реакционную смесь и давление доводят до атмосферного, затем катализатор фильтруют. Реакционная среда гомогенна. Подкисляют реакционную среду с помощью 10 мл 2 н. водного раствора серной кислоты. Нагревают реакционную смесь при автогенном давлении в течение 30 мин при 200oС. Охлаждают реакционную среду, разбавляют ацетонитрилом и анализируют путем высокоэффективной жидкостной хроматографии. Выход этилванилина составил 39%. Формула изобретения
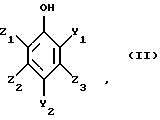 в которой Y1 и Y2, одинаковые или различные, обозначают -СНО или -СН2ОН; Z1, Z2 и Z3, одинаковые или различные, обозначают атом водорода, линейный или разветвленный алкенил С2-С4, С1-С4-алкил или С1-С4-алкокси, фенил, гидроксил, нитро, атом галогена, подвергают селективному окислению, при котором группа в положении 2 окисляется до карбоксигруппы и возможная гидроксиметильная группа в положении 4 окисляется до формильной группы, в присутствии основания и катализатора на основе металла М1, выбранного из металлов группы Ib и 8 Периодической системы элементов. 2. Способ по п. 1, отличающийся тем, что используют фенольное соединение формулы II, в которой Z1, Z2 и Z3, одинаковые или различные, обозначают атом водорода, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, винил, аллил, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, фенил, атом фтора, хлора или брома. 3. Способ по одному из пп. 1 и 2, отличающийся тем, что используют фенольное соединение общей формулы II, в которой 1 обозначает С1-С4-алкокси, Z2 и Z3 обозначают атом водорода, Y1 и Y2 одинаковые и обозначают формил или гидроксиметил. 4. Способ по одному из пп. 1-3, отличающийся тем, что фенольное соединение формулы II представляет собой 2,4-диформилфенол, 1,2-дигидрокси-3,5-диформилбензол, 1-гидрокси-2-метокси-4,6-диформилбензол (4,6-диформилгваякол), 1-гидрокси-2-этокси-4,6-диформилбензол (4,6-диформилгветол), 4,6-ди(гидроксиметил)гваякол, 4,6-ди(гидроксиметил)гветол. 5. Способ по одному из пп. 1-4, отличающийся тем, что фенольное соединение формулы II окисляют в жидкой фазе с помощью молекулярного кислорода или кислородсодержащего газа в водной среде, содержащей основный агент, в присутствии катализатора на основе металла М1, выбираемого среди металлов группы Ib и 8 Периодической системы элементов и содержащего, в случае необходимости, в качестве активатора такие металлы, как кадмий, церий, висмут. 6. Способ по п. 5, отличающийся тем, что катализатор является катализатором на основе платины и/или палладия. 7. Способ по одному из п. 5 или 6, отличающийся тем, что катализатор на основе платины или палладия используют в форме платиновой черни, палладиевой черни, оксида платины, оксида палладия или благородного металла, нанесенного на носитель, такой как сажа. 8. Способ по одному из пп. 5-7, отличающийся тем, что количество используемого катализатора, выраженное отношением массы металла М1 к массе фенольного соединения формулы II, составляет 0,01 – 10%, предпочтительно 0,04-2%. 9. Способ по одному из пп. 5-8, отличающийся тем, что активатором является органическое или неорганическое производное висмута, выбранное из группы, включающей оксиды висмута, гидроксиды висмута, соли висмута с минеральными водородными кислотами, соли висмута с минеральными оксикислотами. 10. Способ по п. 9, отличающийся тем, что производное висмута выбирают из группы, включающей оксиды висмута, гидроксиды висмута, хлорид висмута, нитрат висмута, нейтральный сульфат висмута. 11. Способ по одному из пп. 5-10, отличающийся тем, что количество активатора выбирают таким образом, чтобы в среде находилось, с одной стороны, по меньшей мере 0,1 маc. % металла-активатора по отношению к массе введенного металла 1, а, с другой стороны, 10-900 ррм маc. металла М1 по отношению к фенольному соединению формулы II. 12. Способ по одному из пп. 5-11, отличающийся тем, что реакцию окисления ведут при температуре 30-200oС, преимущественно при 40-160oС. 13. Способ по одному из пп. 5-12, отличающийся тем, что работают под давлением 1-20 бар. 14. Способ по одному из пп. 1-13, отличающийся тем, что окисление проводят в водной среде, содержащей растворенный основный агент, преимущественно гидроокись натрия или калия, в количестве 0,5-10 молей минерального основания на 1 моль фенольного соединения формулы II. 15. Способ по одному из пп. 12 и 14, отличающийся тем, что в случае использования платинового катализатора температура реакции составляет 100-160oС, а количество используемого основания составляет 1 – 3 молей на 1 моль фенольного соединения формулы II. 16. Способ по одному из пп. 12 и 14, отличающийся тем, что в случае использования палладиевого катализатора температура реакции составляет 30-200oС, предпочтительно 30-100oС, а количество используемого основания составляет 2-4 моля на 1 моль фенольного соединения формулы II. 17. Способ по одному из пп. 1-16, отличающийся тем, что исходные субстраты отвечают формулам (IIа), (IIв), (IIс) и (IId) 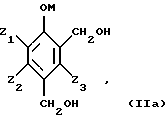 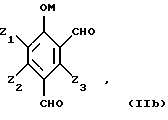 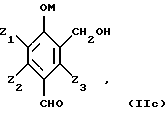 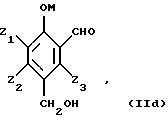 в формулах (IIа)-(IId) М – атом водорода и/или катион металла группы (Iа); Z1, Z2, Z3 имеют значения, определенные в пп. 1-3. 18. Способ по п. 17, отличающийся тем, что соединение формулы (IIb) получено окислением поли(гидроксиметил)фенолов формулы (IIа) с помощью молекулярного кислорода или кислородсодержащего газа в водной щелочной фазе в присутствии катализатора на основе металла группы 8 Периодической системы, преимущественно платины или палладия, содержащего, в случае необходимости, в качестве активатора такие металлы, как кадмий, церий, висмут. 19. Способ по одному из п. 17 или 18, отличающийся тем, что поли(гидроксиметил)фенолы формулы (IIа) получены способом в два этапа, состоящим из гидроксиметилирования фенола, незамещенного на положениях орто и пара по отношению к гидроксильной группе, общей формулы (I) 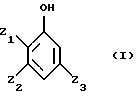 до получения поли(гидроксиметил)фенола, содержащего, по меньшей мере, одну гидроксиметильную группу в положении орто и пара по отношению к гидроксильной группе, общей формулы (IIа) 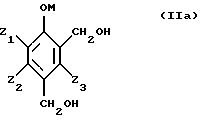 с помощью формальдегида или генератора формальдегида в водной фазе в присутствии основания щелочного или щелочноземельного металла, окисления в щелочной водной фазе полученного поли(гидроксиметил)фенола формулы (IIа) с помощью молекулярного кислорода или кислородсодержащего газа в присутствии катализатора на основе металла группы 8 Периодической системы, содержащего, в случае необходимости, металл, используемый в качестве активатора, без промежуточного выделения поли(гидроксиметил)фенолов. 20. Способ по п. 19, отличающийся тем, что фенол формулы (I) представляет собой фенол, пирокатехин, гваякол, гветол, 3-метоксифенол, 3-этоксифенол, 3-изопропоксифенол, 3-трет-бутилоксифенол, м-крезол, о-крезол. 21. Способ по п. 19, отличающийся тем, что реакцию окисления соединений формулы (IIа) проводят в интервале температур 10-100oC, преимущественно 20-60oС. 22. Способ получения 4-гидроксибензальдегида путем декарбоксилирования 3-карбокси-4-гидроксибензальдегида, отличающийся тем, что 3-карбокси-4-гидроксибензальдегид получают, подвергая фенольное соединение, несущее формильную и/или гидроксиметильную группы в положении 2 и 4, селективному окислению, при котором группы в положении 2 окисляются до карбоксильной группы, возможно, гидроксиметильная группа в положении 4 окисляется до формильной группы, согласно способу, описанному в одном из пп. 1-15. 23. Способ по п. 22, отличающийся тем, что осуществляют декарбоксилирование кислоты путем добавления протоновой кислоты минерального происхождения, преимущественно соляной кислоты или серной кислоты, или органической кислоты, до получения рН ниже или равного 3. 24. Способ по одному из пп. 22 и 23, отличающийся тем, что реакционную среду нагревают при температуре 120 – 350oС, предпочтительно при 150-220oС, и после охлаждения выделяют полученный 4-гидроксибензальдегид. 25. Способ получения ванилина, отличающийся тем, что окисляют 4,6-диформилгваякол или 4,6-ди(гидроксиметил)гваякол, или 4-формил-6-гидроксиметилгваякол, или 4-гидроксиметил-6-формилгваякол до 5-карбоксиванилина согласно способу, описанному в одном из пп. 1-15, затем удаляют карбоксильную группу в положении 5 и получают ванилин. 26. Способ получения этилванилина, отличающийся тем, что окисляют 4,6-диформилгветол или 4,6-ди(гидроксиметил)гветол, или 4-формил-6-гидроксиметилгветол, или 4-гидроксиметил-6-формилгветол до 5-карбоксиэтилванилина согласно способу, описанному в одном из пп. 1-15, затем удаляют карбоксильную группу, расположенную в положении 5, и получают этилванилин. |
||||||||||||||||||||||||||
