Патент на изобретение №2183964
|
||||||||||||||||||||||||||
(54) ЭКСТРАКТ СОИ, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
(57) Реферат: Изобретение относится к области медицины. Соевый экстракт содержит 0,6 – 1,5 вес. ч. сапонинов сои группы В в расчете на 1 вес.ч. глюкозидных изофлавонов, содержащихся по меньшей мере в количестве 13% в экстракте. Проводят экстракцию обезжиренных соевых бобов или муки алифатическими спиртами или их водными смесями при реципрокном отношении 3:2 – 2:3. Экстракт концентрируют, очищают. Экстрагируют алифатическими углеводородами, не смешивающимися с водой, спиртами, не смешивающимися с водой. Экстракт концентрируют и сушат. Фармацевтическая композиция содержит экстракт сои для лечения и профилактики предклимактерических и постклимактерических симптомов, алкоголизма, для лечения рака молочной железы, простаты. Изобретение позволяет повысить эффективность средств. 3 с. и 8 з.п. ф-лы, 1 ил., 3 табл. Изобретение касается новых экстрактов, получаемых путем экстрагирования зрелых цельных бобов сои или обезжиренной соевой муки Glycine max (L.) Merril: семейство – Leguminosae, их приготовления и композиций, содержащих эти экстракты. Новые экстракты характеризуются содержанием в них изофлавонов и сапонинов при определенном их соотношении. Известно, что соя содержит сапонины и изофлавоновые компоненты в дополнение к сахарам и аминокислотам, равно как белки и минеральные соли, в количествах, которые зависят от географического происхождения сои и от условий, в которых данное растение было выращено и собрано. Содержащиеся в сое сапонины могут быть разделены на три класса на основе химической структуры их тритерпеновых компонентов – сапонины сои групп А, В и Е (K.Okubo et al., 1994, ACS Symp., Ser. 546, 330). 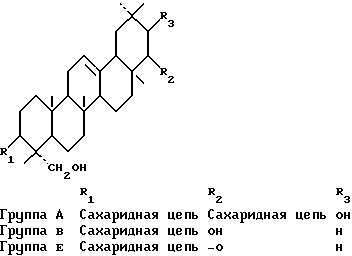 Изофлавоновые компоненты включают в себя глюкозидные изофлавоны (даидзин, генистин и глицитин), которые могут включать в себя ацильные радикалы, например малонильные радикалы, соединенные сахаридной цепью. 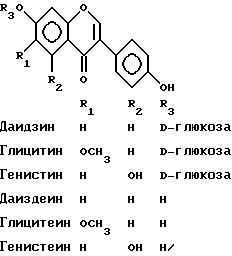 В соответствии с биомедицинской литературой и опубликованной в последние годы эпидемиологической информацией, особенно в связи с населением стран Востока, в значительной степени использующим кулинарные продукты на основе сои, употребление такой пищи в значительной степени снижает предклимактерические и постклимактерические проявления у женщин (A.Cassidy, 1996, Ртос. Nutrition Soc. , 55, 339-417). Эти эффекты, для которых пока нет достаточно точного научного обоснования, обычно связывают с генистеином, даидзеином и глицитеином, являющимися изофлавоновыми агликонами, которые присутствуют в различных пищевых продуктах, приготовленных с использованием сои. Изофлавоны обычно воспринимаются как растительные эстрогены, а во многих исследованиях in vitro было показано, что эти соединения действуют в соответствии с механизмом, обеспечивающим конкуренцию эстрогенам млекопитающих, притом что их активность оценивается в 500-1000 раз ниже, чем у эстрадиола (D.A.Shutt & P.I.Сох, 1972, J. Endocrinol, 52, 299-310). Далее, в соответствии с биомедицинской литературой и недавно опубликованной эпидемиологической информацией, конкретно касающейся групп населения Востока, где в большей степени принято употребление сои в пищу, употребление такой пищи связано со значительным снижением частоты рака молочной железы у женщин и аденомы простаты у мужчин (A.Nomura, B.E. Henderson, J.Lee, 1978, Amer. J, Clin. Nutrition, 31, 2020-2025; T.Hirayama, 1986, In “Diet, Nutrition & Cancer”, 41-53, eds. Y.Hayashi, M.Nagao, T.Sugimura, S.Takayama, L. Tomatis, L. M. Wattenberg & G.N.Wogan, Jap. Sci. Soc. Press, Tokyo; R.K.Severson, A. M. Y. Nomura, J.S.Grove, G.N.Stem-merman, 1989, Cancer Res., 49, 1857-1860). Также эти факты, которые пока не получили обоснованного научного объяснения, обычно связывают с генистеином, даидзеином и глицитеином, являющимися изофлавоновыми агликонами, которые содержатся в различных пищевых продуктах на основе сои. Эти изофлавоны были исследованы в моделях in vitro с целью определения их способности взаимодействовать с протеинкиназами, в частности с тирозинкиназой, т. е. ферментами, которые, по-видимому, играют важную роль в пролиферации опухолевых клеток. В последнее время были предприняты многочисленные попытки получить лекарственные средства, основанные на соевых экстрактах, направленные на профилактику предклимактерических и постклимактерических симптомов, а также предназначенные для профилактики и лечения раковых опухолей. Некоторые выданные патенты и заявки на патенты описывают композиции новых соевых экстрактов, получаемых путем химического или ферментативного гидролиза глюкозидных изофлавонов, содержащихся в соевых бобах или проростках сои (японские заявки Kikkoman Corp. – J-08291191, J-07173148, J-0511707566; заявка на международный патент G.E.Kelly, WO 93/23069). Все эти публикации касаются исключительно приготовления изофлавонов в высоких концентрациях и их активностей в отношении контроля предклимактерических и постклимактерических расстройств, а также их противоопухолевых активностей. К настоящему времени установлено, что в отличие от сообщавшегося ранее экстракты, которые содержат глюкозидные изофлавоны и соевые сапонины группы В в определенном соотношении, оказываются гораздо более активными по сравнению с “чистыми” изофлавонами как в отношении профилактики, так и лечения предклимактерических и постклимактерических симптомов и предотвращения или лечения раковых опухолей. Еще один аспект настоящего изобретения, связанный с данным экстрактом, касается злоупотребления алкоголем, алкогольной зависимости или алкогольного привыкания. Все эти явления могут быть объединены общим термином – “алкоголизм”: все они составляют серьезную проблему для всего современного общества (G.L.Gessa, 1994, “Bisogno compulsive di bere e principio del piacere” [“The compulsion to drink and the pleasure principle”], Med. tossicodipend. [“Med. Dru Dependence], II, 5). В Италии, например, более 9% всего населения (примерно 5 млн. человек) являются “глубокими пьяницами”, а более 1 млн. человек страдают алкогольной зависимостью (F.P.Calamo-Spechhia, 1991, “Epidemiologia dell’alcolismo in Italia” [“Epidemiology of alcoholism in Italy”], Atti VII Congr. Naz. S.I.A. [Repts 7th Natl. Congr. S.I.A.], Mediserve, Rome, 295-301). Указанные цифры возрастают тогда, когда в расчет принимают такие страны как США, где более 13 млн. человек характеризуются алкогольной зависимостью. Пристрастие к алкоголю и настоящая алкогольная зависимость приводят к очень значительным общественно-экономическим потерям (с 1991 года в США такие потери составляли примерно 200 млрд. долларов в год) и обусловливают серьезные социальные и психологические проблемы у тех, кто подвержен таким зависимостям. Существующие попытки лечения алкоголизма, дополняющие психологические способы (“групповая терапия” и т.п.), связаны с применением лекарственных средств, таких как дисульфирам и карбамид кальция, которые влияют на метаболизм спиртов с подавлением печеночной адьдегиддегидрогеназы – в результате возрастает количество ацетальдегидов, являющихся индуктором рвотного рефлекса, а также всех других нежелательных явлений, сопровождающих употребление алкоголя. В соответствии с предыдущим уровнем техники единственными растениями, применяемыми в лечении алкоголизма, являются пуерария Pueraria lobata (препарат корней Radix puerarie) и шалфей Salvia multiorrhiza, которые имеют широкое распространение в традиционой китайской медицине и являлись объектом представления в патентных заявках WО 93/00896 и WO 96/35441. В дополнение к применению этих экстрактов в данных патентных заявках описано применение чистых соединений, таких как даидзеин и их полусинтетические производные (WО 93/00896), или дитерпеноидов, таких как таншинон и милтирон (WО 96/35441). Влияние на алкогольдегидрогеназу с проявлением вышеописанных побочных действий было установлено для изофлавоновых производных, хотя именно такой механизм для дитерпеноидных соединений был исключен. Более того, в патентной заявке WO 96/36332 описано действие форсколина в снижении потребления алкоголя. Неожиданно было установлено, что экстракты, содержащие глюкозидные изофлавоны и сапонины сои группы В в определенных соотношениях, могут быть с успехом использованы для снижения умышленного употребления алкоголя. Эти экстракты оказываются существенно более эффективными по сравнению с “чистыми” изофлавонами и действуют в соответствии с механизмом, который отличается от того, который связан с подавлением активности алкогольдегидрогеназы, поскольку содержание спирта в плазме остается неизменным. В дополнение к упоминавшимся заявкам в международной патентной заявке WO 96/10341 описаны пищевые или оздоровительные продукты, включая хорошо очищенные гипокотили семян сои. При этом не описана процедура экстракции, а также не определено соотношение изофлавонов и сапонинов, что восполнено настоящим изобретением. В патенте США 4428876 представлен способ выделения сапонинов и флавоноидов из бобовых растений. Описанная в этом патенте экстракция сои с использованием 0,4%-ного водного раствора едкого натра приводит в конечном счете к получению такого экстракта, который отличается от того, что получают согласно данному изобретению. Опять-таки не было сделано определений соотношения сапонинов и изофлавонов, выполненного в настоящем изобретении. В японском патенте 59088064 представлено выделение и применение только сапонинов. То же самое относится и к германскому патенту 34-00-258. Сходным образом японский патент 61036225 касается выделения и очистки сапонинов, а японский патент 62005917 – приготовления очищенных сапонинов, которые полностью свободны от изофлавонов. Японский патент 4036242 касается получения чистого сапонина или экстракта, характеризующегося высоким отношением “сапонин/изофлавон”, являющегося противовоспалительным препаратом. В европейской патентной заявке А-426998 описано получение изофлавонов из сои, в частности генистина и даидзинма-лоната. При этом в ней нет описания экстракции сапонинов и определения соотношений между изофлавонами и сапонинами. В японском патенте 63245648 описано получение пищевого соевого продукта, не содержащего сапонинов и изофлавонов, которые рассматриваются как те жесткие компоненты, которые делают данный вид пищи малосъедобным. В статье M. Messina et al., 1991, (J. Natl. Cancer Inst., v.83, No.8, 541-546) охарактеризована роль соевых продуктов в снижении риска развития рака, о которой уже сообщалось в научной литературе. Однако ни в этой статье, ни вообще в литературе не сообщалось о соевом экстракте, содержащем сапонины и изофлавоны в соотношении, определенном в настоящем изобретении: в этих работах лишь рассматривались фармакологические проявления, наблюдаемые при использовании конкретного экстракта. В настоящем изобретении соответственно представлен экстракт, который содержит 0,6 – 1,5 вес.ч., предпочтительно 1 вес.ч. сапонинов сои группы В, к одной весовой части глюкозидных изофлавонов, при этом содержание глюкозидных изофлавонов в данном экстракте по весу должно составлять по меньшей мере 13%. Как показано методами HPLC-MS сапонины сои группы B, которые обладают позитивным эффектом на активность изофлавоновых компонентов, характеризуются следующей структурой: 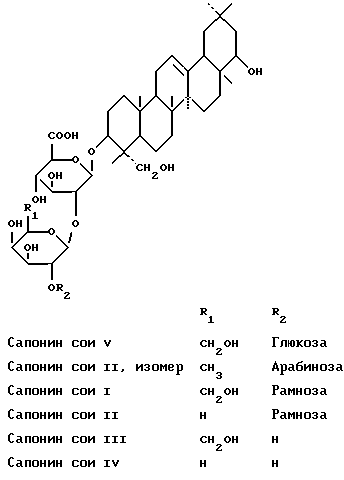 Далее настоящее изобретение связано со способом получения указанного выше экстракта, который отличается тем, что он включает в себя следующие стадии: a) экстрагирование зрелых цельных соевых бобов или обезжиренной соевой муки с использованием алифатических спиртов или смеси этих спиртов с водой; b) концентрирование экстракта, полученного на стадии (а); c) очистка концентрированного экстракта стадии (b) от маслянистых и липофильных компонентов путем обработки алифатическими углеводородами; d) экстрагирование активных компонентов не смешивающимися с водой алифатическими спиртами; е) концентрирование экстракта, полученного на стадии (d), и его высушивание. В частности, экстракты согласно изобретению могут быть получены путем экстракции необработанных цельных соевых бобов или обезжиренной соевой муки, содержащих сапонины сои группы В и глюкозидные изофлавоны в реципрокном соотношении 3: 2 – 2:3 с использованием алифатических спиртов самих по себе или их смесей с водой: предпочтительно смесью этилового спирта и воды, такого как 95% чистый этанол. После концентрирования и очистки от маслянистых и липофильных компонентов путем обработки алифатическими углеводородами (например, n-гексаном или n-гептаном) активные компоненты экстрагируются с помощью не смешивающихся с водой алифатических спиртов, таких как n-бутанол, изобутанол и изоамиловый спирт. После концентрирования в меньший объем органическую фазу высушивают при пониженном давлении. Далее настоящее изобретение представляет модификацию описанного выше способа, в которой после стадий (b) или (с) концентрированный спиртовой экстракт подвергают стадии (d’), после которой следует стадия (е): d’) адсорбция активных компонентов на полистиреновой адсорбционной колонке, струйная промывка этой колонки водой и элюция активных компонентов этанолом. В соответствии с этой модификацией типичный экстракт согласно изобретению может быть получен в результате адсорбции активных компонентов (ивофлавоны и сапонины), которые присутствуют в концентрированном спиртовом экстракте растительного материала, с использованием полистиреновой адсорбционной смолы, такой как дуолитная смола или любая смола XAD, в частности смола XAD1180 благодаря ее слабой кислотности, а затем в результате элюции смеси изофлавонов и сапонинов сои группы В с помощью этилового спирта после тщательного вымывания колонки струей воды с целью удаления солей и других неактивных компонентов. Полученный в таких условиях экстракт содержит от 13% до 17% (по весу) изофлавонов и 0,6 – 1,5 частей (по весу) сапонинов сои группы В, в зависимости от качества использовавшегося растительного материала, в расчете на 1 вес. ч. глюкозидных изофлавонов. Этот экстракт также содержит значительное количество полифенольных веществ, для которых подтверждается существенность в связи с проявлением свойств, характерных для этого экстракта. Вариант изложенного выше способа и его модификации включает в себя следующие стадии: f) суспендирование экстракта, полученного на стадии (е) в смеси смешивающегося с водой спирта и воды и разведение его несмешивающимся с водой апротонным растворителем; g) нагревание смеси, полученной на стадии (f), обеспечивающее растворение, с последующим оставлением при комнатной температуре; h) отбор преципитированных сапонинов сои группы В с помощью фильтрации; i) отделение органической фазы от водной фазы и концентрирование органической фазы с последующим высушиванием ее с получением изофлавоновых компонентов; и j) смешивание сапонинов, полученных на стадии (h), и изофлавонов, полученных на стадии (i), с целью получения итогового экстракта. Соответственно экстракты согласно изобретению, причем даже те, которые отличаются очень высоким содержанием глюкозидных изофлавонов и сапонинов сои группы В, при соблюдении указывавшегося выше соотношения могут быть предпочтительно получены из экстрактов, полученных в соответствии с описанным выше способом или его модификацией. Для этой цели процедура может быть осуществлена следующим путем: упомянутый экстракт суспендируют в смешивающемся с водой спирте, таком как этанол или метанол, при содержании воды 10 – 50% по объему, и разводят в несмешивающемся с водой растворителе, таком как метиленхлорид или этилацетат. Полученную гетерогенную смесь нагревают с целью обеспечения полного растворения экстракта и оставляют при комнатной температуре, в результате чего происходит осаждение сапонинов сои группы В. Сапонины, чистота которых превышает 90%, отбирают с помощью фильтрования. Изофлавоновые компоненты, характеризующиеся чистотой свыше 80%, получают из маточного водного раствора путем отделения органической фазы и ее выпаривания и высушивания. Затем сапонины и изофлавоны могут быть смешаны с целью получения экстракта, характеризующегося наивысшим из возможных содержанием глюкозидных изофлавонов и характеризующегося содержанием сапонинов сои группы В на уровне 0,6 – 1,5 частей (по весу) в расчете на 1 вес.ч. глюкозидных изофлавонов. Предпочтительными условиями проведения отдельных стадий способа согласно изобретению являются следующие. При этом единицами измерения частей объема являются литры (л), а единицами весового измерения являются килограммы (кг). Стадия (а). Растительный материал предпочтительно экстрагируют 12-17 объемами растворителя в расчете на 1 вес.ч. биомассы. Температуру экстракции целесообразно поддерживать на уровне выше 55oС. Каждую экстракцию целесообразно проводить на протяжении не менее 4 ч. В дополнение к этанолу подходящими растворителями являются, помимо прочего, метанол, пропанол и изопропанол. Эти растворители могут содержать до 10% воды. Стадия (b). Целесообразно проводить концентрирование экстракта при температуре ниже 50oС в условиях пониженного давления. Экстракт целесообразно концентрировать до содержания спирта 65 – 75%. Стадия (с). Очистку целесообразно проводить с использованием 0,3-0,6 объемов алифатических углеводородов в расчете на 1 часть (по весу) растительного материала. Подходящей процедурой является та, которая обеспечивает экстрагирование маслянистых и липофильных соединений. Стадия (d). Активные соединения целесообразно экстрагировать с использованием 0,2-0,4 объемов спиртового несмешивающегося с водой растворителя на 1 экстракцию при расчете на 1 вес.ч. растительного материала; предпочтительным является проведение трех экстракций. Стадия (е). Экстракт, полученный на стадии (d), целесообразно концентрировать при температуре ниже 50oС в условиях пониженного давления. Стадии (f). Экстракт, полученный на стадии (е), целесообразно суспендировать в 5-10 объемах (в расчете на 1 часть экстракта) водорастворимого спирта с использованием объемного соотношения спирта и воды 2:8 – 3:7. Апротонный, несмешивающийся с водой растворитель целесообразно использовать в количестве от 2 до 5 объемов в расчете на 1 вес.ч. экстракта стадии (е). Стадия (g). Для достижения полного растворения смесь целесообразно нагреть и выдержать в условиях нагревания с обратным холодильником. Затем смесь целесообразно выдержать при комнатной температуре в течение 15-24 ч. Стадия (i). Органическую фазу целесообразно концентрировать путем упаривания при температуре ниже 30oС в условиях пониженного давления. Стадия (j). Предпочтительно сапонины, полученные на стадии (h), и глюкозидные изофлавоны, полученные на стадии (g), используют для приготовления спиртового раствора, который содержит сапонины и глюкозидные изофлавоны в соотношении 1:1, при этом этот раствор затем целесообразно подвергнуть концентрированию до высыхания при температуре ниже 50oС в условиях пониженного давления. Количество изофлавонов и сапонинов сои группы В определяют с помощью ВЭЖХ с использованием колонки SupelcoSil LC-ABZ (250  4,6 мм) и тройной элюционной среды с градиентом, включающим в себя (А) воду (СF3СООН-0,01%), (В) ацетонитрил (СF3СООН – 0,01%) и (С) метанол (CF3COOH-0,01%). Отдельные компоненты могут быть идентифицированы и охарактеризованы с помощью масс-спектрометрии в сочетании с ВЭЖХ через термораспыляющую границу раздела.
Экстракты согласно изобретению отличаются от ранее известных экстрактов их специфическим воздействием.
В отношении климактерических расстройств “приливы” крови, бессонница и депрессия являются наиболее распространенными симптомами климакса, от которых страдают женщины в этот период жизни. Они сопровождаются снижением или прекращением работы яичников и, как результат, снижением выработки эстрогенов и увеличением выработки лютеинизирующего гормона (ЛГ; и фолликулостимулирующего гормона (ФСГ).
В недавнем исследовании (E.M.Duker et al., 1991, Planta Med., 57, 420) сообщалось о том, что в результате овариэктомии (удаления яичников) у самок крыс наблюдается связь между случайным возрастанием уровня ЛГ и изменениями температуры кожи. Такая взаимосвязь между уровнем ЛГ и “приливами”, которая наблюдается не только у являющихся моделью крыс, но и у женщин, подтверждает то, что доза секретируемого ЛГ может рассматриваться в качестве информативного параметра в анализе психоневротических и эндокринных проявлений активных эндокринных соединений.
В таблице 1 показаны результаты, которые были получены тогда, когда на подвергшихся овариэктомии самках крыс испытывали воздействие двух отдельных фракций (изофлавоны и сапонины сои группы В) и экстрактов согласно изобретению.
Самки крыс были подвергнуты овариэктомии с применением известных методик. Спустя 15 дней после операции животных подвергали воздействию тестируемых препаратов путем однократного ежедневного перорального введения в течение 15 дней. Животных умерщвляли через 3 часа после последнего введения препарата. Кровь центрифугировали немедленно после этого и полученную сыворотку хранили при -25oС до момента определения содержания ЛГ радиоиммунным методом, в соответствии с методом, описанным Нис-уэндером с соавт. (Niswender et al., 1986, Proc. Soc. Exp. Biol. Med., 128, 807).
Как можно видеть, введение экстрактов согласно изобретению приводило к статистически существенному снижению уровня ЛГ, которое было более существенным по сравнению с тем, которое определяется суммой отдельных компонентов (эффект синергизма).
Экстракты, использовавшиеся в повторных воздействиях на здоровых животных, не приводили к каким-либо макроскопическим или микроскопическим изменениям в органах или системах у самцов животных, в то время как у самок они модифицировали вес матки и скелета, что подтверждает их эстрогенную активность.
Когда экстракты согласно изобретению вводились женщинам в процессе менопаузы (независимо от того, происходит ли это естественным путем или в результате хирургического вмешательства), они приводили к изменению содержания ЛГ в плазме и снижали климактерические расстройства, такие как “приливы” или депрессия и т.п., в течение нескольких дней воздействия, а при таком же воздействии на протяжении длительного периода также было отмечено снижение уровня деминерализации костей.
Экстракты согласно изобретению также обладали отчетливой антипролиферационной активностью. В таблице 2 показана антипролиферационная активность в отношении линии клеток опухоли яичников (OVCA 433).
Клетки культивировали в монослойной культуре с использованием минимальной культуральной среды с добавлением телячьей сыворотки и 200 ед./мл пенициллина с целью поддержания стерильности среды. Для воспроизводимости результатов тестирования клетки обрабатывали трипсином каждую неделю, высевали при плотности 80 тыс. клеток на 1 мл и инкубировали при 37oС в атмосфере воздуха при содержании 5% СO2 и наличии влажности. Для тестирования активности данных соединений клетки помещали в лунки планшета “Фалькон” (Falcon 3046, Becton Dickinson, NY) в концентрации 100 тыс. клеток на 1 мл и при минимальном количестве субстрата. Спустя 24 ч субстрат замещали свежей порцией субстрата и добавляли предназначенные для тестирования соединения, растворенные в абсолютном этиловом спирте. Контрольные варианты обрабатывали точно таким же образом, за исключением того, что предназначенные для тестирования соединения отсутствовали. Описанную выше обработку повторяли с интервалом в сутки в течение всего периода тестирования, составившего 72 ч. Уровень подавления пролиферации клеток оценивали путем прямого подсчета их количества: при этом рост контрольных вариантов сравнивали с ростом вариантов тестирования, подвергнутых “обработке”. Как было установлено, экстракты согласно изобретению проявляли антипролиферативную активность, которая была больше суммы антипролиферативных активностей входящих в него компонентов (активность по типу синергизма). Соединения согласно изобретению подавляли пролиферацию клеток in vivo: это было подтверждено при измерении размеров опухолей, пересаженных бестимусным мышам линии “naked”, что было осуществлено обычными методиками, описанными в литературе. Введение этим животным экстракта в дозах от 10 до 500 мг/кг приводило к отчетливой дегенерации анализируемых опухолей, вплоть до их полного рассасывания у значительной части подопытных особей.
Что касается ингибирующего действия на употребление алкоголя, то такой эффект был исследован с использованием употребляющих алкоголь крыс, представляющих специализированную линию “сардинийская, предпочитающая алкоголь” (Sp) (F. Fadda, E. Mosca, G.Colombo, G.L.Gessa, 1990, “Alcohol preferring rats: Genetic sensitivity to alcohol-induced stimulation of dopamine metabolism”, Physiol. Behav. , 47, 727). Эти животные, которые при организации для них свободного выбора между этиловым спиртом и водой потребляют 6-7 г спирта в расчете на 1 кг веса тела в день (при том, что спирт разбавлен водой втрое), были в последние годы успешно использованы при определении влияния различных соединений на добровольное употребление алкоголя: см., например, A. Balakleevsky, G. Colombo, F.Fadda, G.L.Gessa, 1990, “Ro 19-4603, a benzo-diazepine receptor inverse agonist, attenuates voluntary ethanol consumption in rats selectively bred for high ethanol preference”, Alcohol, 25, 449-452; F.Fadda, В. Garau, G.Colombo, G.L.Gessa, 1992, “Isradipine and other calcium channel antagonists attenuate ethanol consumption in ethanol-preferring rats”. In “Alcoholism: Clinical & Experimental Research”, 16, 449-452.
Животные, которых содержали в нормальных условиях, могли свободно выбирать между водой (вода присутствовала всегда) и алкоголем (10%-ный объемный раствор в воде), который предлагался только в течение 4 часов в сутки (т.е. в первые четыре темных часа при обычном суточном режиме освещения). Количество употребленных воды и алкоголя регистрировали ежедневно в одно и то же время. Кормили животных вволю (ad libitum). После того, как достигалась стабилизация соотношения употребляемых воды и алкоголя, экстракт при дозе 1000 мг на 1 кг (при суспендировании его в воде) вводили перорально при его объемном количестве 2 мг/кг в день в течение 7 последовательных дней. В качестве контроля использовали идентичный объем наполнителя. По окончании обработки употребление алкоголя регистрировали до тех пор, пока не достигались показатели, которые были установлены до проведения тестирования.
Таблица 3 показывает влияние повторяющегося перорального введения 1000 мг/кг соевого экстракта на употребление алкоголя.
Данные таблицы 3 позволяют сделать заключение, что соевый экстракт в существенной степени уменьшает уровень употребления алкоголя. Снижение употребления алкоголя остается стабильным на протяжении всех 7 дней тестирования и затем ослабевает по окончании воздействия. Более того, можно видеть, что снижение употребления алкоголя оказывается более существенным по сравнению с тем эффектом, который определяется суммой эффектов отдельных компонентов экстракта (эффект синергизма).
Далее, настоящее изобретение также связано с фармацевтической композицией, которая содержит определяемый выше экстракт в качестве своего активного компонента. В частности, настоящее изобретение связано с фармацевтической композицией, содержащей этот экстракт и предназначенной для профилактики или лечения предклимактерических и постклимактерических симптомов, фармацевтической композицией, содержащей данный экстракт и предназначенный для профилактики и лечения рака молочной железы у женщин и аденомы простаты у мужчин, а также фармацевтической композицией, содержащей данный экстракт и предназначенной для профилактики или лечения алкоголизма.
Продукты или экстракты согласно изобретению могут быть приготовлены подходящим образом в виде таблеток, мягких или твердых желатиновых капсул, гранулированного порошка, пригодного для приготовления готовых к употреблению растворов, или жидких форм в соответствии с растворимостью данных продуктов. Дозы экстракта согласно изобретению варьируются в пределах 30 – 500 мг в случае однократного или неоднократного суточного введения, предпочтительно 200 мг при введении дважды в день. Целесообразным способом введения является пероральный способ.
Нижеследующие примеры иллюстрируют настоящее изобретение.
Пример 1. Получение соевого экстракта, характеризующегося 15% весовым содержанием изофлавонов и соотношением 1:1,5 глюкозидных изофлавонов и сапонинов сои группы В, путем очистки с использованием растворителей.
10 кг обезжиренной соевой муки, содержащей 0,2% глюкозидных изофлавонов и 0,3% сапонинов сои группы В, подвергали кипячению с обратным холодильником пятикратно с 30 л 95%-ного этилового спирта. Полученные спиртовые экстракты смешивали и концентрировали до объема 5 л при пониженном давлении. Концентрат разводили в 1,5 л воды и четырежды экстрагировали в 5 л н-гексана. Гексановую фазу удаляли, а концентрированную спиртовую фазу экстрагировали четырежды с использованием 2,5 л н-бутанола. Органическую фазу концентрировали и высушивали при пониженном давлении. Было получено 133 г экстракта, содержащего 15% изофлавонов по весу и 22,5% сапонинов сои группы В по весу.
ВЭЖХ-диаграмма экстракта, полученного с помощью описанной в данном примере процедуры, показана на чертеже.
Пример 2. Получение соевого экстракта, характеризующегося 15% весовым содержанием изофлавонов и соотношением 1:1,5 глюкозидных изофлавонов и сапонинов сои группы В, путем очистки с использованием полистиреновой смолы.
Водный экстракт, полученный согласно примеру 1, не подвергают экстрагированию в н-бутаноле, а обрабатывают полиэтоксилированным касторовым маслом (Cremophor 4,6 мм) и тройной элюционной среды с градиентом, включающим в себя (А) воду (СF3СООН-0,01%), (В) ацетонитрил (СF3СООН – 0,01%) и (С) метанол (CF3COOH-0,01%). Отдельные компоненты могут быть идентифицированы и охарактеризованы с помощью масс-спектрометрии в сочетании с ВЭЖХ через термораспыляющую границу раздела.
Экстракты согласно изобретению отличаются от ранее известных экстрактов их специфическим воздействием.
В отношении климактерических расстройств “приливы” крови, бессонница и депрессия являются наиболее распространенными симптомами климакса, от которых страдают женщины в этот период жизни. Они сопровождаются снижением или прекращением работы яичников и, как результат, снижением выработки эстрогенов и увеличением выработки лютеинизирующего гормона (ЛГ; и фолликулостимулирующего гормона (ФСГ).
В недавнем исследовании (E.M.Duker et al., 1991, Planta Med., 57, 420) сообщалось о том, что в результате овариэктомии (удаления яичников) у самок крыс наблюдается связь между случайным возрастанием уровня ЛГ и изменениями температуры кожи. Такая взаимосвязь между уровнем ЛГ и “приливами”, которая наблюдается не только у являющихся моделью крыс, но и у женщин, подтверждает то, что доза секретируемого ЛГ может рассматриваться в качестве информативного параметра в анализе психоневротических и эндокринных проявлений активных эндокринных соединений.
В таблице 1 показаны результаты, которые были получены тогда, когда на подвергшихся овариэктомии самках крыс испытывали воздействие двух отдельных фракций (изофлавоны и сапонины сои группы В) и экстрактов согласно изобретению.
Самки крыс были подвергнуты овариэктомии с применением известных методик. Спустя 15 дней после операции животных подвергали воздействию тестируемых препаратов путем однократного ежедневного перорального введения в течение 15 дней. Животных умерщвляли через 3 часа после последнего введения препарата. Кровь центрифугировали немедленно после этого и полученную сыворотку хранили при -25oС до момента определения содержания ЛГ радиоиммунным методом, в соответствии с методом, описанным Нис-уэндером с соавт. (Niswender et al., 1986, Proc. Soc. Exp. Biol. Med., 128, 807).
Как можно видеть, введение экстрактов согласно изобретению приводило к статистически существенному снижению уровня ЛГ, которое было более существенным по сравнению с тем, которое определяется суммой отдельных компонентов (эффект синергизма).
Экстракты, использовавшиеся в повторных воздействиях на здоровых животных, не приводили к каким-либо макроскопическим или микроскопическим изменениям в органах или системах у самцов животных, в то время как у самок они модифицировали вес матки и скелета, что подтверждает их эстрогенную активность.
Когда экстракты согласно изобретению вводились женщинам в процессе менопаузы (независимо от того, происходит ли это естественным путем или в результате хирургического вмешательства), они приводили к изменению содержания ЛГ в плазме и снижали климактерические расстройства, такие как “приливы” или депрессия и т.п., в течение нескольких дней воздействия, а при таком же воздействии на протяжении длительного периода также было отмечено снижение уровня деминерализации костей.
Экстракты согласно изобретению также обладали отчетливой антипролиферационной активностью. В таблице 2 показана антипролиферационная активность в отношении линии клеток опухоли яичников (OVCA 433).
Клетки культивировали в монослойной культуре с использованием минимальной культуральной среды с добавлением телячьей сыворотки и 200 ед./мл пенициллина с целью поддержания стерильности среды. Для воспроизводимости результатов тестирования клетки обрабатывали трипсином каждую неделю, высевали при плотности 80 тыс. клеток на 1 мл и инкубировали при 37oС в атмосфере воздуха при содержании 5% СO2 и наличии влажности. Для тестирования активности данных соединений клетки помещали в лунки планшета “Фалькон” (Falcon 3046, Becton Dickinson, NY) в концентрации 100 тыс. клеток на 1 мл и при минимальном количестве субстрата. Спустя 24 ч субстрат замещали свежей порцией субстрата и добавляли предназначенные для тестирования соединения, растворенные в абсолютном этиловом спирте. Контрольные варианты обрабатывали точно таким же образом, за исключением того, что предназначенные для тестирования соединения отсутствовали. Описанную выше обработку повторяли с интервалом в сутки в течение всего периода тестирования, составившего 72 ч. Уровень подавления пролиферации клеток оценивали путем прямого подсчета их количества: при этом рост контрольных вариантов сравнивали с ростом вариантов тестирования, подвергнутых “обработке”. Как было установлено, экстракты согласно изобретению проявляли антипролиферативную активность, которая была больше суммы антипролиферативных активностей входящих в него компонентов (активность по типу синергизма). Соединения согласно изобретению подавляли пролиферацию клеток in vivo: это было подтверждено при измерении размеров опухолей, пересаженных бестимусным мышам линии “naked”, что было осуществлено обычными методиками, описанными в литературе. Введение этим животным экстракта в дозах от 10 до 500 мг/кг приводило к отчетливой дегенерации анализируемых опухолей, вплоть до их полного рассасывания у значительной части подопытных особей.
Что касается ингибирующего действия на употребление алкоголя, то такой эффект был исследован с использованием употребляющих алкоголь крыс, представляющих специализированную линию “сардинийская, предпочитающая алкоголь” (Sp) (F. Fadda, E. Mosca, G.Colombo, G.L.Gessa, 1990, “Alcohol preferring rats: Genetic sensitivity to alcohol-induced stimulation of dopamine metabolism”, Physiol. Behav. , 47, 727). Эти животные, которые при организации для них свободного выбора между этиловым спиртом и водой потребляют 6-7 г спирта в расчете на 1 кг веса тела в день (при том, что спирт разбавлен водой втрое), были в последние годы успешно использованы при определении влияния различных соединений на добровольное употребление алкоголя: см., например, A. Balakleevsky, G. Colombo, F.Fadda, G.L.Gessa, 1990, “Ro 19-4603, a benzo-diazepine receptor inverse agonist, attenuates voluntary ethanol consumption in rats selectively bred for high ethanol preference”, Alcohol, 25, 449-452; F.Fadda, В. Garau, G.Colombo, G.L.Gessa, 1992, “Isradipine and other calcium channel antagonists attenuate ethanol consumption in ethanol-preferring rats”. In “Alcoholism: Clinical & Experimental Research”, 16, 449-452.
Животные, которых содержали в нормальных условиях, могли свободно выбирать между водой (вода присутствовала всегда) и алкоголем (10%-ный объемный раствор в воде), который предлагался только в течение 4 часов в сутки (т.е. в первые четыре темных часа при обычном суточном режиме освещения). Количество употребленных воды и алкоголя регистрировали ежедневно в одно и то же время. Кормили животных вволю (ad libitum). После того, как достигалась стабилизация соотношения употребляемых воды и алкоголя, экстракт при дозе 1000 мг на 1 кг (при суспендировании его в воде) вводили перорально при его объемном количестве 2 мг/кг в день в течение 7 последовательных дней. В качестве контроля использовали идентичный объем наполнителя. По окончании обработки употребление алкоголя регистрировали до тех пор, пока не достигались показатели, которые были установлены до проведения тестирования.
Таблица 3 показывает влияние повторяющегося перорального введения 1000 мг/кг соевого экстракта на употребление алкоголя.
Данные таблицы 3 позволяют сделать заключение, что соевый экстракт в существенной степени уменьшает уровень употребления алкоголя. Снижение употребления алкоголя остается стабильным на протяжении всех 7 дней тестирования и затем ослабевает по окончании воздействия. Более того, можно видеть, что снижение употребления алкоголя оказывается более существенным по сравнению с тем эффектом, который определяется суммой эффектов отдельных компонентов экстракта (эффект синергизма).
Далее, настоящее изобретение также связано с фармацевтической композицией, которая содержит определяемый выше экстракт в качестве своего активного компонента. В частности, настоящее изобретение связано с фармацевтической композицией, содержащей этот экстракт и предназначенной для профилактики или лечения предклимактерических и постклимактерических симптомов, фармацевтической композицией, содержащей данный экстракт и предназначенный для профилактики и лечения рака молочной железы у женщин и аденомы простаты у мужчин, а также фармацевтической композицией, содержащей данный экстракт и предназначенной для профилактики или лечения алкоголизма.
Продукты или экстракты согласно изобретению могут быть приготовлены подходящим образом в виде таблеток, мягких или твердых желатиновых капсул, гранулированного порошка, пригодного для приготовления готовых к употреблению растворов, или жидких форм в соответствии с растворимостью данных продуктов. Дозы экстракта согласно изобретению варьируются в пределах 30 – 500 мг в случае однократного или неоднократного суточного введения, предпочтительно 200 мг при введении дважды в день. Целесообразным способом введения является пероральный способ.
Нижеследующие примеры иллюстрируют настоящее изобретение.
Пример 1. Получение соевого экстракта, характеризующегося 15% весовым содержанием изофлавонов и соотношением 1:1,5 глюкозидных изофлавонов и сапонинов сои группы В, путем очистки с использованием растворителей.
10 кг обезжиренной соевой муки, содержащей 0,2% глюкозидных изофлавонов и 0,3% сапонинов сои группы В, подвергали кипячению с обратным холодильником пятикратно с 30 л 95%-ного этилового спирта. Полученные спиртовые экстракты смешивали и концентрировали до объема 5 л при пониженном давлении. Концентрат разводили в 1,5 л воды и четырежды экстрагировали в 5 л н-гексана. Гексановую фазу удаляли, а концентрированную спиртовую фазу экстрагировали четырежды с использованием 2,5 л н-бутанола. Органическую фазу концентрировали и высушивали при пониженном давлении. Было получено 133 г экстракта, содержащего 15% изофлавонов по весу и 22,5% сапонинов сои группы В по весу.
ВЭЖХ-диаграмма экстракта, полученного с помощью описанной в данном примере процедуры, показана на чертеже.
Пример 2. Получение соевого экстракта, характеризующегося 15% весовым содержанием изофлавонов и соотношением 1:1,5 глюкозидных изофлавонов и сапонинов сои группы В, путем очистки с использованием полистиреновой смолы.
Водный экстракт, полученный согласно примеру 1, не подвергают экстрагированию в н-бутаноле, а обрабатывают полиэтоксилированным касторовым маслом (Cremophor ) и растворяют в смолистых остатках концентрирования спиртовой фазы. Полученную таким образом смесь суспендируют в очищенной воде (5 л) и наносят на колонку со смолой XAD1180. Затем колонку поливают струей воды с целью полного удаления солей, углеводов и поверхностно-активных агентов и затем элюируют примерно 10 л 95%-ного этилового спирта. После концентрирования и высушивания спиртового элюата получают 130 г экстракта, характеризующегося тем же самым составом, что и экстракт, полученный согласно примеру 1.
Пример 3. Получение соевого экстракта, характеризующегося 43% весовым содержанием изофлавонов и соотношением 1:1 глюкозидных изофлавонов и сапонинов сои группы В.
20 г экстракта, полученного в примерах 1 или 2, суспендируют в 1 л водного 20%-ного раствора этилового спирта и разводят в 0,5 л этилацетата. Эту суспензию подвергают нагреванию в противотоке при мощном перемешивании до тех пор, пока не произойдет полного растворения, а затем оставляют на ночь. Осажденные в результате сапонины (38 г: чистота – 93%) выделяют с помощью фильтрования и затем разделяют этилацетатсодержащий и водосодержащий маточный раствор. Органическую фазу концентрируют при пониженном давлении и высушивают. Изофлавоновый остаток (37 г: чистота – 81%) растворяют в 1 л этилового спирта и смешивают с 32 г кристаллизоанных сапонинов с целью получения продукта, который бы содержал изофлавоны и сапонины в соотношении 1: 1. Спиртовой раствор концентрируют до высыхания при пониженном давлении и получаютр 69 г экстракта, характеризующегося 43%-ным весовым содержанием глюкозидных изофлавонов и 43%-ным весовым содержанием сапонинов сои группы В.
Пример 4. Получение твердых желатиновых капсул, содержащих соевый экстракт, мг: ) и растворяют в смолистых остатках концентрирования спиртовой фазы. Полученную таким образом смесь суспендируют в очищенной воде (5 л) и наносят на колонку со смолой XAD1180. Затем колонку поливают струей воды с целью полного удаления солей, углеводов и поверхностно-активных агентов и затем элюируют примерно 10 л 95%-ного этилового спирта. После концентрирования и высушивания спиртового элюата получают 130 г экстракта, характеризующегося тем же самым составом, что и экстракт, полученный согласно примеру 1.
Пример 3. Получение соевого экстракта, характеризующегося 43% весовым содержанием изофлавонов и соотношением 1:1 глюкозидных изофлавонов и сапонинов сои группы В.
20 г экстракта, полученного в примерах 1 или 2, суспендируют в 1 л водного 20%-ного раствора этилового спирта и разводят в 0,5 л этилацетата. Эту суспензию подвергают нагреванию в противотоке при мощном перемешивании до тех пор, пока не произойдет полного растворения, а затем оставляют на ночь. Осажденные в результате сапонины (38 г: чистота – 93%) выделяют с помощью фильтрования и затем разделяют этилацетатсодержащий и водосодержащий маточный раствор. Органическую фазу концентрируют при пониженном давлении и высушивают. Изофлавоновый остаток (37 г: чистота – 81%) растворяют в 1 л этилового спирта и смешивают с 32 г кристаллизоанных сапонинов с целью получения продукта, который бы содержал изофлавоны и сапонины в соотношении 1: 1. Спиртовой раствор концентрируют до высыхания при пониженном давлении и получаютр 69 г экстракта, характеризующегося 43%-ным весовым содержанием глюкозидных изофлавонов и 43%-ным весовым содержанием сапонинов сои группы В.
Пример 4. Получение твердых желатиновых капсул, содержащих соевый экстракт, мг:Соевый экстракт, полученный согласно примеру 1 – 200,0 Лактоза – 67,5 Микрокристаллическая целлюлоза – 22,5 Коллоидная двуокись кремния – 3,0 “Кросскармеллоза” натрия (перекрестно сшитая полимерная карбоксиметилцеллюлоза натрия) – 21,0 Тальк – 8,0 Стеарат магния – 3,0 Пример 5. Приготовление таблеток, содержащих соевый экстракт, мг: Соевый экстракт, полученный согласно примеру 3 – 400,0 Полисахариды – 155,5 Микрокристаллическая целлюлоза – 57,0 Гидроксипропилметилцеллюлоза – 12,0 Гидрированное растительное масло – 19,5 Коллоидная двуокись кремния – 3,0 Стеарат магния – 3,0э Формула изобретения
РИСУНКИ
|
||||||||||||||||||||||||||
