Патент на изобретение №2182156
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ ОЛИГОПЕПТИДОВ, СОДЕРЖАЩИЕ D-АЛКИЛТРИПТОФАН И СПОСОБНЫЕ АКТИВИРОВАТЬ ВЫСВОБОЖДЕНИЕ ГОРМОНА РОСТА
(57) Реферат: В предлагаемом изобретении описываются пептиды общей формулы A-D-Х-Mrp-B, а также их аддитивные соли с фармацевтически приемлемыми органическими или неорганическими кислотами, где заместители А, D, Х или В имеют указанные в описании значения. Полученные соединения способны активировать высвобождение гормона роста. Их введение в организм пероральным путем увеличивает эту активность. 2 c. и 11 з.п. ф-лы, 1 табл. Изобретение относится к олигопептидным производным, содержащим аминокислоту D-2-алкилтриптофан, которые способны высвобождать гормон роста (ГР) из соматотропных клеток и активны при пероральном введении. Повышение уровня гормона роста (GH) у млекопитающих после введения соединений, индуцирующих высвобождение GH, может привести к акселерации роста и повышению мышечной массы и повышенной продуктивности молока, если после введения достигают достаточно высоких концентраций ГР. Кроме того, известно, что повышение уровня гормона роста у млекопитающих можно достичь введением известных средств для его высвобождения, таких как гормоны высвобождения гормона роста (GHRH). Повышение уровня гормона роста у млекопитающих можно также достичь путем введения пептидов, высвобождающих гормон роста, некоторые из которых ранее были описаны, например, в патентах США 4 223 019, США 4 223 020, США 4 223 021, США 4 224 316, США 4 226 857, США 4 228 155, США 4 228 156, США 4 228 157, США 4 228 158, США 4 410 512, США 4 410 513, США 4 411 890 и США 4 839 344. Поэтому в настоящее время требуются весьма простые олигопептиды с короткой цепью, способные стимулировать высвобождение гормона роста, при условии легкой и удобной методики их получения, а также легкой очистки и изготовление рецептуры, которая активна при пероральном введении. Deghenghi et al. (Journal of Pediatric Endocrinology and Metabolism, 8, 311-313 (1995)) описали аминоацилпроизводные тетрапептидов, которые активны in vivo в высвобождении гормона роста. В WO 96/10040 описаны тетрапептиды, содержащие D-2-алкилтриптофан и способные стимулировать высвобождение гормона роста при пероральном введении. Deghenghi et al. (Life Sciences, vol.54, 18, 1321-1328, 1994) обсуждали ГР-высвобождающую активность гексапептида гексарелина. Было установлено, что олигопептиды с очень короткой цепью имеющие, по меньшей мере, один остаток D-2-алкилтриптофана (2-Мrр), обладают активностью высвобождения гормона роста (GH) из соматотропных клеток. Другим отличительным признаком настоящего изобретения является очень высокая активность и благоприятная величина отношения активности при пероральном введении к силе воздействия при пероральном введении, которыми обладают даже самые короткие трипептиды этого ряда. Олигопептиды настоящего изобретения имеют формулу: A-D-X-D-Mrp-B где А представляет водород, 2-аминоизобутирил, 4-аминобутирил, D относится к декстро-изомеру, Х представляет Мrр, где Мrр обозначает 2-алкилтриптофан формулы: 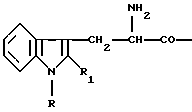 где R представляет водород, СНО, SO2СН3, мезитилен-2-сульфонил, РО3(СН3)2, РО3Н2; R1 представляет С1-С3-алкильную группу, или Х представляет остаток защищенного серина, Ser(Y), где Y может быть бензилом, n-хлорбензилом, 4-метоксибензилом, 2,4,6,-триметоксибензилом, трет-бутилом; В представляет NR2R3, где R2 и R3, которые могут быть одинаковыми или различными, представляют водород или C1-С3-алкильную группу; группу OR4, где R4 представляет водород или C1-С3-алкильную группу; или В представляет группу C-Lys-NH2, где С представляет Phe или Мrр. Изобретение основано на том, что различные олигопептиды с короткой цепью, которые активируют высвобождение и повышают уровни гормона роста в крови животных, характеризуются тем, что все из них содержат в пептидной цепи D-изомер 2-алкилтриптофана (D-2-Me-Trp или D-Mrp). Олигопептиды, включенные в объем изобретения, определяются следующей формулой: A-D-X-D-Mrp-B где А представляет водород, 2-аминоизобутирил, 4-аминобутирил, D относится к декстро-изомеру, Х представляет Мrр, где Мrр обозначает 2-алкилтриптофан формулы: 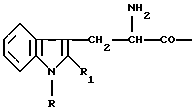 где R представляет водород, СНО,SО2СН3, мезитилен-2-сульфонил, РО3(СН3)2, РО3Н2; R1 представляет C1-С3-алкильную группу, или Х представляет остаток защищенного серина, Ser(Y), где Y может быть бензилом, п-хлорбензилом, 4-метоксибензилом, 2,4,6,-триметоксибензилом, трет-бутилом; В представляет NR2R3, где R2 и R3, которые могут быть одинаковыми или различными, представляют водород или C1-С3-алкильную группу; OR4, где R4 представляет водород или C1-С3-алкильную группу; или В представляет группу C-Lys-NH2, где С представляет Phe или Мrр, и аддитивные соли с фармацевтически приемлемыми органическими или неорганическими кислотами любого одного из этих полипептидов. Использованная здесь аббревиатура остатков аминокислот находится в соответствии со стандартной номенклатурой для пептидов: Lys = L-лизин. Кроме того, Aib = 2-аминоизобутирил; GAB = 4-аминобутирил; Mrp = 2-алкилтриптофан; Bzl = бензил; p-Cl-Bzl = п-хлорбензил; Mob = 4-метоксибензил; Tmob = 2,4,6 -триметоксибензил; tbu = трет-бутил; For = формил; Mts = мезитилен-2-сульфонил. В соответствии с настоящим изобретением алкил обозначает низший алкил, содержащий от 1 до 3 атомов углерода. Примерами низшего алкила являются метил, этил, пропил, изопропил. Среди них метильная группа значительно предпочтительна. Все трехбуквенные аббревиатуры аминокислот, которым предшествует “D”, означают аминокислотный остаток с D-конфигурацией. Когда аминокислота обозначается только трехбуквенной аббревиатурой, она имеет L-конфигурацию. Предпочтительными соединениями настоящего изобретения, высвобождающими гормон роста, являются: (a) GAB-D-Mrp-D-Mrp-Phe-Lys-NH2; (b) GAB-D-Mrp-D-Mrp-Mrp-Lys-NH2; (c) Aib-D-Mrp-D-Mrp-NH2; (d) Aib-D-Mrp-Mrp-NH2; (e) Aib-D-Ser(Bzl)-D-Mrp-NH2; где Мrр представляет 2-метилтриптофан, GAB и Aib такие, как определено выше, и аддитивные соли с фармацевтически приемлемыми органическими или неорганическими кислотами любого одного из этих олигопептидов. Эти соединения предпочтительно вводят пероральным методом, но их можно также вводить интраназально или парентерально, или их можно получить в виде тивной формы для регулируемого высвобождения, таких как биоразлагаемые капсулы, микросферы, подкожные имплантанты и тому подобное. Заявленные олигопептидные производные можно синтезировать по обычным методикам химии пептидов как в твердой фазе, так и в растворе, или при помощи классических методов, известных в данной области. Синтез в твердой фазе начинается с С-концевой части пептида. Подходящий исходный материал можно получить, например, присоединением требуемой защищенной альфа-аминокислоты к хлормителированной смоле, гидроксиметилированной смоле, бензгидриламиновой смоле (ВНА) или к пара-метилбензгидриламиновой смоле (р-Ме-ВНА). В качестве примера хлорметилированной смолы приводится твердый материал с товарным знаком BIOBEADS  SX1, поставляемый BioRad Laboratories, Richmond, California. Получение гидроксиметилсмолы описывается Bodansky et al., Chem. Ind. (London) 38,15997, (1966). Смола ВНА описана Pietta and Marshall, Chem. Comm. , 650 (1970), и выпускается на рынок фирмой Peninsula Laboratories Inc., Belmont, California.
После начального присоединения защитную группу альфа-аминокислоты можно удалить при помощи различных кислотных реагентов, включающих трифторуксусную кислоту (ТФК) или соляную кислоту (НС1), растворенную в органических растворителях при комнатной температуре. После удаления защитной группы альфа-аминокислоты остальные защищенные аминокислоты можно связать в желаемом порядке. Каждую защищенную аминокислоту обычно вводят в реакцию в трехкратном избытке с использованием подходящей карбоксильной активирующей группы, такой как дициклогексилкарбодиимид (DCC) или диизопропилкарбодиимид (DIC), растворенной, например, в метиленхлориде (CH2Cl2) или демитилформамиде (ДМФ) и их смесях. После завершения образования целевой аминокислотной последовательности целевой пептид можно отщепить от носителя-смолы обработкой реагентом, таким как фтористый водород (HF), который отщепляет не только пептид от смолы, но также обычные защитные группы боковых цепей. Когда используют хлорметилированную смолу или гидроксиметилированную смолу, обработка HF приводит к образованию кислотного пептида в свободной форме. Когда используют смолу ВНА или р-Ме-ВНА, обработка HF приводит непосредственно к образованию амидного пептида в свободной форме.
Обсуждаемая выше методика в твердой фазе известна в данной области и была описана Atherton and Sheppard, Solid Phase Peptide Synthesis (IRL Press, Oxford, 1989).
Некоторые методы синтеза в растворе, которые можно использовать для синтеза пептидных частей изобретения, подробно описываются Bodansky et al., Peptide Synthesis, 2nd edition, John Wiley and Sons, New York, n.y., 1976, and jones, The Chemical Synthesis of Peptides (Clarendon Press, Oxford, 1994).
Эти соединения вводят животным и людям в эффективной дозе, которую может легко определить специалист в данной области и которая может изменяться в зависимости от возраста, пола и веса пациента. Например, для людей, когда соединения вводят внутривенно, предпочтительная доза находится в пределах от около 0,1 до 10 мкг общего пептида на 1 кг веса тела. Когда соединение вводят перорально, обычно необходимы более высокие количества. Например, для перорального введения человеку уровень доз обычно составляет от около 30 до около 1000 мкг полипептида на 1 кг веса тела. Точный уровень легко определяют эмпирически на основании приведенного выше описания.
Композиции, которые содержат в качестве активного ингредиента органические или неорганические аддитивные соли описанных выше олигопептидов и их комбинации, необязательно в смеси с наполнителем, разбавителем, матрицей или покрытием для замедленного высвобождения (активного ингредиента), также включены в объем настоящего изобретения. Особенно интересны фармацевтические композиции с замедленным высвобождением, содержащие биоразрушаемые матрицы, пригодные для подкожной имплантации. Примеры этих матриц описываются в W09222600 и W09512629.
Активность этих соединений in vivo определяли на десятидневных крысах, которым подкожно вводили дозу в 300 мкг/кг или различные дозы при изучении соотношения доза-отклик по методике, описанной подробно авторами R. Deghenghi et al. Life Sciences, 54, 1321 (1994). Результаты сведены в таблицу, причем высвобожденный гормон роста (GH) измеряли через 15 мин после введения.
Изобретение далее иллюстрируется следующими примерами: SX1, поставляемый BioRad Laboratories, Richmond, California. Получение гидроксиметилсмолы описывается Bodansky et al., Chem. Ind. (London) 38,15997, (1966). Смола ВНА описана Pietta and Marshall, Chem. Comm. , 650 (1970), и выпускается на рынок фирмой Peninsula Laboratories Inc., Belmont, California.
После начального присоединения защитную группу альфа-аминокислоты можно удалить при помощи различных кислотных реагентов, включающих трифторуксусную кислоту (ТФК) или соляную кислоту (НС1), растворенную в органических растворителях при комнатной температуре. После удаления защитной группы альфа-аминокислоты остальные защищенные аминокислоты можно связать в желаемом порядке. Каждую защищенную аминокислоту обычно вводят в реакцию в трехкратном избытке с использованием подходящей карбоксильной активирующей группы, такой как дициклогексилкарбодиимид (DCC) или диизопропилкарбодиимид (DIC), растворенной, например, в метиленхлориде (CH2Cl2) или демитилформамиде (ДМФ) и их смесях. После завершения образования целевой аминокислотной последовательности целевой пептид можно отщепить от носителя-смолы обработкой реагентом, таким как фтористый водород (HF), который отщепляет не только пептид от смолы, но также обычные защитные группы боковых цепей. Когда используют хлорметилированную смолу или гидроксиметилированную смолу, обработка HF приводит к образованию кислотного пептида в свободной форме. Когда используют смолу ВНА или р-Ме-ВНА, обработка HF приводит непосредственно к образованию амидного пептида в свободной форме.
Обсуждаемая выше методика в твердой фазе известна в данной области и была описана Atherton and Sheppard, Solid Phase Peptide Synthesis (IRL Press, Oxford, 1989).
Некоторые методы синтеза в растворе, которые можно использовать для синтеза пептидных частей изобретения, подробно описываются Bodansky et al., Peptide Synthesis, 2nd edition, John Wiley and Sons, New York, n.y., 1976, and jones, The Chemical Synthesis of Peptides (Clarendon Press, Oxford, 1994).
Эти соединения вводят животным и людям в эффективной дозе, которую может легко определить специалист в данной области и которая может изменяться в зависимости от возраста, пола и веса пациента. Например, для людей, когда соединения вводят внутривенно, предпочтительная доза находится в пределах от около 0,1 до 10 мкг общего пептида на 1 кг веса тела. Когда соединение вводят перорально, обычно необходимы более высокие количества. Например, для перорального введения человеку уровень доз обычно составляет от около 30 до около 1000 мкг полипептида на 1 кг веса тела. Точный уровень легко определяют эмпирически на основании приведенного выше описания.
Композиции, которые содержат в качестве активного ингредиента органические или неорганические аддитивные соли описанных выше олигопептидов и их комбинации, необязательно в смеси с наполнителем, разбавителем, матрицей или покрытием для замедленного высвобождения (активного ингредиента), также включены в объем настоящего изобретения. Особенно интересны фармацевтические композиции с замедленным высвобождением, содержащие биоразрушаемые матрицы, пригодные для подкожной имплантации. Примеры этих матриц описываются в W09222600 и W09512629.
Активность этих соединений in vivo определяли на десятидневных крысах, которым подкожно вводили дозу в 300 мкг/кг или различные дозы при изучении соотношения доза-отклик по методике, описанной подробно авторами R. Deghenghi et al. Life Sciences, 54, 1321 (1994). Результаты сведены в таблицу, причем высвобожденный гормон роста (GH) измеряли через 15 мин после введения.
Изобретение далее иллюстрируется следующими примерами:Пример 1 С использованием методики синтеза в твердой фазе, как описано в “Solid phase peptid synthesis technique by E. Atherton and R.С.Sheppard, IRL Press, Oxford University Press, 1984, и с использованием флуоренилметоксикарбонила (Fmoc) в качестве защитной группы был получен пептид: GAB-D-2-Mrp-D-2-Mrp-Phe-Lys-NH2 где Мrр представляет 2-метилтриптофан, мол.масса 779,9, найденная 778,4; чистота (ВЭЖХ) 98,0%. Пример 2 Аналогично примеру 1 был получен следующий пептид: GAB-D-Mrp-D-Mrp-Mrp-Lys-NH2, где Мrр представляет 2-метилтриптофан, мол.масса 830,8, найденная 831,3; чистота (ВЭЖХ) 98,0%. Пример 3 Аналогично примеру 1 был получен следующий пептид: Aib-D-2-Mrp-D-2-Mrp-NH2, где Мгр представляет 2-метилтриптофан, мол.масса 502,6, найденная 503,3; чистота (ВЭЖХ) 99,0%. Пример 3 Аналогично примеру 1 был получен следующий пептид: Aib-D-2-Mrp-D-2-Mrp-NH2, где Мrр представляет 2-метилтриптофан, мол.масса 502,6, найденная 503,3; чистота (ВЭЖХ) 99,0%. Пример 4 Аналогично примеру 1 был получен следующий пептид: Aib-D-2-Mrp-2-Mrp-NH2, где Мгр представляет 2-метилтриптофан, мол.масса 502,6, найденная 503,3; чистота (ВЭЖХ) 99,0%. Пример 5 Аналогично примеру 1 был получен следующий пептид: Aib-D-Ser(Bzl)-D-Mrp-NH2, где Мrр представляет 2-метилтриптофан, мол.масса 479,6, найденная 480,5; чистота (ВЭЖХ) 99,0%. Формула изобретения
где А представляет 2-аминоизобутирил, 4-аминобутирил; D обозначает декстро-изомер; Х представляет Mrp, где Mrp обозначает 2-алкилтриптофан формулы 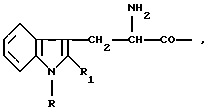 где R представляет водород; R1 представляет С1-С3-алкильную группу; или Х представляет остаток защищенного серина, Ser(Y), где Y может быть бензилом, п-хлорбензилом, 4-метоксибензилом, 2,4,6-триметоксибензилом, трет-бутилом; В представляет NR2R3, где R2 и R3, каждый в отдельности, представляют водород; или В представляет группу C-Lys-NH2, где С представляет Phe или Mrp, и аддитивные соли с фармацевтически приемлемыми органическими или неорганическими кислотами любого из этих полипептидов. 2. Пептид по п. 1, где Mrp представляет 2-метилтриптофан. 3. Пептид по п. 1, где В представляет C-LysNH2, где С определен выше. 4. Пептид по п. 1, имеющий формулу GAB-D-Mrp-D-Mrp-Phe-Lys-NH2. 5. Пептид по п. 1, имеющий формулу GAB-D-Mrp-D-Mrp-Mrp-Lys-NH2. 6. Пептид по п. 1, имеющий формулу Aib-D-Mrp-D-Mrp-NH2. 7. Пептид по п. 1, имеющий формулу Aib-D-Ser(Bzl)-D-Mrp-NH2. 8. Пептид по пп. 4-7, где Mrp представляет 2-метилтриптофан. 9. Пептиды по пп. 1-8, обладающие способностью активации высвобождения гормона роста у животного. 10. Пептиды по п. 9, где указанное животное является млекопитающим. 11. Фармацевтическая композиция, проявляющая активность в отношении активации высвобождения гормона роста у животных, включающая в качестве активного ингредиента пептид по пп. 1-10 в эффективном количестве, причем указанный пептид может находиться, необязательно, в смеси с носителями и наполнителями. 12. Фармацевтическая композиция по п. 11, в форме для парентерального, перорального введения, введения с регулируемым высвобождением подкожных имплантатов. 13. Композиция по п. 11, в форме для перорального введения. РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 05.12.2008
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
