Патент на изобретение №2181728
|
||||||||||||||||||||||||||
(54) ПЕПТИД, СТИМУЛИРУЮЩИЙ МИГРАЦИЮ НЕЙТРОФИЛОВ
(57) Реферат: Изобретение относится к новому пептиду на основе молекулы интерлейкина-8 общей формулы 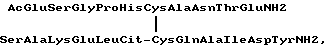 стимулирующему миграцию нейтрофилов. Предлагаемое соединение не только обладает хемоаттрактантной активностью, но его стимулирующее воздействие на миграцию нейтрофилов на 15-29% выше, чем у ИЛ-8. 3 табл. Изобретение относится к области биотехнологии, а именно к пептидам, обладающим хемоаттрактантной активностью, в частности стимулирующим миграцию нейтрофилов. В настоящее время наиболее изученным хемоттрактантом из числа природных соединений является интерлейкин-8 (ИЛ-8) (Wals A., Peveri P., Aschauer H. Et all, BBRC, 1987, 149, р. 755-759). За последнее десятилетие влияние ИЛ-8 на активацию нейтрофилов, а также механизм проведения сигнала внутрь клетки были детально изучены. Проведено сравнение с такими хемоаттрактантами, как С5а, FMLP, PAF, LTB4. Результаты проведенных исследований свидетельствуют, что ИЛ-8 ведет себя как классический хемотактический агонист. Он усиливает хемотаксис, стимулирует выброс белков и ферментов, например желатиназы, B12 связывающего белка, эластазы,  -глюкуронидазы, миелопероксидазы из внутриклеточных органелл (экзоцитоз), через активацию NADPH-оксидазы вызывает респираторный взрыв, активируя 5-липооксигеназу, усиливает синтез биологически активных липидов, приводит к увеличению концентрации внутриклеточного несвязанного кальция ([Са2+]). Кроме того, ИЛ-8 является стимулятором ангиогенеза.
ИЛ-8 является полипептидом длиною 72 аминокислотных остатка, третичная структура которого стабилизирована двумя дисульфидными связями.
В настоящее время этот хемокин получают, как правило, методами генной инженерии (Lowman H.B. et all J. Biol. Chem., 1996, 271, р. 14344-14352).
Однако возможно получение его химическим синтезом. (Clark-Lewis et all, Proc. Nat1/ Acad. Sci USA, 1993, 90, 3574-3577). Указанный процесс достаточно сложен и трудоемок, а получаемый ИЛ-8, являющийся прототипом заявляемого изобретения, весьма лабилен, и его активность, в частности в отношении стимуляции миграции нейтрофилов, недостаточно высока.
Задачей, стоявшей перед авторами, являлось создание вещества, обладающего более высокой активностью и более простого в получении.
Указанная задача была решена созданием синтетического пептида, включающего в себя фрагмент (1) ИЛ-8 (29-38): -глюкуронидазы, миелопероксидазы из внутриклеточных органелл (экзоцитоз), через активацию NADPH-оксидазы вызывает респираторный взрыв, активируя 5-липооксигеназу, усиливает синтез биологически активных липидов, приводит к увеличению концентрации внутриклеточного несвязанного кальция ([Са2+]). Кроме того, ИЛ-8 является стимулятором ангиогенеза.
ИЛ-8 является полипептидом длиною 72 аминокислотных остатка, третичная структура которого стабилизирована двумя дисульфидными связями.
В настоящее время этот хемокин получают, как правило, методами генной инженерии (Lowman H.B. et all J. Biol. Chem., 1996, 271, р. 14344-14352).
Однако возможно получение его химическим синтезом. (Clark-Lewis et all, Proc. Nat1/ Acad. Sci USA, 1993, 90, 3574-3577). Указанный процесс достаточно сложен и трудоемок, а получаемый ИЛ-8, являющийся прототипом заявляемого изобретения, весьма лабилен, и его активность, в частности в отношении стимуляции миграции нейтрофилов, недостаточно высока.
Задачей, стоявшей перед авторами, являлось создание вещества, обладающего более высокой активностью и более простого в получении.
Указанная задача была решена созданием синтетического пептида, включающего в себя фрагмент (1) ИЛ-8 (29-38):AcGluSerGlyProHisCysAlaAsnThrGluNH2 и модифицированный фрагмент (2) ИЛ-8 (2-10): SerAlaLysGluLeuCitCysGlnAlaIleAcpTyrNH2, и имеющего соответственно следующий состав: 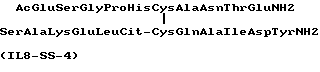 Синтез пептида IL8-SS-4 осуществлялся общепринятыми методами твердофазного синтеза и состоял из трех основных этапов: синтез фрагментов 1 и 2 и их сшивка. Синтез фрагмента 1. Синтез осуществлялся традиционными методами твердофазного синтеза полипептидов на основе последовательного наращивания пептидной цепи на метилбензгидриламинополимере. Для защиты боковых радикалов использовали следующие группы: для гистидина – тозильную; для цистеина – 3-нитро-2-пиридинсульфенильную; для глутаминовой кислоты, серина, треонина – соответствующие бензиновые эфиры; для аспарагина – тритильную. Для проведения синтеза в реакционный сосуд загружали 0,3 г метилбензгидриламинополимера с емкостью 1,0 ммоль/г (Sigma). Пептидную цепь наращивали до цистеина по схеме, приведенной в таблице 1, а начиная с цистеина – по схеме, приведенной в таблице 2. На стадии конденсации были использованы 3-кратные избытки активированных производных аминокислот. Контроль полноты протекания реакции конденсации осуществляли с помощью нингидринового теста. По завершении сборки полипептидной цепи на полимере Вос-защита с аминогруппы глутаминовой кислоты была удалена, и по схеме, приведенной в таблице 2 (п.2,3,4,5,6), альфа-аминогруппа пептида была ацетилирована уксусным ангидридом в течение 30 мин. Полученный пептидил-полимер был высушен в вакуум-эксикаторе над пятиокисью фосфора до постоянного веса. 0,7 г пептидил-полимера перенесли в реактор установки для работы с жидким фтористым водородом, добавили 0,5 мл м-крезола, охладили до -78oС и обработали 4,5 мл безводного фтористого водорода. Смесь выдерживали при 0oС 1 час, затем фтористый водород упаривали с помощью водоструйного насоса. Остаток перенесли на фильтр Шотта и промыли эфиром. Полученный продукт растворили в 10 мл трифторуксусной кислоты и по каплям прилили к 100 мл эфира. Кристаллический осадок отфильтровали с помощью фильтра Шотта, промыли эфиром и высушили в вакуум-эксикаторе. Индивидуальный продукт был получен с помощью высокоэффективной препаративной жидкостной хроматографии (ВПЖХ). Однородность пептида определяли по данным ВЭЖХ на колонке Delta РАС С 18 100А 3,9  150 мм при скорости потока 1 мм/мин и элюции 0,1% трифторуксусной кислотой в градиенте 10-50% ацетонитрила. Время удерживания 10,45 мин, чистота по оптической плотности на 230 нм > 95%, выход составил 30 мг (8%).
Аминокислотный состав был подтвержден с помощью аминокислотного анализа гидролизата пептида на приборе Alpha Plus LKB.
Синтез фрагмента 2. Синтез проводился на автоматическом синтезаторе “Applied Biosystems 430A” с использованием модифицированного пакета программ. Для синтеза использовался метилбензгидриламинполимер.
В качестве временной защиты боковых радикалов аминокислот использовали следующие группы: для лизина-2 – хлорбензилоксикарбонильную; для серина и глутаминовой кислоты – соответствующие бензиловые эфиры; для цистеина – метоксибензильную; для тирозина-2,6 дихлорбензильную.
При синтезе фрагмента 2 были использованы неприродные аминокислоты: е-аминокапроновая кислота и цитруллин. Деблокирование в процессе синтеза осуществлялось неразбавленной трифторуксусной кислотой. Нейтрализацию проводили во время конденсации путем прибавления строго фиксированного количества диизопропилэтиламина непосредственно в реакционный сосуд (метод “in situ” – М. Schnolzer, R. Alewood, Int. J. Peptide Protein Res., 40, 1992, р. 180-193). Пептидная цепь наращивалась последовательным присоединением производных аминокислот с помощью 1-гидроксибензотриазоловых эфиров.
В реактор загрузили 0,15 г метил-бензгидриламин-полимера (Sigma) с емкостью 1,0 ммоль/г, и после сборки полипептидной цепи получили 0,52 г пептидил-полимера. Пептидил-полимер обработали 4,5 мл безводного фтористого водорода в присутствии 0,5 мл м-крезола, как описано выше при синтезе фрагмента 1. В результате получено 0,17 г грубого продукта, который далее очищали с помощью препаративной ВЭЖХ.
Однородность полученного пептида подтверждали данными ВЭЖХ на колонке Delta РАС С18, 5ukm 100А, 3,9 150 мм при скорости потока 1 мм/мин и элюции 0,1% трифторуксусной кислотой в градиенте 10-50% ацетонитрила. Время удерживания 10,45 мин, чистота по оптической плотности на 230 нм > 95%, выход составил 30 мг (8%).
Аминокислотный состав был подтвержден с помощью аминокислотного анализа гидролизата пептида на приборе Alpha Plus LKB.
Синтез фрагмента 2. Синтез проводился на автоматическом синтезаторе “Applied Biosystems 430A” с использованием модифицированного пакета программ. Для синтеза использовался метилбензгидриламинполимер.
В качестве временной защиты боковых радикалов аминокислот использовали следующие группы: для лизина-2 – хлорбензилоксикарбонильную; для серина и глутаминовой кислоты – соответствующие бензиловые эфиры; для цистеина – метоксибензильную; для тирозина-2,6 дихлорбензильную.
При синтезе фрагмента 2 были использованы неприродные аминокислоты: е-аминокапроновая кислота и цитруллин. Деблокирование в процессе синтеза осуществлялось неразбавленной трифторуксусной кислотой. Нейтрализацию проводили во время конденсации путем прибавления строго фиксированного количества диизопропилэтиламина непосредственно в реакционный сосуд (метод “in situ” – М. Schnolzer, R. Alewood, Int. J. Peptide Protein Res., 40, 1992, р. 180-193). Пептидная цепь наращивалась последовательным присоединением производных аминокислот с помощью 1-гидроксибензотриазоловых эфиров.
В реактор загрузили 0,15 г метил-бензгидриламин-полимера (Sigma) с емкостью 1,0 ммоль/г, и после сборки полипептидной цепи получили 0,52 г пептидил-полимера. Пептидил-полимер обработали 4,5 мл безводного фтористого водорода в присутствии 0,5 мл м-крезола, как описано выше при синтезе фрагмента 1. В результате получено 0,17 г грубого продукта, который далее очищали с помощью препаративной ВЭЖХ.
Однородность полученного пептида подтверждали данными ВЭЖХ на колонке Delta РАС С18, 5ukm 100А, 3,9 150 мм, при скорости потока 1 мл/мин и элюции 0,1% трифторуксусной кислотой при градиенте 10-40% ацетонитрила.
Время удерживания составило 11,84 мин, чистота по оптической плотности на 230 нм > 95%, выход – 30 мг (14%). Аминокислотный состав был подтвержден с помощью аминокислотного анализа гидролизата пептида на приборе Alpha Plus LKB.
Сшивка фрагментов 1 и 2. 7 мг пептида 1 (5,6 ммоль) растворили в 1 мл 0,1 М Na2HPO4 при рН 4,5, а 12 мг пептида 2 (8,55 ммоль) растворили в 2 мл того же буфера. Растворы смешали в колбе на 10 мл и перемешивали на магнитной мешалке при комнатной температуре. Через 1.5 часа с помощью контроля методом ВЭЖХ определили, что пептид 1 практически исчез и образовался новый продукт, который был выделен на препаративной ВЭЖХ колонке Waters Prep Nova РАК С18, 6ukm, 60 A, 19 150 мм, при скорости потока 1 мл/мин и элюции 0,1% трифторуксусной кислотой при градиенте 10-40% ацетонитрила.
Время удерживания составило 11,84 мин, чистота по оптической плотности на 230 нм > 95%, выход – 30 мг (14%). Аминокислотный состав был подтвержден с помощью аминокислотного анализа гидролизата пептида на приборе Alpha Plus LKB.
Сшивка фрагментов 1 и 2. 7 мг пептида 1 (5,6 ммоль) растворили в 1 мл 0,1 М Na2HPO4 при рН 4,5, а 12 мг пептида 2 (8,55 ммоль) растворили в 2 мл того же буфера. Растворы смешали в колбе на 10 мл и перемешивали на магнитной мешалке при комнатной температуре. Через 1.5 часа с помощью контроля методом ВЭЖХ определили, что пептид 1 практически исчез и образовался новый продукт, который был выделен на препаративной ВЭЖХ колонке Waters Prep Nova РАК С18, 6ukm, 60 A, 19 300 mm.
Однородность пептида определяли по данным ВЭЖХ на колонке Delta РАС С18, 100А, 3,9 300 mm.
Однородность пептида определяли по данным ВЭЖХ на колонке Delta РАС С18, 100А, 3,9 150 мм, при скорости потока 1 мл/мин и элюции 0,1% трифторуксусной кислотой при градиенте 10-50% ацетонитрила.
Время удерживания составило 10,50 мин, чистота по оптической плотности на 230 нм > 95%, выход – 7,7 мг (49%). Аминокислотный состав был подтвержден с помощью аминокислотного анализа гидролизата полученного соединения на приборе Alpha Plus LKB.
Хемотактическую активность пептидов изучали с помощью метода миграции нейтрофилов под агарозой.
Нейтрофильные клетки получали путем фракционирования свежей донорской крови на градиенте фиколл-пака (уд. плотность 1078) путем центрифугировании при 400 g. После центрифугирования собирали клетки из осадка, примесь эритроцитов удаляли с помощью гипотонического шока дистиллированной водой в течение 40 секунд. После двукратного отмывания физиологическим раствором клетки ресуспендировали в среде Игла с добавлением 10% телячьей фетальной сыворотки. Концентрация клеток, используемая в реакции – 30 млн клеток в 1 мл среды.
Агарозную среду готовили в день исследования. Для проведения реакции использовали 1% раствор агарозы (тип 11, ЕЕО, Sigma) в среде 199, содержащей 10% телячьей фетальной сыворотки.
В агарозном геле, разлитом в чашки Петри диаметром 40 мм, после застывания пробойником пробивали на одном уровне по три отверстия па расстоянии 3 мм. В левую лунку вносили по 10 мкл культуральной среды Игла для определения спонтанной миграции клеток, в центральную – 10 мкл клеточной взвеси нейтрофилов, в правую лунку по 10 мкл изучаемого пептида в соответствующих разведениях. Чашки Петри инкубировали полтора часа при температуре 37o.
После инкубации чашки Петри вынимали, заливали 10% раствором формалина на ночь, затем сливали раствор формалина, удаляли агарозный диск и проводили дофиксацию метанолом в течение 10 минут.
Окрашивание зон миграции производили красителем Романовского-Гимзе. Результат реакции учитывали с помощью линейки на аппарате для чтения микрофильмов.
Окончательный результат реакции выражали в индексах миграции, являющихся отношением длины пробега клеток в опыте (изучаемые препараты) к длине пробега клеток в контроле (культуральная среда).
Полученные результаты приведены в таблице 3.
Полученные данные свидетельствуют, что полученный пептид не только обладает хемоаттрактантной активностью, но его стимулирующее воздействие на миграцию нейтрофилов на 15-29% выше, чем у ИЛ-8.
Проведенные испытания пептидов при внутривенном введении в дозе до 5,0 мг/кг путем инъекции соединения в физиологическом растворе в хвостовую вену белых беспородных мышей и перрорально до 20 мг/мышь не выявили токсичность для заявляемого соединения. 150 мм, при скорости потока 1 мл/мин и элюции 0,1% трифторуксусной кислотой при градиенте 10-50% ацетонитрила.
Время удерживания составило 10,50 мин, чистота по оптической плотности на 230 нм > 95%, выход – 7,7 мг (49%). Аминокислотный состав был подтвержден с помощью аминокислотного анализа гидролизата полученного соединения на приборе Alpha Plus LKB.
Хемотактическую активность пептидов изучали с помощью метода миграции нейтрофилов под агарозой.
Нейтрофильные клетки получали путем фракционирования свежей донорской крови на градиенте фиколл-пака (уд. плотность 1078) путем центрифугировании при 400 g. После центрифугирования собирали клетки из осадка, примесь эритроцитов удаляли с помощью гипотонического шока дистиллированной водой в течение 40 секунд. После двукратного отмывания физиологическим раствором клетки ресуспендировали в среде Игла с добавлением 10% телячьей фетальной сыворотки. Концентрация клеток, используемая в реакции – 30 млн клеток в 1 мл среды.
Агарозную среду готовили в день исследования. Для проведения реакции использовали 1% раствор агарозы (тип 11, ЕЕО, Sigma) в среде 199, содержащей 10% телячьей фетальной сыворотки.
В агарозном геле, разлитом в чашки Петри диаметром 40 мм, после застывания пробойником пробивали на одном уровне по три отверстия па расстоянии 3 мм. В левую лунку вносили по 10 мкл культуральной среды Игла для определения спонтанной миграции клеток, в центральную – 10 мкл клеточной взвеси нейтрофилов, в правую лунку по 10 мкл изучаемого пептида в соответствующих разведениях. Чашки Петри инкубировали полтора часа при температуре 37o.
После инкубации чашки Петри вынимали, заливали 10% раствором формалина на ночь, затем сливали раствор формалина, удаляли агарозный диск и проводили дофиксацию метанолом в течение 10 минут.
Окрашивание зон миграции производили красителем Романовского-Гимзе. Результат реакции учитывали с помощью линейки на аппарате для чтения микрофильмов.
Окончательный результат реакции выражали в индексах миграции, являющихся отношением длины пробега клеток в опыте (изучаемые препараты) к длине пробега клеток в контроле (культуральная среда).
Полученные результаты приведены в таблице 3.
Полученные данные свидетельствуют, что полученный пептид не только обладает хемоаттрактантной активностью, но его стимулирующее воздействие на миграцию нейтрофилов на 15-29% выше, чем у ИЛ-8.
Проведенные испытания пептидов при внутривенном введении в дозе до 5,0 мг/кг путем инъекции соединения в физиологическом растворе в хвостовую вену белых беспородных мышей и перрорально до 20 мг/мышь не выявили токсичность для заявляемого соединения.
Формула изобретения
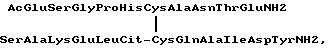 стимулирующий миграцию нейтрофилов. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 23.11.2005
Извещение опубликовано: 20.11.2006 БИ: 32/2006
|
||||||||||||||||||||||||||
