Патент на изобретение №2181049
|
||||||||||||||||||||||||||
(54) ИСПОЛЬЗОВАНИЕ АМИНОПУРИНОВЫХ ПРОТИВОВИРУСНЫХ СОЕДИНЕНИЙ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЛАТЕНТНЫХ ИНФЕКЦИЙ, ВЫЗВАННЫХ ВИРУСОМ ГЕРПЕСА
(57) Реферат: Изобретение относится к медицине, конкретно – к фармакологии и химиотерапии. Предложен новый способ профилактики в виде снижения развития или снижения реактивации латентной инфекции вируса герпеса введением соединения формулы (А) 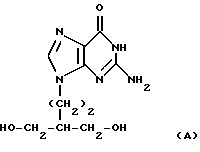 или формулы (B) 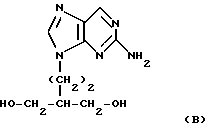 .
Изобретение отличает возможность профилактики спустя 18 ч и вплоть до 4 сут после инфицирования. 3 з.п. ф-лы, 3 табл. .
Изобретение отличает возможность профилактики спустя 18 ч и вплоть до 4 сут после инфицирования. 3 з.п. ф-лы, 3 табл.
Данное изобретение относится к лечению латентных инфекций, вызванных вирусами герпеса. Когда он используется здесь, термин “лечение” включает и профилактику, когда это уместно. В ЕР-А-141927 (Beecham Group p.l.с.) раскрывается пенцикловир, соединение формулы (А): 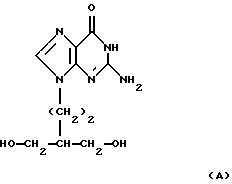 и его соли, фосфатные эфиры и ацильные производные в качестве противовирусных соединений. Гидрат натриевой соли пенцикловира раскрыт в ЕР-А-216459 (Beecham Group p. 1.с.). Пенцикловир и его антивирусная активность описывается также в реферате Р. VII-5, p.l93 публикации “Abstracts of 14th Int. Congress of Microbiology”, Manchester, England, 7-13 September 1986 (Boyd et al). Активными при пероральном приеме биопредшественниками соединения формулы (А) являются соединения формулы 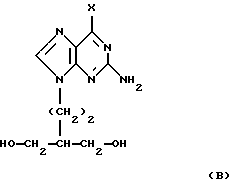 и их соли и производные определенные формулой (А); в которой Х является C1-6 алкоксилом, NH2 или водородом. Соединения формулы (В), в которой Х является C1-6 алкоксилом или NH2, раскрыты в ЕР-А-141927, а соединения формулы (В), в которой Х является водородом, раскрытые в ЕР-А-182024 (Beecham Group p.1.с.), являются предпочтительными пролекарствами. Особенно предпочтительным примером соединения формулы (В) является соединение, в котором Х является водородом, и в котором две ОН-группы находятся в форме ацетильного производного, описанное в примере 2 ЕР-А-182024, здесь далее называемое фамцикловиром. Соединения формул (А) и (В) и их соли и производные описаны как полезные при лечении инфекций, вызываемых вирусами герпеса, такими как Herpes simplex типа 1 и Herpes simplex типа 2. Предшествующая работа показала, что если антивирусное лечение задерживается на более, чем несколько часов после инфецирования, то устанавливается латентность. Если установилась латентность инфекции, инфекция может возобновляться. В настоящее время показано на мышах, что лечение фамцикловиром может предотвращать установление компетентной латентности, когда лечение начинается через 18 часов (первый эксперимент) и вплоть до 4 суток (второй эксперимент) после инфицирования. В настоящее время было также показано, что латентность можно предотвратить в эксперименте на мышах с нарушенной иммунной системой. Потенциальное клиническое преимущество состоит в том, что больного в пределах 4 дней после контакта можно лечить фамцикловиром для предотвращения не только острой инфекции, но также и развития латентности и, таким образом избежать рецидивов. Кроме того, полагают, что может происходить медленная естественная потеря латентно инфецированных клеток, и может быть потребоваться повторное инфицирование для поддержания наличия латентно инфицированных клеток путем установления латентности в новых клетках. Поэтому подавляющее лечение фамцикловиром в течение продолжительного периода (до нескольких лет) может препятствовать новым клеткам становиться латентно инфицированными. Тогда результатом будет радикальное излечение, причем после этого у больного не будет рецидивов. Соответственно, настоящее изобретение представляет способ лечения латентной инфекции, вызванной вирусом герпеса, у людей, который включает введение человеку, нуждающемуся в таком лечении, эффективного количества соединения формулы (А): 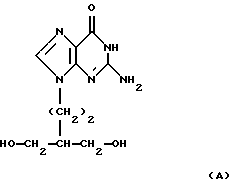 или его биопредшественника или фармацевтически приемлемой соли, фосфатного эфира и/или ацильного производного любого из указанных ранее соединений. Термин “ацильное производное” используется здесь, чтобы включить любое производное соединений формулы (А), в котором присутствует одна или более ацильных групп. Такие производные включены в качестве биопредшественников соединений формулы (А) в дополнение к тем производным, которые сами по себе биологически активны. Соединение формулы (А) может быть в одной из форм, раскрытых в ЕР-А-216459 (Beecham Group p.1.e.). Примерами биопредшественников, фармацевтически приемлемых солей и производных являются соединения, описанные в вышеупомянутых европейских патентах, предмет которых приведен здесь для сведения. Конкретным соединением формулы (В), представляющим интерес является 9-(4-ацетокси-3-ацетоксиметилбут-1-ил)-2-аминопу-рин, известный как фамцикловир (ФЦВ), хорошо абсорбируемая пероральная форма пенцикловира (ПЦВ). Соединение формулы (А), биопредшественники, соли и производные могут быть получены, как описано в вышеупомянутых европейских патентах. Соединение, в частности фамцикловир, может вводиться людям парентеральным путем и может быть преобразовано в форму сиропа, таблеток или капсул. Когда оно изготавливается в виде таблеток, может использоваться любой фармацевтический носитель, подходящий для получения таких твердых композиций, например, стеарат магния, крахмал, лактоза, глюкоза, рис, мука и мел. Соединение может быть также представлено в форме проглатываемых капсул, например из желатина, вмещающих это соединение, или в форме сиропа, раствора или суспензии. Подходящие жидкие фармацевтические носители включают этиловый спирт, глицерин, физиологический раствор и воду, к которой могут добавляться вкусовые и подкрашивающие вещества для получения сиропа. Также предусматриваются лекарственные формы с длительным выделением, например, таблетки, имеющие покрытие, растворяющееся в кишечнике. Для парентерального введения изготавливаются жидкие лекарственные формы, в виде единичных доз, содержащие соединение и стерильный носитель. Соединение, в зависимости от носителя и концентрации, может быть или суспендировано или растворено. Парентеральные растворы обычно готовятся путем растворения соединения в носителе и фильтр-стерилизации перед заполнением или подходящего сосуда или ампулы и запечатыванием. Целесообразно, чтобы адьюванты, такие как местные анестетики, консерванты и буферные вещества, также растворялись в носителе. Для увеличения стабильности, композиция может вымораживаться после заполнения сосудов, а вода – удалятся под вакуумом. Парентеральные суспензии готовят по существу таким же образом, за исключением того, что соединение суспендируется в носителе вместо растворения и стерилизуется путем воздействия этиленоксида перед суспендированием в стерильном носителе. Целесообразно, чтобы в композицию включался поверхностно-активный или смачивающий агент для облегчения равномерного распределения соединения изобретения. Предпочтительные парентеральные лекарственные формы включают водные лекарственные формы с использованием стерильной воды или физиологического раствора с рН, равным примерно 7,4 или более, в частности, содержащие гидрат натриевой соли пенцикловира. Как обычно принято на практике, композиции обычно сопровождаются написанными или напечатанными инструкциями по применению при соответствующем медицинском лечении. Соответствующая единичная доза (дозированная форма) может содержать от 50 мг до 1 г активного ингредиента, например 100-500 мг. Такие дозы могут вводиться 1-4 раза в день, или более обычно, 2 или 3 раза в день. Эффективная доза соединения будет, в основном, находиться в интервале от 0,2 до 40 мг на кг веса тела в сутки или, более обычно, от 10 до 20 мг/кг в сутки. В случае фамцикловира единичная доза составляет 125 мг, 250 мг, 500 мг или 750 мг, предпочтительно, 125 мг или 250 мг. Для предотвращения формирования компетентной латентности лечение предпочтительно проводится как можно скорее после контакта с вирусом, предпочтительно в пределах 18 часов, хотя приемлемо его начало в течение до 4 дней. Период лечения составляет обычно 3-14 дней, более обычно 5-10 дней, часто 7 дней, Для лечения установленного рецидивного заболевания период лечения составляет до 5 лет, например, до 1, 2, 3, 4 и 5 лет. Данное изобретение также предоставляет использование соединения формулы (А) или биопредшественника или фармацевтически приемлемой соли, фосфатного эфира и/или ацильного производного любого из указанных соединений для изготовления медикамента для использования при лечении латентной инфекции, вызванной вирусами герпеса. Такое лечение может проводиться по способу, который описан здесь ранее. Данное изобретение, кроме того, предоставляет фармацевтическую композицию для использования при лечении латентной инфекции, вызванной вирусами герпеса, которая включает эффективное количество соединения формулы (А), или биопредшестсвенника, или фармацевтически приемлемой соли, фосфатного эфира и/или ацильного производного любого из соединений, и фармацевтически приемлемый носитель. Такие композиции могут быть изготовлены таким же образом, как описано здесь далее. Соединение формулы (А) и его пролекарства проявляют синергетическое антивирусное действие в сочетании с интерферонами; и поэтому лечение с использованием комбинированных продуктов, включающих эти два компонента для последовательного или сопутствующего введения одним и тем же или разными путями охватывается обьемом данного изобретения. Следующие результаты исследований на животных иллюстрируют изобретение. Эксперименты на мышах, инфицированных вирусом HSV-1 Кожную инфекцию создавали путем инокулирования в мочку уха мышей HSV-1 (SC16) и исследовали действие фамцикловира при пероральном введении на латентную вирусную инфекцию. Мышей самок BALB/c (Bantin and Kingman, Kingston, Hull, UK) закупали в 3-х-4-х недельном возрасте и заражали спустя неделю. Суспензию вируса (10 мкл), содержащую 5  104 бое, инокулировали в кожу мочки левого уха. Толщину кожи измеряли ежедневно у отдельных мышей с помощью винтового микрометра (Nash et al., 1980 J. Gen. Virol. 48, 351-357). Этих мышей содержали в течение 3 (эксперимент 1) или 4 (эксперимент 2) месяцев и затем забивали. Тройничный узел и цервикальный дорзальный корневой узел удаляли и культивировали совместно те культуры, которые показывали репликацию вируса, регистрировали как положительные.
Эксперимент 1 104 бое, инокулировали в кожу мочки левого уха. Толщину кожи измеряли ежедневно у отдельных мышей с помощью винтового микрометра (Nash et al., 1980 J. Gen. Virol. 48, 351-357). Этих мышей содержали в течение 3 (эксперимент 1) или 4 (эксперимент 2) месяцев и затем забивали. Тройничный узел и цервикальный дорзальный корневой узел удаляли и культивировали совместно те культуры, которые показывали репликацию вируса, регистрировали как положительные.
Эксперимент 1В первом эксперименте мышей начинали лечить в пределах 18 часов и лечение прекращали на 10 день после инфицирования. Из 24 нелеченных контрольных мышей у 12 выявлена латентная инфекция в тройничном ганглии (ТГ) и у 20 выявлена латентная инфекция в цервикальном дозральном корневом ганглии (ДКГ). У всех 24 контрольных мышей выявлена или ТГ, или ДКГ латентность. Ни у одной из мышей, которых лечили ФЦВ не выявлена какая-либо латентность. Эксперимент 2 Во втором эксперименте противовирусное лечение начиналось на 2, 3, 4 и 5 день после инфицирования (п.и.) и прекращалось на 10 день п.и.. Соединения давались с питьевой водой без ограничений при концентрации 1 мг/мл (примерно 100 мг/кг/сутки). Результаты представлены в табл. 1. Через четыре месяца латентный вирус мог реактивироваться в эксплантах ганглиев (ипсилатеральных и контралатеральных тройничных и дорзальных корневых) от всех из 16 котрольных мышей. Латентный вирус не реактивировался из ганглиев подвергнутых лечению ФЦВ мышей, за исключением ипсилатеральных ганглиев, и только когда начало терапии откладывалось до 4 дней п.и. (2/16) или 5 дней п.и. (6/16). Сходные результаты были получены, когда соединения вводили дважды в сутки ежедневно через зонд в количестве 50 мг/кг на дозу. Эксперимент 3 Мышей подвергали иммуносупрессии циклоспорином А(ЦиА) со дня -2 по день = 10 (причем день 0 является днем инфицирования). Группы мышей были: нелечившимися (контрольная) или лечившимися фамцикловиром перорально в дозе 50 мг/кг дважды в день, начиная с 22 часа после инфицирования до 5,5 или 10,5 дней. Ганглии исследовали на реактивацию инфицирующего вируса через 1 или 4 месяца, и результаты показаны в табл.2. Эксперименты на мышах, инфицированных вирусом HSV-2 Каждую инфекцию создавали путем инокуляции в мочку уха мышей HSV-2 (Вrу) и исследовали действие фамцикловира при пероральном приеме на латентную вирусную инфекцию. Лечение состояло в приеме 50 мг/кг дважды в день в течение 5 дней, начиная с 22 часа после инфекции. В табл.3 показано число мышей/группу с положительной латентной инфекцией в тройничном или цервикальном дорзальном корневом ганглии. Формула изобретения
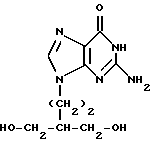 или его биопредшественника формулы В 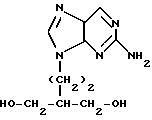 или фармацевтически приемлемой соли любого из указанных соединений спустя по меньшей мере 18 ч после заражения. 2. Способ по п.1, отличающийся тем, что лекарство вводят для снижения развития и реактивации латентной инфекции, вызванной вирусом простого герпеса типа 1. 3. Способ по п.1, отличающийся тем, что лекарство вводят для снижения развития и реактивации латентной инфекции, вызванной вирусом простого герпеса типа 2. 4. Способ по п.1, отличающийся тем, что лекарство вводят в дозе 125 мг, 250 мг, 500 мг, 750 мг или 1 г один, два или три раза в день. Приоритет по пунктам: 12.12.1994 по пп.1, 2, 4; 24.08.1995 по п.3. РИСУНКИ
|
||||||||||||||||||||||||||
