Патент на изобретение №2176243
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИНДОЛА
(57) Реферат: Изобретение относится к способу получения производных индола общей формулы 1, представляющих интерес в качестве полупродуктов в синтезе пирролоиндолов и митомициноидов, где R1 и R2 означают ОСН3, R означает Ph (la), или R означает трет-Вr-Ph (1б), или R означает СН3 (1в); или R1 и R2 означают Н, R означает Ph (1г), или R означает р-СН3 (1д), или R означает р-Вr-Ph (1е), или R означает p-Cl-Ph (1ж). Способ заключается в нагревании производных 2-тозиламиноарилфурилметана формулы 2 в насыщенном растворе газообразного хлороводорода в этаноле при температуре 70-78oС в течение 10-30 минут. Способ позволяет получать соединения с выходом 70-75%, снизить осмоление реакционной массы. 2 табл. 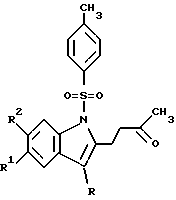 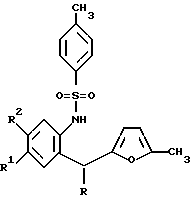
Изобретение относится к области органической химии – синтезу гетероциклических соединений – производных индола, представляющих интерес в качестве полупродуктов в синтезе пирролоиндолов и митомициноидов. Изобретение включает разработку способа получения производных индола общей формулы I: 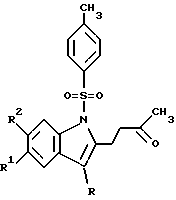 Ia R1=R2=OCH3, R = Ph; б R1 = R2 = OCH3; R = m-Br-Ph, в R1 = R2 = OCH3; R = CH3; г R1 = R2 = H, R = Ph; д R1= R2 = H, R = p-CH3-Ph; e R1 = R2 = H, R =p-Br-Ph, ж R1 = R2 = H, R =p-Cl-Ph. В литературе отсутствуют данные по синтезу этих соединений. Однако, принимая во внимание приведенные в работах [Danishefsky S.J., Schkeryantz J. M. Synlett, 1995, 5, 475; Vice S.F., Friesen R.W., Dmitrienko G.I. Tetrahedron Lett. , 1985, 26, 165] сведения по применению производных индола в синтезе противоопухолевых препаратов, в частности, для получения пирролоиндольной структуры – основного фрагмента митомициноидов, соединения 1а-ж являются перспективными и представляют значительный интерес как полупродукты для получения новых соединений, обладающих биологической активностью. В ряду общих методов синтеза производных индола широко известен способ Рейссерта [Общая органическая химия. – Пер. с англ. / Под ред. Н.К. Кочеткова. – М.: Химия, 1985. – Т. 8. – С. 551]. По этому методу образование производных индола происходит в результате восстановительной циклизации эфиров орто-нитрофенилпировиноградной кислоты, получаемых в ходе катализируемой основаниями конденсации эфиров щавелевой кислоты с орто-нитротолуолами, содержащими активированную метильную группу. 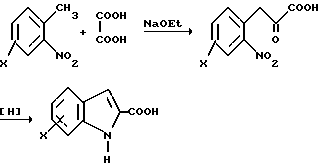 Главным недостатком этого способа является ограничение по выбору исходных орто-нитротолуолов и, как следствие, невозможность введения в бензольное кольцо индола донорных заместителей. Поэтому описанный способ получения индолов не является универсальным. Существует несколько модификаций метода Рейссерта. Во всех случаях в качестве исходных реагентов используются бензилкарбонильные соединения или их аналоги, содержащие в орто-положении ароматического кольца NO2 или NH2 группу. Общими недостатками всех модификаций являются либо трудность получения исходных соединений либо, как и для метода Рейссерта, ограничения в применимости реакции. Наиболее близким из известных способов получения производных индола является способ синтеза 3-(5-метилфур-2-ил)-2-(3-оксобутен-1-ил)индола, в котором в качестве исходного соединения использовано производное фурил(арил)метана-бис(5-метилфур-2-ил)-2-нитрофенил-метан [Butin A.V., Abaev V. Т. , Stroganova T.A., Gutnov V.Т. Molecules, 1997, 2, 62-68]. Производное индола с выходом 57% было получено в результате восстановления бис(5-метилфур-2-ил)-2-нитрофенилметана хлористым оловом в присутствии HCl или (CH3)3SiCl: 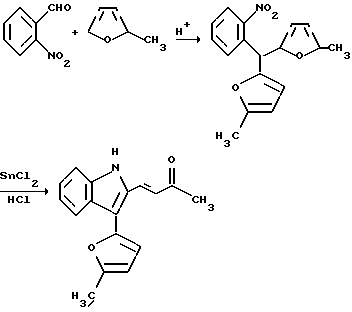 Основным недостатком этого метода является невозможность использования в качестве исходных соединений производных фурил(арил)метана, содержащих в бензольном кольце донорные заместители в пара-положении к нитрогруппе и, как следствие, невозможность получения индолов с донорными группами в бензольном кольце индола. Цель изобретения – разработка способа получения производных индола 1 с 3-оксобутильным фрагментом в положении 2 индольного цикла, позволяющего вводить в бензольное кольцо индольного цикла различные заместители; повышение выхода целевых продуктов, снижение осмоления реакционной массы. Поставленная цель достигается тем, что в соединениях общей формулы I образование индольного фрагмента происходит в результате рециклизации фуранового кольца производных фурил(арил)метана при нагревании производных 2-тозиламиноарилфурилметана в насыщенном растворе газообразного хлороводорода в этаноле при температуре 70 -78oC в течение 10-30 минут. 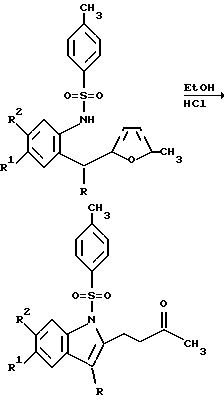 Отличием предлагаемого способа получения производных индолов I является использование в качестве исходного соединения производных 2-тозиламиноарилфурилметана, фурановый цикл которых выступает в роли скрытого карбонильного соединения. Следует отметить, что исходные производные 2-тозиламиноарилфурилметана могут быть легко получены с выходами 60-80% алкилированием 2-алкилфуранов доступными 2-тозиламиноарил-R-карбинолами по методу, аналогичному приведенному в работе [Gutnov A.V., Butin A.V., Abaev V.T., Krapivin G.D., Zavodnik V.E. Molecules, 1999, 4, 204-218]. Применение насыщенного раствора газообразного хлороводорода в этаноле позволяет избежать осмоления реакционной массы, добиться высоких выходов целевых продуктов и полной конверсии исходных производных 2-тозиламиноарилфурилметана в индолы в течение непродолжительного времени. Таким образом, совокупность существенных признаков, изложенных в формуле изобретения, позволяет достичь желаемого технического результата. Индивидуальность и строение синтезированных соединений I подтверждены данными ПМР-спектроскопии и элементного анализа. Примеры осуществления заявляемого способа получения производных индола: Пример 1. N-n-Тозил-5,6-диметокси-2-(3-оксобутил)-3- фенилиндол (Iа) 4,53 г (0,01 моль) 4,5-диметокси-2-N-n- тозиламинофенил(5-метилфур-2-ил)фенилметана растворяли в 100 см3 насыщенного раствора газообразного хлороводорода в этаноле и выдерживали на водяной бане при температуре 30oC в течение 4 часов (240 мин). Реакционную смесь разбавляли водой до объема 500 см3 образовавшийся осадок отделяли фильтрацией, сушили и кристаллизовали из этанола, получая 3,17 г (70%) индола Iа. Тпл = 176oC (гексан – хлористый метилен). Найдено для C27H27NO5S,%: C 67,35; H 5,48; N 3,02; Вычислено: C 67,22; H 5,66; N 2,94. ПМР спектр (CDCl3, 60 МГц): 2,07 (3H, с, CH3); 2,27 (3H, с, CH3), 2,70.. .2,93 (2H, м,  -CH2 ); 3,05…3,24 (2H, м, -CH2 ); 3,05…3,24 (2H, м,  -CH2); 3,73 (3H, с, OCH3,); 3,93 (3H, с, OCH3); 6,68 (3H, с, HInd); 7,07. 7,67 (9H, м, HAr); 7,83 (1H, с, HInd).
ИК спектр (в вазелиновом масле): 1700 см-1 (CO).
Пример 2. N-n-Toзил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндол (Ia) получают аналогичным образом, используя 4,53 г (0,01 моль) 4,5-диметокси-2-N-n-тозиламинофенил(5-метилфур-2-ил)фенилметана и 100 см3 насыщенного раствора газообразного хлороводорода в этаноле, проводя реакцию при температуре 60oC. Продолжительность реакции в этих условиях составляет 90 мин; выход продукта реакции 3,26 г (72%).
Пример 3. N-n-Тозил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндол (Iа) получают аналогичным образом, используя 4,53 г (0,01 моль) 4,5-диметокси-2-N-n-тозиламинофенил(5-метилфур-2-ил)фенилметана и 100 см3 насыщенного раствора газообразного хлороводорода в этаноле, проводя реакцию при температуре 70oC. Продолжительность реакции составляет 30 мин; выход продукта реакции 3,31 г (73%).
Пример 4. N-n-Тозил-5,6-диметокси-2-(3- оксобутил)-3-фенилиндол (Iа) получают аналогичным образом, используя 4,53 г (0,01 моль) 4,5-диметокси-2-N-n- тозиламинофенил(5-метилфур-2-ил)фенилметана и 100 см3 насыщенного раствора газообразного хлороводорода в этаноле, проводя реакцию при кипении реакционной массы (78oC). Продолжительность реакции составляет 10 мин; выход продукта реакции 3,40 г (75%).
В таблице 1 приведены данные о влиянии температуры проведения реакции на длительность процесса и выход N-n-тозил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндола (Iа) (примеры 1-4).
Таким образом, оптимальным вариантом является проведение реакции при 70-78oC, поскольку в этом случае выход N-n-тозил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндола (Iа) достигает 73-75%, а длительность процесса составляет 10-30 мин.
Заявляемым способом получен ряд производных индола 1б-ж, выходы, температуры плавления и спектральные характеристики которых приведены в таблице 2. -CH2); 3,73 (3H, с, OCH3,); 3,93 (3H, с, OCH3); 6,68 (3H, с, HInd); 7,07. 7,67 (9H, м, HAr); 7,83 (1H, с, HInd).
ИК спектр (в вазелиновом масле): 1700 см-1 (CO).
Пример 2. N-n-Toзил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндол (Ia) получают аналогичным образом, используя 4,53 г (0,01 моль) 4,5-диметокси-2-N-n-тозиламинофенил(5-метилфур-2-ил)фенилметана и 100 см3 насыщенного раствора газообразного хлороводорода в этаноле, проводя реакцию при температуре 60oC. Продолжительность реакции в этих условиях составляет 90 мин; выход продукта реакции 3,26 г (72%).
Пример 3. N-n-Тозил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндол (Iа) получают аналогичным образом, используя 4,53 г (0,01 моль) 4,5-диметокси-2-N-n-тозиламинофенил(5-метилфур-2-ил)фенилметана и 100 см3 насыщенного раствора газообразного хлороводорода в этаноле, проводя реакцию при температуре 70oC. Продолжительность реакции составляет 30 мин; выход продукта реакции 3,31 г (73%).
Пример 4. N-n-Тозил-5,6-диметокси-2-(3- оксобутил)-3-фенилиндол (Iа) получают аналогичным образом, используя 4,53 г (0,01 моль) 4,5-диметокси-2-N-n- тозиламинофенил(5-метилфур-2-ил)фенилметана и 100 см3 насыщенного раствора газообразного хлороводорода в этаноле, проводя реакцию при кипении реакционной массы (78oC). Продолжительность реакции составляет 10 мин; выход продукта реакции 3,40 г (75%).
В таблице 1 приведены данные о влиянии температуры проведения реакции на длительность процесса и выход N-n-тозил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндола (Iа) (примеры 1-4).
Таким образом, оптимальным вариантом является проведение реакции при 70-78oC, поскольку в этом случае выход N-n-тозил-5,6-диметокси-2-(3-оксобутил)-3-фенилиндола (Iа) достигает 73-75%, а длительность процесса составляет 10-30 мин.
Заявляемым способом получен ряд производных индола 1б-ж, выходы, температуры плавления и спектральные характеристики которых приведены в таблице 2.
Формула изобретения
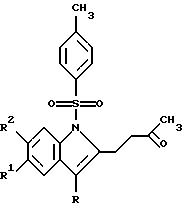 I a R1=R2=ОСН3, R=Ph; б R1=R2=ОСН3; R=m-Br-Ph; в R1=R2=ОСН3; R=СН3; г R1=R2=Н, R=Ph, д R1=R2=Н, R=р-СН3-Рh; е R1=R2=Н, R=р-Br-Ph; ж R1=R2=Н, R=р-Cl-Ph, включающий образование индольного фрагмента в результате рециклизации фуранового кольца производных фурил(арил)метана при нагревании производных 2-тозиламиноарилфурилметана 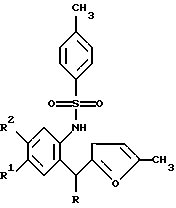 в насыщенном растворе газообразного хлороводорода в этаноле при температуре 70-78oС в течение 10-30 мин. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 24.02.2005
Извещение опубликовано: 20.02.2006 БИ: 05/2006
|
||||||||||||||||||||||||||
