Патент на изобретение №2173689
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ 12,13-ЭПОКСИТИЛОЗИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ
(57) Реферат: Описываются новые производные 12,13-эпокситилозина формулы I, где R обозначает O, R1 обозначает CHO или CH(OCH3)2, R2 обозначает H или микарозил и —- обозначает одинарную связь; либо где R обозначает NOH, R1 обозначает CHO или CH(OCH3)2, R2 обозначает H или микарозил и —- обозначает одинарную или двойную связь; или соединения формулы II, где R обозначает H или микарозил. Соединения проявляют антимикробное действие. Описываются также способы их получения. 2 с. и 15 з.п.ф-лы. 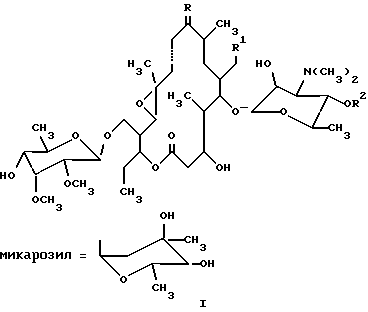 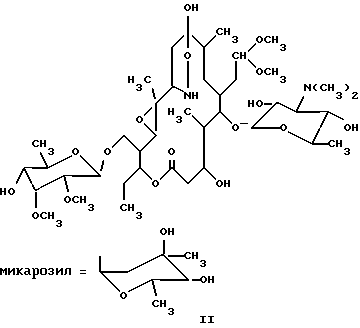
1) Область техники, к которой относится изобретение Настоящее изобретение относится к производным тилозина, новым синтетическим продуктам из класса макролидов, проявляющим антимикробное действие. Более конкретно, изобретение относится к производным 12,13-эпокситилозина формулы I 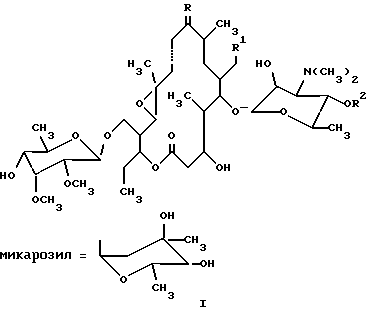 где R обозначает O, R1 обозначает CHO или CH(OCH3)2, R2 обозначает H или микарозил и — обозначает одинарную связь; либо где R обозначает NOH, R1 обозначает CHO или CH(OCH3)2, R2 обозначает H или микарозил и —- обозначает одинарную или двойную связь; и к соединениям формулы II 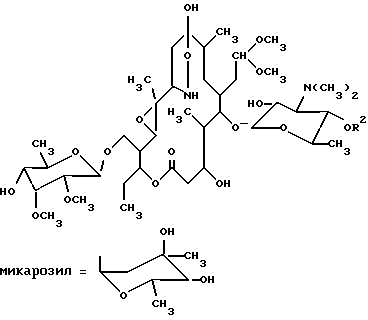 где R2 обозначает H или микарозил, а также к способам получения этих соединений. 2) Известный уровень техники Был осуществлен ряд модификаций диеновой части 16-членного тилозинового кольца. Известно, что присоединением тиолов получали простые 11-тиоэфиры тилозина (S. Omura, патент США 4594338). Известно также, что каталитической гидрогенизацией диена и оксимированием в положениях C-9 и C-20 тилозина были получены 10,11,12,13-тетрагидропроизводные, соответственно их оксимы (A. Naranda, патент США 5023240). Известно, что селективное окисление тилозина позволяло получать 12,13-эпоксипроизводные (A. K. Mallams, патент США 4808575). Были также получены дигидро- и тетрагидропроизводные других 16-членных макролидов с 12,13-эпоксигруппой. Кроме того, известно, что каталитической гидрогенизацией маридомицина получали 13-гидрокси-10,11,12,13-тетрагидромаридомицин [M.Muroi, Chem. Pharm. Bull. 24 (1976), 450], где восстановление C10-C11-двойной связи осуществляли размыканием оксиранового цикла, в то время как каталитической гидрогенизацией розамицина получили 10,11-дигидропроизводное с сохранением 12,13-эпоксигруппы. Более того, известно, что оксимированием розамицина и его 12,13-деэпоксипроизводного были получены C-20 альдоксимы (H.Reinmann, патент США 4056616). В известной литературе 10,11-дигидропроизводные 12,13-эпокситилозина и их C-9 оксимы, 12,13-эпокситилозиноксимы, а также 10,11-дигидро-12,13-эпоксисоединения с 9,11-эпоксииминовым мостиком не описаны, а также нигде не описаны способы получения упомянутых в настоящем описании производных тилозина. 3) Описание изобретения и варианты его выполнения Было установлено, что производные 12,13-эпокситилозина формулы I 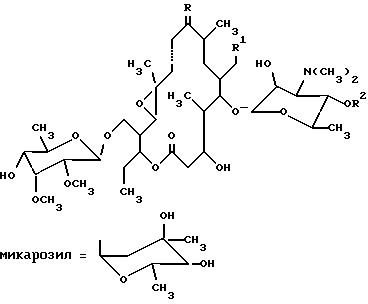 где R обозначает O, R1 обозначает CHO или CH(OCH3)2, R2 обозначает H или микарозил и —- обозначает одинарную связь; либо где R обозначает NOH, R1 обозначает CHO или CH(OCH3)2, R3 обозначает H или микарозил и —- обозначает одинарную или двойную связь; и соединения формулы II 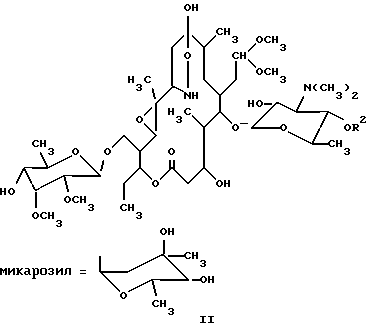 где R обозначает H или микарозил, могут быть получены способом, в котором соединение формулы III 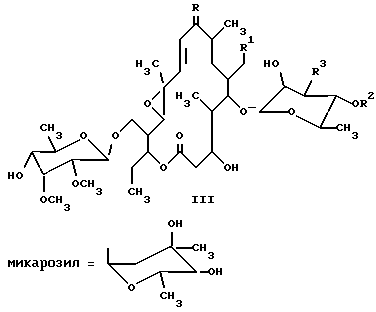 A) где R1 обозначает CHO или CH(OCH2)2, R2 обозначает H или микарозил и R3 обозначает N(CH3)2 или N-(OCH3)2, когда R2 обозначает H; подвергают гидрогенизации в органическом растворителе, прежде всего в низшем C1-C3алифатическом спирте, в присутствии 2-5 вес.% палладия на угле под давлением водорода 0,2-0,5 МПа и при комнатной температуре в течение 5-8 ч, после чего полученное соединение формулы I, где R обозначает O, R1 обозначает CH(OCH3)2, R2 обозначает H или микарозил и —- обозначает одинарную связь, необязательно подвергают оксимированию 3-6 эквивалентами гидроксиламингидрохлорида в пиридине или низшем спирте с добавлением основания, такого как пиридин (или Na2CO3), в токе азота при комнатной температуре или температуре кипения с обратным холодильником в течение 3-7 ч и затем необязательно подвергают гидролизу ацетальной группы в смеси ацетонитрила с 0,2H HCl (1:1) или смеси ацетонитрила с 1%-ной трифторуксусной кислотой в воде (1:2) при комнатной температуре в течение 2 ч; либо Б) где R1 обозначает CH(OCH3)2, R2 обозначает H или микарозил и R3 обозначает N(CH3)2 подвергают оксимированию, как описано выше, и полученные продукты: соединение формулы I, где R обозначает NOH, R1 обозначает CH(OCH3)2, R2 обозначает H или микарозил и —- обозначает двойную связь, и соединение формулы II, где R2 обозначает H или микарозил, разделяют путем колоночной хроматографии на силикагеле и ацетальную группу необязательно подвергают гидролизу описанным путем. В соответствии с настоящим изобретением новые соединения выделяют обычной экстракцией галоидированными углеводородами, такими как четыреххлористый углерод, хлороформ или хлористый метилен, из водных щелочных растворов и упариванием до сухого остатка. При необходимости выделение реакционных продуктов или очистку для спектрального анализа проводят на колонке с силикагелем (Silicagel 60 фирмы Merck Co., 230-400 меш/ASTH, 60-230 меш/ASTH соответственно) в системе растворителей хлористый метилен/метанол/гидроксид аммония: A (90:9:1,5) или Б (90:9:0,5). Идентификацию новых соединений производили УФ- и ЯМР-спектроскопией. Эти новые соединения проявляют антибактериальное действие и могут быть использованы в качестве промежуточных продуктов при получении новых производных тилозина. Ниже изобретение проиллюстрировано на примерах, которые не ограничивают объем изобретения. Пример 1 20-диметилацеталь 10,11-дигидро-12,13-эпокситилозина (1) 2,4 г (2,4 ммоля) 20-диметилацеталя 12,13-эпокситилозина растворяют в 240 мл этанола, добавляют 0,72 г 10%-ного Pd/C и смесь гидрогенизуют при комнатной температуре и давлении водорода 0,2 МПа в течение 8 ч. После завершения реакции катализатор отделяют фильтрованием, этанол выпаривают под пониженным давлением до получения сухого продукта, который затем хроматографируют на колонке с силикагелем. Выход: 1,25 г (52%), Rf (A): 0,65; 1H-ЯМР (CDCl3, част./млн): 5,10 (1H, d, 1”), 4,58 (1H, d, 1”’), 4,24 (1H, d, 1′), 3,64 (3H, s, 3”’OMe), 3,51 (3H, s, 2”’OMe), 3,39 (3H, s, 20-OMe), 3,24 (3H, s, 20-OMe), 2,52 (6H, s, NMe2), 1,34 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част./млн): 212,31 (s, C-9), 170,48 (s, C-1), 103,27 (d, C-1′), 102,94 (d, C-20), 99,36 (d, C-1”’), 96,54 (d, C-1”), 60,66 (q, 3”’OMe), 59,28 (s, C-12), 58,30 (q, 2”’OMe), 58,27 (d, C-13), 53,21 (q, 20-OMe), 50,43 (q, 20-OMe), 33,87 (t, C-10), 28,95 (t, C-11), 18,36 (q, C-22). Пример 2 10,11-дигидро-12,13-эпокситилозин (2) 2 г (2,1 ммоля) 12,13-эпокситилозина растворяют в 200 мл этанола, добавляют 0,4 г 10%-ного Pd/C и гидрогенизуют при комнатной температуре и давлении водорода 0,4 МПа в течение 7 ч. Продукт выделяют аналогично описанному в примере 1. Выход: 0,92 г (46%), Rf (A): 0,54; 1H-ЯМР (CDCl3, част. /млн): 9,67 (1H, s, CHO), 5,09 (1H, d, 1”), 4,58 (1H, d, 1”’), 4,25 (1H, d, 1′), 3,65 (3H, s, 3”’OMe), 3,50 (3H, s, 2”’OMe), 2,51 (6H, s, NMe2), 1,23 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част. /млн): 212,33 (s, C-9), 202,86 (d, C-20), 170,46 (s, C-1), 103,25 (d, C-1′), 99,36 (d, C-1”’), 96,74 (d, C-1”), 60,66 (q, 3”’OMe), 59,29 (s, C-12), 58,37 (q, 2”’OMe; d, C-13), 33,87 (t, C-10), 28,95 (t, C-11), 18,36 (q, C-22). Пример 3 20-диметилацеталь 10,11-дигидро-12,13-эпоксидезмикозина (3) Способ A 2,5 г (2,9 ммоля) N-оксид 20-диметилацеталя 12,13-эпоксидезмикозина растворяют в 250 мл этанола, добавляют 1,25 г 10%-ного Pd/C и гидрогенизуют при комнатной температуре и давлении водорода 0,5 МПа в течение 7 ч. Продукт выделяют аналогично описанному в примере 1. Выход: 1,27 г (52%), Rf (A): 0,57; 1H-ЯМР (CDCl3, част. /млн): 4,56 (1H, d, 1”’), 4,25 (1H, d, 1′), 3,64 (3H, s, 3”’OMe), 3,51 (3H, s, 2”’OMe), 3,38 (3H, s, 20-OMe), 3,22 (3H, s, 20-OMe), 2,52 (6H, s, NMe2), 1,33 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част./млн): 212,31 (s, C-9), 170,25 (s, C-1), 103,23 (d, C-1′), 102,80 (d, C-20), 99,34 (d, C-1”’), 60,45 (q, 3”’OMe), 59,27 (s, C-12), 58,28 (q, 2”’OMe), 58,23 (d, C-13), 53,25 (q, 20-OMe), 50,45 (q, 20-OMe), 33,88 (t, C-10), 28,99 (t, C-11), 18,38 (q, C-22). Способ Б 3 г (3,6 ммоля) 20-диметилацеталя 12,13-эпоксидезмикозина растворяют в 250 мл этанола, добавляют 0,6 г 10%-ного Pd/C и гидрогенизуют при комнатной температуре и давлении водорода 0,5 МПа в течение 8 ч. Продукт, полученный выделением аналогично описанному в примере 1, идентичен продукту, полученному по способу A. Пример 4 10,11-дигидро-12,13-эпоксидезмикозин (4) 2,4 г (3 ммоля) 12,13-эпоксидезмикозина растворяют в 100 мл этанола, добавляют 0,72 г 10%-ного Pd/C и гидрогенизуют при комнатной температуре и давлении водорода 0,3 МПа в течение 8 ч. Выделение осуществляют аналогично описанному в примере 1. Выход: 1,3 г (54%), Rf (A): 0,45; 1H-ЯМР (CDCl3, част./млн): 9,65 (1H, s, CHO), 4,55 (1H, d, 1”’), 4,24 (1H, d, 1′), 3,64 (3H, s, 3”’OMe), 3,51 (3H, s, 2”’OMe), 2,51 (6H, s, NMe2), 1,34 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част. /млн): 212,30 (s, C-9), 202,36 (d, C-20), 170,27 (s, C-1), 103,29 (d, C-1′), 99,34 (d, C-1”’), 60,47 (q, 3”’OMe), 59,28 (s, C-12), 58,27 (q, 2”’OMe; d, C-13), 33,89 (t, C-10), 28,97 (t, C-11), 18,37 (q, C-22). Пример 5 Оксим 20-диметилацеталя 10,11-дигидро-12,13-эпокситилозина (5) 3 г (3 ммоля) соединения 1 растворяют в 39 мл пиридина, добавляют 1,25 г (18 ммолей) гидроксиламингидрохлорида и перемешивают в токе азота при комнатной температуре в течение 7 ч. Реакционный раствор разбавляют 150 мл воды, подщелачивают до pH 9 добавлением 10%-ного NaOH и под пониженным давлением упаривают до одной трети объема. Проводят экстракцию хлороформом (2 порции по 60 мл до pH 6, 2 порции по 60 мл до pH 9,5). Объединенные экстракты с pH 9,5 промывают насыщенным раствором NaHCO3, сушат (K2CO3) и упаривают до сухого остатка. Выход: 1,83 г (61,3%), Rf (A): 0,45; 1H-ЯМР (ДМСО, част./млн): 10,23 (1H, s, 9-NOH), исчезает при смешении с D2O, 4,99 (1H, d, 1”), 4,45 (1H, d, 1”’), 4,22 (1H, d, 1′), 3,49 (3H, s, 3”’OMe), 3,45 (3H, s, 2”’OMe), 3,23 (3H, s, 20-OMe), 3,14 (3H, s, 20-OMe), 2,46 (6H, s, NMe2, 1,25 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част./млн): 173,19 (s, C-1), 161,69 (s, C-9), 104,17 (d, C-1′), 102,06 (d, C-20), 100,64 (d, C-1”’), 96,65 (d, C-1”), 62,30 (s, C-12), 61,69 (d, C-13), 61,43 (q, 3”’OMe), 59,09 (q, 2”’OMe), 16,32 (q, C-22). Пример 6 Оксим 20-диметилацеталя 10,11-дигидро-12,13-эпоксидезмикозина (6) 2 г (2,4 ммоля) соединения 3 растворяют в 20 мл метанола, добавляют 0,64 г Na2CO3, а также 0,84 г (12,3 ммоля) гидроксиламингидрохлорида и перемешивают в токе азота при температуре кипения с обратным холодильником в течение 3 ч. Реакционный раствор сливают в 60 мл воды и продукт выделяют экстракцией с изменением величины pH аналогично описанному в примере 5. Выход: 1,1 г (54%), Rf (A): 0,33; 1H-ЯМР (ДМСО, част./млн): 10,22 (1H, s, 9-NOH), исчезает при смешении с D2O, 4,43 (1H, d, 1”’), 4,19 (1H, d, 1′), 3,47 (3H, s, 3”’OMe), 3,43 (3H, s, 2”’OMe), 3,21 (3H, s, 20-OMe), 3,12 (3H, s, 20-OMe), 2,42 (6H, s, NMe2), 1,24 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част./млн): 172,98 (s, C-1), 161,62 (s, C-9), 103,98 (d, C-1′), 102,05 (d, C-20), 100,51 (d, C-1”’), 62,27 (s, C-12), 61,73 (d, C-13), 61,42 (q, 3”’OMe), 59,09 (q, 2”’OMe), 16,30 (q, C-22). Пример 7 Оксим 10,11-дигидро-12,13-эпокситилозина (7) и оксим 10,11-дигидро-12,13-эпоксидезмикозина (8) 2 г (2 ммоля) соединения (5) растворяют в смеси 20 мл ацетонитрила с 20 мл 0,2H HCl и перемешивают при комнатной температуре в течение 2 ч. Реакционный раствор разбавляют 20 мл воды, подщелачивают до pH 9 добавлением NaOH, экстрагируют 2 порциями по 30 мл хлороформа, сушат (K2CO3) и упаривают до сухого остатка. Сырой продукт хроматографируют на колонке с силикагелем. Выход: 0,64 г (34%) соединения 7, Rf (Б): 0,30; 1H-ЯМР (ДМСО, част./млн): 10,23 (1H, s, 9-NOH), исчезает при смешении с D2O, 9,67 (1H, s, CHO), 4,95 (1H, d, 1”), 4,45 (1H, d, 1”’), 4,21 (1H, d, 1′), 3,49 (3H, s, 3”’OMe), 3,45 (3H, s, 2”’OMe), 2,47 (6H, s, NMe2), 1,25 (3H, s, 12-CH3); 13C-ЯМР (CDCl3, част. /млн): 203,11 (d, C-20), 173,18 (s, C-1), 161,65 (s, C-9), 104,15 (d, C-1′), 100,62 (d, C-1”’), 96,63 (d, C-1”’), 62,30 (s, C-12), 61,76 (d, C-13), 61,42 (q, 3”’OMe), 59,25 (q, 2”’OMe), 16,46 (q, C-22); и 0,35 г (23%) соединения 8, Rf (Б): 0,22; 1H-ЯМР (ДМСО, част./млн): 10,21 (1H, s, 9-NOH), исчезает при смешении с D2O, 9,68 (1H, s, CHO), 4,43 (1H, d, 1”’), 4,18 (1H, d, 1′), 3,46 (3H, s, 3”’OMe), 3,43 (3H, s, 2”’OMe), 2,45 (6H, s, NMe2), 1,22 (3H, s, 12-CHз); 13C-ЯМР (CDCl3, част. /млн): 202,98 (d, C-20), 172,97 (s, C-1), 161,63 (s, C-9), 103,98 (d, C-1′), 100,33 (d, C-1”’), 62,29 (s, C-12), 61,73 (d, C-13), 61,40 (q, 3”’OMe), 59,23 (q, 2”’OMe), 16,45 (q, C-22). Пример 8 Оксим 10,11-дигидро-12,13-эпоксидезмикозина (8) 1,3 г (1,5 ммоля) соединения 6 растворяют в смеси 13 мл ацетонитрила с 26 мл 1%-ной трифторуксусной кислоты в воде и перемешивают при комнатной температуре в течение 2 ч. Продукт выделяют аналогично описанному в примере 7. Выход: 1 г (81%) соединения, по спектральным характеристикам идентичного соединению 8 в примере 7. Пример 9 Оксим 20-диметилацеталя 12,13-эпоксидезмикозина (9) и 20-диметилацеталь 9-гидрокси-10,11-дигидро-12,13-эпокси-9,11- (эпоксиимино)дезмикозина (10) 2 г (2,4 ммоля) 12,13-эпоксидезмикозин-20-диметилацеталя растворяют в 16 мл пиридина, добавляют 1,0 г (14,4 ммоля) гидроксиламингидрохлорида и смесь перемешивают в токе азота при комнатной температуре в течение 4 ч. В реакционную смесь добавляют 160 мл воды, подщелачивают до pH 9 добавлением 10%-ного NaOH и экстрагируют 2 порциями по 80 мл хлороформа. Объединенные экстракты сушат и упаривают до сухого остатка. 1,76 г сырого продукта хроматографируют на колонке с силикагелем в системе растворителей A. Выход: 0,43 г (24%) соединения 9, Rf (A): 0,38; 1H-ЯМР (ДМСО, част./млн): 10,42 (1H, s, 9-NOH), исчезает при смешении с D2O, 6,58 (1H, d, 11), 6,43 (1H, d, 10), 4,46 (1H, d, 1”’), 4,23 (1H, d, 1′), 3,50 (3H, s, 3”’OMe), 3,45 (3H, s, 2”’OMe), 3,23 (3H, s, 20-OMe), 3,14 (3H, s, 20-OMe), 2,47 (6H, s, NMe2); 13C-ЯМР (CDCl3, част./млн): 172,82 (s, C-1), 158,86 (s, C-9), 136,33 (d, C-11), 115,86 (d, C-10), 104,15 (d, C-1′), 102,12 (d, C-20), 100,58 (d, C-1”’), 63,94 (d, C-13), 61,43 (q, 3”’OMe), 59,38 (s, C-12), 59,11 (q, 2”’OMe), 14,81 (s, C-22); и 0,83 г (47%) соединения 10, Rf (A): 0,32; 2H-ЯМР (ДМСО, част. /млн): 4,45 (1H, d, 1”’), 4,22 (1H, d, 1′), 3,49 (3H, s, 3”’OMe), 3,45 (3H, s, 2”’OMe), 3,23 (3H, s, 20-OMe), 3,14 (3H, s, 20-OMe), 2,46 (6H, s, NMe2); 13C-ЯМР (CDCl3, част./млн): 170,04 (s, C-1), 110,23 (s, C-9), 104,08 (d, C-1′), 102,51 (d, C-20), 100,24 (d, C-1”’), 63,37 (d, C-13), 61,44 (q, 3”’OMe), 60,67 (s, C-12), 59,13 (q, 2”’OMe), 54,34 (d, C-11), 15,24 (s, C-22). Формула изобретения
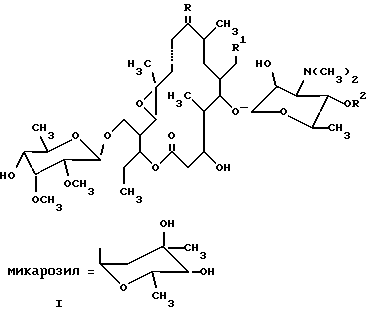 где R обозначает О, R1 обозначает СНО или СН(ОСН3)2, R2 обозначает Н или микарозил и —– обозначает одинарную связь; либо где R обозначает NОН, R1 обозначает СНО или СН(ОСН3)2, R2 обозначает Н или микарозил и —- обозначает одинарную или двойную связь; или соединение формулы II 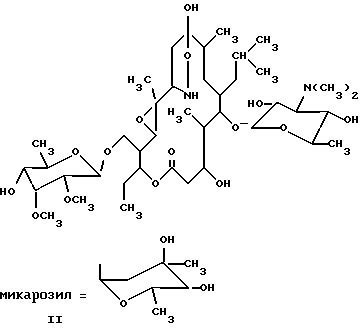 где R обозначает Н или микарозил. 2. Соединение формулы I по п.1, представляющее собой 20-диметилацеталь 10,11-дигидро-12,13-эпокситилозина. 3. Соединение формулы I по п.1, представляющее собой 10,11-дигидро-12,13-эпокситилозин. 4. Соединение формулы I по п.1, представляющее собой 20-диметилацеталь 4′-демикарозил-10,11-дигидро-12,13-эпокситилозина. 5. Соединение формулы I по п.1, представляющее собой 4′-демикарозил-10,11-дигидро-12,13-эпокситилозина. 6. Соединение формулы I по п.1, представляющее собой оксим 20-диметилацеталя 10,11-дигидро-12,13-эпокситилозина. 7. Соединение формулы I по п.1, представляющее собой оксим 20-диметилацеталя 4′-демикарозил-10,11-дигидро-12,13-эпокситилозина. 8. Соединение формулы I по п.1, представляющее собой оксим 10,11-дигидро-12,13-эпокситилозина. 9. Соединение формулы I по п.1, представляющее собой оксим 4′-демикарозил-10,11-дигидро-12,13-эпокситилозина. 10. Соединение формулы I по п.1, представляющее собой оксим 20-диметилацеталя 12,13-эпокситилозина. 11. Соединение формулы I по п.1, представляющее собой оксим 20-диметилацеталя 4′-демикарозил-12,13-эпокситилозина. 12. Соединение формулы I по п.1, представляющее собой оксим 12,13-эпокситилозина. 13. Соединение формулы I по п.1, представляющее собой оксим 4′-демикарозил-12,13-эпокситилозина. 14. Соединение формулы II по п.1, представляющее собой 20-диметилацеталь 9-гидрокси-10,11-дигидро-12,13-эпокси-9,11-(эпоксиимино)тилозина. 15. Соединение формулы II по п.1, представляющее собой 20-диметилацеталь 4′-демикарозил-9-гидрокси-10,11-дигидро-12,13-эпокси-9,11-(эпоксиимино)тилозина. 16. Способ получения производных 12,13-эпокситилозина формулы I 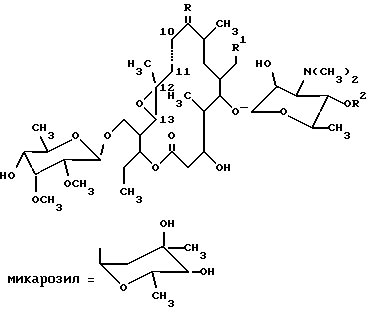 где R обозначает О; R1 обозначает СНО или СН(ОСН3)2; R2 обозначает Н или микарозил; линия —- обозначает одинарную связь, отличающийся тем, что соединение формулы III 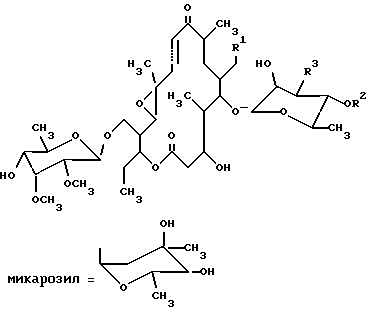 где R1 обозначает СНО или СН(ОСН3)2; R2 обозначает Н или микарозил; R3 обозначает N(СН3)2 или N-(ОСН3)2 при условии, что R2 обозначает Н, подвергают реакции гидрогенизации в органическом растворителе, предпочтительно в низшем C1-C3 алифатическом спирте, в присутствии 2 – 5%-ного палладия на угле, под давлением водорода 0,2 – 0,5 Мра при комнатной температуре в течение 5 – 8 ч. 17. Способ получения производных 12,13-эпокситилозина формулы I 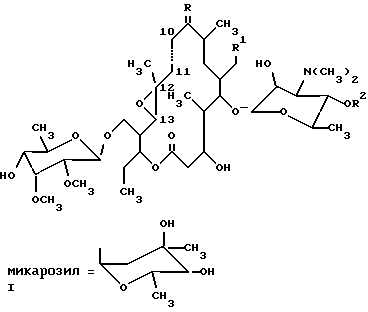 где R имеет значение NОН; R1 обозначает СНО или СН(ОСН3)2; R2 обозначает Н или микарозил; линия —- обозначает одинарную или двойную связь, и соединения формулы II 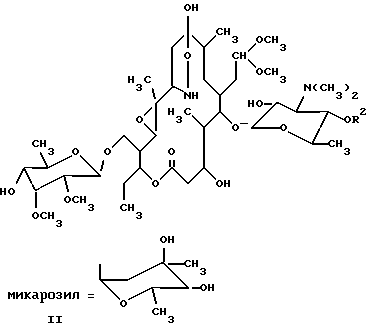 где R2 обозначает Н или микарозил, отличающийся тем, что соединение формулы I, где R обозначает О, R1 обозначает СН(ОСН3)2, R2 обозначает Н или микарозил, а линия —- обозначает одинарную связь, подвергают реакции оксимирования 3 – 6 эквивалентами гидрохлорида гидроксиламина в пиридине или низшем спирте в присутствии основания, такого, как пиридин или Nа2СО3, в токе азота при комнатной температуре или температуре кипения с обратным холодильником в течение 3 – 7 ч с последующим необязательным гидролизом ацетальной группы; или соединение формулы III, где R1 имеет значение СН(ОСН3)2, R2 имеет значение Н или микарозил, R3 имеет значение N(СН3)2, подвергают реакции оксимирования описанным методом, и полученные соединения формулы I, где R обозначает NОН, R1 обозначает СН(ОСН3)2, R2 обозначает Н или микарозил, линия —- обозначает двойную связь, и соединения формулы II, где R2 обозначает Н или микарозил, разделяют путем колоночной хроматографии на силикагеле с последующим необязательным гидролизом ацетальной группы. MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 14.08.2002
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||
