Патент на изобретение №2170231
|
||||||||||||||||||||||||||
(54) ИМИДАЗОЛИДИНЫ, ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛОМ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
(57) Реферат: Имидазолидины общей формулы I, в которой (Н) представляет собой насыщенный гетероциклический радикал, включающий 4-7 атомов и содержащий либо атом кислорода, азота или серы, причем атом азота может быть замещен низшим алкилом, а атом серы может быть окислен; либо два атома кислорода, причем указанный гетероцикл может быть замещен одним или несколькими низшими алкилами; Ar – фенил, возможно замещенный двумя радикалами, выбранными из CF3, CN, алкоксила или алкилтионила; Х – кислород или сера; Y – кислород или радикал NH; R3 – Н, алкил, возможно замещенный галогеном или гидроксилом, свободным или этерифицированным карбоксильным или цианорадикалом, а также их аддитивные соли, обладают антиандрогенной активностью. 3 c. и 6 з.п.ф-лы. 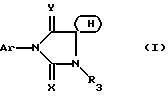
Настоящее изобретение относится к новым имидазолидинам, замещенным гетероциклом, к способу их получения и полученным промежуточным продуктам, к их применению в качестве медикаментов и содержащим их фармацевтическим композициям. В японской патентной заявке J 48087030 приводится описание 3- фенил 2-тио-гидантоинов, представленных как ингибиторы прорастания некоторых растений. Во французском патенте 2329276 приводится описание имидазолидинов, о которых говорится, что они обладают антиандрогенной активностью. Однако продукты, являющиеся предметом указанного патента, отличаются от продуктов настоящей патентной заявки. Таким образом, предметом настоящего изобретения являются соединения формулы (I): 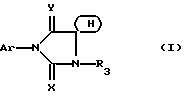 в которой: (Н) представляет собой насыщенный гетероциклический радикал, включающий от 4 до 7 атомов и содержащий: либо атом кислорода, азота или серы, с возможностью оксидирования, причем атом азота может быть замещен радикалом, выбранным среди значений R3, либо два атома кислорода и, возможно, один атом бора, замещенный фенильным радикалом, причем полученный таким образом гетероцикл может быть замещен на уровне атома углерода оксо- радикалом, одним или несколькими алкильными радикалами, которые также могут быть замещены, или циклоалкильным радикалом, включающим от 4 до 7 атомов; Ar представляет собой арильный радикал, который может быть замещен одним или несколькими радикалами, выбранными среди: 1. галогенных атомов и радикалов: циано-, нитро-, трифторметильного, трифторметоксильного, гидроксильного, карбоксильного свободного, превращенного в соль, в сложный эфир или аминированного; 2 радикала 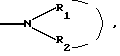 в котором атом азота может быть оксидирован, a R1 и R2: в котором атом азота может быть оксидирован, a R1 и R2:либо, одинаковые или различные, могут быть выбраны среди атома водорода и алкильных радикалов, с возможностью замещения, либо образуют вместе с атомом азота, с которым они связаны, моноциклический радикал, включающий 5, 6 или 7 атомов, или радикал, состоящий из конденсированных циклов, включающих от 8 до 14 атомов, причем указанные радикалы, одинаковые или различные, могут включать один или несколько других гетероатомов, выбранных среди атомов кислорода, азота и серы, и могут быть замещены; 3. алкильного, алкоксильного, алкилтионильного и арилтионильного радикалов, с возможностью замещения; 4. алкильного 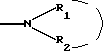 и алкоксильного и алкоксильного 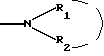 радикалов, радикалов, 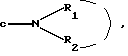 как указано выше.
X представляет собой атом кислорода или серы; как указано выше.
X представляет собой атом кислорода или серы;Y представляет собой атом кислорода или серы или радикал NH; R3 выбран среди атома водорода, арильных радикалов, алкильного, алкенильного и алкинильного радикалов с возможностью прерывания одним или несколькими атомами кислорода, азота или серы, которые могут быть оксидированы, причем все указанные радикалы могут быть замещены, при этом заместитель или заместители цикла, который может составлять радикал 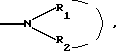 и алкильного, арильного, алкоксильного, алкенильного и алкинильного радикалов, о которых указано выше, что они могут быть замещены, выбраны среди галогенных атомов и радикалов, таких как гидроксильный, который может быть превращен в соль, в сложный эфир или в простой эфир, алкоксильный, арилоксильный, алкильный, галоалкоксильный, галоалкильный, меркаптильный, алкилтионильный и арилтионильный, в которых атом серы может быть оксидирован, ацильный, ацилоксильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, циано-, нитро-, амино-, моно- или диалкиламино-, арильный и арилалкильный, причем два последних радикала могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов, гидроксильного, алкильного, алкоксильного, трифторметильного, трифторметоксильного, нитро-, циано-, карбоксильного свободного, превращенного в соль или в сложный эфир, и тетразолильного, причем все атомы серы могут быть оксидированы с получением сульфоксида или сульфона.
При этом вышеуказанные продукты формулы (I) могут находиться в любой изомерной, рацемической, энантиомерной и диастереоизомерной форме, а также в виде аддитивных солей с минеральными и органическими кислотами или с минеральными и органическими основаниями вышеуказанных продуктов формулы (I).
Для определения вышеуказанных заместителей, а также в нижеследующем, используемые определения могут иметь следующие значения: и алкильного, арильного, алкоксильного, алкенильного и алкинильного радикалов, о которых указано выше, что они могут быть замещены, выбраны среди галогенных атомов и радикалов, таких как гидроксильный, который может быть превращен в соль, в сложный эфир или в простой эфир, алкоксильный, арилоксильный, алкильный, галоалкоксильный, галоалкильный, меркаптильный, алкилтионильный и арилтионильный, в которых атом серы может быть оксидирован, ацильный, ацилоксильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, циано-, нитро-, амино-, моно- или диалкиламино-, арильный и арилалкильный, причем два последних радикала могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов, гидроксильного, алкильного, алкоксильного, трифторметильного, трифторметоксильного, нитро-, циано-, карбоксильного свободного, превращенного в соль или в сложный эфир, и тетразолильного, причем все атомы серы могут быть оксидированы с получением сульфоксида или сульфона.
При этом вышеуказанные продукты формулы (I) могут находиться в любой изомерной, рацемической, энантиомерной и диастереоизомерной форме, а также в виде аддитивных солей с минеральными и органическими кислотами или с минеральными и органическими основаниями вышеуказанных продуктов формулы (I).
Для определения вышеуказанных заместителей, а также в нижеследующем, используемые определения могут иметь следующие значения:Гетероциклический радикал, который обозначает (Н), может быть выбран среди радикалов насыщенных гетероциклов, как указано выше, хорошо известных специалистам. В качестве примера, причем этот перечень не является исчерпывающим, можно назвать: с одной стороны, радикалы, включающие атом кислорода, азота или серы, такие, в частности, как радикалы: 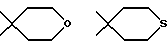 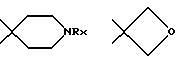 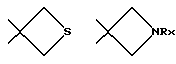 в которых Rx выбран среди значений R3, как указано выше, в частности среди атома водорода и алкильных радикалов, с возможностью прерывания одним или несколькими атомами кислорода, азота или серы, с возможностью оксидирования, причем алкильные радикалы могут быть замещены, как указано выше и в дальнейшем; с другой стороны, радикалы, включающие два атома кислорода и, возможно, один атом бора, такие, в частности, как радикалы: 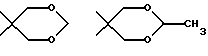 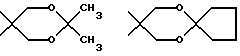 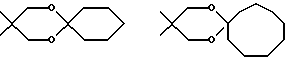 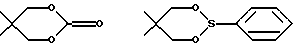 Гетероциклический радикал (Н) предпочтительно включает 6 атомов. Термин алкильный радикал означает линейный или разветвленный алкильный радикал, включающий не более 12 атомов углерода, такой, например, как метильный, этильный, пропильный, изопропильный, бутильный, изобутильный втор-бутильный, трет-бутильный, пентильный, изопентильный, втор-пентильный, трет-пентильный, неопентильный, гексильный, изогексильный, втор-гексильный, трет- гексильный, гептильный, октильный, децильный, ундецильный, додецильный радикал. Предпочтение отдается алкильным радикалам, содержащим не более 4 атомов углерода, и, в частности, метильному, этильному, пропильному, изопропильному радикалам. Термин алкенильный радикал означает линейный или разветвленный алкенильный радикал, включающий не более 12 атомов углерода, такой, например, как винильный, аллильный, 1-пропенильный, бутенильный, пентенильный, гексенильный радикал. Среди алкенильных радикалов предпочтение отдается тем, которые включают 4 атома углерода, таким как аллильный, пропенильный или бутенильный радикалы. Термин алкинильный радикал означает линейный или разветвленный алкинильный радикал, включающий не более 12 атомов углерода, такой, например, как этинильный, пропаргильный, бутинильный, пентинильный или гексинильный радикал. Среди алкинильных радикалов предпочтение отдается тем, которые включают 4 атома углерода, таким как пропаргильный радикал. Термин алкоксильный радикал означает линейный или разветвленный радикал, включающий не более 12 и предпочтительно 4 атома углерода, такой как, в первую очередь, метоксильный, этоксильный, пропоксильный или изопропоксильный, а также линейный, вторичный или третичный бутоксильный радикал. Термин циклоалкильный радикал означает, главным образом, циклопропильный; циклобутильный радикалы, и, в первую очередь, циклопентильный, циклогексильный и циклогептильный радикалы. Под арильным радикалом понимают арильные карбоциклические радикалы, такие как фенильный или нафтильный, или арильные гетероциклические моноциклические радикалы с 5 или 6 атомами или состоящие из конденсированных циклов, включающих один или несколько гетероатомов, выбранных, в первую очередь, среди кислорода, серы и азота. Среди арильных гетероциклических радикалов, включающих 5 атомов, можно назвать такие радикалы, как фурильный, тиенильный, пирролильный, тиазолильный, оксазолильный, имидазолильный, тиадиазолильный, пиразолильный, изоксазолильный, тетразолильный. Среди арильных гетероциклических радикалов, включающих 6 атомов, можно назвать такие радикалы, как пиридильный, пиримидинильный, пиридазинильный, пиразинильный. Среди конденсированных арильных радикалов можно назвать такие радикалы, как индолильный, бензофурильный, бензотиенильный, хинолинильный. Предпочтение отдается фенильному, тетразолильному и пиридильному радикалам. Под арилалкильным радикалом понимают радикалы, полученные в результате комбинирования вышеуказанных алкильных и арильных радикалов. Предпочтение отдается бензильному, фенилэтильному, пиридилметильному, пиридилэтильному или тетразолилметильному радикалу. Под галогенным атомом понимают, разумеется, атомы фтора, хлора, брома или йода. Предпочтение отдается атомам фтора, хлора или брома. В качестве частных примеров алкильных радикалов, замещенных одним или несколькими галогенами или галоалкилами, можно назвать такие радикалы, как монофтор-, хлор-, бром- или йодметильный или – этильный, дифтор-, дихлор- или дибромметильный, трифторметильный. В качестве частных примеров алкоксильных радикалов, замещенных одним или несколькими галогенами или галоалкоксилами, можно назвать такие радикалы, как бромэтоксильный, трифторметоксильный, трифторэтоксильный или же пентафторэтоксильный. В качестве частных примеров замещенных арильных или аралкильных радикалов, причем этот перечень не является исчерпывающим, можно назвать те, в которых фенильный радикал замещен в орто-, мета- и пара-положении одним или несколькими радикалами, выбранными среди атома фтора и алкилтионильного, гидроксильного, гидроксиалкильного, алкоксильного, трифторметильного, трифторэтильного, пентафторэтильного и цианильного радикалов. Под ацильным радикалом понимают, в первую очередь, радикал, включающий не более 7 атомов углерода, такой как формильный, ацетильный, пропионильный, бутирильный или бензоильный радикал, однако он может также представлять собой валерильный, гексаноильный, акрилоильный, кротоноильный или карбамоильный радикал. Под ацилоксильным радикалом понимают радикалы, в которых ацильные радикалы имеют вышеуказанное значение, и, например, формилоксильный, ацетоксильный, пропионилоксильный, бутирилоксильный или бензоилоксильный радикалы. Термин арилоксильный радикал означает, в первую очередь, радикалы, в которых арильный радикал соответствует определенному выше, как, например, в фенокси. Термин арилалкоксильный радикал означает, в первую очередь, радикалы, в которых арильный радикал и алкоксильный радикалы означают радикалы, соответствующие определенным выше, как, например, в бензилокси, фенилэтокси или фенилизопропокси. Термин арилтионильный радикал означает, в первую очередь, радикалы, в которых арильный радикал означает радикалы, как указано выше, как, например, в фенилтио, пиридилтио или пиримидилтио, имидазолилтио или N-метилимидазолилтио. Термин алкилтионильный радикал означает, в первую очередь, радикалы, в которых алкильный радикал такой, как указано выше, как, например, в метилтио, этилтио, пропилтио, изопропилтио, бутилтио, втор-бутилтио, трет-бутилтио, изопентилтио или изогексилтио; алкилтионильный радикал может быть замещен, как, например, в гидроксиметилтио, аминоэтилтио, галоалкилтио, как, в первую очередь, бромэтилтио, трифторметилтио, трифторэтилтио или же пентафторэтилтио, арилалкилтио, как, например, бензилтио или фенетилтио. Атомы серы могут быть не оксидированы, как в алкилтионильных, арилтионильных радикалах, или же, наоборот, они могут быть оксидированы, что приводит к получению алкилсульфинильного, арилсульфинильного, алкилсульфонильного или арилсульфонильного радикалов: алкилсульфинил и алкилсульфонил означают радикалы, в которых алкильный радикал выбран, например, среди значений, указанных выше для алкильного радикала, как, например, метилсульфинильный, этилсульфинильный, метилсульфонильный или этилсульфонильный радикалы; арилсульфинил и арилсульфонил означают арилтионильные радикалы, в которых арильный радикал выбран, например, среди значений, указанных выше для арильного радикала, как, например, фенилсульфинильный или -сульфонильный, пиридилсульфинильный или -сульфонильный, пиримидилсульфинильный или -сульфонильный, имидазолилсульфинильный или -сульфонильный или N- метилимидазолилсульфинильный или -сульфонильный радикалы. Карбоксильный радикал (карбоксильные радикалы) продуктов формулы (I) могут быть превращены в соль, аминированы или превращены в сложный эфир с помощью различных групп, хорошо известных специалистам. Под карбокси, превращенным в сложный эфир, понимают, например, алкилоксикарбонильные радикалы, такие как, например, метоксикарбонильный, этоксикарбонильный, пропоксикарбонильный, н-бутил-, трет-бутилоксикарбонильный, или же бензилоксикарбонильный радикал, причем указанные алкильные радикалы могут быть замещены одним или несколькими радикалами, выбранными, например, среди галогенных атомов и радикалов, таких как гидроксильный, алкоксильный, ацильный, ацилоксильный, алкилтионильный, аминный или арильный, как, например, в хлорметильной, гидроксипропильной, пропионилоксиметильной, метилтиометильной, диметиламиноэтильной, бензильной или фенетильной группах. Можно назвать радикалы, образованные с помощью легкорасщепляемых сложноэфирных остатков, таких как метоксиметильные и этоксиметильные радикалы; ацилоксиалкильные радикалы, такие как пивалоилоксиметильный, пивалоилоксиэтильный, ацетоксиметильный или ацетоксиэтильный; алкилоксикарбонилоксиалкильные радикалы, такие как метоксикарбонилоксиметильный или -этильный, изопропилоксикарбонилоксиметильный или -этильный радикалы. Перечень подобных сложноэфирных радикалов можно найти, например, в патенте ЕР 0034536. Под аминированным карбокси понимают группы типа – 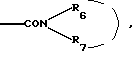 в которых радикалы R6 и R7, одинаковые или различные, представляют собой атом водорода или алкильный радикал, включающий от 1 до 4 атомов углерода, как, например, метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, втор-бутильный или трет-бутильный радикалы.
В группах в которых радикалы R6 и R7, одинаковые или различные, представляют собой атом водорода или алкильный радикал, включающий от 1 до 4 атомов углерода, как, например, метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, втор-бутильный или трет-бутильный радикалы.
В группах 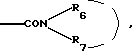 определенных выше, предпочтение отдается тем, в которых радикал определенных выше, предпочтение отдается тем, в которых радикал 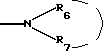 представляет собой аминный, моно- или диметиламинный, моно- или диэтиламинный, метилэтиламинный, монопропиламинный или монобутиламинный.
Радикал представляет собой аминный, моно- или диметиламинный, моно- или диэтиламинный, метилэтиламинный, монопропиламинный или монобутиламинный.
Радикал 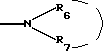 может также представлять собой гетероцикл, который может содержать или не содержать дополнительный гетероатом. Можно назвать такие радикалы, как пирролильный, имидазолильный, индолильный, пиперидинный, морфолинный, пиперазинильный. Предпочтение отдается таким радикалам, как пиперидинный, морфолинный или пиперазинильный, с возможностью замещения, или второму атому азота, как, например, в метилпиперазиниле, фторметилпиперазиниле, этилпиперазиниле, пропилпиперазиниле, фенилпиперазиниле или бензилпиперазиниле; в двух последних радикалах фенильный и бензильный радикалы могут быть замещены, как, например, в хлорфениле или трифторфениле.
Под карбокси, превращенным в соль, понимают соли, образованные с помощью эквивалента натрия, калия, лития, кальция, магния или аммония. Можно также назвать соли, образованные с помощью органических оснований, таких как метиламин, пропиламин, триметиламин, диэтиламин, триэтиламин, N,N-диметилэтаноламин, три (гидроксиметил) аминометан, этаноламин, пиридин, пиколин, дициклогексиламин, морфолин, бензиламин, прокаин, лизин, аргинин, гистидин, N-метилглюкамин.
Предпочтение отдается натриевой соли.
Под гетероциклическим радикалом, включающим один или несколько гетероатомов, понимают, например, моноциклические, гетероциклические насыщенные радикалы, такие как оксиранильный, оксоланильный, диоксоланильный, пирролидинильный, имидазолидинильный, пиразолидинильный, пиперидильный, пиперазинильный или морфолинильный.
Под радикалами: алкильным, алкенильным или алкинильным, с возможностью прерывания гетероатомом, выбранным среди атомов серы, кислорода или азота, понимают радикалы, включающие один или несколько из указанных атомов, одинаковых или различных по структуре, причем очевидно, что указанные гетероатомы не могут располагаться с краю радикала. Назвать можно, например, алкоксиалкильные радикалы, такие как метоксиметильный, метоксиэтильный или пропилоксипропильный, алкоксиалкоксиалкильные радикалы, такие как метоксиэтоксиметильный, или же алкилтиоалкильные радикалы, такие как, например, пропилтиопропильный, пропилтиоэтильный, метилтиометильный.
Под гидроксильным радикалом, превращенным в сложный эфир, в простой эфир или защищенным, понимают соответственно радикалы может также представлять собой гетероцикл, который может содержать или не содержать дополнительный гетероатом. Можно назвать такие радикалы, как пирролильный, имидазолильный, индолильный, пиперидинный, морфолинный, пиперазинильный. Предпочтение отдается таким радикалам, как пиперидинный, морфолинный или пиперазинильный, с возможностью замещения, или второму атому азота, как, например, в метилпиперазиниле, фторметилпиперазиниле, этилпиперазиниле, пропилпиперазиниле, фенилпиперазиниле или бензилпиперазиниле; в двух последних радикалах фенильный и бензильный радикалы могут быть замещены, как, например, в хлорфениле или трифторфениле.
Под карбокси, превращенным в соль, понимают соли, образованные с помощью эквивалента натрия, калия, лития, кальция, магния или аммония. Можно также назвать соли, образованные с помощью органических оснований, таких как метиламин, пропиламин, триметиламин, диэтиламин, триэтиламин, N,N-диметилэтаноламин, три (гидроксиметил) аминометан, этаноламин, пиридин, пиколин, дициклогексиламин, морфолин, бензиламин, прокаин, лизин, аргинин, гистидин, N-метилглюкамин.
Предпочтение отдается натриевой соли.
Под гетероциклическим радикалом, включающим один или несколько гетероатомов, понимают, например, моноциклические, гетероциклические насыщенные радикалы, такие как оксиранильный, оксоланильный, диоксоланильный, пирролидинильный, имидазолидинильный, пиразолидинильный, пиперидильный, пиперазинильный или морфолинильный.
Под радикалами: алкильным, алкенильным или алкинильным, с возможностью прерывания гетероатомом, выбранным среди атомов серы, кислорода или азота, понимают радикалы, включающие один или несколько из указанных атомов, одинаковых или различных по структуре, причем очевидно, что указанные гетероатомы не могут располагаться с краю радикала. Назвать можно, например, алкоксиалкильные радикалы, такие как метоксиметильный, метоксиэтильный или пропилоксипропильный, алкоксиалкоксиалкильные радикалы, такие как метоксиэтоксиметильный, или же алкилтиоалкильные радикалы, такие как, например, пропилтиопропильный, пропилтиоэтильный, метилтиометильный.
Под гидроксильным радикалом, превращенным в сложный эфир, в простой эфир или защищенным, понимают соответственно радикалы 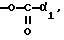  или -O-P, образованные на основе гидроксильного радикала, с использованием методов, хорошо известных специалистам, и в которых P представляет собой защитную группу, a или -O-P, образованные на основе гидроксильного радикала, с использованием методов, хорошо известных специалистам, и в которых P представляет собой защитную группу, a  1, 1,  2 и 2 и  3 представляют собой алкильный, алкенильный, алкинильный, арильный или арилалкильный радикал, включающий не более 12 атомов углерода, с возможностью замещения, как определено выше, в частности, для R3.
Примеры защитной группы P, а также образование защищенного гидроксильного радикала приводятся, в частности, в широко используемой специалистами книге Теодора У. Грина “Защитные группы в органическом синтезе”, изданной в 1981 г. Гарвардским университетом (Wiley-Interscience Publishers, John Wiley & Sons).
Защитная группа гидроксильного радикала, которую может представлять P, может быть выбрана в нижеприведенном перечне: например, формил, ацетил, хлорацетил, бромацетил, дихлорацетил, трихлорацетил, трифторацетил, метоксиацетил, феноксиацетил, бензоил, бензоилформил, n-нитробензоил. Можно также назвать такие группы, как этоксикарбонильная, метоксикарбонильная, пропоксикарбонильная, 3 представляют собой алкильный, алкенильный, алкинильный, арильный или арилалкильный радикал, включающий не более 12 атомов углерода, с возможностью замещения, как определено выше, в частности, для R3.
Примеры защитной группы P, а также образование защищенного гидроксильного радикала приводятся, в частности, в широко используемой специалистами книге Теодора У. Грина “Защитные группы в органическом синтезе”, изданной в 1981 г. Гарвардским университетом (Wiley-Interscience Publishers, John Wiley & Sons).
Защитная группа гидроксильного радикала, которую может представлять P, может быть выбрана в нижеприведенном перечне: например, формил, ацетил, хлорацетил, бромацетил, дихлорацетил, трихлорацетил, трифторацетил, метоксиацетил, феноксиацетил, бензоил, бензоилформил, n-нитробензоил. Можно также назвать такие группы, как этоксикарбонильная, метоксикарбонильная, пропоксикарбонильная,    -трихлорэтоксикарбонильная, бензилоксикарбонильная, трет- бутоксикарбонильная, 1-циклопропилэтоксикарбонильная, тетрагидропиранильная, тетрагидротиопиранильная, метокситетрагидропиранильная, тритильная, бензильная, 4-метоксибензильная, бензоилгидрильная, трихлорэтильная, 1-метил 1-метоксиэтильная, фталоильная, пропионильная, бутирильная, изобутирильная, валерильная, изовалерильная, оксалильная, сукциноильная и пивалоильная, фенилацетильная, фенилпропионильная, мезильная, хлорбензоильная, паранитробензоильная, пара-трет-бутилбензоильная, каприлоильная, акрилоильная, метилкарбамоильная, фенилкарбамоильная, нафтилкарбамоильная.
P может также представлять радикал -трихлорэтоксикарбонильная, бензилоксикарбонильная, трет- бутоксикарбонильная, 1-циклопропилэтоксикарбонильная, тетрагидропиранильная, тетрагидротиопиранильная, метокситетрагидропиранильная, тритильная, бензильная, 4-метоксибензильная, бензоилгидрильная, трихлорэтильная, 1-метил 1-метоксиэтильная, фталоильная, пропионильная, бутирильная, изобутирильная, валерильная, изовалерильная, оксалильная, сукциноильная и пивалоильная, фенилацетильная, фенилпропионильная, мезильная, хлорбензоильная, паранитробензоильная, пара-трет-бутилбензоильная, каприлоильная, акрилоильная, метилкарбамоильная, фенилкарбамоильная, нафтилкарбамоильная.
P может также представлять радикал 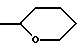 или же производное кремния, такое как триметилсилил.
Радикал или же производное кремния, такое как триметилсилил.
Радикал 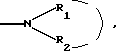 который представляет аминный, моноалкиламинный, диалкиламинный радикал или же гетероцикл, может быть выбран среди значений, определенных выше для который представляет аминный, моноалкиламинный, диалкиламинный радикал или же гетероцикл, может быть выбран среди значений, определенных выше для 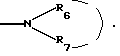 Радикалы -алкил 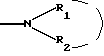 и -алкокси и -алкокси 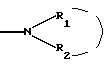 такие, как в указанных радикалах алкил, алкокси и такие, как в указанных радикалах алкил, алкокси и 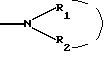 имеют значения, указанные выше, как, например, в N,N-диметиламинометильном или N,N-диметиламиноэтоксильном радикалах.
Аминный радикал и, в частности, имеют значения, указанные выше, как, например, в N,N-диметиламинометильном или N,N-диметиламиноэтоксильном радикалах.
Аминный радикал и, в частности, 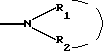 обозначает также аминный радикал, замещенный одним или двумя алкильными радикалами, выбранными среди алкильных радикалов, как определено выше, которые также замещены, как указано выше, в частности, одним или несколькими радикалами, выбранными среди галогенных атомов и таких радикалов, как гидроксильный, алкоксильный, цианильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, как, например, в гидроксиалкильном, цианоалкильном и карбоксиалкильном радикалах.
Когда продукты формулы (I), как указано выше, содержат аминный радикал, превращаемый в соль с помощью кислоты, само собой разумеется, что соли кислот также являются частью изобретения.
Аддитивными солями с минеральными или органическими кислотами продуктов формулы (I) могут быть, например, соли, полученные с помощью кислот, таких как хлористо-водородная, азотная, серная, фосфорная, пропионовая, уксусная, муравьиная, бензойная, малеиновая, фумаровая, янтарная, винная, лимонная, щавелевая, глиоксиловая, аспарагиновая, аскорбиновая, бромистый водород, йодистый водород, такие алкилмоносульфокислоты, как, например, метансульфокислота, этансульфокислота, пропансульфокислота, такие алкилдисульфокислоты, как, например, метандисульфокислота, обозначает также аминный радикал, замещенный одним или двумя алкильными радикалами, выбранными среди алкильных радикалов, как определено выше, которые также замещены, как указано выше, в частности, одним или несколькими радикалами, выбранными среди галогенных атомов и таких радикалов, как гидроксильный, алкоксильный, цианильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, как, например, в гидроксиалкильном, цианоалкильном и карбоксиалкильном радикалах.
Когда продукты формулы (I), как указано выше, содержат аминный радикал, превращаемый в соль с помощью кислоты, само собой разумеется, что соли кислот также являются частью изобретения.
Аддитивными солями с минеральными или органическими кислотами продуктов формулы (I) могут быть, например, соли, полученные с помощью кислот, таких как хлористо-водородная, азотная, серная, фосфорная, пропионовая, уксусная, муравьиная, бензойная, малеиновая, фумаровая, янтарная, винная, лимонная, щавелевая, глиоксиловая, аспарагиновая, аскорбиновая, бромистый водород, йодистый водород, такие алкилмоносульфокислоты, как, например, метансульфокислота, этансульфокислота, пропансульфокислота, такие алкилдисульфокислоты, как, например, метандисульфокислота,  – этандисульфокислота, – этандисульфокислота,  – этандисульфокислота, такие арилмоносульфокислоты, как бензолсульфокислота, и арилдисульфокислоты.
В первую очередь можно назвать соли, полученные, например, с помощью хлористо-водородной кислоты или метансульфокислоты.
Предметом настоящего изобретения являются, в частности, продукты формулы (I), как указано выше, в которой (Н) представляет собой: – этандисульфокислота, такие арилмоносульфокислоты, как бензолсульфокислота, и арилдисульфокислоты.
В первую очередь можно назвать соли, полученные, например, с помощью хлористо-водородной кислоты или метансульфокислоты.
Предметом настоящего изобретения являются, в частности, продукты формулы (I), как указано выше, в которой (Н) представляет собой:либо радикал 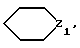 в котором: в котором:Z1 представляет собой атом кислорода, серы, с возможностью оксидирования с получением сульфоксида или сульфона, или радикал – N-R4, в котором R4 выбран среди атома водорода и алкильного, алкилфенильного и фенильного радикалов, с возможностью замещения одним или несколькими радикалами, выбранными среди галогенных атомов и радикалов, таких как гидроксильный, алкоксильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, и фенильный, который сам может быть замещен одним или несколькими радикалами, выбранными среди галогенных атомов, радикалов, таких как гидроксильный, алкильный, алкоксильный, трифторметильный, трифторметоксильный, нитрильный, цианильный и карбоксильный свободный, превращенный в соль или в сложный эфир; либо радикалу 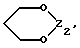 в котором: в котором:Z2 представляет собой либо радикал -CH2-, с возможностью замещения одним или двумя алкильными радикалами, циклоалкильным радикалом или оксо-радикалом, включающим от 4 до 7 атомов, либо атом бора, замещенный фенильным радикалом; Ar представляет собой арильный радикал, который может быть замещен одним или несколькими радикалами, выбранными среди галогенных атомов и таких радикалов, как циано-, нитро-, трифторметильный, трифторметоксильный, гидроксильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, алкильный, алкоксильный, алкилтионильный, арилтионильный, аминный, моно- или диалкиламинный, аминоалкильный, моно- или диалкиламиноалкильный, аминоалкоксильный, моно- или диалкиламиноалкоксильный, пирролидинильный, пиперидильный, морфолинный и пиперазинильный, с возможностью замещения на уровне второго атома азота алкильным, фенилалкильным, алкилфенильным или фенильным радикалом, которые могут быть сами замещены одним или несколькими радикалами, выбранными среди галогенных атомов и гидроксильного и алкоксильного радикалов; X представляет собой атом кислорода или серы; Y представляет собой атом кислорода или серы или радикал NH; R3 выбран среди атома водорода, арильного радикала и алкильного, алкенильного и алкинильного радикалов, с возможностью прерывания одним или несколькими атомами кислорода, азота или серы с возможностью оксидирования, причем все указанные радикалы могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов и радикалов, таких как гидроксильный, который может быть превращен в соль, в сложный эфир или в простой эфир, алкоксильный, арилоксильный, алкильный, трифторметильный, трифторметоксильный, карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный, цианильный, нитрильный, аминный, моно- или диалкиламинный, фенильный, бензильный и фенетильный, которые сами могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов и радикалов, таких как гидроксильный, алкильный, алкоксильный, цианильный, нитрильный и трифторметильный, причем указанные продукты формулы (I) могут находиться в любой изомерной рацемической, энантиомерной и диастереоизомерной форме, а также аддитивные соли с минеральными и органическими кислотами или с минеральными и органическими основаниями вышеуказанных продуктов формулы (I). Среди указанных продуктов предметом настоящего изобретения являются, в первую очередь, продукты формулы (I), как указано выше, в которой Ar представляет собой фенильный или пиридильный радикал, который может быть замещен, как указано выше, а (Н), R3, X и Y имеют приведенные выше значения, причем указанные продукты формулы (I) могут находиться в любой изомерной рацемической, энантиомерной и диастереоизомерной форме, а также аддитивные соли с минеральными и органическими кислотами или с минеральными и органическими основаниями вышеуказанных продуктов формулы (I). Среди указанных продуктов предметом настоящего изобретения являются, в первую очередь, продукты формулы (I), как определено выше, отвечающие формуле (F): 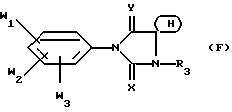 в которой (Н) представляет собой: либо радикал 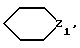 в котором: в котором:Z1 представляет собой атом кислорода, серы, с возможностью оксидирования с получением сульфоксида или сульфона, или радикал -N-R4, в котором R4 выбран среди атома водорода и алкильных радикалов, с возможностью замещения одним или несколькими радикалами, выбранными среди галогенных атомов и радикалов, таких как гидроксильный, алкоксильный и карбоксильный свободный, превращенный в соль, в сложный эфир или аминированный; либо радикал 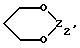 в котором: в котором:Z2 представляет собой либо радикал -CH2-, с возможностью замещения одним или двумя алкильными радикалами, циклоалкильным радикалом или оксо-радикалом, включающим от 4 до 7 атомов, либо атом бора, замещенный фенильным радикалом; W1, W2 и W3, одинаковые или различные, выбраны среди атома водорода, галогенных атомов и радикалов, таких как гидроксильный, алкоксильный, цианильный, аминный, моно- или диалкиламинный, нитрильный, трифторметильный, карбоксильный свободный, превращенный в сложный эфир, аминированный или превращенный в соль, алкилтионильный и арилтионильный; R3 выбран среди атома водорода и радикалов, каких как алкильный, который может быть замещен одним или несколькими заместителями, выбранными среди галогенных атомов и гидроксильных радикалов, с возможностью превращения в соль или в простой эфир, алкоксильный и карбоксильный свободный, превращенный в сложный эфир, аминированный или превращенный в соль. X представляет собой атом кислорода или серы; Y представляет собой атом кислорода или радикал NH; причем указанные продукты формулы (F) могут находиться в любой изомерной, рацемической, энантиомерной и диастереоизомерной форме, а также аддитивные соли с минеральными и органическими кислотами или с минеральными и органическими основаниями вышеуказанных продуктов формулы (F). Среди предпочтительных продуктов настоящего изобретения можно конкретнее назвать продукты формулы (I), такие, как указано выше, имеющие следующие наименования: – 4-(2,4-диоксо 1-(4-гидроксибутил) 8-окса 1,3-диазаспиро (4.5) декан 3-ил) 2-(трифторметил)бензонитрил, – 4-(2,4-диоксо 1-(2-фторэтил) 8-окса 1,3-диазаспиро (4.5) декан 3-ил) 2-(трифторметил)бензонитрил, – 3-(4-циано 3-(трифторметил)фенил) 2,4-диоксо 8-окса 1,3- диазаспиро (4.5) декан 1-ацетонитрил, – 4-(2,4-диоксо 1-(4-гидроксибутил) 8-тиа 1,3-диазаспиро (4.5) декан 3-ил) 2-(трифторметил)бензонитрил. Предметом настоящего изобретения также является способ получения продуктов формулы (I), как определено выше, отличающийся тем, что в присутствии третичного основания продукт формулы (II): Ar – N = C = X в которой X имеет вышеуказанное значение, Ar также имеет приведенное выше значение, в которой возможные функциональные группы могут быть защищены, вводится в реакцию: либо с продуктом формулы (III):  в которой (H) имеет вышеуказанное значение, а R’3 имеет значение, приведенное выше для R3, в которой возможные функциональные группы могут быть защищены для получения продукта формулы (Ia): 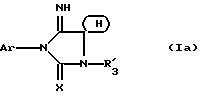 в которой Ar, (H) и R’3 имеют вышеуказанные значения; либо с продуктом формулы (X): 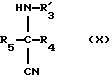 в которой R’3 имеет вышеуказанное значение, a R4 и R5, одинаковые или различные, представляют собой гидроксиалкильный радикал, в котором гидроксильная функциональная группа может быть защищена, для получения, в случае возможного устранения защиты гидроксильных радикалов, диола формулы (IV): 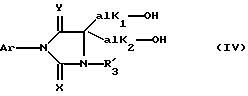 в которой Ar, X и R’3 имеют вышеуказанные значения, Y также имеет значение, приведенное выше, a alK1 и alK2, одинаковые или различные, представляют собой алкильный радикал, продукт формулы (IV), который вводят в реакцию: либо с соединением формулы (V): 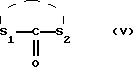 в которой S1 и S2, одинаковые или различные, представляют собой атом водорода или алкильный радикал, с возможностью замещения, или же S1 и S2 образуют вместе с C=O циклоалканонный радикал, включающий от 4 до 7 атомов, для получения продукта формулы (Ib): 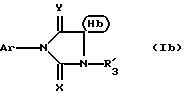 в которой (Hb) представляет собой насыщенный гетероцикл, содержащий от 4 до 7 атомов, включающий два атома кислорода и который может быть замещен циклоалкильным радикалом или одним или двумя алкильными радикалами, которые сами могут быть замещены; либо с фосгеном, или производным фосгена, или N,N’- карбонилдиимидазолом, для получения продукта формулы (Ic): 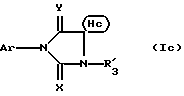 в которой Ar, Y, X и R’3 имеют вышеуказанные значения, а (Hc) представляет собой насыщенный гетероцикл, содержащий от 4 до 7 атомов, включающий два атома кислорода и замещенный на уровне атома углерода оксо-радикалом; либо с соединением формулы (VI): R-B (ОН)2 в которой R представляет собой фенильный радикал, для получения продукта формулы (Id): 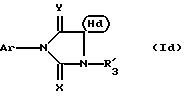 в которой Ar, Y, X и R’3 имеют вышеуказанные значения, a (Hd) представляет собой насыщенный гетероцикл, содержащий от 4 до 7 атомов, включающий два атома кислорода и один атом бора, замещенный фенильным радикалом; продукт формулы (IV), в котором, при желании и при необходимости, можно защитить гидроксильные радикалы для получения продукта формулы (IV’); полученные таким образом продукты формул (Ia), (Ib), (Ic), (Id) и (IV’), как указано выше, которые при желании и при необходимости можно подвергнуть любой или нескольким из нижеуказанных реакций в произвольной последовательности: а) реакции выделения возможных защитных групп, которые могут быть включены в R’3, с последующим воздействием, в случае необходимости, агентом этерификации, аминирования или солеобразования; б) реакции гидролиза группы >C=NH для получения карбонильной функциональной группы; в) реакции превращения группы >C=O в группу >C=S; г) реакции превращения группы (групп) >C=S в группу >C=O; д) когда R’3 представляет собой алкоксиалкильный радикал – реакции превращения R’3 в гидроксиалкильный радикал; е) когда R’3 представляет собой атом водорода – воздействию реактива формулы Hal-R”3, в которой R”3 имеет значения R’3, за исключением значения водорода, a Hal является галогенным атомом для получения продуктов формул (Ia), (Ib), (Ic), (Id) и (IV’), как указано выше, в которых R”3 имеет указанное ранее значение; ж) при желании – воздействию на продукты, полученные в п. е), агентом выделения возможных защитных групп, которые может включать R”3, или, при необходимости, воздействию агента этерификации, аминирования или солеобразования; продукт формул (Ib) и (IV’), как указано выше, который можно подвергнуть реакции, указанной выше в п. е), для получения гидролизом продукта формулы (VII): 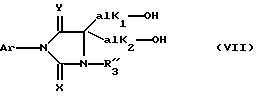 в которой Ar, X, Y, alK1, alK2 и R”3 имеют вышеуказанные значения, и который подвергают тем же реакциям, что и продукт формулы (IV), как определено выше, для получения соответствующих продуктов формул (Ib), (Ic) или (Id), в которых R”3 имеет вышеуказанное значение; продукты формул (Ia), (IV), (IV’), (VII), (Ib), (Ic) и (Id), как указано выше, которые, при необходимости и при желании, можно подвергнуть любой или нескольким из нижеуказанных реакций в произвольной последовательности: – реакции солеобразования с помощью минеральной или органической кислоты или основания для получения соответствующей соли; – реакции выделения возможных защитных групп, которые могут быть включены в защищенные функциональные группы. Воздействие продуктов формулы (II) на продукты формулы (III) или (X) осуществляется прежде всего в органическом растворителе, таком как тетрагидрофуран или дихлорэтан, однако можно также использовать и простой этиловый эфир или изопропиловый эфир. Реакция выполняется в присутствии третичного основания, такого как триэтиламин или же пиридин или метилэтилпиридин. Реакция продукта формулы (IV), как определено выше, с соединением формулы (V), как определено выше, для получения продукта формулы (Ib), как определено выше, может производиться в обычных условиях, хорошо известных специалистам, и, в частности, как указано в книге Теодора У. Грина “Защитные группы в органическом синтезе”, выходные данные которой приведены выше. Для случаев, когда и S1, и S2 представляют собой атом водорода, описание реакции приводится, в частности, в статье L. Hough, J.К.N. Jones and М.S. Magson. J. Chem. Soc., 1525 (1952 год). Один из радикалов S1 и S2 может, в частности, представлять собой атом водорода или метильный или трет-бутильный радикал, а второй – метильный радикал. Радикалы S1 и S2 могут также образовывать вместе с C=O циклоалканонный радикал, такой, в частности, как циклопентанонный, циклогексанонный или циклогептанонный. Описание реакции подобных соединений формулы (V) с продуктом формулы (IV), как определено выше, приводится в статье W. A. R. van Heeswijk, J.В. Goedhart and J. F. G. Vliegenthart, Carbohydr. Res. 58, 337 (1977 г.). Получение продукта формулы (Ic), как определено выше, на основе продукта формулы (IV), как определено выше, может осуществляться путем выполнения реакции с фосгеном или его производным, таким, в частности, как трифосген или же N,N’- карбонилдиимидазол, как описано, например, в статьях W. N. Haworth and C.R. Porter. J. Chem. Soc. 151 (1930 год); R.L. Letsinger and K.K. Ogilvie, J. Org. Chem. 32, 296 (1967 год); J.P. Kutney and A.H. Ratcliffe, Synth. Commun. 5, 47 (1975 год). Получение продукта формулы (Id), как определено выше, путем выполнения реакции продукта формулы (IV) с продуктом формулы (VI) может осуществляться, как указано, в частности, в статье R.J. Ferrier, Methods Carbohydr. Chem. VI, 419-426 (1972 год). Оба гидроксильных радикала продукта формулы (IV), как определено выше, могут быть защищены для получения продукта (IV’), как определено выше, в частности путем воздействия дигидропираном или хлорсиланом, таким как, например, трет- бутилдиметилсилилхлорид. Возможные функциональные группы, которые может содержать R3 и которые могут быть защищены, являются гидроксильными или аминными функциями. Для защиты указанных функциональных групп используются обычные защитные группы. Можно, например, назвать следующие защитные группы аминного радикала: трет-бутил, трет-амил, трихлорацетил, хлорацетил, бензогидрил, тритил, формил, бензилоксикарбонил. В качестве защитной группы гидроксильного радикала можно назвать такие радикалы, как формальный, хлорацетильный, тетрагидропиранильный, триметилсилильный, трет-бутилдиметилсилильный. Разумеется, что вышеприведенный перечень не ограничителен и что использовать можно и другие защитные группы, например, группы, известные в химии пептидов. Перечень подобных защитных групп приводится, например, во французском патенте BF 2499995, содержание которого приводится здесь для справки. Возможные реакции выделения защитных групп осуществляются как описано в указанном патенте BF 2499995. Предпочтительным методом выделения является кислый гидролиз с использованием кислот, выбранных среди таких кислот, как хлористо-водородная, муравьиная, трифторуксусная, бензолсульфокислота или паратолуолсульфокислота. Предпочтение отдается хлористо-водородной кислоте. Возможная реакция гидролиза группы >C=NH с получением кетоновой группы также предпочтительно выполняется с использованием кислоты, такой как водная хлористо-водородная кислота, например при температуре кипения. Когда гидролиз группы >C=NH с получением карбонильной группы выполняется на молекуле, также включающей группу >C=S, последняя может быть превращена в группу >C=O. В этом случае свободный радикал ОН, который может включать R3, может быть преобразован в радикал SH. Реакция превращения группы (групп) >C=O в группу >C=S осуществляется с помощью так называемого реактива Лауссона формулы: 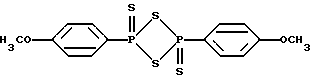 который выпускается в продажу, например, фирмой ФЛУКА и описание которого приводится, например, в статье Bull. Soc. Chim. Belg. том 87, N 3 (1987 год), стр. 229. Когда требуется превратить две функциональные группы >C=O в функциональные группы >C=S, операция выполняется в присутствии избыточного количества реактива Лауссона. Это относится и к случаю, когда операция выполняется на основе молекулы, включающей функциональную группу >C=S и функциональную группу >C= O, и требуется превратить указанную функциональную группу >C=O в группу >C=S. Однако, когда операция выполняется на основе молекулы, включающей две функциональные группы >C=O, и требуется получить продукт, включающий только одну функциональную группу >C=S, операция выполняется при недостатке реактива Лауссона. В этом случае получают, как правило, смесь трех продуктов: каждого из двух продуктов, включающих одну функциональную группу >C=O и одну функциональную группу >C=S, и продукт, включающий две функциональные группы >C=S. Указанные продукты могут затем быть разделены обычными методами, например методом хроматографии. Воздействие на продукт формулы (Ia), (Ib), (Ic), (Id) или (IV’) реактивом формулы Hal-R”3 осуществляется в присутствии сильного основания, такого как гидрид натрия или калия. Можно также производить реакцию переноса фазы в присутствии четвертичных солей аммония, таких как трет-бутиламмоний. Защитными группами, которые может содержать заместитель R”3, могут быть, например, группы из числа перечисленных выше для R3. Реакции выделения защитных групп выполняются в условиях, указанных выше. Удаление трет-бутилдиметилсилильной группы может производиться, например, с помощью хлористо-водородной кислоты. Возможное превращение в сложный эфир продуктов формулы (I), как указано выше, в которой R”3 содержит свободный радикал ОН, осуществляется в обычных условиях. Использовать можно, например, кислоту или функциональное производное, например, ангидрид, такой как уксусный ангидрид, в присутствии основания, такого как пиридин. Возможное превращение в сложный эфир или в соль продуктов формулы (I), как указано выше, в которой R”3 представляет собой группу COOH, выполняется в обычных условиях, хорошо известных специалистам. Возможное аминирование продуктов формулы (I), как указано выше, в которой R”3 включает радикал COOH, выполняется в обычных условиях. Использовать можно первичный или вторичный амин на функциональном производном кислоты, например, симметричный или смешанный ангидрид. Предметом настоящего изобретения также является способ получения продуктов формулы (I’): 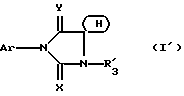 в которой Ar, X, Y, R’3 и (H) имеют вышеуказанные значения и отличающейся тем, что продукт формулы (VIII): Ar – Hal в которой Ar имеет вышеуказанное значение, a Hal представляет собой галогенный атом, вводят в реакцию с продуктом формулы (IX): 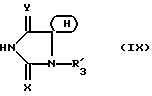 в которой X, Y, R’3 и (H) имеют вышеуказанные значения, причем реакция производится в присутствии катализатора и, при необходимости, растворителя. Что касается продуктов формулы (VIII), то термин Hal означает, в первую очередь, атом хлора, однако он может также являться атомом бора или йода. Ролью катализатора, по всей вероятности, является улавливание выделяющегося галогенида водорода, и, соответственно, способствование реакции конденсации продукта формулы (VIII) с продуктом формулы (IX) для получения искомого продукта. Более конкретно предметом настоящего изобретения является вышеописанный метод, при котором катализатором является природный металл, в виде окисла или основания. Когда используемым катализатором является металл, таким металлом может быть медь или никель. При этом он может быть в чистом виде, в форме окиси металла или же солей металла. Солями металлов могут быть хлорид или ацетат. Когда используемым катализатором является основание, этим основанием может быть, например, гидроокись натрия или гидроокись калия; в реакционную среду при желании может быть добавлен диметилсульфоксид. Более конкретно предметом настоящего изобретения является вышеописанный способ, при котором роль катализатора может играть окисел одновалентной или двухвалентной меди, медь в форме металла или основание, такое как гидроокись натрия или гидроокись калия. При использовании в качестве катализатора металлической меди, ее предпочтительнее использовать в виде порошка. Предметом изобретения является, в частности, описанный выше способ, в котором в качестве катализатора используется окисел, содержащий одновалентную медь. Используемый растворитель выбирается, в первую очередь, среди эфиров с высокой температурой кипения, таких как, например, дифениловый эфир, диглим, триглим и диметилсульфоксид, однако использовать можно также, например, масло с высокой температурой кипения, такое как парафин или вазелин. Предметом настоящего изобретения является, в частности, описанный выше способ, отличающийся тем, что процесс протекает в присутствии растворителя эфирного типа, такого как дифениловый эфир, диглим, триглим и диметилсульфоксид. Предметом изобретения в первую очередь является описанный выше способ, в котором в качестве растворителя используется дифениловый спирт или триглим. Вышеописанный способ получения искомого продукта может протекать под давлением или при атмосферном давлении, желательно при повышенной температуре. Таким образом, предметом настоящего изобретения является описанный выше способ, отличающийся тем, что реакция протекает при температуре выше 100oC, причем желательно, чтобы эта температура превышала 150oC. Более конкретно предметом настоящего изобретения является описанный выше способ, особенностью которого является то, что реакция продолжается более 2 часов. Конкретным предметом настоящего изобретения является вышеописанный способ, отличающийся тем, что реакция протекает в присутствии окисла, содержащего одновалентную медь, в триглиме, при температуре, равной или превышающей 200oC, и в течение более 3 часов. Продукты, являющиеся предметом настоящего изобретения, обладают интересными фармакологическими свойствами; в частности они фиксируются на андрогенных рецепторах и обладают антиандрогенной активностью. Указанные свойства иллюстрируются тестами, приведенными в экспериментальной части настоящей заявки. Благодаря указанным свойствам описанные выше продукты формулы (I) настоящего изобретения могут использоваться в качестве медикаментов для: лечения аденом и новообразований простаты, а также доброкачественной гипертрофии простаты, как самостоятельно, так и в сочетании с аналогами ЛГРГ. Они могут также использоваться при лечении доброкачественных и злокачественных опухолей, обладающих андрогенными рецепторами, в частности рака грудной железы, кожи, яичников, мочевого пузыря, лимфатической системы, почек и печени; лечения кожных заболеваний, таких как акне, гиперсебореи, облысения или гирсутизма. Таким образом, указанные продукты могут использоваться в дерматологии как самостоятельно, так и в сочетании с антибиотиками, такими как производные азелаиновой и фузидиновой кислот, эритромицин, а также производные ретинойной кислоты или ингибитор 5  -редуктаза, такого как (5 -редуктаза, такого как (5  , 17 , 17 )-1,1-диметилэтил 3-оксо 4-аза-андрост-1-ен 17-карбоксамид (или финастерид, мерк 11-й вып.) – для лечения акне, облысения или гирсутизма. Они могут также использоваться в сочетании со стимулятором роста волос, таким как миноксидил – при лечении облысения.
Указанные выше продукты формулы (I) могут также использоваться в ветеринарии при лечении расстройств поведения, таких как агрессивность, андрогенозависимых заболеваний, таких как circum analum у собак и опухоли с наличием андрогенных рецепторов. Они могут также использоваться при химической кастрации животных.
Описанные выше продукты формулы (I) в радиоактивной форме (тритий, углерод – 14, йод – 125 или фтор – 18) могут также использоваться в качестве специальных меток андрогенных рецепторов. Они могут также использоваться и в диагностике, в медицинских снимках.
Таким образом, предметом настоящего изобретения является применение в качестве медикаментов определенных выше продуктов формулы (I), допустимых с фармацевтической точки зрения, и, в первую очередь, вышеописанных продуктов формулы (F), допустимых с фармацевтической точки зрения.
Предметом настоящего изобретения для применения в качестве медикаментов являются следующие продукты: )-1,1-диметилэтил 3-оксо 4-аза-андрост-1-ен 17-карбоксамид (или финастерид, мерк 11-й вып.) – для лечения акне, облысения или гирсутизма. Они могут также использоваться в сочетании со стимулятором роста волос, таким как миноксидил – при лечении облысения.
Указанные выше продукты формулы (I) могут также использоваться в ветеринарии при лечении расстройств поведения, таких как агрессивность, андрогенозависимых заболеваний, таких как circum analum у собак и опухоли с наличием андрогенных рецепторов. Они могут также использоваться при химической кастрации животных.
Описанные выше продукты формулы (I) в радиоактивной форме (тритий, углерод – 14, йод – 125 или фтор – 18) могут также использоваться в качестве специальных меток андрогенных рецепторов. Они могут также использоваться и в диагностике, в медицинских снимках.
Таким образом, предметом настоящего изобретения является применение в качестве медикаментов определенных выше продуктов формулы (I), допустимых с фармацевтической точки зрения, и, в первую очередь, вышеописанных продуктов формулы (F), допустимых с фармацевтической точки зрения.
Предметом настоящего изобретения для применения в качестве медикаментов являются следующие продукты:– 4-(2,4-диоксо 1-(4-гидроксибутил) 8-окса 1,3-диазаспиро (4.5) декан 3-ил) 2-(трифторметил)бензонитрил, – 4-(2,4-диоксо 1-(2-фторэтил) 8-окса 1,3-диазаспиро (4.5) декан 3-ил) 2-(трифторметил)бензонитрил, – 3-(4-циано 3-(трифторметил) фенил) 2,4-диоксо 8-окса 1,3- диазаспиро (4.5) декан 1-ацетонитрил, – 4-(2,4-диоксо 1-(4-гидроксибутил) 8-тиа 1,3-диазаспиро (4.5) декан 3-ил) 2-(трифторметил)бензонитрил. Указанные продукты могут применяться внутрь, парентеральным, перлингвальным, ректальным путем или нанесением на кожу. Предметом настоящего изобретения также являются фармацевтические композиции, отличающиеся тем, что они включают, в качестве действующего начала, как минимум один из определенных выше медикаментов. Указанные композиции могут быть представлены в виде растворов или взвесей для инъекций, таблеток, пилюль, капсул, сиропов, суппозиториев, кремов, мазей, гелей и лосьонов. Композиции могут также быть представлены в виде липосом. Указанные фармацевтические формы производятся обычными методами. Действующее начало может вводиться в основы, обычно используемые при изготовлении фармацевтических композиций, такие как водные и безводные связующие, тальк, аравийская камедь, лактоза, амидон, стеарат магния, какао-масло, жиры животного или растительного происхождения, производные парафина, гликоли, различные увлажняющие, диспергирующие или эмульсионные агенты, консерванты. Обычно применяемые дозы могут, в зависимости от особенностей больного и от заболевания, составлять, например, от 10 до 500 мг в день для взрослых при приеме внутрь. Продукты формулы (II), используемые на начальном этапе настоящего изобретения, могут быть получены в результате воздействия фосгеном, когда X представляет собой атом кислорода, и тиофосгеном, когда X является атомом серы на соответствующий амин формулы (А): Ar-NH2 Пример подобного приготовления приводится в патенте ЕЭС ЕР 0494819. Когда Ar представляет собой фенильный радикал, описание продукта подобного типа приводится также во французском патенте BF 2329276, а амины формулы (A) описаны в патенте – ЕР 0002892 и во французском патенте BF 2142804. Продукты формулы (X) общеизвестны или могут быть получены на основе соответствующего циангидрина согласно методу, описание которого приводится в статьях J. Am. Chem. Soc. (1953 год), 15, 4841, BEIL I 4 526 или J. Org. Chem. 27 2901 (1962 год). Продукты формулы (X), в которых R’3 не является атомом водорода, могут быть получены путем воздействия продукта формулы R”3 Hal на 2-циано 2-аминопропан в условиях, указанных выше для воздействия R”3 Hal на продукты формулы (Ia). Пример приготовления подобного типа описан в статье Jilek et Coil. Collect. Czech. Chem. Comm. 54 (8) 2248 (1989 год). Продукты формул (VIII) и (IX), используемые на начальном этапе вышеуказанного способа для получения продуктов формулы (I’), как определено выше, общеизвестны и приобретаются в торговой сети, но они могут быть получены обычными методами, хорошо известными специалистам. Получение продуктов формулы (IX) описано, в частности, в нижеперечисленных статьях: – Zhur. Preklad. Khim. 28, 969-75 (1955 год) (CA 50, 4881a, 1956 год) – Tetrahedron 43, 1753 (1987 год) – J. Org. Chem. 52, 2407 (1987 год) – Zh. Org. Khim. 21, 2006 (1985 год) – J. Fluor. Chem. 17, 345 (1981 год) или в патентах: – немецком патенте DRP 637318 (1935 год) – патенте ЕР 0130875 – японском патенте JP 81121524 Продукты формулы (IX), являющиеся производными гидантоина, широко используются и цитируются в специализированной литературе, например в следующих статьях: – J. Pharm. Pharmacоl., 67, том 19 (4), стр. 209-16 (1967 год) – Khim. Farm. Zh., 67, том 1 (5), стр. 51-2 – немецкий патент 2217914 – патент ЕЭС 0091596 – J. Chem. Soc. Perkin. Trans. 1, стр. 219-21 (1974 год) Описанные выше продукты формулы (III), такие как продукты, используемые в приготовлении описанных ниже примеров, встречаются в торговой сети. В качестве примера можно назвать: – 4-аминотетрагидро-2Н-пиран-4-карбонитрил – 4-аминотетрагидро-2Н-тиопиран-4-карбонитрил – 4-амино-1-метилпиперидин-4-карбонитрил Предметом настоящего изобретения в качестве новых промышленных продуктов, в частности в качестве новых промышленных продуктов, используемых в качестве промежуточных продуктов для получения продуктов формулы (I), как описано выше, являются продукты формул (IV) и (IX), как определено выше, в которых Ar имеет вышеуказанное значение, за исключением фенильного радикала, замещенного двумя радикалами, выбранными среди галогенных атомов и радикалов, таких как циано-, нитро-, трифторметильный и карбоксильный свободный, превращенный в соль, аминированный или превращенный в сложный эфир. Приводимые далее примеры иллюстрируют настоящее изобретение, вместе с тем не ограничивая его. ПРИМЕР 1: 4-(4-имино-2-оксо-8-окса-1,3-диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил ЭТАП 1: 4-амино-тетрагидро-2Н-пиран-4-карбонитрил Поочередно вводят 8 мл гидрата окиси аммония, 1,58 г хлористого аммония, 1,23 г цианистого натрия, охлаждают полученный раствор в ледяной метаноловой ванне примерно до -7oC и добавляют при температуре  0oC 2 мл тетрагидро-4Н-пиран 4-она, дают температуре подняться до уровня комнатной и энергично взбалтывают в течение 18 ч. Затем трижды экстрагируют с помощью метиленхлорида, промывают соляным раствором и высушивают. Таким образом получают 2,49 г искомого продукта (в виде прозрачных кристаллов) (tпл 0oC 2 мл тетрагидро-4Н-пиран 4-она, дают температуре подняться до уровня комнатной и энергично взбалтывают в течение 18 ч. Затем трижды экстрагируют с помощью метиленхлорида, промывают соляным раствором и высушивают. Таким образом получают 2,49 г искомого продукта (в виде прозрачных кристаллов) (tпл  46-47oC).
Физический анализ: 46-47oC).
Физический анализ:Инфракрасный спектр: (CHCl3) см-1 NH2 3390-3374-3324 C  N 2225 N 2225NH2 деформ. 1605 ЭТАП 2: 4-(4-имино-2-оксо-8-окса-1,3-диазаспиро [4.5] декан- 3-ил)-2-(трифторметил)бензонитрил 883 мг продукта, полученного на вышеописанном этапе 1, вводят в 7 мл 1,2-дихлорэтана и 0,3 мл триэтиламина. Затем температуру доводят примерно до -7oC и по капле добавляют за 15 мин 6,4 мл продукта, полученного в приготовлении примера 7 патентной заявки ЕЭС 0494819, после чего температуре дают подняться до уровня комнатной. Затем смесь выдерживают в течение 1 ч, выпаривают досуха и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (7:1). В результате получают 1,85 г целевого продукта (в виде белых кристаллов) (tпл 249-250oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 OH/NH 3340-3295 C  N 2240 N 2240C=O 1750 Сопряженная система ароматическое соединение 1678-1612-1572-1508 ПРИМЕР 2: 4-(2,4-диоксо-8-окса-1,3-диазаспиро [4.5] декан-3-ил)-2- (трифторметил)бензонитрил 1,66 г продукта, полученного в примере 1, вводят в 30 мл метанола, 10 мл трихлорметана, 10 мл 2 н. хлористо-водородной кислоты и за 50 минут доводят до температуры кипения, после чего добавляют 100 мл воды и трижды экстрагируют с помощью этилацетата. Затем промывают органическую фазу соляным раствором, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (85 : 15). Затем растворяют в 100 мл изопропанола при температуре около +70oC, фильтруют и концентрируют, замораживают в течение 1 ч, центрифугируют и высушивают. В результате получают 1,425 г целевого продукта (в виде белых кристаллов) (tпл 192-193oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 Поглощение в области OH/NH C  N 2240 N 2240C=O 1790-1732 Ароматические соединения 1614-1582-1506 ПРИМЕР 3: 4-(2,4-диоксо-1-(4-гидроксибутил)-8-окса-1,3- диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Для начала вводят 55 мг 50-процентного гидрида натрия, после чего добавляют по капле за 25 мин 340 мг продукта, полученного в примере 2, и 25 мл диметилсульфоксида. Затем промывают с использованием 0,5 мл диметилсульфоксида и через 20 мин после прекращения выделения водорода добавляют 0,41 г 4- йодбутокситриметилсилана и дают воздействовать в течение 18 ч при комнатной температуре. Затем раствор вливают в 10 мл воды и четырежды экстрагируют с помощью эфира. Органическую фазу промывают водой, а затем соляным раствором, высушивают и поглощают в смеси 10 мл метанола и 1 мл 2 н. хлористо-водородной кислоты. По истечении 30 мин вливают в 20 мл насыщенного раствора хлористого натрия, трижды экстрагируют с помощью трихлорметана и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (8: 2), в результате чего получают 369 мг целевого продукта (в виде белого рыхлого пенистого продукта). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 ОН 3626-3485 C  N 2235 N 2235C=O 1775-1721 Ароматические соединения 1615-1602-1577-1505 ПРИМЕР 4: 4-(2,4-диоксо-1-(2-гидроксиэтил)-8-окса-1,3- диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Для начала вводят 82 мг 50-процентного гидрида натрия, 510 мг продукта, полученного в примере 2, 4 мл диметилсульфоксида, промывают с использованием 0,5 мл диметилсульфоксида и через 20 мин после прекращения выделения водорода добавляют в один прием 572 мг 2-йодэтоксиметил-трет-бутилсилана и доводят раствор за 1 ч 30 мин до температуры +40oC, а затем за 18 ч до комнатной температуры. После этого раствор вливают в 40 мл воды, содержащей около 0,2 г первичного фосфата калия и четырежды экстрагируют с помощью эфира, промывают водой, а затем соляным раствором и высушивают. Затем производят очистку на двуокиси кремния, используя в качестве элюанта метиленхлорид и этилацетат. После этого поглощают в 16 мл метанола, 3 мл 2 н. хлористо-водородной кислоты и нагревают в течение 40 мин при температуре +40oC. Затем вливают в 50 мл бикарбоната натрия (1/2), трижды экстрагируют с помощью трихлорметана, промывают соляным раствором и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (8:2), в результате чего получают 451 мг целевого продукта (в виде белых кристаллов) (tпл 196-197oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 OH/NH 3450 C  N 2240 N 2240>=O 1775-1718 Ароматические соединения 1615-1576-1508 ПРИМЕР 5: 4-(2,4-диоксо-1-(3-гидроксипропил)-8-окса-1,3- диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Операции выполняются, как в примере 4, на основе 109 мг хлористого натрия (1/2), 510 мг продукта, полученного в примере 2, и 4 мл диметил-сульфоксида, после чего промывают с использованием 0,5 мл диметил-сульфоксида и через 20 мин после прекращения выделения водорода добавляют 1,004 г 3- бромпропоксидифенил-трет-бутилсилана и доводят температуру раствора примерно до +50oC. Затем, действуя как в примере 4, поглощают в 30 мл метанола, 10 мл 2 н. хлористо-водородной кислоты, 10 мл трихлорметана и доводят до температуры кипения. После очистки на двуокиси кремния, с использованием в качестве элюанта метиленхлорида и ацетона (8:2), получают 441 мг целевого продукта (в виде белых кристаллов) (tпл 155-156oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 Комплексное поглощение в области NH/OH C  N 2240 N 2240>=O 1778-1714 Ароматические соединения 1618-1580-1539-1511 ПРИМЕР 6: 3-(4-циано-3-(трифторметил)фенил)-2,4-диоксо-8- окса-1,3-диазаспиро [4.5] декан 1-этилбутират Операции выполняются, как в примере 3, на основе 123 мг 50- процентного гидрида натрия, 510 мг продукта, полученного в примере 2, 3,5 мл диметилсульфоксида, после чего промывают с использованием 0,5 мл диметилсульфоксида и через 15 мин после прекращения выделения водорода добавляют 454 мг 4-бромбутирата этила и за 50 мин доводят температуру до +40oC. Затем вливают в 40 мл воды, содержащей 0,4 г первичного фосфата калия, четырежды экстрагируют с помощью эфира, промывают органическую фазу водой, а затем соляным раствором, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и этилацетат (85:15). В результате получают 584 мг целевого продукта (в виде белых кристаллов) (tпл 129-130oC). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 C  N 2230 N 2230>=О 1776-1722 Ароматические соединения 1614-1575-1505 ПРИМЕР 7: 3-(4-циано-3-(трифторметил)фенил)-2,4-диоксо-8- окса-1,3-диазаспиро [4.5] декан-1-бутановая кислота Для начала вводят 522 мг продукта, полученного в примере 6, 20 мл метанола, нагревают до температуры +30oC, доводят температуру до уровня комнатной и добавляют 2 мл 2 н. гидрата окиси натрия, после чего выдерживают в течение 4 ч 30 мин, вливают в 30 мл H2О и доводят pH до 2-3. Затем трижды экстрагируют с помощью этилацетата, промывают органическую фазу водой, а затем соляным раствором, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и метанол (9:1), после чего сгущают порошкованием в 0,2 мг изопропанола и 5 мл эфира. В результате получают 345 мг целевого продукта (в виде белых кристаллов) (tпл 151-152oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 Комплексное поглощение в области NH/OH C  N 2240 N 2240> = O 1780-1720 Ароматические соединения 1615-1581-1510 ПРИМЕР 8: 3-(4-метоксифенил)-8-окса-1,3-диазаспиро [4.5] декан-2,4-дион Операции выполняются, как на этапе 2 примера 1, на основе 380 мг продукта, полученного на этапе 1 примера 1, 4 мл 1,2- дихлорэтана и 0,25 мл триэтиламина, после чего температуру доводят до -5oC и добавляют по капле 450 мг 4-метоксифенилизоцианата, промывают с использованием 1 мл 1,2-дихлорэтана и дают температуре подняться до уровня комнатной. По истечении 1 ч центрифугируют, высушивают и поглощают в 20 мл метанола, 6 мл трихлорметана, 6 мл 2 н. хлористо-водородной кислоты и доводят раствор за 2 ч до температуры кипения. Затем концентрируют, поглощают в 30 мл воды, экстрагируют 5 раз с помощью этилацетата, промывают органическую фазу бикарбонатом натрия (1/2), а затем соляным раствором, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (85:15). В результате получают 493 мг целевого продукта (в виде белых кристаллов) (tпл 253-254oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 Поглощение в области OH/NH C=O 1774-1715 Ароматические соединения 1609-1590-1518 ПРИМЕР 9: 4-(2,4-диоксо-1-(2-фторэтил)-8-окса-1,3-диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Для начала вводят 55 мг 50-процентного гидрида натрия, добавляют по капле примерно за 20 мин 340 мг продукта, полученного в примере 2, и 3 мл диметилсульфоксида и промывают с использованием 0,2 мл диметилсульфоксида. Через 20 мин после прекращения выделения водорода добавляют 0,1 мл 1-бром 2-фторэтана и нагревают в течение 1 ч 20 мин при температуре +50oC. Затем вливают в 10 мл ледяной воды, содержащей 0,2 г первичного фосфата калия, и экстрагируют 5 раз с помощью эфира. Органическую фазу промывают водой, а затем соляным раствором, высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (85:15), высушивают и подвергают кристаллизации из изопропанола. В результате получают 281 мг целевого продукта (в виде белых кристаллов) (tпл 192-193oC). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 C=O 1777-1723 C  N 2238 N 2238Ароматические соединения 1616-1576-1505 ПРИМЕР 10: 3-(4-циано-3-(трифторметил)фенил)-2,4-диоксо-8- окса-1,3-диазаспиро [4.5]декан-1-ацетонитрил Для начала вводят 55 мг 50-процентного гидрида натрия и добавляют по капле за 20 мин 340 мг продукта, полученного в Примере 2, 2,5 мл диметилсульфоксида и промывают с использованием 0,5 мл диметилсульфоксида. Через 15 мин после прекращения выделения водорода добавляют 0,1 мл бромацетонитрила и выдерживают в течение 1 ч. Затем вливают в 15 мл воды, содержащей около 0,3 г первичного фосфата калия, трижды экстрагируют с помощью этилацетата, промывают водой, а затем соляным раствором, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (85:15). Полученный смолистый продукт растворяют при температуре около +40oC в смеси 15 мл метиленхлорида и 30 мл изопропанола, после чего концентрируют до кристаллизации. В результате получают 267 мг целевого продукта (в виде белых кристаллов) (tпл 210-211oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 C  N 2238 N 2238>=O 1782-1730 Ароматические соединения 1612-1570-1504 ПРИМЕР 11: 3-(4-метилтиофенил)-8-окса-1,3-диазаспиро [4.5]декан 2,4-дион Операции выполняются, как в примере 8, на основе 380 мг 4- метилтио-фенилизоцианата, 4 мл 1,2-дихлорэтана и 0,15 мл триэтиламина. В результате получают 513 мг целевого продукта (tпл 256- 257oC). Инфракрасный спектр: (вазелиновое масло) см-1 Поглощение в области OH/NH >=O 1776-1720 Ароматические соединения 1500 ПРИМЕР 12: 4-(4-имино-2-оксо-8-тиа-1,3-диазаспиро [4.5] декан-3-ил)-2-(трифторметил)бензонитрил ЭТАП 1: 4-аминотетрагидро-2Н-тиопиран-4-карбонитрил Операции выполняются, как на этапе 1 примера 1, на основе 8 мл гидрата окиси аммония, 1,58 г хлористого аммония, 1,23 г цианистого натрия, 2,51 г тетрагидро-4Н-тиопиран 4-она, которые подвергаются взбалтыванию в течение 18 ч при комнатной температуре. Затем трижды экстрагируют с помощью метиленхлорида, промывают соляным раствором и высушивают. Таким образом получают 2,88 г искомого продукта (в виде белых кристаллов) (tпл 51-52oC). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 NH2 3398-3381-3321 NH2 деформ. 1617-1584 C  N 2225 N 2225ЭТАП 2: 4-(4-амино-2-оксо-8-тиа-1,3-диазаспиро [4.5] дeкaн-3-ил)-2-(трифторметил)бензонитрил Операции выполняют, как на этапе 2 примера 1, на основе 1,42 г продукта, полученного на вышеописанном Этапе 1, 14 мл 1,2- дихлорэтана, 0,5 мл триэтиламина; температуру доводят примерно за 20 мин до уровня от -10oC до -5oC и добавляют 9,1 мл продукта, полученного в приготовлении Примера 7 патентной заявки ЕЭС 0494819, после чего температуре дают подняться до уровня комнатной. Затем выдерживают в течение 1 ч 20 мин, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (9:1). В результате получают 2,49 г целевого продукта (в виде белых кристаллов) (tпл 226-227oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 NH 3330-3250-3210-3170-3120 C  N 2240 N 2240C=O 1750 C=N 1675-1658 Ароматические соединения 1612-1572-1510 ПРИМЕР 13: 4-(2,4-диоксо-8-тиа-1,3-диазаспиро [4.5] декан-3- ил)-2-(трифторметил)бензонитрил Операции выполняются, как в примере 2, на основе 2,34 продукта, полученного в примере 12, 25 мл метанола, 5 мл трихлорметана, к которым добавляют 4,5 мл 2 н. хлористо-водородной кислоты и доводят за 1 ч до температуры кипения. Затем подвергают очистке на двуокиси кремния, с использованием в качестве элюанта метиленхлорида и ацетона (95:5) и выполняют рекристаллизацию из изопропанола. Таким образом получают 368 мг целевого продукта (в виде белых кристаллов) (tпл 209-210oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 OH/NH 3340 C  N 2245 N 2245>C=O 1781-1736 Ароматические соединения 1612-1576-1508 ПРИМЕР 14: 4-(2,4-диоксо-1-(4-гидроксибутил)-8-тиа-1,3- диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Операции выполняются, как в примере 3, на основе 55 мг 50- процентного гидрида натрия, после чего добавляют по капле за 20 мин 355 мг продукта, полученного в примере 13, и 2,5 мл диметилсульфоксида и промывают с использованием 0,5 мл диметилсульфоксида. Через 20 мин после прекращения выделения водорода добавляют 0,41 г 4-иодбутокси-триметилсилана. Затем вливают в 25 мл воды, содержащей 0,1 г первичного фосфата калия, трижды экстрагируют с помощью эфира, промывают органическую фазу водой, а затем соляным раствором и высушивают. После этого поглощают в 10 мл метанола, 1 мл 2 н. хлористо-водородной кислоты, выдерживают 30 мин, вливают в 30 мл хлористого натрия (1/2), трижды экстрагируют с помощью этилацетата, промывают соляным раствором и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (9: 1), в результате чего получают 317 мг целевого продукта (в виде белых кристаллов) (tпл 139-140oC). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 ОН 3628 C  N 2235 N 2235>C=O 1774-1722 Ароматические соединения 1615-1601-1505 ПРИМЕР 15: 4-(2,4-диоксо-8,8-диоксидо-8-тиа-1,3-диазаспиро [4.5] декан-3-ил)-2-(трифторметил)бензонитрил Для начала вводят 355 мг продукта, полученного в примере 12, 4 мл метиленхлорида и добавляют за 20 мин при температуре от +22oC до +25oC 990 мг метахлорнадбензойной кислоты, 20 мл метиленхлорида и промывают с использованием 1 мл метиленхлорида. Затем выдерживают в течение 1 ч, добавляют 15 мл тиосульфата натрия и энергично взбалтывают в течение 10 мин. После этого добавляют 15 мл насыщенного раствора бикарбоната натрия, трижды экстрагируют с помощью этилацетата, промывают водой, а затем соляным раствором и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (95:5) и выполняют кристаллизацию из изопропанола. В результате получают 365 мг целевого продукта (в виде белых кристаллов) (tпл 257-258oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 C  N 2235 N 2235>=O 1790-1735 SO2 1297-1133 Ароматические соединения 1613-1575-1508 ПРИМЕР 16: 4-(2,4-диоксо-8-оксидо-8-тиа-1,3-диазаспиро [4.5] декан-3-ил)-2-(трифторметил)бензонитрил (Изомер А) Для начала вводят 355 мг продукта, полученного в примере 13, 20 мл метанола, 4 мл водного раствора метапериодата натрия и доводят до температуры кипения. Затем метанол выпаривают, поглощают в 20 мл воды и четырежды экстрагируют с помощью этилацетата, промывают органическую фазу соляным раствором и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (95:5), в результате чего получают 900 мг сульфоксида изомера А. После этого выполняют рекристаллизацию из ацетона и получают 292 мг целевого продукта, называемого изомером А (tпл 260-277oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 Комплексное поглощение в области NH/OH C  N 2235 N 2235>=O 1789-1725 S–> O 1010 Ароматические соединения 1612-1572-1509 ПРИМЕР 17: 4-(2,4-диоксо-8-оксидо-8-тиа-1,3-диазаспиро [4.5] декан-3-ил)-2-(трифторметил)бензонитрил (Изомер Б) Операции выполняются, как в примере 16, с очисткой на двуокиси кремния, с использованием в качестве элюанта метиленхлорида и метанола (9:1). Таким образом получают 80 мг сульфоксида изомера Б, который подвергают рекристаллизации из ацетона, в результате чего получают 72 мг целевого продукта, называемого изомером Б (tпл 295oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 Поглощение в области NH/OH C  N 2240 N 2240>C=O 1797-1730 S–>O 1015 Ароматические соединения 1618-1580-1509 ПРИМЕР 18: 3-(4-циано-3-(трифторметил)фенил)-2,4-диоксо-8- тиа-1,3-диазаспиро [4.5] декан-1-этилбутират Операции выполняются, как в примере 6, на основе 96 мг 50- процентного гидрида натрия, с введением в течение около 20 мин 390 мг продукта, полученного в примере 13, 2,5 мл диметилсульфоксида. Затем промывают с использованием 0,5 мл диметилсульфоксида. Через 20 мин после прекращения выделения водорода добавляют 370 мг 4-бромбутирата этила и за 1 ч доводят температуру раствора до +40oC. Затем вливают в 15 мл ледяной воды, содержащей 0,1 г первичного фосфата калия, четырежды экстрагируют с помощью эфира, промывают органическую фазу водой, а затем соляным раствором и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и этилацетат (95: 5), в результате чего получают 449 мг целевого продукта (в виде белого рыхлого пенистого продукта). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 C  N 2236 N 2236>=O 1774-1723 Ароматические соединения 1615-1575-1505 ПРИМЕР 19: 3-(4-циано-3-(трифторметил)фенил)-2,4-диоксо-8- тиа-1,3-диазаспиро [4.5] декан-1-бутановая кислота Операции выполняются, как в примере 7, на основе 440 мг продукта, полученного в примере 18, 20 мл метанола, 2 мл 2 н. гидрата окиси натрия, которые взбалтывают в течение 3 ч 30 мин при комнатной температуре и добавляют 3 мл 2 н. хлористо-водородной кислоты. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и метанол (95:5), и получают 346 мг целевого продукта (в виде белых кристаллов) (tпл 197-198oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 C  N 2235 N 2235>=O 1770-1725 Кислота 1710 Ароматические соединения 1615-1575-1505 ПРИМЕР 20: 4-(4-имино-8-метил-2-тиоксо-1,3,8-триазаспиро [4.5] декан-3-ил) 2-(трифторметил)бензонитрил ЭТАП 1: 4-амино-1-метилпиперидин-4-карбонитрил Операции выполняются, как на этапе 1 примера 1, на основе 8 мл гидрата окиси аммония, 1,58 г хлористого аммония, 1,23 г цианистого натрия, с добавлением 2,5 мл 1-метилпиперидона. Затем взбалтывают в течение 18 ч при комнатной температуре, трижды экстрагируют с помощью трихлорметана, промывают органическую фазу соляным раствором и высушивают. Таким образом получают 2,41 г искомого продукта (в виде желто-оранжевого сиропа). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 NH2 3378-3320 C  N 2226 N 2226NH2 деформ. 1602 ЭТАП 2: 4-(4-имино-8-метил-2-тиоксо-1,3,8-триазаспиро [4.5] декан- -3-ил) 2-(трифторметил)бензонитрил Операции выполняются, как на этапе 2 примера 1, на основе 140 мг продукта, полученного на вышеописанном этапе 1, 1,5 мл 1,2- дихлорэтана, 0,1 мл триэтиламина, в которые добавляют по капле 230 мг продукта, полученного в приготовлении примера 11 патентной заявки ЕЭС 0494819, и 1,5 мл 1,2-дихлорэтана. Затем выдерживают в течение 2 ч, выпаривают досуха и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (8 : 2). В результате получают 315 мг целевого продукта (в виде кристаллов цвета слоновой кости) (tпл 264oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 NH  3190 3190C  N 2240 N 2240>=NH 1700-1688-1678 Ароматические соединения 1618-1580-1518-1505 ПРИМЕР 21: 4-(8-метил-4-оксо-2-тиоксо-1,3,8-триазаспиро [4.5] декан-3-ил) 2-(трифторметил)бензонитрил Для начала вводят 300 мг продукта, полученного в примере 20, 6 мл метанола, 1,5 мл 2 н. хлористо-водородной кислоты и доводят за 1 ч до температуры кипения, а затем до комнатной температуры. Затем вливают в 20 мл гидрата окиси аммония (1/2), насыщают хлористым натрием, трижды экстрагируют с помощью этилацетата и высушивают. Затем очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и метанол (9:1). В результате получают 260 мг целевого продукта (в виде белых кристаллов) (tпл 229-230oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 OH/NH 3330-3340 + ассоцииров. C  N 2236 N 2236C=O 1757 Ароматические соединения 1614-1580-1514-1502 ПРИМЕР 22: 4-(4-имино-8-метил-2-оксо-1,3,8-триазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Операции выполняют, как на этапе 2 примера 20, на основе 153 мг продукта, полученного на этапе 1 примера 20, 1,5 мл 1,2- дихлорэтана и 0,1 мл триэтиламина, которые помещают в ледяную ванну, добавляют 1 мл продукта, полученного в приготовлении примера 7 патентной заявки ЕЭС ЕР 0494819, после чего температуре дают подняться до уровня комнатной. Затем выдерживают в течение 1 ч, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и метанол (7:3). В результате получают 277 мг целевого продукта (в виде белых кристаллов) (tпл 199-200oC). Физический анализ: Инфракрасный спектр: (вазелиновое масло) см-1 NH 3290-3240-3130 C  N 2224 N 2224C=O 1746 C=NH 1677-1669 Ароматические соединения 1609-1568-1512 ПРИМЕР 23: 4-(2,4-диоксо-8-метил-1,3,8-триазаспиро [4.5] декан-3-ил)-2-(трифторметил)бензонитрил Операции выполняются, как в примере 2, на основе 3 г продукта, полученного в примере 22, 70 мл метанола, 17 мл 2 н. хлористо-водородной кислоты, которые доводят за 1 ч 30 мин до температуры кипения. Затем вливают под 200 мл гидрата окиси аммония + 100 г льда, насыщенного хлористым натрием, четырежды экстрагируют с помощью этилацетата, промывают соляным раствором, высушивают и очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и метанол (9:1). После кристаллизации из метиленхлорида и простого изопропилового эфира получают 2,12 г целевого продукта (в виде белых кристаллов) (tпл 188-189oC). Физический анализ: Инфракрасный спектр: (CHCl3) см-1 =C-NH 3445 C  N 2230 N 2230>=O 1789-1729 Ароматические соединения 1615-1576-1505 ПРИМЕР 24: 4-(8,8-диметил)-2,4-диоксо-7,9-диокса-1,3- диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил ЭТАП 1: 1,3 бис [(тетрагидро-2H-пиран-2-ил)окси] 2-пропанон 9 г 2,5-дигидрокси-1,4-диоксан-2,5-диметанола вводят в 60 мл диоксана и доводят температуру взвеси за 15 мин до температуры порядка +70oC, после чего температуру доводят до уровня комнатной. Затем добавляют 20 мл 3,4-дигидро-2Н-пирана и 300 мг моногидратной паратолуолсульфокислоты и выдерживают температуру на уровне около +40oC, после чего выдерживают в течение ночи при комнатной температуре. Затем раствор вливают в смесь 300 мл насыщенного раствора бикарбоната натрия +10 мл триэтиламина и четырежды экстрагируют с помощью метиленхлорида. Затем органическую фазу промывают соляным раствором и высушивают. После очистки пропусканием через двуокись кремния, с использованием в качестве элюанта этилциклоацетата и триэтиламина (8:2), получают 17 г искомого продукта (в виде бледно-желтого сиропа). Анализы: Инфракрасный спектр: (CHCl3) см-1 Отсутствие ОН O=C 1736 ЭТАП 2: 2-амино-3-((тетрагидро-2Н-пиран-2-ил)окси)-2- (((тетрагидро-2Н-пиран-2-ил)окси)метил)пропаннитрил 5,6 г продукта, полученного на вышеописанном Этапе 1, вводят в 8 мл гидрата окиси аммония, доводят температуру примерно до -5oC и добавляют поочередно 1,58 г хлористого аммония и 1,23 цианистого натрия и примерно за 40 мин дают температуре подняться до уровня комнатной, после чего нагревают при взбалтывании при температуре +40  5oC в течение ночи. Затем температуре дают опуститься до уровня комнатной и трижды экстрагируют с помощью трихлорметана, промывают органическую фазу соляным раствором и высушивают.
После очистки на двуокиси кремния, с использованием в качестве элюанта этилциклоацетата и триэтиламина (3:7), получают 4,41 мг искомого продукта (в виде бледно-желтого сиропа).
Анализы: 5oC в течение ночи. Затем температуре дают опуститься до уровня комнатной и трижды экстрагируют с помощью трихлорметана, промывают органическую фазу соляным раствором и высушивают.
После очистки на двуокиси кремния, с использованием в качестве элюанта этилциклоацетата и триэтиламина (3:7), получают 4,41 мг искомого продукта (в виде бледно-желтого сиропа).
Анализы:Инфракрасный спектр: (CHCl3) см-1 -CN 2235 NH2 3390-3317 ЭТАП 3: 4-(5-имино-2-оксо-4,4-бис (((тетрагидро-2Н-пиран-2-ил) окси)метил)-1-имидазолидинил)2-(трифторметил)бензонитрил 570 мг продукта, полученного на вышеописанном этапе 2, вводят в 5 мл простого изопропилового эфира и 0,28 мл триэтиламина, после чего температуру доводят до -30oC и добавляют за 1 ч раствор 1,2- дихлорэтана при 18,4 г % г и 2,32 г продукта, полученного в приготовлении 1. Затем добавляют 4 мл метиленхлорида и дают температуре подняться до уровня комнатной, выдерживают примерно 2 ч и высушивают. После очистки на двуокиси кремния, с использованием в качестве элюанта метиленхлорида и ацетона (9:1), получают 700 мг искомого продукта. Анализы: Инфракрасный спектр: (CHCl3) см-1 NH 3442-3317 -CN 2235 C=O 1757 C=N 1670 Ароматические соединения 1614-1575-1505 ЭТАП 4: 4-(4,4-бис(гидроксиметил)-2,5-диоксо-1-имидазолидинил)-2- (трифторметил)бензонитрил 300 мг продукта, полученного на вышеописанном этапе 3, вводят в 3 мл метанола и 1,5 мл 2 н. хлористо-водородной кислоты и доводят за 1 ч 30 мин до температуры кипения. Затем температуре дают опуститься до уровня комнатной, вливают в 5 мл бикарбоната, четырежды экстрагируют с помощью этилацетата и промывают насыщенным раствором хлористого натрия и высушивают. После этого очищают на двуокиси кремния, используя в качестве элюанта метиленхлорид и метанол (9:1). Затем поглощают в 20 мл изопропанола при температуре кипения, концентрируют и получают 225 мг искомого продукта (в виде белых кристаллов) (tпл 207-208oC). Анализы: Инфракрасный спектр: (вазелиновое масло) см-1 OH/NH 3525-3365-3250 CN 2240 C=O 1778-1738 Ароматические соединения 1618-1578-1506 ЭТАП 5: 4-(8,8-диметил)-2,4-диоксо-7,9-диокса-1,3- диазаспиро [4.5] декан 3-ил)-2-(трифторметил)бензонитрил Для начала вводят 0,329 г продукта, полученного на вышеописанном этапе 4, 0,5 мл 2,2-диметоксипропана, 0,02 г паратолуолсульфокислоты, 5 мл ацетона, выдерживают при взбалтывании в течение 4 ч, после чего выполняют гидролиз с использованием раствора бикарбоната натрия и экстрагируют с помощью этилацетата. Затем органические фазы объединяют, промывают водой, высушивают, фильтруют и концентрируют. После этого подвергают хроматографии на двуокиси кремния, используя в качестве элюанта метиленхлорид и ацетон (95: 5). Затем выполняют рекристаллизацию из изопропанола и получают 0,240 г целевого продукта (в виде белых кристаллов) (tпл 203oC). Анализы: Инфракрасный спектр: (вазелиновое масло) см-1 CN 2240 C=O 1782-1730 Ароматические соединения 1615-1580-1507 ПРИМЕР 25 Были приготовлены таблетки, имеющие следующий состав: Продукт примера 3: 100 мг Основа для готовой таблетки: 300 мг (Деталировка основы: лактоза, амидон, тальк, стеарат магния). Фармакологические исследования продуктов, являющихся предметом изобретения Исследование воздействия продуктов изобретения на андрогенный рецептор Самцы крыс Спраг-Даулей EOPS весом от 180 до 200 г, кастрированные за 24 часа, умерщвляются, после чего у них вырезают простаты, взвешивают и гомогенизируют при температуре 0oC с помощью трубчатого измельчителя стекло-стекло в забуференном растворе (Tris 10 ммоль, сахароза 0,25 моль, ФМСФ (фенилметансульфонилфторид) 0,1 ммоль, молибдат натрия 20 ммоль, HCl pH 7,4, к которым добавляют 2 ммоль ДТТ (DL дитиотреитол) из расчета 1 г ткани на 8 мл буферного раствора. Затем гомогенат подвергают ультрацентрифугированию (209 000 г х 30 мин) при температуре 0oC. Полученные таким образом аликвоты надосадочной жидкости (цитозол) подвергаются инкубации в течение 30 мин и в течение 24 ч при температуре 0oC при постоянной концентрации (T) тритированного тестостерона, и в присутствии возрастающих концентраций (от 0 до 2500  10-9 моль), либо холодного тестостерона, либо тестируемых продуктов. Концентрация связанного тритированного тестостерона (B) измеряется затем в каждом инкубате методом адсорбции углем-декстраном.
Расчет относительного связующего воздействия (ARL) 10-9 моль), либо холодного тестостерона, либо тестируемых продуктов. Концентрация связанного тритированного тестостерона (B) измеряется затем в каждом инкубате методом адсорбции углем-декстраном.
Расчет относительного связующего воздействия (ARL)Прочерчивают две кривые: процент связанного тритированного гормона B/T в зависимости от логарифма концентрации холодного контрольного гормона и B/T в зависимости от логарифма концентрации холодного тестируемого продукта. Затем определяют прямую уравнения I50= (B/Tмакс + B/Tмин)/2, в котором: B/Tмакс = % связанного тритированного гормона для инкубации данного тритированного гормона при концентрации T; B/T мин = % связанного тритированного гормона для инкубации данного тритированного гормона при концентрации T в присутствии большого избытка холодного гормона (2500  10-9 моль).
Пересечения прямой I50 и кривых позволяют вычислить концентрацию холодного контрольного гормона (CH) и холодного тестируемого продукта (CX), которые ослабляют на 50% связь тритированного гормона с рецептором. Относительное связующее воздействие (ARL) тестируемого продукта определяется с помощью уравнения ARL = 100 (CH)/(CX).
При этом получают следующие результаты, выраженные в ARL: 10-9 моль).
Пересечения прямой I50 и кривых позволяют вычислить концентрацию холодного контрольного гормона (CH) и холодного тестируемого продукта (CX), которые ослабляют на 50% связь тритированного гормона с рецептором. Относительное связующее воздействие (ARL) тестируемого продукта определяется с помощью уравнения ARL = 100 (CH)/(CX).
При этом получают следующие результаты, выраженные в ARL:Контрольный продукт (тестостерон): 100 Продукты примеров – ARL: Инкубация 24 часа 3 – 6 10 – 5р Формула изобретения
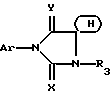 в которой (Н) представляет собой насыщенный гетероциклический радикал, включающий 4 – 7 атомов, и содержащий либо атом кислорода, азота или серы, причем атом азота может быть замещен низшим алкилом, а атом серы может быть окислен, либо два атома кислорода, причем указанный гетероцикл может быть замещен одним или несколькими низшими алкилами; Ar представляет собой фенил, который может быть замещен двумя радикалами, выбранными среди CF3, CN, алкоксила или алкилтионила; Х представляет собой атом кислорода или серы; Y представляет собой атом кислорода или радикал NH; R3 представляет собой атом водорода, низший алкил, который может быть замещен атомом галогена или гидроксильным, свободным или этерифицированным карбоксильным или цианорадикалом, причем указанные продукты могут находиться в любой изомерной, рацемической, энантиомерной и диастереомерной форме, и также аддитивные соли с минеральными и органическими кислотами или минеральными или органическими основаниями вышеуказанных продуктов формулы I. 2. Соединения формулы I по п.1, в которой (Н) представляет собой либо радикал 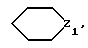 в котором Z1 представляет атом кислорода, серы или радикал -N-R4, в котором R4 выбран среди атома водорода и низшего алкила, циано, либо радикал 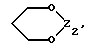 в котором Z2 представляет собой радикал -СН2– с возможностью замещения одним или двумя низшими алкильными радикалами; Ar, X, Y и R3 имеют значения, указанные в п.1, причем указанные продукты формулы I могут находиться в любой изомерной, рацемической, энантиомерной и диастереомерной форме, и также аддитивные соли с минеральными и органическими кислотами или минеральными или органическими основаниями вышеуказанных продуктов формулы I. 3. Соединения формулы I по п.1 или 2, в которой R3 представляет собой атом водорода или низший алкил, который может быть замещен атомом галогена или гидроксильным, или свободным, или этерифицированным карбоксильным радикалом, причем указанные продукты формулы I могут находиться в любой изомерной, рацемической, энантиомерной и диастереомерной форме, и также аддитивные соли с минеральными и органическими кислотами или минеральными или органическими основаниями вышеуказанных продуктов формулы I. 4. Соединения общей формулы I по п.1, отличающиеся тем, что они представляют собой 4-[2,4-диоксо-1-(4-гидроксибутил)-8-окса-1,3-диазаспиро-[4,5]декан-3-ил] -2-(трифторметил)бензонитрил, 4-[2,4-диоксо-1-(2-фторэтил)-8-окса-1,3-диазаспиро[4,5] декан-3-ил] -2-(трифторметил)бензонитрил, 3-[4-циано-3-(трифторметил)фенил]-2,4-диоксо-8-окса-1,3-диазаспиро-[4,5] декан-1-ацетонитрил, 4-[2,4-диоксо-1-(4-гидроксибутил)8-тиа-1,3-диазаспиро-[4,5] декан-3-ил] -2-(трифторметил)бензонитрил. 5. Соединения формулы I, как указано в п.1 или 2, отличающиеся тем, что они обладают антиандрогенной активностью и применяются в качестве лекарственных средств. 6. Соединения формулы I, как указано в п.3, отличающиеся тем, что они обладают антиандрогенной активностью и применяются в качестве лекарственных средств. 7. Соединения формулы I по п.1, отличающиеся тем, что они представляют собой 4-[2,4-диоксо-1-(4-гидроксибутил)-8-окса-1,3-диазаспиро[4,5] декан-3-ил] -2-(трифторметил)бензонитрил, 4-[2,4-диоксо-1-(2-фторэтил)-8-окса-1,3-диазаспиро[4,5]декан-3-ил]-2-(трифторметил)бензонитрил, 3-[4-циано-3-(трифторметил)фенил]-2,4-диоксо-8-окса-1,3-диазаспиро-[4,5] декан-1-ацетонитрил, 4-[2,4-диоксо-1-(4-гидроксибутил)8-тиа-1,3-диазаспиро[4,5] декан-3-ил]-2-(трифторметил)бензонитрил, обладающие антиандрогенной активностью и применяемые в качестве лекарственных средств. 8. Способ получения имидазолинов формулы I как указано в п.1, отличающийся тем, что соединение формулы II Ar – N = C = X, в которой Х и Ar имеют вышеуказанные значения, а возможные функциональные группы могут быть защищены, вводится во взаимодействие с соединением формулы III 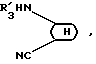 в которой (Н) имеет вышеуказанное значение, а R’3 имеет значение, приведенное выше для R3, в которой возможные функциональные группы могут быть защищены для получения продуктов формулы Ia 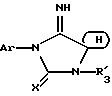 в которой Ar, (H) и R’3 имеют вышеуказанные значения, в присутствии третичного основания и полученный продукт формулы Ia, в которой Ar, (H) и R’3 имеют вышеуказанные значения, при желании и необходимости подвергают любой или нескольким из нижеуказанных реакций в произвольной последовательности: а) реакции выделения возможных защитных групп, которые могут быть включены в R’3, с последующим воздействием, в случае необходимости, агентом этерификации, аминирования или солеобразования; б) реакция гидролиза группы С=NH для получения карбонильной функциональной группы; в) реакции превращения группы С=O в группу C=S; г) реакции превращения группы (групп) C= S в группу С=O; д) когда R’3 представляет собой алкоксиалкильный радикал – реакции превращения R’3 в гидроксиалкильный радикал; е) когда R’3 представляет собой атом водорода – воздействию реактива формулы Hal = R”3, в которой R”3 имеет значения R’3, за исключением значения водорода, а Hal является галогенным атомом, для получения продуктов формулы Iа, как указано выше, в которых R’3 имеет указанное ранее значение. 9. Фармацевтическая композиция, обладающая антиандрогенной активностью, отличающаяся тем, что в качестве действующего начала она содержит по меньшей мере одно соединение формулы I по п.1. RH4A – Выдача дубликата патента Российской Федерации на изобретение
Дата выдачи дубликата: 07.09.2004
Наименование лица, которому выдан дубликат:
Извещение опубликовано: 10.10.2004 БИ: 28/2004
PD4A – Изменение наименования обладателя патента Российской Федерации на изобретение
(73) Новое наименование патентообладателя:
Извещение опубликовано: 10.11.2004 БИ: 31/2004
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 29.09.2006
Извещение опубликовано: 10.01.2008 БИ: 01/2008
|
||||||||||||||||||||||||||
