Патент на изобретение №2170091
|
||||||||||||||||||||||||||
(54) АНТИАЛЛЕРГИЧЕСКОЕ И ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО
(57) Реферат: Изобретение относится к медицине, конкретно к лекарственным средствам, проявляющим антиаллергическое, антиастматическое и противовоспалительное действие. Предложено применение гепатопротектора формулы I в качестве антиаллергического и противовоспалительного средства. 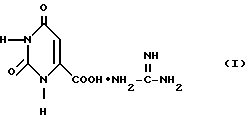 Предложенное средство имеет более низкую токсичность. 2 табл. Изобретение относится к области фармакологии, в частности, к лекарственным средствам, проявляющим антиастматические, противовоспалительные и антиаллергические свойства. Указанные свойства позволяют предполагать возможность применения данного соединения в качестве препарата для базисной терапии ряда аллергических заболеваний: бронхиальной астмы, атонических дерматитов, аллергическиих конъюктивитов и др. Из известных антиаллергических/антиастматических препаратов по типу фармакологических эффектов к заявляемому соединению наиболее близки кромогликат натрия (интал) и глюкокортикостероид будесонид. Кортикостероиды широко используются в качестве противовоаллергических средств при лечении аллергических заболеваний, однако вызывают целый спектр выраженных побочных эффектов, особенно при использовании таблетированных форм, что лимитирует их назначение больным [1,2]. Кромогликат натрия (интал) эффективен только при ингаляционном пути введения и лишь в случае легких проявлений аллергических заболеваний [2] . Известные антигистаминные препараты обладают выраженными побочными эффектами и, кроме того, не оказывают терапевтического действия при бронхиальной астме, аспириновой триаде, астме физического усилия и др. [3]. В связи с этим актуальной является попытка поиска новых соединений в других химических классах, на основе которых можно разработать высокоэффективные и экономически выгодные лекарственные препараты для лечения аллергических заболеваний. Целью предлагаемого изобретения является создание лекарственного средства, обладающего антиаллергическим/антиастматическим, противовоспалительным действием и низкой токсичностью. Поставленная цель достигается применением известного гепатопротектора формулы I: 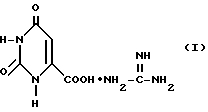 в качестве антиаллергического и противовоспалительного средства. Соединение I относится к классу кислотно-аддитивных солей оротовой кислоты, которое получается по методике, приведенной в патенте РФ N 2047606. В научно-технической и патентной литературе соединение I в качестве антиаллергического и противовоспалительного средства не описано и в медицине не применялось. МЕТОДЫ ИССЛЕДОВАНИЙ И РЕЗУЛЬТАТЫ ИЗУЧЕНИЯ ФАРМАКОЛОГИЧЕСКОГО ДЕЙСТВИЯ СОЕДИНЕНИЯ I 1. Определение острой токсичности Изучена острая токсичность веществ в опытах на белых мышах весом 18-20 г с определением ЛД50 по методу Прозоровского [4] при внутрибрюшинном введении. Наблюдение за животными проводили в течение 48 ч после введения препарата. Результаты исследований показали, что ЛД50 исследуемого соединения больше 4000 мг/кг. Это свидетельствует о низкой токсичности заявляемого соединения. 2. ИЗУЧЕНИЕ АНТИАНАФИЛАКТИЧЕСКОЙ АКТИВНОСТИ СОЕДИНЕНИЯ I НА ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ АНТИГЕН – ИНДУЦИРОВАННОГО СОКРАЩЕНИЯ ГЛАДКИХ МЫШЦ ТРАХЕИ IN VITRO В эксперименте использовались морские свинки весом 350-500 г. Морскую свинку сенсибилизировали внутримышечным введением овальбумина в дозе 10 мкг/кг и 100 мг Al(ОН)3 на свинку. Эксперимент начинали через 3-4 недели от начала сенсибилизации. Препарат изолированной трахеи готовили по Blattner с соавт. [5]. Извлеченную трахею разрезали на кольца по 2 хряща в каждом. Полученные кольца (по 5 штук) соединяли в цепочку и разрезали хрящи. Подготовленную цепочку помещали в термостатируемую камеру, содержащую раствор Кребса-Хенсляйта. Исходная нагрузка на препарат составляла 0,7 г. Сокращение вызывали добавлением в культуральную среду овальбумина в концентрации 1-10 мкг/мл. Исследуемое соединение вносили в концентрации 104--10-9 М на высоте анафилактической контрактуры, когда кривая амплитуды сокращения выходила на плато. Контролем служил максимальный сократительный ответ гладкомышечных клеток препарата трахеи на воздействие гистамином(10-5 М). Величину релаксации гладкомышечного препарата трахеи выражали в процентах от максимальной амплитуды сокращения, вызываемого добавлением в инкубационную среду медиатора. Регистрацию ответа препарата трахеи проводили в изотоническом режиме с помощью механотрона 6МХ2Б и самописца КСП-4. IC50 определяли по методу Личфилда-Вилкоксона. Результаты проведенного исследования (табл. 1) показали, что соединение I обладает существенной релаксирующей активностью на данной модели, превосходящей в условиях данной модели (анафилактическая контрактура) активность теофиллина и кромогликата натрия. 3. ИЗУЧЕНИЕ АНТИАНАФИЛАКТИЧЕСКОЙ АКТИВНОСТИ СОЕДИНЕНИЯ I НА МОДЕЛИ ЭКСПЕРИМЕНТАЛЬНОЙ АСТМЫ IN VIVO В эксперименте использовались морские свинки весом 350-500 г. Животных сенсибилизировали введением овальбумина в дозе 20 мкг/кг овальбумина + 100 мг Al(ОН)3 на свинку по Anderson [6]. Через 21 день после начала сенсибилизации животных наркотизировали этаминалом натрия (40 мг/кг внутрибрюшинно). Разрешающую дозу овальбумина вводили внутривенно (V.jugularis). Исследуемое соединение вводили также внутривенно (1 мг/кг) за 2 -3 мин до внесения разрешающей дозы овальбумина (150-200 мкг/кг). Бронхоспастическую реакцию моделировали по Konzett – Rossler [7]. Аппарат искусственного дыхания, связанный с датчиком (Ugo Basile), с помощью которого регистрировали изменения сопротивления дыхательных путей воздушному потоку, подсоединялся через канюлю к препарированной трахее. Эффект исследуемого соединения оценивали по степени предупреждения бронхоспазма, выраженной в процентах по отношению к контролю. Анализ эффективности соединения проводился в сравнении с кромогликатом динатрия (интал). Полученные данные представлены в табл. 2. 4. ИЗУЧЕНИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТИ СОЕДИНЕНИЯ I НА МОДЕЛИ ОСТРОГО ВОСПАЛЕНИЯ Модель ПАФ-индуцированного отека у крыс по методу Ezeamuzie и Urnezurike [8] В эксперименте были использованы крысы-самцы весом 200-300 г. Полный адъювант Фрейнда (ПАФ) вводили субплантарно по 0,1 мл в правую лапу. Исследуемое соединение вводили внутрижелудочно в дозе 10 мг/кг в 0,5 мл 1%-ного раствора крахмала за 24 и 2 ч до введения флогогенногоагента. Объем лап измерялся через 24 ч после инициации процесса с помощью плетизмометра (Ugo Basile). Терапевтическую эффективность соединения сравнивали с активностью известного противовоспалительного препарата – индометацина. Процент угнетения воспалительной реакции рассчитывали по формуле 1I:  где П – объем правой лапы Опыт – леченые животные; Л – объем левой лапы Контроль – нелеченые животные. Изучаемое соединение оказывало существенное противовоспалительное действие: торможение ПАФ-индуцированного отека составило 56%. Индометацин тормозил отек на 82%, однако вызвал гибель всех получавших внутрижелудочно этот препарат животных. В случае использования исследуемого соединения I не было зарегистрировано ни одного случая гибели животных. 5. ИЗУЧЕНИЕ ПРОТИВОАЛЛЕРГИЧЕСКОЙ АКТИВНОСТИ СОЕДИНЕНИЯ I В эксперименте были использованы линейные мыши-самцы СВА массой 18-20 г. В качестве аллергена применяли пикрилхлорид и эритроциты барана. Исследуемое соединение вводили внутрижелудочно три раза в дозе 10 мг/кг в 0,5 мл 1%-ного раствора крахмала за 24, 2 ч до и 2 ч после введения разрешающей дозы аллергена. Количество животных в каждой группе составляло 10-12. Терапевтическую эффективность изучаемого соединения сравнивали с действием эталонного глюкокортикостероидного препарата будесонида. Торможение развития аллергического отека вычисляли по формуле II. 5.1. МОДЕЛЬ КОНТАКТНОЙ ГИПЕРЧУВСТВИТЕЛЬНОСТИ К ПИКРИЛХЛОРИДУ У МЫШЕЙ ПО МЕТОДУ Taraure(9) Мышей сенсибилизировали нанесением на выбритый участок живота, 1 мл 3%-ного раствора пикрилхлорида в ацетоне. Через 7 суток разрешающую дозу пикрилхлорида (0,025 мл 3%-ного раствора) наносили на обе поверхности правого уха. Через 24 ч после индукции отека мышей забивали, уши отрезали и взвешивали. Аллергическую реакцию оценивали по изменению веса правого уха относительно интактного левого. Противоаллергический эффект исследуемого соединения изучали, анализируя разницу увеличения веса правого уха у леченых и нелеченых животных согласно формуле II. Торможение развития отека правого уха у леченых животных составило 63  5,5%; у будесонида при внутрижелудочном введении в условиях данной модели эффект был также значителен и составил 73 5,5%; у будесонида при внутрижелудочном введении в условиях данной модели эффект был также значителен и составил 73  8,9%.
5.2. МОДЕЛЬ ГИПЕРЧУВСТВИТЕЛЬНОСТИ ЗАМЕДЛЕННОГО ТИПА К ЭРИТРОЦИТАМ БАРАНА У МЫШЕЙ ПО МЕТОДУ Lagrange (10) 8,9%.
5.2. МОДЕЛЬ ГИПЕРЧУВСТВИТЕЛЬНОСТИ ЗАМЕДЛЕННОГО ТИПА К ЭРИТРОЦИТАМ БАРАНА У МЫШЕЙ ПО МЕТОДУ Lagrange (10)Мышей сенсибилизировали введением 0,1 мл (2  107) суспензии эритроцитов подкожно. Через 4 суток разрешающую дозу эритроцитов барана (1 107) суспензии эритроцитов подкожно. Через 4 суток разрешающую дозу эритроцитов барана (1 108) в 0,04 мл вводили субплантарно в правую лапу. Через 24 ч измеряли отек лапы с помощью плетизмометра (Ugo Basile). Терапевтический эффект оценивали по разнице объемов лап (правой и левой) с воспалительным отеком у леченых и нелеченых животных. Торможение развития реакции вычисляли согласно формуле II. Противоаллергический эффект для 1 составил 67 108) в 0,04 мл вводили субплантарно в правую лапу. Через 24 ч измеряли отек лапы с помощью плетизмометра (Ugo Basile). Терапевтический эффект оценивали по разнице объемов лап (правой и левой) с воспалительным отеком у леченых и нелеченых животных. Торможение развития реакции вычисляли согласно формуле II. Противоаллергический эффект для 1 составил 67  3,9% и был сопоставим с эффектом препарата сравнения (кромогликата натрия), который вызвал торможение аллергического ответа на введение антиген, равное 63 3,9% и был сопоставим с эффектом препарата сравнения (кромогликата натрия), который вызвал торможение аллергического ответа на введение антиген, равное 63  4,6% (относительно контроля).
Таким образом, заявляемое соединение обладает антиаллергическим антиастматическим, противовоспалительным действием, сопоставимым в условиях использованных экспериментальных моделей по величине эффекта традиционным лекарственным препаратам с антиаллергическим и антиастматическим действием.
Лтература 4,6% (относительно контроля).
Таким образом, заявляемое соединение обладает антиаллергическим антиастматическим, противовоспалительным действием, сопоставимым в условиях использованных экспериментальных моделей по величине эффекта традиционным лекарственным препаратам с антиаллергическим и антиастматическим действием.
Лтература1. Чучалин А.Г. Бронхиальная астма. В 2-х томах. М., Агар, 1997. 2. Barnes P.J. Glucocorticosteroids. In: Allergy and Allergic Disieses. Ed.by A.B.Kay BlacbveU Science. Oxford. 1997, V.I, 619-641. 3. Гущин И. С. Алллергическое воспаление и его фармакологический контроль. Москва, Фармарус Принт. 1998, с. 141-172. 4. Прозоровский В.Б., Прозоровская М.П. Табличный метод определения ЕД50 веществ с низкой биологической активностью. Фармакология и токсикология, 1980, 6, 733-735. 5. Blattner R., Classen H.G., Dehnert H. et al. Experiments on isolated smooth muscle preparation. Ed. J.M. Barnden a. R.Colson, 1980. 6. Andersson P. Antigen-induced bronchiaal anapylaxis in actively sensitized guineapigs. Allergy 1980, 35, 63-71. 7. Konzett H., Rossler, R. Versuchsanord nung zu untersuchungen an der Bronchialmuskulatur. Naunyn-Schmiedebergs Arch. Exp. Path. Pharmak., 1940, 195, 71-74. 8. Ezamuzie Ch, Urnezurike C.C. Effect ofhistamine H2-receptor antagonists on acute inflammatory of the rat paw oedema. J.Pharmacol., 1989, 41, 261-265. 9. Tarayre J.P., Barbara M., Aliaga М. and Tisne-Versailles. Comparative actions of immunosuppressants, glucocorticoids and non-steroidal anti- inflammatory drugs on various models of delayed hypersensitivity and on a non-immune inflammation in mice. Arzneim.-Forsch. Drug Res., 1990, 40, 1125-1131. 10. Lagrange Ph. Mecanismes de regulation de l’activite des cellules lymphocytaries T: applications a la pathologie infectieuse et tumorale. I. – Hypersensibilite de type retarde et reponse humorale. Pathologie Biologie. 1976, January, 67-73. Формула изобретения
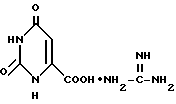 в качестве антиаллергического и противовоспалительного средства. РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 28.07.2008
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
