Патент на изобретение №2169142
|
||||||||||||||||||||||||||
(54) АНАЛОГИ ВИТАМИНА D, СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБЫ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ
(57) Реферат: Изобретение относится к аналогам витамина D формулы I, в которой Q представляет собой С1-С8 гидрокарбиленовый бирадикал; R представляет собой С1-С6 гидрокарбид; выражение гидрокарбид (гидрокарбилен) обозначает радикал (бирадикал), полученный после удаления 1 (2) атома(ов) водорода из неразветвленного, разветвленного или циклического, насыщенного или ненасыщенного углеводорода, или в которой две группы R, взятые вместе с атомом углерода, несущим гидроксильную группу, могут образовывать С3-С8 карбоциклическое кольцо. Описывается также способ их получения, а также способы получения используемых промежуточных продуктов. Соединения обладают иммуномодулирующим и антивоспалительным действием, а также проявляют высокую активность в индуцировании дифференциации и ингибировании нежелательной пролиферации клеток, включая клетки кожи и раковые клетки. 4 с. и 5 з.п.ф-лы, 3 табл. 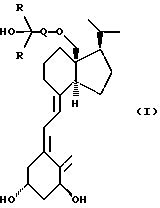
Изобретение относится к ранее неизвестному классу соединений, обладающих иммуномодулирующим и антивоспалительным эффектами, а также проявляющих высокую активность в индуцировании дифференциации и ингибировании нежелательной пролиферации (разрастания) некоторых клеток, включая клетки кожи и раковые клетки. Данное изобретение относится также к фармацевтическим препаратам, содержащим эти соединения, к стандартным дозам этих препаратов и к их применению в лечении и профилактике гиперпаратиреоза, особенно вторичного гиперпаратиреоза, связанного с почечной недостаточностью, для способствования остеогенезу и лечению остеопороза, для лечения неврологических дисфункций, таких как заболевание Альцгеймера, и ряда патологических состояний, включающих сахарный диабет, артериальную гипертонию, угри, облысение, старение кожи, дисбаланс в иммунной системе, для лечения воспалительных заболеваний, таких как ревматоидный артрит и астма, а также заболеваний, характеризующихся аномальной дифференциацией и/или пролиферацией клеток, таких как псориаз и раковые заболевания. Соединения настоящего изобретения представлены общей формулой 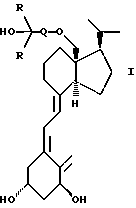 где Q представляет собой C1-C8 гидрокарбиленовый бирадикал, R представляет собой водород или C1-C6 гидрокарбил, или две группы R, взятые вместе с атомом углерода, несущим гидроксильную группу, могут образовывать 3-C8 карбоциклическое кольцо. Предпочтительными соединениями формулы I являются те, в которых Q представляет собой C3-C5 гидрокарбиленовый бирадикал. Более предпочтительными соединениями являются те, в которых Q представляет собой (CH2)n, CH  C-(CH2)n-1, где n = 3, 4 или 5, а R представляет собой метил или этил.
В контексте данного изобретения выражение гидрокарбил (гидрокарбилен) обозначает радикал (бирадикал), полученный в результате удаления 1 (2) атома(ов) водорода, из неразветвленного, разветвленного или циклического, насыщенного или ненасыщенного углеводорода.
Примеры R включают, но не ограничиваясь ими, водород, метильную. трифторметильную, этильную, винильную, н-, изо- и циклопропильную и пропен-2-ильную группы.
Примеры двух R групп, когда они взяты вместе, включают ди-, три-, тетра- и пентаметилен. Примеры Q включают, но не ограничиваясь ими, следующие группы: ди-, три-, тетра-, пента- и гексаметилен, -CH=CH-CH2-, -CH2-CH=CH-CH2-, – CH-CH-СН2CH2-, -C C-(CH2)n-1, где n = 3, 4 или 5, а R представляет собой метил или этил.
В контексте данного изобретения выражение гидрокарбил (гидрокарбилен) обозначает радикал (бирадикал), полученный в результате удаления 1 (2) атома(ов) водорода, из неразветвленного, разветвленного или циклического, насыщенного или ненасыщенного углеводорода.
Примеры R включают, но не ограничиваясь ими, водород, метильную. трифторметильную, этильную, винильную, н-, изо- и циклопропильную и пропен-2-ильную группы.
Примеры двух R групп, когда они взяты вместе, включают ди-, три-, тетра- и пентаметилен. Примеры Q включают, но не ограничиваясь ими, следующие группы: ди-, три-, тетра-, пента- и гексаметилен, -CH=CH-CH2-, -CH2-CH=CH-CH2-, – CH-CH-СН2CH2-, -C C-CH2, -CH2-C C-CH2, -CH2-C C-CH2-, -C C-CH2-, -C C-CH2-CH2– и o-, м- и n-(С6H4)-CH2-.
Особенно предпочтительны следующие группы: R = метил или этил и Q = метилен, этилен, три-, тетраметилен, -C C-CH2-CH2– и o-, м- и n-(С6H4)-CH2-.
Особенно предпочтительны следующие группы: R = метил или этил и Q = метилен, этилен, три-, тетраметилен, -C C-CH2-. C-CH2-.Показано, что 1  ,25-дигидрокси-витамин D3 (1,25 (ОН2)2D3) оказывает влияние на действия и/или производство интерлейкинов (К. Muller et al., Immunol. lett. , 17, (1988), 361-366), что определяет возможность использования этого соединения в лечении заболеваний, характеризующихся дисфункциями иммунной системы, например аутоиммунных заболеваний, СПИДа, реакций организма-хозяина против трансплантата, и отторжения трансплантата или других состояний, характеризующихся аномальной продукцией интерлейкина-1, например воспалительных заболеваний, таких как ревматоидный артрит и астма. Были описаны потенциальные иммунологические свойства аналогов витамина D (L. Binderup, Biochem. Pharmacol., 43, (1992) 1885-1892).
Было показано также, что 1,25(ОН)2D3 способны стимулировать дифференциацию клеток и ингибировать избыточную клеточную пролиферацию (Е.Abe et al. , Proc. Natl. Acad. Sci., USA., 78, (1981), 4990-4994), что позволило предположить, что это соединение может быть полезным при лечении заболеваний, характеризующихся аномальной клеточной дифференциацией и/или пролиферацией, таких как лейкемия, миелофиброз и псориаз.
Кроме того, предполагают возможность использования 1,25(ОН)2D3 или его пролекарства 1 ,25-дигидрокси-витамин D3 (1,25 (ОН2)2D3) оказывает влияние на действия и/или производство интерлейкинов (К. Muller et al., Immunol. lett. , 17, (1988), 361-366), что определяет возможность использования этого соединения в лечении заболеваний, характеризующихся дисфункциями иммунной системы, например аутоиммунных заболеваний, СПИДа, реакций организма-хозяина против трансплантата, и отторжения трансплантата или других состояний, характеризующихся аномальной продукцией интерлейкина-1, например воспалительных заболеваний, таких как ревматоидный артрит и астма. Были описаны потенциальные иммунологические свойства аналогов витамина D (L. Binderup, Biochem. Pharmacol., 43, (1992) 1885-1892).
Было показано также, что 1,25(ОН)2D3 способны стимулировать дифференциацию клеток и ингибировать избыточную клеточную пролиферацию (Е.Abe et al. , Proc. Natl. Acad. Sci., USA., 78, (1981), 4990-4994), что позволило предположить, что это соединение может быть полезным при лечении заболеваний, характеризующихся аномальной клеточной дифференциацией и/или пролиферацией, таких как лейкемия, миелофиброз и псориаз.
Кроме того, предполагают возможность использования 1,25(ОН)2D3 или его пролекарства 1 -OH-D3 для лечения артериальной гипертонии (L. Lind et al., Acta Med. Scand., 222, (1987), 423-427) и сахарного диабета (S. Inomata et al. , Bone Mineral. , 1, (1986), 187-192). Другое применение 1,25(OH)2D3 предполагается на основе последних данных, продемонстрировавших связь между наследственной невосприимчивостью к витамину D и облысением: обработка 1,25(ОН)2D3 может стимулировать рост волос (Editorial, Lancet, March 4, (1989), p. 478). Кроме того, тот факт, что местное применение 1,25(OH)2D3 уменьшает размер сальных желез в ушах самцов сирийских хомяков, демонстрирует, что это соединение может быть полезным для лечения угрей (V.L.Malloy et al. , The Tricontinental Meeting for Investigative Dermatology, Washington, (1989)).
Однако возможности терапевтического применения в таких показаниях сильно ограничены из-за хорошо известной способности 1,25(ОН)2D3 оказывать сильное влияние на кальциевый метаболизм; повышенные концентрации в крови будут быстро давать увеличение гиперкальциемии. Таким образом, это соединение и некоторые из его сильнодействующих синтетических аналогов не вполне удовлетворяют требованиям для использования в качестве лекарственных препаратов в лечении таких заболеваний, как например псориазы, лейкемия или иммунные заболевания, когда требуется постоянное введение относительно высоких доз лекарства.
Недавно было показано, что ряд аналогов витамина D проявляет некоторую селективность в пользу индуцирования клеточной дифференциации/ингибирования клеточной пролиферации по сравнению с влиянием на метаболизм кальция.
Результаты недавних исследований (K.W. Colston et al., Biochem. Pharmacol. , 44, (1992) 693-702 and I.S. Mathiasen et al., Steroid Biochem. Molec. Biol., 46, (1993), 365-371) подтверждают концепцию, что производные витамина D могут ингибировать клеточную пролиферацию при раке молочной железы in vivo.
Соединения настоящего изобретения структурно отличаются от любых известных аналогов витамина D. Все аналоги витамина D, проявляющие биологическую активность по крайней мере такого же порядка величины, как 1,25(ОН)2D3, имеют боковую цепь из по крайней мере четырех последовательных атомов, присоединенных к C-17. В соединениях настоящего изобретения боковая цепь при C-17 уменьшена до 2-пропильной группы, то есть в каркасе боковой цепи существуют только два последовательно соединенных атома. Новые боковые цепи присоединены к C-18, как описано в формуле I. Соединения этого типа не являются сходными с любыми известными соединениями, обладающими похожей активностью витамина D, и предсказание их биологической активности невозможно. Такие радикальные изменения в структуре витамина D обычно ведут к полной потере биологической активности.
Является удивительным, что эти соединения биологически активны и проявляют благоприятную селективность. Соединения изобретения показывают благоприятные антипролиферативные и индуцирующие дифференциацию свойства на клетках U937 и HaCaT (выше, чем у 1,25(ОН)2D3) и очень низкий кальцеурический эффект на крысах (<5% от эффекта, вызываемого 1,25(ОН)2D3).
Соединения данного изобретения пригодны как для местного, так и общего лечения и профилактики заболеваний человека и животных, которые характеризуются аномальной клеточной пролиферацией и/или клеточной дифференциацией, такие как некоторые дерматологические заболевания, включающие псориазы и некоторые виды рака, и/или заболеваний, характеризующихся дисбалансом в иммунной системе, например аутоиммунных заболеваний, включая сахарный диабет, реакции организма-хозяина против трансплантата и отторжение трансплантатов. Соединения изобретения также пригодны для лечения неврологических дисфункций, таких как болезнь Альцгеймера, и для лечения воспалительных заболеваний, таких как ревматоидный артрит и астма. Соединения изобретения могут также применяться для лечения угрей, облысения и гипертензии. В заключение, так как после местного лечения соединениями данного изобретения наблюдается утолщение кожи, эти соединения могут применяться для лечения или профилактики атрофии и старения кожи, включая процессы старения, спровоцированные действием света.
Из-за низкой тенденции этих соединений вызывать гиперкальцемию при продолжительном применении их можно применять при длительном лечении гиперпаратиреоза (особенно вторичного гиперпаратиреоза, связанного с почечной недостаточностью) и для стимуляции остеогенеза и лечения остеопороза.
Данные соединения можно использовать в комбинации с другими фармацевтическими препаратами. При профилактике отторжения трансплантата и реакции трансплантата против организма-хозяина лечение с помощью соединений настоящего изобретения можно полезно сочетать с лечением, например, циклоспорином А.
Соединения формулы I могут быть подходяще получены из 20S-(4-метилфенилсульфонилоксиметил)- де-A, B-прегнан-(8S)-ола (В. Lythgoe, D.A. Roberts and I. Water-house, J. Chem. Soc. Perkin I. (1977), 2608-2612) с помощью реакций, указанных на схемах 1 и 2, приведенных в конце описания.
Когда Q представляет собой -CH2-C -OH-D3 для лечения артериальной гипертонии (L. Lind et al., Acta Med. Scand., 222, (1987), 423-427) и сахарного диабета (S. Inomata et al. , Bone Mineral. , 1, (1986), 187-192). Другое применение 1,25(OH)2D3 предполагается на основе последних данных, продемонстрировавших связь между наследственной невосприимчивостью к витамину D и облысением: обработка 1,25(ОН)2D3 может стимулировать рост волос (Editorial, Lancet, March 4, (1989), p. 478). Кроме того, тот факт, что местное применение 1,25(OH)2D3 уменьшает размер сальных желез в ушах самцов сирийских хомяков, демонстрирует, что это соединение может быть полезным для лечения угрей (V.L.Malloy et al. , The Tricontinental Meeting for Investigative Dermatology, Washington, (1989)).
Однако возможности терапевтического применения в таких показаниях сильно ограничены из-за хорошо известной способности 1,25(ОН)2D3 оказывать сильное влияние на кальциевый метаболизм; повышенные концентрации в крови будут быстро давать увеличение гиперкальциемии. Таким образом, это соединение и некоторые из его сильнодействующих синтетических аналогов не вполне удовлетворяют требованиям для использования в качестве лекарственных препаратов в лечении таких заболеваний, как например псориазы, лейкемия или иммунные заболевания, когда требуется постоянное введение относительно высоких доз лекарства.
Недавно было показано, что ряд аналогов витамина D проявляет некоторую селективность в пользу индуцирования клеточной дифференциации/ингибирования клеточной пролиферации по сравнению с влиянием на метаболизм кальция.
Результаты недавних исследований (K.W. Colston et al., Biochem. Pharmacol. , 44, (1992) 693-702 and I.S. Mathiasen et al., Steroid Biochem. Molec. Biol., 46, (1993), 365-371) подтверждают концепцию, что производные витамина D могут ингибировать клеточную пролиферацию при раке молочной железы in vivo.
Соединения настоящего изобретения структурно отличаются от любых известных аналогов витамина D. Все аналоги витамина D, проявляющие биологическую активность по крайней мере такого же порядка величины, как 1,25(ОН)2D3, имеют боковую цепь из по крайней мере четырех последовательных атомов, присоединенных к C-17. В соединениях настоящего изобретения боковая цепь при C-17 уменьшена до 2-пропильной группы, то есть в каркасе боковой цепи существуют только два последовательно соединенных атома. Новые боковые цепи присоединены к C-18, как описано в формуле I. Соединения этого типа не являются сходными с любыми известными соединениями, обладающими похожей активностью витамина D, и предсказание их биологической активности невозможно. Такие радикальные изменения в структуре витамина D обычно ведут к полной потере биологической активности.
Является удивительным, что эти соединения биологически активны и проявляют благоприятную селективность. Соединения изобретения показывают благоприятные антипролиферативные и индуцирующие дифференциацию свойства на клетках U937 и HaCaT (выше, чем у 1,25(ОН)2D3) и очень низкий кальцеурический эффект на крысах (<5% от эффекта, вызываемого 1,25(ОН)2D3).
Соединения данного изобретения пригодны как для местного, так и общего лечения и профилактики заболеваний человека и животных, которые характеризуются аномальной клеточной пролиферацией и/или клеточной дифференциацией, такие как некоторые дерматологические заболевания, включающие псориазы и некоторые виды рака, и/или заболеваний, характеризующихся дисбалансом в иммунной системе, например аутоиммунных заболеваний, включая сахарный диабет, реакции организма-хозяина против трансплантата и отторжение трансплантатов. Соединения изобретения также пригодны для лечения неврологических дисфункций, таких как болезнь Альцгеймера, и для лечения воспалительных заболеваний, таких как ревматоидный артрит и астма. Соединения изобретения могут также применяться для лечения угрей, облысения и гипертензии. В заключение, так как после местного лечения соединениями данного изобретения наблюдается утолщение кожи, эти соединения могут применяться для лечения или профилактики атрофии и старения кожи, включая процессы старения, спровоцированные действием света.
Из-за низкой тенденции этих соединений вызывать гиперкальцемию при продолжительном применении их можно применять при длительном лечении гиперпаратиреоза (особенно вторичного гиперпаратиреоза, связанного с почечной недостаточностью) и для стимуляции остеогенеза и лечения остеопороза.
Данные соединения можно использовать в комбинации с другими фармацевтическими препаратами. При профилактике отторжения трансплантата и реакции трансплантата против организма-хозяина лечение с помощью соединений настоящего изобретения можно полезно сочетать с лечением, например, циклоспорином А.
Соединения формулы I могут быть подходяще получены из 20S-(4-метилфенилсульфонилоксиметил)- де-A, B-прегнан-(8S)-ола (В. Lythgoe, D.A. Roberts and I. Water-house, J. Chem. Soc. Perkin I. (1977), 2608-2612) с помощью реакций, указанных на схемах 1 и 2, приведенных в конце описания.
Когда Q представляет собой -CH2-C C-CH2– и -C C-CH2– и -C C-CH2-CH2-, то предпочтительны схемы, обозначенные на схемах 3 и 4, приведенных в конце описания, для соединений общей формулы III и II соответственно.
В описании данного изобретения используют следующие стандартные аббревиатуры: 18-Crown-6 = 1,4,7,10,13,16- гексаоксациклооктадекан; DMF = N,N-диметилформамид; Et = этил; “HF” = 5% раствор фтористого водорода в смеси ацетонитрил: вода (7: 1, об/об); LAU = алюмогидрид лития; Me = метил; ЯМР = ядерный магнитный резонанс; PDC = бихромат пиридиния; PPTS = толуол-4-сульфонат пиридиния; Pr = пропил; к.т. = комнатная температура; TBAF = тригидрат фторида тетра-н-бутиламмония; TBDMS = трет-бутилдиметилсилил; THF = тетрагидрофуран; THP = тетрагидро-4Н-пиран-2-ил; TMS = триметилсилил; TSO = толуол-4-сульфонилокси.
Синтезы соединений 801-805 описаны в способах получения 1-5.
Синтезы соединений 806-808 описаны в способах получения 71, 42 и 67.
Синтезы соединений 809-812 описаны в способах получения 72-75.
Соединения общей формулы VII, YO-CR2-Q-X, даны в табл. А.
Соединения данного изобретения предназначены для использования в фармацевтических композициях, которые полезны для лечения заболеваний человека и животных, как описано выше.
Количество соединения формулы I (в дальнейшем именуемое как активный ингредиент), необходимое для терапевтического эффекта, несомненно будет варьироваться в зависимости от конкретного соединения, метода введения и вида млекопитающего. Соединения изобретения могут быть введены парентерально, внутрисуставно, энтерально или местно. Они хорошо поглощаются при энтеральном введении, и этот метод введения является предпочтительным при лечении общих заболеваний. При лечении дерматологических заболеваний, таких как псориаз или глазные заболевания, предпочтительными являются местная или энтеральная формы.
При лечении респираторных заболеваний, таких как астма, аэрозольная форма является предпочтительной.
Несмотря на то что активный ингредиент может вводиться только в виде неочищенного химического соединения, предпочтительным является, чтобы он присутствовал в виде фармацевтического препарата. Обычно активный ингредиент составляет 0,1 части на млн (ppm) до 0,1% веса препарата.
Под термином “стандартная доза” подразумевают единичную, т.е. однократную дозу, которая может быть введена пациенту и может быть легко расфасована, оставаясь в виде физически и химически стабильной стандартной дозы, содержащей либо активное вещество как таковое, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Композиции настоящего изобретения как для использования в ветеринарии, так и в медицине включают активный ингредиент в сочетании с фармацевтически приемлемым носителем и, необязательно, с другими терапевтическими ингредиентами(ом). Носитель(ли) должен быть “приемлемым” в смысле совместимости с другими ингредиентами композиции и не оказывать вредного воздействия на реципиента.
Композиции включают, например, композиции в форме, удобной для перорального, ректального, парентерального (в том числе подкожного, внутримышечного и внутривенного), внутрисуставного и местного применения.
Композиции могут быть представлены в форме стандартной дозы и приготовлены любым способом, хорошо известным в фармацевтике. Все методы включают стадию введения активного ингредиента в ассоциацию с носителем, который составляет один или более вспомогательных ингредиентов. Обычно композиции готовят путем равномерного и однородного введения активного ингредиента в ассоциацию с жидким носителем или тонко измельченным твердым носителем, или с обоими, и затем, по необходимости, придают продукту требуемую препаративную форму.
Композиции настоящего изобретения, пригодные для перорального введения, могут быть в форме раздельных единиц, таких как капсулы, саше, таблетки или лепешки, каждая содержащая заданное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной или безводной жидкости; или в виде эмульсий масло-в-воде или вода-в-масле. Активный ингредиент можно также вводить в виде шариков, лекарственной кашки или пасты.
Таблетки могут быть приготовлены прессованием или формованием активного ингредиента, необязательно с одним или более вспомогательными ингредиентами. Прессованные таблетки могут быть приготовлены путем сжимания в подходящей машине активного ингредиента в свободно-текучей форме, такой как порошок или гранулы, необязательно смешанного со связующим веществом, смазкой, инертным разбавителем, поверхностно-активным или диспергирующим агентом. Формованные таблетки могут быть приготовлены путем формования в подходящей машине смеси порошкообразного активного ингредиента и подходящего носителя, увлажненных инертным жидким разбавителем.
Композиции для ректального введения могут быть в виде свечей, включающих активный ингредиент и носитель такой, как кокосовое масло, или в форме клизмы.
Композиции, пригодные для парентерального введения, обычно включают в себя стерильные масляные или водные препараты активного ингредиента, которые являются предпочтительно изотоническими с кровью реципиента.
Композиции, пригодные для внутрисуставного введения, могут быть в виде стерильных водных препаратов активного ингредиента, который может находиться в микрокристаллической форме, например в виде водной микрокристаллической суспензии. Для внутрисуставного введения активного ингредиента, а также в случае его применения в офтальмологии, могут также использоваться липосомные композиции или биоразлагаемые полимерные системы.
Композиции, пригодные для местного применения, в том числе для лечения глаз, включают жидкие или полужидкие препараты, такие как линименты (жидкие мази), лосьоны, гели, накладки, масло-в-воде или вода-в-масле эмульсии, такие как кремы, мази или пасты, или растворы или суспензии, такие как капли.
В дополнение к вышеупомянутым ингредиентам композиции данного изобретения могут включать один или более дополнительных ингредиентов, таких как разбавители, буферы, ароматизирующие агенты, связующие вещества, поверхностно-активные агенты, загустители, смазки, консерванты, например метилгидроксибензоат (включая антиоксиданты), эмульгирующие агенты и подобные. Композиции могут дополнительно содержать другие терапевтически активные соединения, обычно используемые в лечении вышеупомянутых патологических состояний.
Настоящее изобретение касается также способа лечения пациентов, страдающих от одного из вышеперечисленных патологических состояний, упомянутый способ состоит из введения пациенту, нуждающемуся в лечении, эффективного количества одного или более соединений формулы I, одного или в сочетании с одним или более другими терапевтически активными соединениями, обычно применяемыми в лечении упомянутых патологических состояний. Лечение с помощью настоящих соединений и/или с дополнительными терапевтически активными соединениями может быть одновременным или с интервалами.
При лечении общих заболеваний вводят суточные дозы от 0,1 до 100 мкг, предпочтительно от 0,2 до 25 мкг соединения формулы I. При местном лечении кожных заболеваний применяют мази, кремы или лосьоны, содержащие от 0,1 до 500 мкг/г, предпочтительно от 1 до 100 мкг/г соединения формулы I. Для местного применения в офтальмологии применяют мази, капли или гели, содержащие от 0,1 до 500 мкг/г, предпочтительно от 1 до 100 мкг/г соединения формулы I. Композиции для перорального введения, составленные предпочтительно в виде таблеток, капель или капсул, содержат от 0,05 до 50 мкг, предпочтительно от 0,1 до 25 мкг соединения формулы I на стандартную дозу.
Далее изобретение иллюстрируют с помощью нижеследующих общих методик, способов получения и примеров, не ограничивающих предмет настоящего изобретения.
Общие методики, способы получения и примеры C-CH2-CH2-, то предпочтительны схемы, обозначенные на схемах 3 и 4, приведенных в конце описания, для соединений общей формулы III и II соответственно.
В описании данного изобретения используют следующие стандартные аббревиатуры: 18-Crown-6 = 1,4,7,10,13,16- гексаоксациклооктадекан; DMF = N,N-диметилформамид; Et = этил; “HF” = 5% раствор фтористого водорода в смеси ацетонитрил: вода (7: 1, об/об); LAU = алюмогидрид лития; Me = метил; ЯМР = ядерный магнитный резонанс; PDC = бихромат пиридиния; PPTS = толуол-4-сульфонат пиридиния; Pr = пропил; к.т. = комнатная температура; TBAF = тригидрат фторида тетра-н-бутиламмония; TBDMS = трет-бутилдиметилсилил; THF = тетрагидрофуран; THP = тетрагидро-4Н-пиран-2-ил; TMS = триметилсилил; TSO = толуол-4-сульфонилокси.
Синтезы соединений 801-805 описаны в способах получения 1-5.
Синтезы соединений 806-808 описаны в способах получения 71, 42 и 67.
Синтезы соединений 809-812 описаны в способах получения 72-75.
Соединения общей формулы VII, YO-CR2-Q-X, даны в табл. А.
Соединения данного изобретения предназначены для использования в фармацевтических композициях, которые полезны для лечения заболеваний человека и животных, как описано выше.
Количество соединения формулы I (в дальнейшем именуемое как активный ингредиент), необходимое для терапевтического эффекта, несомненно будет варьироваться в зависимости от конкретного соединения, метода введения и вида млекопитающего. Соединения изобретения могут быть введены парентерально, внутрисуставно, энтерально или местно. Они хорошо поглощаются при энтеральном введении, и этот метод введения является предпочтительным при лечении общих заболеваний. При лечении дерматологических заболеваний, таких как псориаз или глазные заболевания, предпочтительными являются местная или энтеральная формы.
При лечении респираторных заболеваний, таких как астма, аэрозольная форма является предпочтительной.
Несмотря на то что активный ингредиент может вводиться только в виде неочищенного химического соединения, предпочтительным является, чтобы он присутствовал в виде фармацевтического препарата. Обычно активный ингредиент составляет 0,1 части на млн (ppm) до 0,1% веса препарата.
Под термином “стандартная доза” подразумевают единичную, т.е. однократную дозу, которая может быть введена пациенту и может быть легко расфасована, оставаясь в виде физически и химически стабильной стандартной дозы, содержащей либо активное вещество как таковое, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Композиции настоящего изобретения как для использования в ветеринарии, так и в медицине включают активный ингредиент в сочетании с фармацевтически приемлемым носителем и, необязательно, с другими терапевтическими ингредиентами(ом). Носитель(ли) должен быть “приемлемым” в смысле совместимости с другими ингредиентами композиции и не оказывать вредного воздействия на реципиента.
Композиции включают, например, композиции в форме, удобной для перорального, ректального, парентерального (в том числе подкожного, внутримышечного и внутривенного), внутрисуставного и местного применения.
Композиции могут быть представлены в форме стандартной дозы и приготовлены любым способом, хорошо известным в фармацевтике. Все методы включают стадию введения активного ингредиента в ассоциацию с носителем, который составляет один или более вспомогательных ингредиентов. Обычно композиции готовят путем равномерного и однородного введения активного ингредиента в ассоциацию с жидким носителем или тонко измельченным твердым носителем, или с обоими, и затем, по необходимости, придают продукту требуемую препаративную форму.
Композиции настоящего изобретения, пригодные для перорального введения, могут быть в форме раздельных единиц, таких как капсулы, саше, таблетки или лепешки, каждая содержащая заданное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной или безводной жидкости; или в виде эмульсий масло-в-воде или вода-в-масле. Активный ингредиент можно также вводить в виде шариков, лекарственной кашки или пасты.
Таблетки могут быть приготовлены прессованием или формованием активного ингредиента, необязательно с одним или более вспомогательными ингредиентами. Прессованные таблетки могут быть приготовлены путем сжимания в подходящей машине активного ингредиента в свободно-текучей форме, такой как порошок или гранулы, необязательно смешанного со связующим веществом, смазкой, инертным разбавителем, поверхностно-активным или диспергирующим агентом. Формованные таблетки могут быть приготовлены путем формования в подходящей машине смеси порошкообразного активного ингредиента и подходящего носителя, увлажненных инертным жидким разбавителем.
Композиции для ректального введения могут быть в виде свечей, включающих активный ингредиент и носитель такой, как кокосовое масло, или в форме клизмы.
Композиции, пригодные для парентерального введения, обычно включают в себя стерильные масляные или водные препараты активного ингредиента, которые являются предпочтительно изотоническими с кровью реципиента.
Композиции, пригодные для внутрисуставного введения, могут быть в виде стерильных водных препаратов активного ингредиента, который может находиться в микрокристаллической форме, например в виде водной микрокристаллической суспензии. Для внутрисуставного введения активного ингредиента, а также в случае его применения в офтальмологии, могут также использоваться липосомные композиции или биоразлагаемые полимерные системы.
Композиции, пригодные для местного применения, в том числе для лечения глаз, включают жидкие или полужидкие препараты, такие как линименты (жидкие мази), лосьоны, гели, накладки, масло-в-воде или вода-в-масле эмульсии, такие как кремы, мази или пасты, или растворы или суспензии, такие как капли.
В дополнение к вышеупомянутым ингредиентам композиции данного изобретения могут включать один или более дополнительных ингредиентов, таких как разбавители, буферы, ароматизирующие агенты, связующие вещества, поверхностно-активные агенты, загустители, смазки, консерванты, например метилгидроксибензоат (включая антиоксиданты), эмульгирующие агенты и подобные. Композиции могут дополнительно содержать другие терапевтически активные соединения, обычно используемые в лечении вышеупомянутых патологических состояний.
Настоящее изобретение касается также способа лечения пациентов, страдающих от одного из вышеперечисленных патологических состояний, упомянутый способ состоит из введения пациенту, нуждающемуся в лечении, эффективного количества одного или более соединений формулы I, одного или в сочетании с одним или более другими терапевтически активными соединениями, обычно применяемыми в лечении упомянутых патологических состояний. Лечение с помощью настоящих соединений и/или с дополнительными терапевтически активными соединениями может быть одновременным или с интервалами.
При лечении общих заболеваний вводят суточные дозы от 0,1 до 100 мкг, предпочтительно от 0,2 до 25 мкг соединения формулы I. При местном лечении кожных заболеваний применяют мази, кремы или лосьоны, содержащие от 0,1 до 500 мкг/г, предпочтительно от 1 до 100 мкг/г соединения формулы I. Для местного применения в офтальмологии применяют мази, капли или гели, содержащие от 0,1 до 500 мкг/г, предпочтительно от 1 до 100 мкг/г соединения формулы I. Композиции для перорального введения, составленные предпочтительно в виде таблеток, капель или капсул, содержат от 0,05 до 50 мкг, предпочтительно от 0,1 до 25 мкг соединения формулы I на стандартную дозу.
Далее изобретение иллюстрируют с помощью нижеследующих общих методик, способов получения и примеров, не ограничивающих предмет настоящего изобретения.
Общие методики, способы получения и примерыПримеры соединений формулы I перечислены в табл. 1, а соединения общих формул II-VI перечислены в табл. 2. Для 1H ЯМР (300 МГц) и 13C ЯМР (75,6 МГц) спектров значения химических сдвигов (  ) приводятся, если не оговорено иначе, для дейтерохлороформных растворов относительно внутреннего тетраметилсилана ( ) приводятся, если не оговорено иначе, для дейтерохлороформных растворов относительно внутреннего тетраметилсилана ( =0,00), хлороформа ( =0,00), хлороформа ( =7,25 для 1H ЯМР) или дейтерохлороформа ( =7,25 для 1H ЯМР) или дейтерохлороформа ( =76,81 для 13С ЯМР). Значения для мультиплетов, либо определенных (дублет (д), триплет (т), квартет (к)), либо неопределенных (м), даны приблизительно в средней точке, если не указан интервал (с = синглет, шир = широкий).
Эфир представляет собой диэтиловый эфир, высушенный над натрием. ТГФ высушивали над натрием/бензофеноном. Реакции проводили при комнатной температуре, если не оговорено иначе. Рабочая методика включает разбавление соответствующим растворителем (иначе органическим реакционным растворителем), промывку водой и затем соляным раствором, высушивание над безводным сульфатом магния MgSO4 и концентрирование в вакууме с получением остатка. Хроматографию проводят на силикагеле.
Способ получения 1: 20-метил-де-А,B-прегнан-(8S)-ол, соединение 801 =76,81 для 13С ЯМР). Значения для мультиплетов, либо определенных (дублет (д), триплет (т), квартет (к)), либо неопределенных (м), даны приблизительно в средней точке, если не указан интервал (с = синглет, шир = широкий).
Эфир представляет собой диэтиловый эфир, высушенный над натрием. ТГФ высушивали над натрием/бензофеноном. Реакции проводили при комнатной температуре, если не оговорено иначе. Рабочая методика включает разбавление соответствующим растворителем (иначе органическим реакционным растворителем), промывку водой и затем соляным раствором, высушивание над безводным сульфатом магния MgSO4 и концентрирование в вакууме с получением остатка. Хроматографию проводят на силикагеле.
Способ получения 1: 20-метил-де-А,B-прегнан-(8S)-ол, соединение 801Раствор 20S-(4-метилфенилсульфонилоксиметил)-де-A,B-прегнан-(8S)-ола (В. Lythgoe, D. A. Roberts and I. Waterhouse, J. Chem. Soc. Perkin I. (1977), 2608-2612) (0,51 г) в сухом ТГФ (5 мл) кипятят с обратным холодильником в атмосфере аргона с LAH (0,10 г) в течение 5 часов. После охлаждения смесь гасят каплями воды и смесь обрабатывают (эфир). Маслянистый остаток хроматографируют на силикагеле смесью этилацетат/пентан 1:2 с получением соединения, указанного в заголовке. 1H ЯМР: 0,84 (д, 3H), 0,91 (д, 3H), 0,93 (с, 3H), 0,90- 1,92 (м, 13H), 1,98 (м, 1H), 4,07 (м, 1H). Способ получения 2: 8S,18-эпокси-20-метил-де-А,B-прегнан, соединение 802 Соединение 801 (1,7 г) растворяют в бензоле (600 мл) и пиридине (4 мл) и в атмосфере аргона добавляют тетраацетат свинца (19,3 г) (cf. D.F. Maynard, A. W. Norman and W.H. Okamura, J. Org. Chem., 57 (1992) 3214-3217). Реакционную смесь облучают УФ-светом с помощью ртутной лампы Hanau TG 700 W при температуре около 15oС в течение 3 ч 45 мин. Реакционную смесь фильтруют и удаляют растворитель под вакуумом. Остаток смешивают со смесью этилацетат/пентан 1: 3, фильтруют, хроматографируют на силикагеле смесью этилацетат/пентан 1:3 и в результате получают соединение, указанное в заголовке. 1H ЯМР: 0,85 (д, 3H), 0,91 (д, 3H), 0,90-2,10 (м, 13H), 3,70 (м, 2H), 4,14 (д, 1H). Способ получения 3: 8R,18-диацетокси-20-метил-де-A,B-прегнан, соединение 803 К раствору соединения 802 (2,2 г) в уксусном ангидриде (200 мл) добавляют по каплям эфират трифторида бора (26,4 мл) в атмосфере аргона при температуре от -25 до -20oC. Перемешивание продолжают в течение 30 мин при -20oC и в течение 15 мин при комнатной температуре. Смесь вливают в охлаждаемый льдом насыщенный водный раствор бикарбоната натрия (1 л). После перемешивания в течение 1 часа водную фазу экстрагируют эфиром (3 х 300 мл). Объединенные эфирные фазы промывают водой (200 мл) и соляным раствором (250 мл), высушивают над сульфатом магния и упаривают под вакуумом. Хроматографией на силикагеле смесью этилацетат/пентан 1:4 получают соединение, указанное в заголовке. 1H ЯМР: 0,85 (д, 3H), 1,02 (д, 3H), 2,01 (д, 3H), 2,06 (с, 3H), 0,90-2,35 (м, 13H), 3,97 (д, 1H), 4,16 (д, 1H), 4,90 (м, 1H). Способ получения 4: 20-метил-де-А,B-прегнан-8R,18-диол, соединение 804 Соединение 803 (3,0 г) растворяют в метаноле (50 мл) и добавляют водный раствор (20 мл) гидроксида калия (2 г). После перемешивания при 65oC в течение 6,5 часа реакционную смесь фильтруют через силикагель. Фильтрат упаривают досуха под вакуумом и хроматографируют на силикагеле смесью этилацетат/пентан 2:1 с получением соединения, указанного в заголовке. 1H ЯМР: 0,88 (д, 3H), 1,04 (д, 3H), 0,90-2,10 (м, 14H), 2,33 (м, 1H), 3,62 (м, 2H), 3,67 (м, 1H). Способ получения 5: 8R-трет-бутилдиметилсилилокси-20-метил- де-А,В-прегнан-18-ол, соединение 805 Соединение 804 (1,3 г), имидазол (1,0 г) и трет-бутил-диметилсилил хлорид (1,1 г) перемешивают в сухом диметилформамиде (54 мл) при комнатной температуре в течение 4 часов. Реакционную смесь обрабатывают (эфир). Остаток хроматографируют на силикагеле смесью эфир/пентан 1:4 с получением соединения, указанного в заголовке. 1H ЯМР: 0,01 (с, 3H) 0,02 (с, 3H), 0,85 (с, 9H), 0,85 (д, 3H), 1,02 (д, 3H), 090-1,98 (м, 13H), 2,29 (м, 1H), 3,52 -3,70 (м, 3H). Общая методика 1: Алкилирование соединения 805 соединением общей формулы VII с получением соединений общей формулы II Соединение 805 (0,25 г) и соединение общей формулы VII (1,5 ммоль) растворяют в сухом тетрагидрофуране (5 мл) в атмосфере аргона и добавляют гидрид калия (0,23 мл 20%-ной масляной эмульсии). Через 5 мин добавляют раствор 18-краун-6 (200 мг) в сухом тетрагидрофуране (2 мл). После перемешивания в течение 20 мин при комнатной температуре реакционную смесь делят между водой (50 мл) и эфиром (50 мл). Эфирную фазу промывают насыщенным водным раствором хлорида натрия (25 мл) и высушивают над сульфатом магния. После упаривания растворителя под вакуумом остаток хроматографируют на силикагеле смесью эфир/пентан 1:10 (об./об.) и получают соединение общей формулы II. Общая методика 2: Снятие защитных групп соединений общей формулы II или VI с получением соответствующих соединений формулы III или I соответственно обработкой “HF” К раствору соединения общей формулы II или VI (0,05 ммоль) в этилацетате (0,25 мл) добавляют ацетонитрил (1,0 мл) и затем 5% раствор фтористо-водородной кислоты в смеси ацетонитрил: вода 7:1 (0,8 мл) в атмосфере аргона при перемешивании. Перемешивание продолжают в течение 45 мин при температуре окружающей среды. Добавляют насыщенный водный раствор бикарбоната натрия (10 мл), после чего реакционную смесь обрабатывают (этилацетат). Остаток очищают хроматографией (в качестве элюента используют этилацетат или смесь этилацетата и гексана или пентана) и в результате получают соединение общей формулы III или I. Общая методика 3: Окисление соединений общей формулы III с получением соединений общей формулы IV Раствор соединения общей формулы III (0,5 ммоль) и PDC (1,5 ммоль) в дихлорметане (15 мл) перемешивают при к.т. в течение 24 часов. К реакционной смеси добавляют насыщенный водный раствор бикарбоната натрия (50 мл) и обрабатывают (дихлорметан). Хроматографией с использованием смеси этилацетат/пентан 1:3 в качестве элюента получают соединение общей формулы IV. Общая методика 4: Защита гидроксильной группы соединения общей формулы IV (Y’=H) с получением соединения общей формулы V Раствор соединения общей формулы IV (Y’=H) (0,4 ммоль), N-этилдиизопропиламина (0,8 ммоль) и триметилсилилхлорида (0,8 ммоль) в дихлорметане (4 мл) перемешивают в течение 140 мин. Реакционную смесь делят между дихлорметаном (30 мл) и фосфатным буфером (30 мл, pH 6,5). Органическую фазу промывают соляным раствором (30 мл) и высушивают над сульфатом магния. После упаривания растворителя остаток хроматографируют на силикагеле смесью этилацетат/пентан 1:4 в качестве элюента и получают соединение общей формулы V. Общая методика 5: Сочетание [3S-(1Z,3  ,5 ,5 )]-[2-[3,5-бис (трет-бутилдиметилсилилокси)-2-метиленциклогексилиден] -этил] дифенилфосфиноксида с соединением общей формулы V с получением соединения общей формулы VI )]-[2-[3,5-бис (трет-бутилдиметилсилилокси)-2-метиленциклогексилиден] -этил] дифенилфосфиноксида с соединением общей формулы V с получением соединения общей формулы VIИспользуют способ, описанный E.G. Baggiolini, J.A. Iacobell, B.M. Hennessy, A.D. Batcho, J.F. Sereno and M.R. Uskokovic, J. Org. Chem., 51 (1986) 3098-3108. Общая методика 6: Присоединение 2,2-диалкилоксирана к соединению 806 с получением соединения 807 или 808 К раствору соединения 806 (0,21 г) в сухом ТГФ (2 мл) при -78oC медленно добавляют раствор н-бутиллития в гексане (1,6 М, 0,21 мл). После перемешивания при -78oC в течение 40 мин добавляют эфират трифторида бора (0,050 мл) и продолжают перемешивание в течение 10 мин. Добавляют раствор 2,2-диалкилоксирана (алкил = метил или этил) (0,42 ммоль) в сухом ТГФ (2 мл) и продолжают перемешивание при к. т. в течение 1 часа. Добавляют насыщенный раствор хлорида аммония и обрабатывают этилацетатом. После хроматографии получают целевые соединения 807 или 808. Общая методика 7: Реакция соединения 812 с соединением общей формулы H-C  C-CR2(OY) с получением некоторых соединений общей формулы II C-CR2(OY) с получением некоторых соединений общей формулы IIК раствору соединения формулы H-C  C-CR2(OY) (2,2 ммоль) в сухом диоксане (6 мл) при 5oC добавляют н-бутиллитий (1,4 мл, 1,5 М в гексане). После перемешивания в течение 30 мин при 5oC и в течение 1 часа при к. т. добавляют раствор соединения 812 (0,28 г) в диоксане (3 мл) и перемешивают смесь при 90oC в течение 2 дней. Реакционную смесь обрабатывают этилацетатом, хроматографируют смесью эфир/пентан 1:10 (об./об.) и получают соединение общей формулы II.
Способ получения 6: Соединение 201 C-CR2(OY) (2,2 ммоль) в сухом диоксане (6 мл) при 5oC добавляют н-бутиллитий (1,4 мл, 1,5 М в гексане). После перемешивания в течение 30 мин при 5oC и в течение 1 часа при к. т. добавляют раствор соединения 812 (0,28 г) в диоксане (3 мл) и перемешивают смесь при 90oC в течение 2 дней. Реакционную смесь обрабатывают этилацетатом, хроматографируют смесью эфир/пентан 1:10 (об./об.) и получают соединение общей формулы II.
Способ получения 6: Соединение 201Общая методика 1. Исходное соединение VII: соединение 701. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 1H ЯМР: 0,02 (с, 3H), 0,03 (с, 3H), 0,10 (с, 9H), 0,81 (д, 3H), 0,87 (с, 9H), 0,98 (д, 3H), 1,19 (с, 6H), 0,90-1,95 (м, 18H), 2,27 (м, 1H), 3,17 (д, 1H), 3,29 (м, 3H), 3,68 (м, 1H). Способ получения 7: Соединение 301 Общая методика 2. Исходное соединение II: соединение 201. Хроматографический элюент: этилацетат. 1H ЯМР: 0,84 (д, 3H), 1,00 (д, 3H), 1,21 (с, 6H), 0,85-2,10 (м, 20H), 3,31 (м, 1H), 3,20 (д, 1H), 3,31 (м, 3H), 3,72 (м, 1H). Способ получения 8: Соединение 401 Общая методика 3. Исходное соединение III: соединение 301. Хроматографический элюент: этилацетат. 1 H ЯМР: 0,86 (д, 3H), 1,03 (д, 3H), 1,20 (с, 3H), 1,21 (с, 3H), 1,10-2,40 (м, 19H), 2,45 (м, 1H), 3,12 (д, 1H), 3,28 (м, 3H). Способ получения 9: Соединение 501 Общая методика 4. Исходное соединение IV: соединение 401. Хроматографический элюент: этилацетат/пентан 1:4 (об./об.). 1H ЯМР: 0,08 (с, 9H), 0,84 (д, 3H), 1,02 (д, 3H), 1,18 (с, 6H), 1,10-2,40 (м, 18H), 2,47 (м, 1H), 3,06 (д, 1H), 3,24 (м, 3H). Способ получения 10: Соединение 601 Общая методика 5. Исходное соединение V: соединение 501. Хроматографический элюент: этилацетат/пентан 1:10 (об./об.). 1H ЯМР: 0,06 (м, 12H), 0,08 (с, 9H), 0,83 (д, 3H), 0,87 (с, 9H), 0,88 (с, 9H), 1,02 (д, 3H), 1,18 (с, 6H), 1,00-2,10 (м, 19H), 2,21 (дд, 1H), 2,46 (м, 2H), 2,85 (м, 1H), 2,99 (д, 1H), 3,08 (д, 1H), 3,24 (м, 2H), 4,18 (м, 1H), 4,37 (м, 1H), 4,84 (м, 1H), 5,16 (м, 1H), 5,98 (д, 1H), 6,24 (д, 1H). Способ получения 11: Соединение 202 Общая методика 1. Исходное соединение VII: соединение 702. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 1H ЯМР: 0,02 (с, 3H), 0,03 (с, 3H), 0,08 (с, 9H), 0,81 (т, 6H), 0,82 (д, 3H), 0,86 (с, 9H), 0,98 (д, 3H), 0,90-1,95 (м, 20H), 2,27 (м, 1H), 3,12-3,35 (м, 4H), 3,68 (м, 1H). Способ получения 12: Соединение 302 Общая методика 2. Исходное соединение II: соединение 202. Хроматографический элюент: этилацетат. 1H ЯМР: 0,84 (д, 3H), 0,86 (т, 6H), 1,00 (д, 3H), 0,85-2,10 (м, 22H), 2,30 (м, 1H), 3,15-3,40 (м, 4H), 3,71 (м, 1H). Способ получения 13: Соединение 402 Общая методика 3. Исходное соединение III: соединение 302. Хроматографический элюент: этилацетат. 1H ЯМР: 0,80-0,90 (м, 9H), 1,02 (д, 3H), 1,15-2,50 (м, 22H), 3,10-3,40 (м, 4H). Способ получения 14: Соединение 502 Общая методика 4. Исходное соединение IV: соединение 402. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 1H ЯМР: 0,08 (с, 9H), 0,80 (м, 6H), 0,85 (д, 3H), 1,03 (д, 3H), 1,20-2,40 (м, 20H), 2,48 (м, 1H), 3,04 (д, 1H), 3,23 (м, 3H). Способ получения 15: Соединение 602 Общая методика 5. Исходное соединение V: соединение 502. Хроматографический элюент: этилацетат/пентан 1:10 (об./об.). 1H ЯМР: 0,05 (м, 12H), 0,08 (с, 9H), 0,80 (т, 6H), 0,83 (д, 3H), 0,87 (с, 9H), 0,88 (с, 9H), 1,02 (д, 3H), 1,00-2,12 (М, 21H), 2,21 (дд, 1H), 2,46 (м, 2H), 2,85 (м, 1H), 2,98 (д, 1H), 3,09 (д, 1H), 3,22 (м, 2H), 4,18 (м, 1H), 4,36 (м, 1H), 4,84 (м, 1H), 5,16 (м, 1H), 5,98 (д, 1H), 6,24 (д, 1H). Способ получения 16: Соединение 203 Общая методика 1. Исходное соединение VII: соединение 703. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 1H ЯМР: 0,01 (с, 3H), 0,02 (с, 3H), 0,81 (д, 3H), 0,86 (с, 9H), 0,09-1,95 (м, 31H), 2,27 (м, 1H), 3,26 (дд, 1H), 3,46 (м, 2H), 3,64 (м, 1H), 3,93 (м, 1H), 4,13 (м, 2H), 5,03 (м, 1H). Способ получения 17: Соединение 303 Общая методика 2. Исходное соединение II: соединение 203. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 1H ЯМР: 0,84 (д, 3H), 0,90-2,10 (м, 32H), 3,29 (м, 1H), 3,34 (д, 1H), 3,48 (м, 2H), 3,73 (м, 1H), 3,94 (м, 1H), 4,13 (м, 2H), 5,06 (м, 1H). Способ получения 18: Соединение 403 Общая методика 3. Исходное соединение III: соединение 303. Хроматографический элюент: этилацетат/пентан 1:2 (об./об.). 1H ЯМР: 0,86 (д, 3H), 0,95 (т, 3H), 0,96 (т, 3H), 1,03 (д, 3H), 1,20-2,60 (м, 23H), 3,16 (д, 1H), 3,41 (д, 1H), 3,50 (м, 1H), 3,95 (м, 1H), 4,03 (д, 1H), 4,15 (д, 1H), 5,01 (м, 1H). Способ получения 19: Соединение 603 Общая методика 5. Исходное соединение V: соединение 403. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 1H ЯМР: 0,05 (м, 12H), 0,84 (д, 3H), 0,86 (с, 9H), 0,87 (с, 9H), 0,94 (т, 3H), 0,95 (т, 3H), 1,01 (д, 3H), 0,90-2,12 (М, 3H), 2,20 (дд, 1H), 2,45 (м, 2H), 2,84 (м, 1H), 3,18 (м, 2H), 3,47 (м, 1H), 3,92 (м, 1H), 4,06 (м, 2H), 4,18 (м, 1H), 4,37 (м, 1H), 4,84 (м, 1H), 5,01 (м, 1H), 5,17 (м, 1H), 5,99 (д, 1H), 6,21 (д, 1H). Способ получения 20: Соединение 204 Общая методика 1. Исходное соединение VII: соединение 704. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 1H ЯМР: 0,01 (м, 6H), 0,82 (д, 3H), 0,86 (с, 9H), 1,01 (м, 3H), 1,50 (с, 3H), 1,66 (с, 3H), 0,80-1,95 (м, 18H), 2,34 (м, 1H), 3,26-3,45 (м, 3H), 3,66 (м, 1H), 3,95 (м, 1H), 4,35-4,50 (м, 3H), 7,18 (д, 1H), 7,28 (т, 1H), 7,36 (д, 1H), 7,40 (с, 1H). Способ получения 21: Соединение 304 Общая методика 2. Исходное соединение II: соединение 204. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.), затем этилацетат. 1H ЯМР: 0,84 (д, 3H), 1,03 (м, 3H), 1,51 (с, 3H), 1,67 (с, 3H), 0,90-2,07 (м, 19H), 2,36 (м, 1H), 3,25-3,45 (м, 3H), 3,68 (м, 1H), 3,95 (м, 1H), 4,33-4,52 (м, 3H), 7,17 (д,1H), 7,29 (т, 1H), 7,36 (д, 1H), 7,41 (м, 1H). Способ получения 22: Соединение 404 Общая методика 3. Исходное соединение III: соединение 304. Хроматографический элюент: этилацетат/пентан 1:3 (об./об.). 1H ЯМР: 0,85 (д, 3H), 1,05 (м, 3H), 1,51 (с, 3H), 1,67 (с, 3H), 1,20-2,45 (м, 18H), 2,53 (м, 1H), 3,16 (дд, 1H), 3,34 (м, 1H), 3,39 (м, 1H), 3,95 (м, 1H), 4,33-4,50 (м, 3H), 7,14 (д, 1H), 7,29 (т, 1H), 7,36 (с, 1H), 7,37 (д, 1H). Способ получения 23: Соединение 604 Общая методика 5. Исходное соединение V: соединение 404. Хроматографический элюент: пентан, затем этилацетат/пентан 1:4 (об./об. ). 1H ЯМР: 0,06 (м, 12H), 0,84 (д, 3H), 0,88 (с, 9H), 0,89 (с, 9H), 1,06 (м, 3H), 1,49 (с, 3H), 1,66 (с, 3H), 0,80-2,00 м, 18H), 2,08 (м, 1H), 2,21 (дд, 1H), 2,45 (дд, 1H), 2,56 (шир. д, 1H), 2,85 (м, 1H), 3,20 (м, 2H), 3,37 (м, 1H), 3,95 (м, 1H), 4,19 (м, 1H), 4,37 (м, 4H), 4,83 (м, 1H), 5,16 (м, 1H), 5,99 (д, 1H), 6,23 (д, 1H), 7,14 (д, 1H), 7,26 (т, 1H), 7,33 (д, 1H), 7,33 (с, 1H). Способ получения 24: Соединение 205 Общая методика 1. Исходное соединение VII: соединение 705. Хроматографический элюент: пентан, затем эфир/пентан 1:4 (об./об.) 1H ЯМР: 0,00 (м, 6H), 0,61 (т, 3H), 0,76 (т, 3H), 0,81 (д, 3H), 0,85 (с, 9H), 1,00 (м, 3H), 0,70-2,10 (м, 22H), 2,34 (м, 1H), 3,27 (д, 1H), 3,38 (д, 1H), 3,42 (м, 1H), 3,64 (м, 1H), 4,00 (м, 1H), 4,43 (м, 2H), 4,59 (м, 1H), 7,15 (д, 1H), 7,20-7,40 (м, 3H). Способ получения 25: Соединение 305 Общая методика 2. Исходное соединение II: соединение 205. Хроматографический элюент: этилацетат/пентан 1:2 (об./об.), затем этилацетат. 1H ЯМР: 0,61 (т, 3H), 0,77 (м, 3H), 0,83 (д, 3H), 1,01 (м, 3H), 0,70-2,10 (м, 23H), 2,35 (м, 1H), 3,33 (м, 2H), 3,43 (м, 1H), 3,68 (м, 1H), 4,00 (м, 1H), 4,43 (м, 2H), 4,50 -4,75 (м, 1H), 7,07-7,45 (м, 4H). Способ получения 26: Соединение 405 Общая методика 3. Исходное соединение III: соединение 305. Хроматографический элюент: этилацетат/пентан 1:3 (об./об.). 1H ЯМР: 0,60 (т, 3H), 0,76 (м, 3H), 0,84 (д, 3H), 1,03 (м, 3H), 1,20-2,45 (м, 22H), 2,52 (м, 1H), 3,13 (д, 1H), 3,31 (д, 1H), 3,43 (м, 1H), 4,00 (м, 1H), 4,39 (м, 2H), 4,59 (м, 1H), 7,11 (д, 1H), 7,20-7,40 (м, 3H). Способ получения 27: Соединение 605 Общая методика. 5. Исходное соединение V: соединение 405. Хроматографический элюент: пентан, затем этилацетат/пентан 1:4 (об./об. ). 1H ЯМР: 0,06 (м, 12H), 0,59 (т, 3H), 0,77 (т, 3H), 0,82 (д, 3H), 0,87 (с, 9H), 0,88 (с, 9H), 1,04 (м, 3H), 1,00-2,12 (м, 23H), 2,21 (дд, 1H), 2,45 (дд, 1H), 2,56 (шир.д, 1H), 2,84 (м, 1H), 3,18 (м, 2H), 3,43 (м, 1H), 3,99 (м, 1H), 4,19 (м, 1H), 4,37 (м, 3H), 4,56 (м, 1H), 4,83 (м, 1H), 5,16 (м, 1H), 5,99 (д, 1H), 6,22 (д, 1H), 7,11 (д, 1H), 7,20-7,40 (м, 3H). Способ получения 28: Соединение 206 Общая методика 1. Исходное соединение VII: соединение 706. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 13C ЯМР: 73,6; 71,8; 71,2; 69,0; 58,9; 56,8; 48,3; 41,4; 36,3; 35,1; 31,0; 29,6; 25,7; 24,9; 24,3; 23,2; 22,9; 21,9; 2,4; -4,3; -4,8. Способ получения 29: Соединение 306 Общая методика 2. Исходное соединение II: соединение 206. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 13С ЯМР: 72,0; 70,8; 70,6; 69,0; 59,0; 57,1; 48,7; 40,9; 35,9; 35,0; 31,2; 29,4; 29,1; 28,2; 24,9; 23,5; 23,4; 23,2; 22,0. Способ получения 30: Соединение 406 Общая методика 3. Исходное соединение III: соединение 306. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 13С ЯМР: 221,7; 71,9; 70,4; 70,2; 60,3; 58,5; 52,8; 40,5; 40,3; 36,4; 30,9; 29,5; 28,9; 27,8; 24,5; 24,0; 23,2; 23,0; 19,5. Способ получения 31: Соединение 506 Общая методика 4. Исходное соединение IV: соединение 406. Хроматографический элюент: этилацетат/пентан 1:4 (об./об.). 13С ЯМР: 211,2; 73,6; 72,0; 69,2; 60,3; 58,4; 52,6; 41,2; 40,4; 35,5; 30,8; 29,6; 29,6; 27,5; 24,5; 23,7; 23,0; 22,8; 19,2; 2,4. Способ получения 32: Соединение 606 Общая методика 5. Исходное соединение V: соединение 506. Хроматографический элюент: этилацетат/пентан 1:10 (об./об.). 13С ЯМР: 148.1; 140,9; 135,0; 122,9; 117,9; 111,0; 73,7; 71,9; 71,6; 68,1; 67,3; 58,7; 55,4; 49,0; 45,9; 44,6; 41,4; 35.,4; 31,4; 29,6; 28,6; 27,6; 25,7; 24,9; 23,2; 23,1; 21,9; 18,1; 17,9; 2,4; -4,8; -5,0; -5,3. Способ получения 33: Соединение 207 Общая методика 1. Исходное соединение VII: соединение 707. Хроматографический элюент: эфир/пентан 1:10 (об./об.). Способ получения 34: Соединение 307 Общая методика 2. Исходное соединение II: соединение 207. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 35: Соединение 407 Общая методика 3. Исходное соединение III: соединение 307. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 36: Соединение 507 Общая методика 4. Исходное соединение IV: соединение 307. Хроматографический элюент: этилацетат/пентан 1:4 (об./об.). Способ получения 37: Соединение 607 Общая методика 5. Исходное соединение V: соединение 507. Хроматографический элюент: этилацетат/пентан 1:10 (об./об.). Способ получения 38: Соединение 208 Общая методика 1. Исходное соединение VII: соединение 708. Хроматографический элюент: эфир/пентан 1:10 (об./об.). Способ получения 39: Соединение 308 Общая методика 2. Исходное соединение II: соединение 208. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 40: Соединение 408 Общая методика 3. Исходное соединение III: соединение 308. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 41: Соединение 608 Общая методика 5. Исходное соединение IV: соединение 408. Хроматографический элюент: эфир/пентан 1:4 (об./об.). Способ получения 42: 8R-трет-бутилдиметилсилилокси-20-метил- 18-(5-гидрокси-5-метил-гекс-2-ин-1-илокси)-де-A,B-прегнан (соединение 807) Общая методика 6. Исходное соединение: 2,2-диметилоксиран. Хроматографический элюент: эфир/пентан 1:2 (об./об.), затем эфир. 13C ЯМР: 82,6; 79,4; 71,2; 69,8; 67,8; 58,9; 58,5; 56,8; 48,2; 36,2; 34,7; 34,3; 31,0; 28,4; 27,7; 25,7; 24,2; 23,1; 22,9; 21,7; 18,0; -4,3; -4,8. Способ получения 43: Соединение 309 Общая методика 2. Исходное соединение: соединение 807. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 44: Соединение 409 Общая методика 3. Исходное соединение III: соединение 309. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 45: Соединение 609 Общая методика 5. Исходное соединение IV: соединение 409. Хроматографический элюент: эфир/пентан 1:4 (об./об.). Способ получения 46: Соединение 210 Общая методика 1. Исходное соединение VII: соединение 710. Хроматографический элюент: эфир/пентан 1:4 (об./об.). Способ получения 47: Соединение 310 Общая методика 2. Исходное соединение II: соединение 210. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 48: Соединение 410 Общая методика 3. Исходное соединение III: соединение 310. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 49: Соединение 610 Общая методика 5. Исходное соединение IV: соединение 410. Хроматографический элюент: эфир/пентан 1:10 (об./об.). Способ получения 50: Соединение 211 Общая методика 7. Исходное соединение: 3-метил-3-(тетрагидропиран-2-илокси)-бут-1- ин. Хроматографический элюент: эфир/пентан 1:20 (об./об.). Способ получения 51: Соединение 311 Общая методика 2. Исходное соединение II: соединение 211. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 52: Соединение 411 Общая методика 3. Исходное соединение III: соединение 311. Хроматографический элюент: этилацетат/пентан 1:2 (об./об.). Способ получения 53: Соединение 611 Общая методика 5. Исходное соединение IV: соединение 411. Хроматографический элюент: эфир/пентан 1:10 (об./об.). Способ получения 54: Соединение 212 Общая методика 7. Исходное соединение: 3-этил-3-(тетрагидропиран-2-ил-окси)-пент-1-ин. Хроматографический элюент: эфир/пентан 1:20 (об./об.). Способ получения 55: Соединение 312 Общая методика 2. Исходное соединение II: соединение 212. Хроматографический элюент: этилацетат/пентан 1:2 (об./об.). Способ получения 56: Соединение 412 Общая методика 3. Исходное соединение III: соединение 312. Хроматографический элюент: этилацетат/пентан 1:2 (об./об.). Способ получения 57: Соединение 612 Общая методика 5. Исходное соединение IV: соединение 412. Хроматографический элюент: этилацетат/пентан 1:10 (об./об.). Способ получения 58: Соединение 213 Общая методика 1. Исходное соединение VII: соединение 713. Хроматографический элюент: эфир/пентан 1:10 (об./об.). 13С ЯМР: 95,9; 95,9; 88,5; 88,4; 80,2: 71,2; 70,9; 67,5; 67,5; 63,1; 63,0; 58,9; 58,3; 56,8; 48,1; 36,2; 34,6; 31,8; 30,9; 30,6; 30,6; 29,7; 29,5; 27,7; 25,7; 25,2; 24,2; 23,1; 22,9; 21,6; 20,3; 20,2; 17,9; -4,3; -4,8. Способ получения 59: Соединение 313 Общая методика 2. Исходное соединение II: соединение 213. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 13С ЯМР: 96,0; 88,7; 80,5; 80,4; 71,1; 70,7; 67,8; 67,8; 63,2; 63,1; 59,0; 58,5; 57,1; 48,5; 35,8; 34,9; 32,0; 31,0; 30,8; 29,9; 28,3; 28,2; 25,4; 23,5; 23,5; 23,4; 23,0; 21,9; 20,4; 20,4. Способ получения 60: Соединение 413 Общая методика 3. Исходное соединение III: соединение 313. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 13С ЯМР: 211,3; 96,2; 96,2; 89,1; 79,8; 79,8; 71,1; 68,0; 63,3; 63,3; 60,5; 58,7; 58,5; 52,6; 40,7; 35,4; 32,0; 30,9; 30,7; 29,9; 29,8; 27,7; 25,4; 23,7; 23,2; 23,0; 20,5; 19,3. Способ получения 61: Соединение 613 Общая методика 5. Исходное соединение IV: соединение 413. Хроматографический элюент: эфир/пентан 1:4 (об./об.). 13С ЯМР: 148,2; 140,4; 135,2, 122,8; 118,1; 111,0; 96,0; 88,0; 80,4; 71,8; 70,9; 67,3; 67,1; 63,1; 58,6; 58,2; 55,4; 48,8; 45,8; 44,6; 35,1; 31,8; 31,2; 30,7; 30,6; 29,7; 29,6; 28,6; 27,5; 25,7; 25,2; 23,1; 22,9; 21,9; 20,3; 18,1; 17,9; -4,9; -5; -5,2. Способ получения 62: Соединение 214 Общая методика 1. Исходное соединение VII: соединение 714. Хроматографический элюент: эфир/пентан 1:10 (об./об.). Способ получения 63: Соединение 314 Общая методика 2. Исходное соединение II: соединение 214. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 64: Соединение 414 Общая методика 3. Исходное соединение III: соединение 314. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 65: Соединение 514 Общая методика 4. Исходное соединение IV: соединение 414. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 66: Соединение 614 Общая методика 5. Исходное соединение V: соединение 514. Хроматографический элюент: эфир/пентан 1:4 (об./об.). Способ получения 67: 8R-трет-бутилдиметилсилилокси-20-метил- 18-(5-этил-5-гидрокси-гепт-2-ин-1-илокси)-де-A,B-прегнан (соединение 808) Общая методика 6. Исходное соединение: 2,2-диэтилоксиран. Хроматографический элюент: эфир/пентан 1:2 (об./об.), затем эфир. Способ получения 68: Соединение 315 Общая методика 2. Исходное соединение: соединение 808. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). 13C ЯМР: 82,9; 79,5; 70,8; 70,0; 68,0; 59,0; 58,8; 57,1; 48,6; 35,8; 34,9; 34,5; 31,1; 28,6; 28,2; 23,5; 23,4; 23,0; 21,9. Способ получения 69: Соединение 415 Общая методика 3. Исходное соединение III: соединение 315. Хроматографический элюент: этилацетат/пентан 1:1 (об./об.). Способ получения 70: Соединение 615 Общая методика 5. Исходное соединение IV: соединение 415. Хроматографический элюент: эфир/пентан 1:10 (об./об.). Способ получения 71: 8R-трет-бутилдиметилсилилокси-20-метил- 18-(проп-2-ин-1-илокси)-де-A,B-прегнан. Соединение 806 Раствор соединения 805 (0,45 г), 18-краун-6 (0,36 г) и трет-бутоксид калия (0,31 г) перемешивают в течение 10 мин и добавляют 3-бромпроп-1-ин (0,32 г). После перемешивания в течение 1 часа добавляют другую порцию 3-бромпроп-1-ина (0,32 г), а затем после перемешивания в течение 1 часа окончательно добавляют 3-бромпроп-1-ин (0,32 г) и трет-бутоксид калия (0,62 г). После перемешивания в течение 19 часов реакционную смесь обрабатывают (эфир) и хроматографируют с использованием смеси эфир/пентан 1:20 (об./об.) в качестве элюента с получением соединения 806. 13C ЯМР: 80,0; 73,8; 71,1; 68,2; 58,9; 58,2; 56,9; 48,2; 36,3; 34,8; 31,0; 27,8; 25,7; 24,2; 23,2; 22,8; 21,7; 18,0; -4,3; -4,8. Способ получения 72: 8R-трет-бутилдиметилсилилокси-20- метил-18- (проп-2-ен-1-илокси)-де-А,В-прегнан. Соединение 809 Используют общую методику 1, где “соединение общей формулы VII” заменяют на “3-бромпроп-1-ен”, а продукт “соединение общей формулы II” заменяют на “соединение 809”. 13С ЯМР: 135,1; 115,5; 72,1; 71,2; 68,7; 58,9; 56,9; 48,3; 36,3; 35,1; 31,0; 27,8; 25,7; 24,2; 23,2; 22,9; 22,0; 18,0; -4,3; -4,8. Способ получения 73: 8R-трет-бутилдиметилсилилокси-20-метил- 18-(карбонилметокси)-де-А,В-прегнан. Соединение 810 Через раствор соединения 809 (0,9 г) в смеси дихлорметана (60 мл) и метанола (20 мл) пропускают озон при -70oC в течение 30 мин до тех пор, пока исходное соединение 809 не будет больше обнаруживаться (TLC, смесь эфир/пентан 1:10 (об./об.)). Добавляют трифенилфосфин (0,8 г) и смесь перемешивают при -70oC в течение 30 мин. Растворитель удаляют под вакуумом и остаток хроматографируют смесью эфир/пентан 1:4 (об./об.), а затем эфиром с образованием соединения 810. 13С ЯМР: 201,2; 76,7; 71,0; 70,3; 58,8; 56,7; 48,5; 36,2; 34,6; 31,3; 27,7; 25,7; 24,2; 23,2; 22,8; 21,8; 17,9; -4,3; -4,8. Способ получения 74: 8R-трет-бутилдиметилсилилокси-20-метил-18-(2-гидроксиэтокси)-де-A,B-прегнан. Соединение 811 К охлаждаемому льдом раствору соединения 810 (0,92 г) в смеси ТГФ (20 мл) и метанола (40 мл) добавляют боргидрид натрия (0,43 г). После перемешивания в течение 35 мин смесь упаривают под вакуумом досуха и остаток хроматографируют смесью эфир/пентан 1:7 (об./об.), а затем эфиром с образованием соединения 811. 13C ЯМР: 72,1; 71,1; 69,2; 61,8; 58,8; 56,7; 48,4; 36,2; 34,6; 31,3; 27,8; 25,7; 24,2; 23,1; 22,8; 21,8; 17,9; -4,3; -4,8. Способ получения 75: 8R-трет-бутилдиметилсилилокси-20-иметил-18-[2-(4-метилфенилсульфонилокси)- этокси]-де-A,B-прегнан. Соединение 812 К охлаждаемому льдом раствору соединения 811 (0,69 г) в пиридине (7,5 мл) добавляют 4-толуолсульфонилхлорид (0,70 г). После перемешивания в течение 4 часов при 0oC реакционную смесь обрабатывают эфиром. После хроматографии с использованием смеси эфир/пентан 1:4 (об./об.) получают соединение 812. 13C ЯМР: 144,5; 132,9; 129,6; 127,7; 71,1; 69,4; 69,0; 68,4; 58,7; 56,6; 48,3; 36,2; 34,5; 31,0; 27,7; 25,7; 24,2; 23,1; 22,7; 21,7; 21,4; 17,9; -4,4; -4,8. Способ получения 76: Соединение 509 Общая методика 4. Исходное соединение IV: соединение 409. Хроматографический элюент: этилацетат/пентан 1:4 (об./об.). Способ получения 77: Соединение 515 Общая методика 4. Исходное соединение IV: соединение 415. Хроматографический элюент: этилацетат/пентан 1:4 (об./об.). Пример 1: 1(S),3(R)-дигидрокси-20-метил-18-(5-метил-5- гидрокси-гексилокси)-9,10-втор-прегна-5(Z),7(Е),10(19)- триен (Соединение 101) Способ: общая методика 2. Исходное соединение VI: соединение 601. Хроматографический элюент: этилацетат. 1H ЯМР: 0,85 (м, 9H), 1,03 (д, 3H), 1,00-2,20 (м, 24H), 2,30 (дд, 1H), 2,38 (м, 1H), 2,61 (дд, 1H), 2,86 (м, 1H), 3,12 (с, 2H), 3,29 (м, 2H), 4,24 (м, 1H), 4,42 (м, 1H), 4,98 (м, 1H), 5,30 (м, 1H), 6,03 (д, 1H), 6,38 (д, 1H). Пример 2: 1(S), 3(R)-дигидрокси-20-метил-18-(4-этил-4- гидpoкcи-гeкcилoкcи)-9,10-втop-пpeгнa-5(Z),7(Е), 10(19)-триен (Соединение 102) Способ: общая методика 2. Исходное вещество: соединение 602. Хроматографический элюент: этилацетат. 1H ЯМР: 0,85 (д, 3H), 1,03 (д, 3H), 1,20 (с, 6H), 1,00-2,15 (м, 22H), 2,31 (дд, 1H), 2,44 (м, 1H), 2,61 (дд, 1H), 2,85 (м, 1H), 3,08 (м, 2H), 3,27 (т, 2H), 4,23 (м, 1H), 4,43 (м, 1H), 4,99 (м, 1H), 5,32 (м, 1H), 6,00 (д, 1H), 6,39 (.д, 1H). Пример 3: 1(S),3(R)-дигидрокси-20-метил-18-(4-этил-4- гидрокси-гекс-2-инилокси)-9,10-втор-прегна-5(Z),7(Е),10(19)-триен (Соединение 103) Способ: общая методика 2. Исходное вещество: соединение 603. Хроматографический элюент: этилацетат. 1H ЯМР: 0,85 (д, 3H), 1,00 (т, 6H), 1,00 (д, 3H), 1.00-2,25 (м, 20H), 2,30 (дд, 1H), 2,43 (м, 1H), 2,61 (дд, 1H), 2,87 (м, 1H), 3,10 (д, 1H), 3,30 (д, 1H), 4,09 (м, 2H), 4,23 (м, 1H), 4,43 (м, 1H), 5,00 (м, 1H), 5,32 (м, 1H), 6,03 (д, 1H), 6,39 (д, 1H). Пример 4: 1(S), 3(R)-дигидрокси-20-метил-18-(3-(1-гидрокси- 1-метилэтил)фенилметилокси)-9,10-втор-прегна-5(Z), 7(Е) 10(19)- триен (Соединение 104) Способ: общая методика 2. Исходное вещество: соединение 604. Хроматографический элюент: этилацетат. 1H ЯМР: 0,85 (д, 3H), 1,07 (д, 3H), 1,57 (с, 6H), 0,80-2,15 (м, 16H), 2,30 (дд, 1H), 2,52 (м, 1H), 2,60 (дд, 1H), 2,85 (м, 1H), 3,18 (м, 2H), 4,23 (м, 1H), 4,40 (м, 3H), 4,94 (м, 1H), 5,28 (м, 1H), 5,98 (д, 1H), 6,36 (д, 1H), 7,16 (д, 1H), 7,29 (т, 1H), 7,38 (д, 1H), 7,42 (с, 1H). Пример 5: 1(S), 3(R)-дигидрокси-20-метил-18-(3-(1-гидрокси- 1-этилпропил)фенилметилокси)9,10-втор-прегна-5(Z),7(E) 10(19)-триен (Соединение 105) Способ: общая методика 2. Исходное вещество: соединение 605. Хроматографический элюент: этилацетат. 1H ЯМР: 0,74 (т, 3H), 0,75 (т, 3H), 0,84 (д, 3H), 1,06 (д, 3H), 1,00-2,15 (м, 20H), 2,31 (дд, 1H), 2,52 (м, 1H), 2,60 (дд, 1H), 2,84 (м, 1H), 3,17 (м, 2H), 4,24 (м, 1H), 4,40 (м, 2H), 4,42 (м, 1H), 4,95 (м, 1H), 5,30 (м, 1H), 5,99 (д, 1H), 6,36 (д, 1H), 7,10- 7,35 (м, 4H). Пример 6: 1(S), 3(R)-дигидрокси-20-метил-18-(4-гидрокси-4- метилфенилокси)-9,10-втор-прегна-5(Z),7(E),10(19)-триен (Соединение 106) Способ: общая методика 2. Исходное вещество: соединение 606. Хроматографический элюент: этилацетат. 13С ЯМР: 147,3; 142,4; 133,2; 124,4; 117,1; 111,9; 71,8; 71,0; 70,4; 69,2; 66,5; 58,6; 55,5; 49,2; 45,3; 42,6; 40,8; 35,9; 31,2; 29,1; 28,8; 28,8; 27,9; 24,8; 23,3; 23,1; 22,2. Пример 7: 1(S), 3(R)-дигидрокси-20-метил-18-(5-гидрокси-5- этилгептилокси)-9,10-втор-прегна-5 (Z),7(E),10(19)-триен (Соединение 107) Способ: общая методика 2. Исходное вещество: соединение 607. Хроматографический элюент: этилацетат. Пример 8: 1(S), 3(R)-дигидрокси-20-метил-18-(4-(1-гидpoкси- 1-метилэтил)фенилметилокси)-9,10-втор-прегна-5(Z), 7(Е) 10(19)- триен (Соединение 108) Способ: общая методика 2. Исходное вещество: соединение 608. Хроматографический элюент: этилацетат. Пример 9: 1(S),3(R)-дигидрокси-20-метил-18-(5-гидрокси-5- этилгепт-2-ин-1-илокси)-9,10-втор-прегна-5(Z),7(Е),10(19)-триен (Соединение 109) Способ: общая методика 2. Исходное вещество: соединение 609. Хроматографический элюент: этилацетат. Пример 10: 1(S), 3(R)-дигидрокси-20-метил-18-(4-гидрокси- 4-метилпент-2-ен-1-илокси)-9,10-втор-прегна-5(Z),7(Е),10(19)- триен (Соединение 110) Способ: общая методика 2. Исходное вещество: соединение 610. Хроматографический элюент: этилацетат. Пример 11: 1(S),3(R)-дигидрокси-20-метил-18-(5-гидрокси-5- метилгекс-3-ин-1-илокси)-9,10-втор-прегна-5(Z),7(Е), 10(19)-триен (Соединение 111) Способ: общая методика 2. Исходное вещество: соединение 611. Хроматографический элюент: этилацетат. Пример 12: 1(S),3(R)-дигидрокси-20-метил-18-(5-гидрокси-5- этилгепт-3-ин-1-илокси)-9,10-втор-прегна-5(Z),7(Е), 10(19)-триен (Соединение 112) Способ: общая методика 2. Исходное вещество: соединение 612. Хроматографический элюент: этилацетат. Пример 13: 1( S),3(R)-дигидрокси-20-метил-18-(4-гидрокси-4- метилпент-2-ин-1-илокси)-9,10-втор-прегна-5(Z),7(Е),10(19)-триен (Соединение 113) Способ: общая методика 2. Исходное вещество: соединение 613. Хроматографический элюент: этилацетат. 13С ЯМР: 147,3, 143,1, 133,5, 124,7, 117,1, 112,6, 91,1, 78,4, 71,7, 67,3, 66,6, 65,0, 58,7, 58,4, 55,8, 49,2, 45,5, 42,7, 35,4, 31,6, 31,4, 31,1, 29,1, 27,8, 23,5, 23,2, 22,1. Пример 14: 1(S),3(R)-дигидрокси-20-метил-18-(6-гидрокси-6- метилгептилокси)-9,10-втор-прегна-5(Z),7(Е) 10(19)-триен (Соединение 114) Способ: общая методика 2. Исходное вещество: соединение 614. Хроматографический элюент: этилацетат. Пример 15: 1(S),3(R)-дигидрокси-20-метил-18-(5-гидрокси-5- метилгекс-2-ин-1-илокси)-9,10-втор-прегна-5(Z),7(Е). 10(19)-триен (Соединение 115) Способ: общая методика 2. Исходное вещество: соединение 615. Хроматографический элюент: этилацетат. Пример 16: Капсулы, содержащие соединение 101 Соединение 101 растворяют в арахисовом масле до конечной концентрации 1 мкг/мл масла. При нагревании смешивают 10 весовых частей желатина, 5 весовых частей глицерина, 0,08 весовых частей сорбата калия, 14 весовых частей дистиллированной воды и формуют с получением мягких желатиновых капсул, затем каждую капсулу заполняют 100 мкл масляного раствора соединения 101. Пример 17: Дерматологический крем, содержащий соединение 102 Соединение 102 (0,05 мг) растворяют в миндальном масле (1 г). К этому раствору добавляют минеральное масло (40 г) и самоэмульгирующийся пчелиный воск (20 г). Смесь нагревают до жидкого состояния. После добавления горячей воды (40 мл) смесь хорошо перемешивают. Полученный крем содержит примерно 0,5 мкг соединения 102 на грамм крема. Формула изобретения
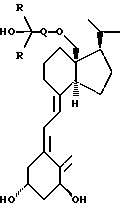 в которой Q представляет собой C1-C8 гидрокарбиленовый бирадикал; R представляет собой C1-C6 гидрокарбил; выражение гидрокарбил (гидрокарбилен) обозначает радикал (бирадикал), полученный после удаления 1 (2) атом(ов) водорода из неразветвленного, разветвленного или циклического, насыщенного или ненасыщенного углеводорода, или в которой две группы R, взятые вместе с атомом углерода, несущим гидроксильную группу, могут образовывать 3-C8 карбоциклическое кольцо. 2. Соединение формулы I по п.1, в котором Q представляет собой C3-C5 насыщенный или ненасыщенный гидрокарбиленовый бирадикал. 3. Соединение формулы I по п.1, в котором Q представляет собой (CH2)n, C  C-(CH2)n-1, где n = 3, 4 или 5, и R представляет собой метил или этил.
4. Соединение по п.1, которое представляет собой: C-(CH2)n-1, где n = 3, 4 или 5, и R представляет собой метил или этил.
4. Соединение по п.1, которое представляет собой:a) 1(S), 3(R)-дигидрокси-20-метил-18-(5-метил-5-гидрокси-гексилокси)-9,10-втор-прегна-5(Z),7(E),10(19)-триен, b) 1(S), 3(R)-дигидрокси-20-метил-18-(4-этил-4-гидрокси-гексилокси)-9,10-втор-прегна-5(Z),7(E),10(19)-триен, c) 1(S), 3(R)-дигидрокси-20-метил-18-(4-этил-4-гидрокси-гекс-2-инилокси)-9,10-втор-прегна-5(Z),7(E),10(19)-триен, d) 1(S), 3(R)-дигидрокси-20-метил-18-(4-гидрокси-4-метилпентилокси)-9,10-втор-прегна-5(Z),7(E),10(19)-триен, e) 1(S), 3(R)-дигидрокси-20-метил-18-(4-гидрокси-4-метилпент-2-ин-1-илокси)-9,10-втор-прегна-5(Z),7(E),10(19)-триен или f) 1(S),3(R)-дигидрокси-20-метил-18-(3-(1-гидрокси-1-метилэтил)фенилметилокси-9,10-втор-прегна-5(Z),7(E),10(19)-триен. 5. Способ получения соединения формулы I по п.1, в котором соединение формулы III 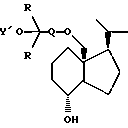 где Y’ представляет собой водород или тетрагидропиранил; R представляет собой метил или этил; Q представляет собой C1-C8 гидрокарбиленовый бирадикал по п.1, окисляют, получая соединение общей формулы IV 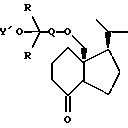 где Y’, R и Q имеют вышеуказанные значения, далее соединение общей формулы IV (Y’ является тетрагидропиранилом; если Y’ представляет водород, то настоящей реакционной стадии предшествует реакция с триметилсилилхлоридом) взаимодействует с оксидом [3S-(1Z,3  ,5 ,5 )]-[2-[3,5-бис(трет-бутилдиметилсилилокси)-2-метиленциклогексилиден] этил] дифенилфосфина и сильным основанием с образованием соединения общей формулы VI )]-[2-[3,5-бис(трет-бутилдиметилсилилокси)-2-метиленциклогексилиден] этил] дифенилфосфина и сильным основанием с образованием соединения общей формулы VI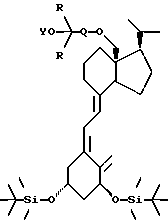 в котором Q и R имеют вышеуказанные значения; Y представляет триметилсилил или тетрагидропиранил, снятие защитной группы с соединения общей формулы VI проводят фтористым водородом или фторидом тетрабутиламмония с образованием целевого соединения формулы I. 6. Способ получения соединения формулы III по п.5, в котором 20S-(4-метилфенилсульфонилоксиметил)-де-A, B-прегнан-(8S)-ол взаимодействует с алюмогидридом лития с образованием 20-метил-де-A,B-прегнан-(8S)-ола, который затем взаимодействует с тетраацетатом свинца при облучении УФ-светом с образованием 8S,18-эпокси-20-метил-де-A,B-прегнана, который затем реагирует с эфиратом трифторида бора и уксусным ангидридом с образованием 8R,18-диацетокси-20-метил-де-A, B-прегнана с последующей реакцией с гидроксидом калия с образованием 20-метил-де-A, B-прегнан-8R, 18-диола, который реагирует с трет-бутилдиметилсилилхлоридом с образованием 8R-трет-бутилдиметилсилилокси-20-метил-де-A, B-прегнан-18-ола, который затем реагирует с основанием в растворителе в присутствии 18-краун-6 и необходимого алкилирующего агента VII YO-CR2-Q-X, где Y представляет триметилсилил или тетрагидропиранил; R представляет метил или этил; Q представляет собой C1-C8 гидрокарбиленовый бирадикал по п.1, с образованием продукта формулы II 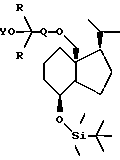 снятие защитной группы проводят фтористым водородом или фторидом тетрабутиламмония с образованием продукта формулы III. 7. Способ получения соединения формулы III по п.5, в котором 8R-трет-бутилдиметилсилилокси-20-метил-де-A, B-прегнан-18-ол взаимодействует с основанием и 3-бромпроп-1-ином с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18-(проп-2-ин-1-илокси)-де-A, B-прегнана, который затем реагирует с сильным основанием, эфиратом трифторида бора и 2,2-диалкилоксираном с образованием соединения 807 или 808, 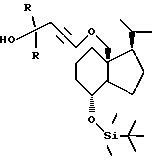 где R представляет собой метил (соединение 807) или этил (соединение 808), снятие защитной группы проводят фтористым водородом или фторидом тетрабутиламмония с образованием продукта формулы III. 8. Способ получения соединения формулы II, где Q представляет собой -C  C-CH2-CH2-, путем взаимодействия 8R-трет-бутилдиметилсилилокси-20-метил-де-A, B-прегнан-18-ола с основанием в присутствии 18-краун-6 и 3-бромпроп-1-ена с получением 8R-трет-бутилдиметилсилилокси-20-метил-18-(проп-2-ен-1-илокси)-де-A, B-прегнана, который затем окисляют озоном с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18-(карбонилметокси)-де-A,B-прегнана, затем восстанавливают его с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18-(2-гидроксиэтокси)-де-A,B-прегнана, который затем реагирует с 4-метилфенилсульфонилхлоридом с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18[2-(4-метилфенилсульфонилокси)-этокси] -де-A, B-прегнана и который, наконец, реагирует с сильным основанием и H-C C-CH2-CH2-, путем взаимодействия 8R-трет-бутилдиметилсилилокси-20-метил-де-A, B-прегнан-18-ола с основанием в присутствии 18-краун-6 и 3-бромпроп-1-ена с получением 8R-трет-бутилдиметилсилилокси-20-метил-18-(проп-2-ен-1-илокси)-де-A, B-прегнана, который затем окисляют озоном с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18-(карбонилметокси)-де-A,B-прегнана, затем восстанавливают его с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18-(2-гидроксиэтокси)-де-A,B-прегнана, который затем реагирует с 4-метилфенилсульфонилхлоридом с образованием 8R-трет-бутилдиметилсилилокси-20-метил-18[2-(4-метилфенилсульфонилокси)-этокси] -де-A, B-прегнана и который, наконец, реагирует с сильным основанием и H-C  C-CR2(OY), где R и Y имеют вышеуказанные значения, с образованием соединения формулы II, где Q представляет собой -C C-CR2(OY), где R и Y имеют вышеуказанные значения, с образованием соединения формулы II, где Q представляет собой -C  C-CH2-CH2. C-CH2-CH2.9. Соединение формулы I по любому одному из пп.1 – 4, полезное в производстве лекарственных препаратов для лечения или профилактики гиперпаратиреоза, для стимуляции остеогенеза и лечения остеопороза, для лечения неврологических дисфункций, таких, как заболевание Альцгеймера, и ряда патологических состояний, включающих сахарный диабет, артериальную гипертонию, угри, облысение, старение кожи (включая старение под действием света), дисбаланс в иммунной системе, лечения воспалительных заболеваний, таких, как ревматоидный артрит и астма, а также заболеваний, характеризующихся аномальной дифференциацией и/или пролиферацией клеток, таких, как псориаз и раковые заболевания. РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 22.03.2007
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
