Патент на изобретение №2168994
|
||||||||||||||||||||||||||
(54) СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА С НИЗКОЙ ГЕПАТОТОКСИЧНОСТЬЮ
(57) Реферат: Изобретение относится к медицине, а именно к фтизиатрии, и химико-фармацевтической промышленности. Предлагаемое средство представляет собой конъюгат изониазида и декстрана с молекулярной массой 63-75 кД, имеющий следующую формулу: 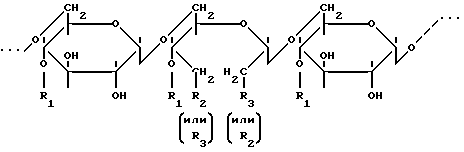 где R1 – Н, остаток глюкозы или полиглюкозильный остаток указанного на рисунке вида, R2 – остаток изониазида формулы 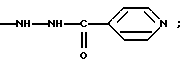 R3 – гидроксильная группа. Технический результат – снижение гепатотоксичности противотуберкулезного средства – изониазида при сохранении его высокотерапевтической эффективности. 2 ил. Изобретение относится к медицине (фтизиатрии) и химико-фармацевтической промышленности. Современное лечение туберкулеза предполагает использование синтетических химиотерапевтических препаратов и их комбинаций. Практически все схемы медикаментозного лечения туберкулеза включают изониазид – гидразид изоникотиновой кислоты. Этот препарат является основным во фтизиатрии в связи с его высокой антимикобактериальной активностью. Вместе с тем изониазид обладает рядом отрицательных свойств. Давно известно его гепатотоксическое действие – от умеренно выраженного жирового гепатоза до фульминантного гепатита, механизм развития которого связан, в частности, с повреждением микросомальной системы окисления и митохондрий. Это обстоятельство определяет необходимость разработки новых, менее токсичных форм изониазида. Известен “Способ лечения генерализованного туберкулезного процесса в эксперименте” (патент N 2087146, авторы: Шкурупий В.А., Курунов Ю.Н., Чернова Т. Г.), в котором используется изониазид-декстран с молекулярной массой (ММ) 20-40 кД (прототип). Исследования этого препарата показали, что он характеризуется меньшей гепатотоксичностью в сравнении с изониазидом. Объем деструктивных изменений гепатоцитов у животных, для лечения которых применялся изониазид-декстран с ММ 20-40 кД, был на 60% меньшим, чем у леченных свободным изониазидом животных. Задачей заявляемого изобретения является снижение гепатотоксичности противотуберкулезного средства – изониазида (при сохранении его высокотерапевтической эффективности), что может быть достигнуто созданием конъюгата изониазида и декстрана с ММ 65-75 кД. Исследования созданного препарата показали, что он оказывает значительно меньшее повреждающее воздействие на гепатоциты, чем конъюгат изониазида и декстрана с ММ 20-40 кД, при использовании обоих в равных разовых дозах по изониазиду и одинаковой схеме лечения. Таким образом, предлагается эффективное средство для лечения туберкулеза с низкой гепатотоксичностью, представляющее собой конъюгат изониазида и декстрана с ММ 65-75 кД. Конъюгат изониазид-декстран имеет следующую формулу: 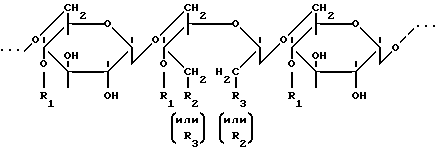 где R1 – H, остаток глюкозы или полиглюкозильный остаток указанного на рисунке вида; R2 – остаток изониазида формулы 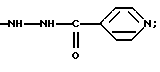 R3 – гидроксильная группа. Препарат применяется в разовых дозах по изониазиду согласно рекомендациям (Машковский М. Д. Лекарственные средства. В 2-х томах. – Вильнюс. – 1993. – Т. 2. – С. 283-284), но в интермиттирующем режиме – 2 раза в неделю. Перечень фигур графических изображений. Фиг. 1. Динамика изменения объемной плотности дистрофически измененных гепатоцитов. Фиг. 2. Динамика изменения объемной плотности зон некрозов в паренхиме печени мышей. На всех фигурах графических изображений: БЦЖ – группа контроля; КФИ (комплексная форма изониазида) – предлагаемый препарат. Сведения, подтверждающие возможность осуществления изобретения с реализацией назначения. 1. Получение конъюгата изониазид-декстран с ММ 65-75 кД. Препарат может быть получен следующим способом. Получение промежуточного продукта – диальдегиддекстрана. К раствору 537 мг декстрана с молекулярной массой 65-75 кД, например 70 кД (декстран-70), в 27 мл дистиллированной воды прибавляли 250 мг NaIO4 в 5,9 мл H2O, перемешивали на магнитной мешалке 45 мин при комнатной температуре. Приливали 7,4 мл чистого этиленгликоля, перемешивали 20 мин. Раствор подвергали диализу в течение 24 часов против 50 объемов дистиллированной воды, осаждали продукт добавлением 228 мл охлажденного (+4-6oC) этанола в течение 24 часов. Взвесь центрифугировали 15 мин при 3000 об/мин. Осадок 3 раза промывали ацетоном и высушивали на воздухе. Выход – 296 мг (54% от теоретического). Получение конъюгата. К раствору 296 мг диальдегиддекстрана (pH 4,6) в 5,2 мл дистиллированной воды прибавляли 0,5 мл 5% CH3COOH (pH 2,9), 265 мг твердого изониазида и перемешивали 20 мин при комнатной температуре. Прибавляли каплю спиртового раствора (фенолфталеина и затем 0,5N NaOH до розовой окраски (pH 8,0). После этого вводили 125 мкл буфера 1 М трис-HCl (pH 7,5) и перемешивали 5 мин (окраска исчезала). Прибавляли 2,96 мл водного раствора NaBH4 (4 мг/мл), перемешивали 30 мин. Раствор конъюгата диализовали 24 часа против 50 объемов дистиллированной воды. Продукт осаждали охлажденным этанолом (189 мл 5 час) и центрифугировали. Осадок 3 раза промывали ацетоном и высушивали на воздухе. Выход – 60% от теоретического (расчет на диальдегиддекстран). Конечный продукт представляет собой растворимый в воде порошок желтовато-белого цвета. Общий выход конъюгата – 32,4% от теоретического, расчет на декстран. Весовое содержание изониазида в конъюгате составляет 6,79% – 9,16% (молярное соотношение изониазид/декстран 34,1 – 47,3). Концентрацию изониазида определяли спектрофотометрически. Конъюгат изониазид-декстран устойчив при 4-6oC при хранении в сухом виде по крайней мере в течение 1,5 лет. Снижения общего содержания изониазида в продукте или его отщепления не обнаружено. С помощью спектроскопии протонного магнитного резонанса было установлено, что изониазид присоединен к декстрану одинарной C-N связью. Двойная связь C=N, группы CHO и COOH отсутствуют. Спектр протонного магнитного резонанса был записан в ИХКиГ СО РАН на ЯМР-спектрометре JEOL FX 90 Q. В инфракрасном спектре (записан ИНХ СО РАН на спектрофотометре SPECORD – IR) имеются полосы поглощения карбонильной группы и пиридинового кольца изониазида. Таким образом, спектральные данные вполне согласуются с химическим строением конъюгата. 2. Сведения, подтверждающие снижение дистрофических и некротических изменений в печени (снижение гепатотоксичности) при использовании предлагаемого препарата. Эксперименты проводили на мышах-самцах линии BALB/c двухмесячного возраста, массой тела 20-22 г. Животных содержали на стандартной лабораторной диете, они имели свободный доступ к воде и пище. Диссеминированный туберкулезный процесс моделировали однократным интраперитонеальным введением животным вакцины БЦЖ (НИИЭМ им. Н.Ф.Гамалеи, г. Москва). Каждому животному вводили 0,5 мл вакцины на физиологическом растворе. У мышей подопытной серии через 1 месяц после заражения развивалось диссеминированное гранулематозное туберкулезное воспаление с поражением всех паренхиматозных органов, что указывало на генерализованность процесса. Животные были разделены на три группы. Первая группа – нелеченные – служила контролем. Мышей второй группы через 1 месяц после заражения начинали лечить в интермиттирующем режиме (2 раза в неделю) внутрибрюшинными инъекциями свободного изониазида в дозе 14 мг на 1 кг массы тела (Машковский М.Д., там же). Мышей третьей группы в те же сроки и в том же режиме лечили комплексной формой изониазида на декстрановой матрице с молекулярной массой 65-75 тысяч Дальтон, т. е. предлагаемым препаратом. Лечение продолжали в течение 5 месяцев. Для исследования органы у животных второй и третьей групп получали через 1, 2, 3 и 5 месяцев от начала лечения, контрольной группы – через 1 и 5 месяцев с момента введения вакцины БЦЖ. Для морфологического исследования в каждой группе использовали по 8-10 мышей. Образцы печени для целей световой и электронной микроскопии брали из края левой латеральной доли и подвергали соответствующим стандартным обработкам согласно рекомендациям (Меркулов Г.А. Курс патолого-гистологической техники. – Л.: Медицина, 1969. – 645 с.; Волкова О.В., Елецкий Ю.К. Основы гистологии и гистологической техники. – М.: Медицина. – 1971. – С. 243-254; Миронов А.А., Комиссарчик Я.Ю., Миронов В.А. Методы электронной микроскопии в биологии и медицине: Методическое руководство. – Спб.: Наука, 1994. – 400 с.). Морфометрическое исследование образцов проводили в соответствии с рекомендациями (Автандилов Г.Г. Медицинская морфометрия. Руководство. – М.: Медицина, 1990. – 384 с.). Препараты печени подвергали морфометрическому изучению с использованием окулярной сетки из 25 точек (Автандилов Г.Г., там же). Подсчитывали объемную плотность некрозов и зон с дистрофическими изменениями гепатоцитов. Результаты морфометрического анализа дистрофических и некротических изменений в паренхиме печени мышей представлены на фиг. 1 и 2. Дистрофические изменения гепатоцитов в группах леченых животных носили характер преимущественно вакуольной дистрофии. В динамике лечения свободным изониазидом дистрофические и некротические изменения в паренхиме печени животных постепенно нарастали. Через 5 мес лечения, в сравнении с 1 мес, у животных этой группы объем дистрофически измененных гепатоцитов увеличился на 20%, объем зон некрозов паренхимы печени – на 28% и величины этих параметров были выше, чем в группе контроля, что связано с токсическим воздействием свободного изониазида и его метаболитов на клетки паренхимы печени. При лечении предлагаемым препаратом объем зон с деструктивными изменениями гепатоцитов, начиная со 2-го месяца, постепенно снижался и через 5 мес лечения объем дистрофически измененных гепатоцитов уменьшился на 46%, некрозов – на 76%, что соответственно в 2,1 и 3,1 раза ниже, чем у животных группы контроля. В целом, объем деструктивных процессов в паренхиме печени животных при лечении предлагаемым препаратом оказался в 2,2 раза меньшим в сравнении с нелеченными животными и в 3,7 раза меньшим в сравнении с леченными свободным изониазидом. 3. Сведения, подтверждающие получение технического результата. Проводя косвенным образом сравнительный анализ токсического поражения печени при использовании предлагаемого препарата и прототипа, получили следующие результаты. В исследованиях прототипа (Чернова Т.Г. Морфологические изменения в печени при хроническом генерализованном туберкулезном процессе и лечении пролонгированным препаратом изониазида в эксперименте / Дис. … канд. мед. наук. – Новосибирск. – 1993. – 199 с.) показано, что объем деструктивных изменений в паренхиме печени через 3 мес лечения был на 60% меньшим, чем при лечении свободным изониазидом в эти же сроки. Согласно данным наших исследований, через 3 мес лечения предлагаемым препаратом объем деструктивных изменений в печени оказался в 2,25 раза меньшим, чем у животных, получавших в течение этого периода свободный изониазид. При этом, начиная со второго месяца лечения предлагаемым препаратом, объем дистрофических и некротических изменений в паренхиме печени постепенно снижался и через 5 мес лечения был в 3,7 раза меньшим, в сравнении с леченными свободным изониазидом животными. Формула изобретения
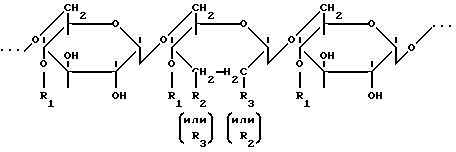 где R1 – H, остаток глюкозы или полиглюкозильный остаток указанного на рисунке вида; R2 – остаток изониазида формулы 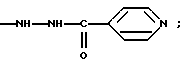 R3 – гидроксильная группа. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 07.12.2002
Номер и год публикации бюллетеня: 10-2004
Извещение опубликовано: 10.04.2004
|
||||||||||||||||||||||||||
