Патент на изобретение №2398800
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) N-АЛКИЛАЗАКРАУНСОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ В КАЧЕСТВЕ ОПТИЧЕСКИХ МОЛЕКУЛЯРНЫХ СЕНСОРОВ ДЛЯ ОПРЕДЕЛЕНИЯ КАТИОНОВ ЩЕЛОЧНЫХ И ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
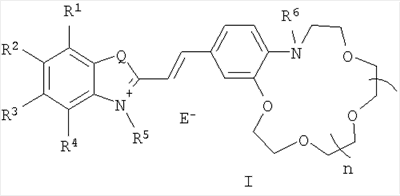
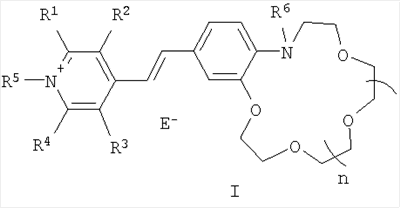
Изобретение относится к органической химии, а именно к новому типу соединений – N-алкилазакраунсодержащим стириловым красителям общей формулы I:
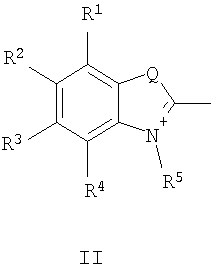
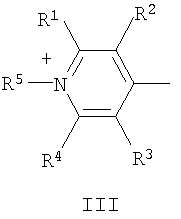
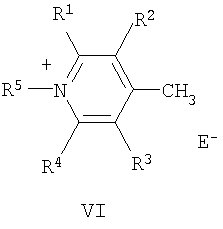
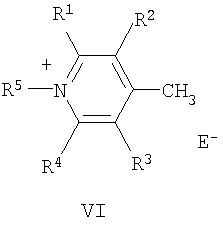
в которой А+ – гетероциклический остаток формулы (II) или (III):
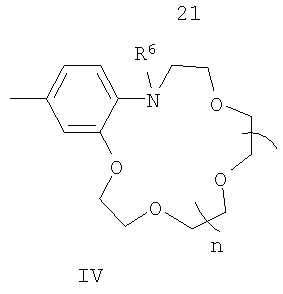
В в формуле (I) – фрагмент N-алкилбензоазакраун-эфира формулы (IV):
где R6 – низший алкил; n=0-3; к способу их получения, а также к новым композитным пленочным материалам на основе красителей (I), проявляющим эффективные оптические хемосенсорные свойства по отношению к катионам щелочных и щелочноземельных металлов. 3 н. и 1 з.п. ф-лы, 4 табл.
Изобретение относится к органической химии и химии материалов, а именно к новому типу соединений общей формулы (I):
в которой А+ – гетероциклический остаток формулы (II) или (III):
где R1-R4 – атом водорода, низший алкил, низшая алкоксильная группа, два заместителя R1 и R2 или R3 и R4 вместе составляют С4Н4-бензогруппу; R5 – алкил; Q – атом серы, группа СН=СН; Е в формуле (I) = Cl, Br, I, ClO4, PF6, BF4, TsO, CH3SO3, CF3SO3, CH3OSO3; В в формуле (I) – фрагмент N-алкилбензоазакраун-эфира формулы (IV):
где R6 – низший алкил; n=0-3; а также к новым полимерным пленкам и мембранам на основе красителей (I). Полученные соединения и композитные материалы на их основе могут быть использованы в составе оптических хемосенсоров для колориметрического и люминесцентного определения катионов щелочных и щелочноземельных металлов, например, в составе полимерных пленок, мембран и ультратонких пленок для определения микроколичеств указанных ионов в биологических жидкостях, в промышленных водах и стоках, для мониторинга окружающей среды. Изобретение относится также к способам получения таких соединений и материалов. Указанный тип соединений и пленочные хемосенсорные композитные материалы на их основе, их свойства и способ получения в литературе не описаны. Заявляемый новый тип соединений имеет структуру, не относящуюся ни к одному из известных типов структур. Предложенный класс соединений содержит неизвестное ранее сочетание фрагментов стирилового красителя и моноазакраун-эфира, конденсированных таким образом, что атом азота макрогетероцикла находится в сопряжении с бензольным циклом и в пара-положении к этиленовой группе, что и позволяет отнести эти соединения к новому типу красителей. Известны катионные красители стирилового ряда [Berlin L., Reister О., “Methoden zur Herstellung von Cyaninen (Polymethinen)”, In “Methoden der Organischen Chemie”, Edn. Miller E, B. 5/1 d, Georg Thieme Verlag, Stuttgart, 1972, 227; Фикен Г.Е. Цианиновые красители. В кн. Химия синтетических красителей. Под ред. Венкатарамана К., т.4, Л.: Химия, 1975, 207; Гордон П., Грегори П. “Органическая химия красителей”, М.: Мир, 1987, 344], особенностью строения которых является наличие четвертичного гетероциклического ядра, связанного посредством двойной углерод-углеродной связи с замещенным бензольным ядром. Эти красители не способны к комплексообразованию с катионами металлов и аммония, поскольку не имеют макрогетероциклического фрагмента. В литературе описаны стириловые красители, в которых гетероциклический остаток соединен через одну двойную углерод-углеродную связь с фрагментом N-фенилазакраун-эфира [Ушаков Е.Н., Громов С.П., Федорова О.А., Алфимов М.В., Изв. АН. Сер. хим., 1997, 484]. Для них характерны наличие поглощения в области 500-550 нм и способность к комплексообразованию с катионами щелочных и щелочноземельных металлов. Однако константы устойчивости таких комплексов с катионами металлов невысоки из-за слабого участия атома азота макроцикла в координации катиона металла и из-за конформационной подвижности макроцикла N-фенилазакраун-эфира. Это не позволяет использовать стириловые красители с фрагментом N-фенилазакраун-эфира в качестве эффективных оптических молекулярных сенсоров на катионы металлов и аммония. В литературе описаны стириловые красители, в которых гетероциклический остаток соединен через одну двойную углерод-углеродную связь с фрагментом краун-эфира или тиакраун-эфира [Громов С.П., Федорова О.А., Фомина М.В., Алфимов М.В., Патент 2012574 РФ, Бюл. изобр., 1994, Целью настоящего изобретения является новый тип соединений – N-алкильные производные азакраунсодержащих стириловых красителей, в которых атом азота, входящий в состав фрагмента моноазакраун-эфира, находится в сопряжении с бензольным циклом и в пара-положении к этиленовой группе. Задачей изобретения является также разработка способа получения целевых продуктов, доказательство их строения и изучение их комплексообразующих, ионохромных и ионофлуорохромных свойств. Поставленная цель достигается структурой заявляемого нового типа стириловых красителей общей формулы (I) и способом их получения, заключающимся в том, что четвертичные соли метальных производных гетероциклических оснований общих формул (V) и (VI):
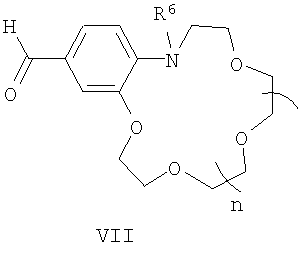
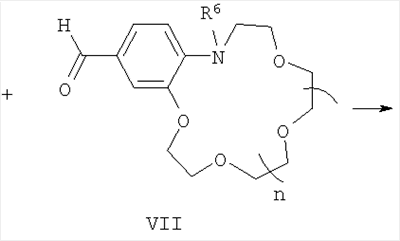
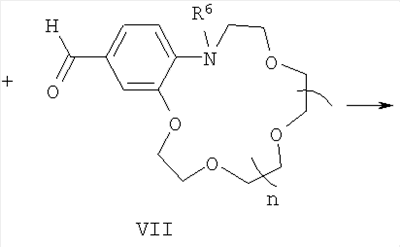
где R1-R5, Q и Е имеют указанные выше значения для формулы (I), при этом Е в формуле (I) и в формулах (V), (VI) могут быть одинаковыми или разными; подвергают взаимодействию с формильными производными N-алкилбензоазакраун-эфиров общей формулы (VII):
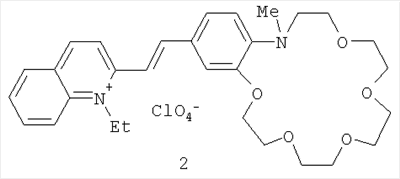
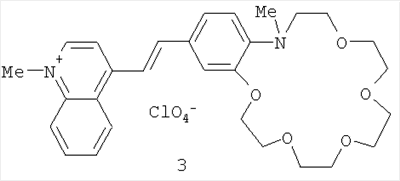
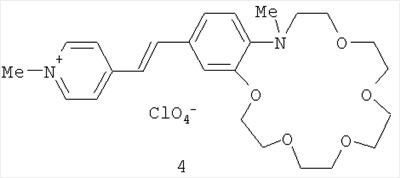
где R6 и n имеют указанные выше значения для формулы (I). Процесс проводят в среде органического растворителя, например спирта, в присутствии органических оснований, таких как пиридин, пиперидин, пирролидин, триэтиламин (или без них) при температурах 20-140°С. Реакцию можно проводить с последующей заменой анионов в (I) обработкой кислотами, солями кислот с иными противоионами (или без замены аниона). Конденсация указанных четвертичных солей метильных производных гетероциклических оснований общих формул (V) и (VI) с формильными производными N-алкилбензоазакраун-эфиров общей формулы (VII) до настоящего времени не была известна. Согласно предлагаемому способу синтез стириловых красителей общей формулы (I) осуществляют конденсацией активированной в четвертичных солях гетероциклических оснований общих формул (V) и (VI) метильной группы с карбонильной группой формильных производных азакраун-эфиров общей формулы (VII) с образованием двойной углерод-углеродной связи. Строение полученных соединений общей формулы (I) доказано с помощью спектроскопии ЯМР 1H и 13С, электронной спектроскопии, а также данными элементного анализа (примеры 1-9). Пример 1. Перхлорат 3-этил-2-[(E)-2-(13-метил-2,3,5,6,8,9,12,13-октагидро-11H-1,4,7,10,13-бензотетраоксаазациклопентадецин-16-ил)этенил]-1,3-бензотиазолия-3. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 27 мг (0.10 ммоля) перхлората 3-этил-2-метилбензотиазолия, 37 мг (0.12 ммоля) формильного производного N-метилбензоаза-15-краун-5-эфира, 0.03 мл пиридина и 5 мл абс. этанола. Реакционную смесь нагревают при кипении на масляной бане в течение 10 ч, охлаждают до -10°С, осадок отфильтровывают, четырежды промывают холодным абс. этанолом и высушивают на воздухе. Получают 49 мг (выход 89%) красителя в виде темно-красных кристаллов, т.пл. 194-196°С. Спектр ЯМР 1Н (500 МГц, в ДМСО-d6, 30°С): 1.46 (т, 3 Н, MeCH2, J=7.3 Гц); 2.95 (с, 3 Н, MeN); 3.43 (т, 2 Н, CH2CH2H, J=7.3 Гц); 3.59 (с, 4 Н, 2 CH2O); 3.63 (м, 4 Н, 2 CH2O); 3.87 (м, 4 Н, CH2CH2H, CH2CH2OAr); 4.24 (м, 2 Н, CH2OAr); 4.90 (к, 2 Н, CH2N+, J=7.3 Гц); 6.91 (д, 1 Н, Н(14), J=8.6 Гц); 7.55 (д, 1 Н, Н(17), J=1.8 Гц); 7.57 (д.д, 1 Н, Н(15), J=8.6 Гц, J=1.8 Гц); 7.70 (д, 1 Н, СН=CHHet, 3Jтранс=15.4 Гц); 7.73 (м, 1 Н, Н(6)); 7.82 (м, 1 Н, Н(5)); 8.10 (д, 1 Н, CH=CHHet, 3Jтранс=15.4 Гц); 8.19 (д, 1 Н, Н(4), J=8.6 Гц); 8.35 (д, 1 Н, Н(7), J=7.7 Гц). Спектр ЯМР 13С (125 МГц, в ДМСО-d6, 27°С): 13.88 (MeCH2); 39.84 (MeN); 43.73 (CH2N+); 54.33 (CH2CH2N); 68.23 (CH2OAr); 68.37 (CH2O); 68.56 (CH2O); 68.88 (CH2O); 68.94 (CH2O); 69.08 (CH2O); 70.06 (CH2O); 107.83 (CH=CHHet); 112.19 (C(17)); 115.61 (C(14)); 115.94 (C(4)); 124.04 (C(7)); 124.97 (C(16)); 126.59 (C(15)); 127.48 (C(8)); 127.70 (С(6)); 129.10 (С(5)); 140.77 (С(9)); 146.46 (С(13а)); 149.20 (С(17а)); 150.07 (CH=CHHet); 171.04 (C(2)). УФ-спектр (ацетонитрил), нм: 518 ( Найдено, %; С 54.74; Н 5.79; N 4.81. C26H33ClN2O8S. Вычислено, %: С 54.88; Н 5.85; N 4.92. Пример 2. Перхлорат 3-этил-2-[(E)-2-(16-метил-2,3,5,6,8,9,11,12,15,16-декагидро-14H-1,4,7,10,13,16-бензопентаоксаазациклооктадецин-19-ил)этенил]-1,3-бензотиазолия-3. Получен аналогично примеру 1 из перхлората 3-этил-2-метилбензотиазолия и формильного производного N-метилбензоаза-18-краун-6-эфира с выходом 70% в виде темно-красных кристаллов, т.пл. 186-188°С. Спектр ЯМР 1H (500 МГц, в ДМСО-d6, 30°С): 1.45 (т, 3 Н, МеСН2, J=7.3 Гц); 3.02 (с, 3 Н, MeN); 3.53 (м, 4 Н, CH2O); 3.56 (м, 4 Н, 2 CH2O); 3.59 (т, 2 Н, CH2CH2N, J=5.9 Гц); 3.62 (м, 4 Н, 2 CH2O); 3.75 (т, 2 Н, CH2CH2N, J=5.9 Гц); 3.86 (м, 2 Н, CH2CH2OAr); 4.22 (м, 2 Н, CH2OAr); 4.90 (к, 2 Н, CH2N+, J=7.3 Гц); 6.88 (д, 1 Н, Н(17), J=8.2 Гц); 7.56 (уш.с, 1 Н, Н(20)); 7.58 (д.д, 1 Н, Н(18), J=8.2 Гц, J=1.8 Гц); 7.69 (д, 1 Н, СН=CHHet, 3Jтранс=15.4 Гц); 7.72 (м, 1 Н, Н(6)); 7.82 (м, 1 Н, Н(5)); 8.10 (д, 1 Н, СH=CHHet, 3Jтранс=15.4 Гц); 8.19 (д, 1 Н, Н(4), J=8.6 Гц); 8.35 (д, 1 Н, Н(7), J=7.7 Гц). Спектр ЯМР 13С (125 МГц, в ДМСО-d6, 30°С): 13.76 (MeCH2); 40.70 (MeN); 43.61 (CH2N+); 53.88 (CH2CH2N); 67.78 (CH2OAr); 68.72 (CH2CH2OAr); 69.16 (CH2O); 69.65 (CH2CH2N, CH2O); 69.77 (CH2O); 69.87 (CH2O); 70.11 (CH2O); 70.42 (CH2O); 107.39 (CH=CHHet); 112.57 (C(20)); 115.57 (C(17)); 115.79 (C(4)); 123.92 (C(7)); 124.54 (C(19)); 126.86 (C(18)); 127.34 (C(8)); 127.57 (C(6)); 129.00 (C(5)); 140.69 (C(9)); 146.02 (C(16a)); 148.70 (C(20a)); 150.01 (CH=CHHet); 170.89 (C(2)). УФ-спектр (ацетонитрил), нм: 526 ( Найдено, %: С 54.65; Н 6.08; N 4.39. C28H37ClN2O9S. Вычислено, %: С 54.85; Н 6.08; N 4.57. Пример 3. Перхлорат 1-этил-2-[(E)-2-(13-метил-2,3,5,6,8,9,12,13-октагидро-11H-1,4,7,10,13-бензотетраоксаазациклопентадецин-16-ил)этенил]хинолиния. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 16 мг (0.06 ммоля) перхлората 1-этил-2-метилхинолиния, 22 мг (0.07 ммоля) формильного производного N-метилбензоаза-15-краун-5-эфира, 0.02 мл пирролидина и 3 мл абс. этанола. Реакционную смесь нагревают при кипении на масляной бане в течение 10 ч, охлаждают до -10°С, осадок отфильтровывают, четырежды промывают холодным абс. этанолом и высушивают на воздухе. Получают 19 мг (выход 57%) красителя в виде темно-сиреневых кристаллов, т.пл. 199-201°С. Спектр ЯМР 1Н (500 МГц, в ДМСО-d6, 30°С): 1.56 (т, 3 Н, МеСН2, J=7.3 Гц); 2.91 (с, 3 Н, MeN); 3.36 (т, 2 Н, CH2CH2N J=7.3 Гц); 3.59 (с, 4 Н, 2 CH2O); 3.63 (м, 4 Н, 2 CH2O); 3.87 (м, 4 Н, CH2CH2H, CH2CH2OAr); 4.24 (м, 2 Н, CH2OAr); 5.12 (к, 2 Н, CH2N+, J=7.3 Гц); 6.91 (д, 1 Н, Н(14), J=8.6 Гц); 7.49 (уш.д, 1 Н, Н(15), J=8.6 Гц); 7.50 (уш.с, 1 Н, Н(17)); 7.57 (д, 1 Н, СН=CHHet, 3Jтранс=15.4 Гц); 7.89 и 8.14 (2 м, по 1 Н каждый, Н(6) и Н(7)); 8.25 (д, 1 Н, СР=CHHet, 3Jтранс=15.4 Гц); 8.30 и 8.50 (д.д. и д, по 1 Н каждый, Н(5) и Н(8), J=8.2 Гц, J=1.4 Гц и J=9.1 Гц); 8.54 (д, 1 Н, Н(3), J=9.1 Гц); 8.91 (д, 1 Н, Н(4), J=9.1 Гц). УФ-спектр (ацетонитрил), нм: 507 ( Найдено, %: С 59.92; Н 6.31; N 4.87. C28H35ClN2O8. Вычислено, %: С 59.73; Н 6.27; N 4.98. Пример 4. Перхлорат 1-этил-2-[(E)-2-(16-метил-2,3,5,6,8,9,11,12,15,16-декагидро-14H-1,4,7,10,13,16-бензопентаоксаазациклооктадецин-19-ил)этенил]хинолиния. Получен аналогично примеру 3 из перхлората 1-этил-2-метилхинолиния и формильного производного N-метилбензоаза-18-краун-6-эфира с выходом 50% в виде темно-сиреневых кристаллов, т.пл. 184-186°С. Спектр ЯМР 1H (500 МГц, в ДМСО-d6, 30°С): 1.56 (т, 3 Н, МеСН2, J=7.3 Гц); 2.98 (с, 3 Н, MeN); 3.53 (м, 6 Н, CH2CH2H, 2 CH2O); 3.56 (м, 4 Н, 2 CH2O); 3.63 (м, 4 Н, 2 CH2O); 3.75 (т, 2 Н, CH2CH2H, J=5.9 Гц); 3.87 (м, 2 Н, CH2CH2OAr); 4.24 (м, 2 Н, CH2OAr); 5.12 (к, 2 Н, CH2N+, J=7.3 Гц); 6.89 (д, 1 Н, Н(17), J=8.2 Гц); 7.49 (д.д, 1 Н, Н(18), J=8.2 Гц, J=1.8 Гц); 7.50 (уш.с, 1 Н, Н(20)); 7.56 (д, 1 Н, СН=CHHet, 3Jтранс=15.4 Гц); 7.89 и 8.13 (2 м, по 1 Н каждый, Н(6) и Н(7)); 8.25 (д, 1 Н, CH=CHHet, 3Jтранс=15.4 Гц); 8.29 и 8.49 (2 д, по 1 Н каждый, Н(5) и Н(8), J=8.2 Гц и J=9.1 Гц); 8.53 (д, 1 Н, Н(3), J=9.1 Гц); 8.89 (д, 1 Н, Н(4), J=9.1 Гц). УФ-спектр (ацетонитрил), нм: 512 ( Найдено, %: С 59.32; Н 6.46; N 4.61. C30H39ClN2O9. Вычислено, %: С 59.35; Н 6.48; N 4.61. Пример 5. Перхлорат 1-метил-4-[(E)-2-(16-метил-2,3,5,6,8,9,11,12,15,16-декагидро-14H-1,4,7,10,13,16-бензопентаоксаазациклооктадецин-19-ил)этенил]хинолиния. В двугорлой колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 19 мг (0.07 ммоля) перхлората 1,4-диметилхинолиния, 31 мг (0.09 ммоля) формильного производного N-метилбензоаза-18-краун-6-эфира, 0.02 мл пирролидина и 4 мл абс. этанола. Реакционную смесь нагревают при кипении на масляной бане в темноте в атмосфере аргона в течение 10 ч и охлаждают до -10°С. Образовавшийся осадок отфильтровывают, четырежды промывают холодным абс. этанолом и высушивают на воздухе. Получают 29 мг (выход 66%) красителя в виде темно-фиолетовых кристаллов, т.пл. 224-225°С. Спектр ЯМР 1Н (500 МГц, в ДМСО-d6, 30°С): 2.94 (с, 3 Н, MeN); 3.46 (т, 2 Н, CH2N, J=5.9 Гц); 3.56 (м, 4 Н, 2 СН2О); 3.59 (с, 4 Н, 2 CH2O); 3.63 (м, 4 Н, 2 CH2O); 3.74 (т, 2 Н, CH2CH2N, J=5.9 Гц); 3.87 (м, 2 Н, CH2CH2OAr); 4.26 (м, 2 Н, CH2OAr); 4.48 (с, 3 Н, MeN+); 6.88 (д, 1 Н, Н(17), J=8.2 Гц); 7.40 (д.д, 1 Н, Н(18), J=8.2 Гц, J=1.4 Гц); 7.58 (уш.с, 1 Н, Н(20)); 8.03 (м, 1 Н, Н(6)); 8.12 (м, 2 Н, СН=СН); 8.24 (м, 1 Н, Н(7)); 8.38 (м, 2 Н, Н(3), Н(8)); 9.04 (д, 1 Н, Н(5), J=8.6 Гц); 9.12 (д, 1 Н, Н(2), J=6.4 Гц). УФ-спектр (ацетонитрил), нм: 519 ( Найдено, %: С 58.75; Н 6.31; N 4.64. C29H37ClN2O9. Вычислено, %: С 58.73; Н 6.29; N 4.72. Пример 6. Иодид 1-метил-4-[(E)-2-(13-метил-2,3,5,6,8,9,12,13-октагидро-11H-1,4,7,10,13-бензотетраоксаазациклопентадецин-16-ил)-1-этенил]пиридиния. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 69 мг (0.29 ммоля) иодида 1,4-диметилпиридиния, 100 мг (0.32 ммоля) формильного производного N-метилбензоаза-15-краун-5-эфира, 0.07 мл пиперидина и 7 мл метанола. Реакционную смесь нагревают при кипении на масляной бане в течение 26 ч, затем тщательно упаривают в вакууме. Остаток четырежды экстрагируют кипящим бензолом, нерастворившееся вещество отделяют декантацией и высушивают на воздухе. Получают 137 мг (выход 89%) красителя в виде темно-красных кристаллов, т.пл. 210-212°С. Спектр ЯМР 1H (500 МГц, в ДМСО-d6, 30°С): 2.83 (с, 3 Н, MeN); 3.23 (т, 2 Н, CH2N, J=7.2 Гц); 3.58 (с, 4 Н, 2 CH2O); 3.61 (м, 4 Н, 2 CH2O); 3.86 (м, 4 Н, CH2CH2N, CH2CH2OAr); 4.17 (м, 2 Н, CH2OAr); 4.20 (с, 3 Н, MeN+); 6.88 (д, 1 Н, Н(14), J=8.3 Гц); 7.21 (д.д, 1 Н, Н(15), J=8.3 Гц, J=1.3 Гц); 7.29 (д, 1 Н, Н(17), J=1.3 Гц); 7.32 (д, 1 Н, CH=CHPy, 3Jтранс=16.2 Гц); 7.90 (д, 1 Н, CH=CHPy, 3Jтранс=16.2 Гц); 8.08 (д, 2 Н, Н(3), Н(5), J=6.6 Гц); 8.74 (д, 2 Н, Н(2), Н(6), J=6.6 Гц). Спектр ЯМР 13С (125 МГц, в ДМСО-d6, 30°С): 39.42 (MeN); 46.46 (MeN+); 54.54 (CH2N); 67.77 (CH2OAr); 68.19 (CH2O); 68.58 (CH2O); 68.70 (CH2O); 68.94 (2 СН2О), 70.00 (CH2O); 110.29 (С(17)); 116.15 (С(14)); 119.32 (СН=CHPy); 122.43 (С(3), С(5)); 123.17 (С(15)); 126.81 (С(16)); 141.24 (CH=CHPy); 144.31 (С(13а)); 144.44 (С(2), С(6)); 149.88 (С(17а)); 152.91 (С(4)). УФ-спектр (ацетонитрил), нм: 456 ( Найдено, %: С 50.18; Н 6.29; N 4.95. C23H31IN2O4·1.5H2O. Вычислено, %: С 49.92; Н 6.19; N 5.06. Пример 7. Иодид 1-метил-4-[(Е)-2-(16-метил-2,3,5,6,8,9,11,12,15,16-декагидро-14H-1,4,7,10,13,16-бензопентаоксаазациклооктадецин-19-ил)-1-этенил]пиридиния. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 45 мг (0.19 ммоля) иодида 1,4-диметилпиридиния, 80 мг (0.23 ммоля) формильного производного N-метилбензоаза-18-краун-6-эфира, 0.04 мл пирролидина и 6 мл абс. этанола. Реакционную смесь нагревают при кипении на масляной бане в течение 25 ч, затем тщательно упаривают в вакууме. Остаток четырежды экстрагируют кипящим бензолом, нерастворившееся вещество отделяют декантацией и высушивают на воздухе. Получают 59 мг (выход 54%) красителя в виде темно-красных кристаллов, т.пл. 163-164°С. Спектр ЯМР 1H (500 МГц, в ДМСО-d6, 30°С): 2.90 (с, 3 Н, MeN); 3.41 (т, 2 Н, CH2N, J=6.0 Гц); 3.54 (м, 4 Н, 2 CH2O); 3.55 (м, 4 Н, 2 CH2O); 3.62 (м, 4 Н, 2 CH2O); 3.72 (т, 2 Н, CH2CH2N, J=6.0 Гц); 3.85 (м, 2 Н, CH2CH2OAr); 4.17 (м, 2 Н, CH2OAr); 4.20 (с, 3 Н, MeN+); 6.86 (д, 1 Н, Н(17), J=8.2 Гц); 7.22 (д.д, 1 Н, Н(18), J=8.2 Гц, J=1.4 Гц); 7.30 (уш.с, 1 Н, Н(20)); 7.32 (д, 1 Н, CH=CHPy, 3Jтранс=15.9 Гц); 7.91 (д, 1 Н, CH=CHPy, 3Jтранс=15.9 Гц); 8.08 (д, 2 Н, Н(3), Н(5), J=6.6 Гц); 8.75 (д, 2 Н, Н(2), Н(6), J=6.6 Гц). Спектр ЯМР 13С (125 МГц, в ДМСО-d6, 30°С): 40.08 (MeN); 46.42 (MeN+); 53.82 (CH2N); 67.37 (CH2OAr); 68.78 (CH2CH2OAr); 69.23 (CH2O); 69.37 (CH2CH2N); 69.61 (CH2O); 69.82 (2 CH2O); 70.10 (CH2O), 70.31 (CH2O); 110.68 (С(20)); 116.30 (С(17)); 119.16 (CH=CHPy); 122.37 (С(3), С(5)); 123.36 (С(18)); 126.54 (С(19)); 141.24 (CH=CHPy); 143.94 (С(16а)); 144.42 (С(2), С(6)); 149.48(С(20а)); 152.92 (С(4)). УФ-спектр (ацетонитрил), нм: 456 ( Найдено, %: С 51.66; Н 6.02; N 4.78. C25H35IN2O5·0.5H2O. Вычислено, %: С 51.82; Н 6.26; N 4.83. Пример 8. Перхлорат 1-метил-4-[(Е)-2-(16-метил-2,3,5,6,8,9,11,12,15,16-декагидро-14H-1,4,7,10,13,16-бензопентаоксаазациклооктадецин-19-ил)-1-этенил]пиридиния. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 12 мг (0.06 ммоля) перхлората 1,4-диметилпиридиния, 24 мг (0.07 ммоль) формильного производного N-метилбензоаза-18-краун-6-эфира, 0.02 мл пирролидина и 3 мл абс. этанола. Реакционную смесь нагревают при кипении на масляной бане в темноте в атмосфере аргона в течение 11 ч и охлаждают до -10°С. Образовавшийся осадок отфильтровывают, четырежды промывают холодным абс. этанолом и высушивают на воздухе. Получают 23 мг (выход 73%) красителя в виде темно-красных кристаллов, т.пл. 191-193°С. Спектр ЯМР 1Н (500 МГц, в ДМСО-d6, 30°С): 2.89 (с, 3 Н, MeN); 3.40 (т, 2 Н, CH2N, J=5.9 Гц); 3.53 (м, 4 Н, 2 CH2O); 3.55 (м, 4 Н, 2 CH2O); 3.62 (м, 4 Н, 2 СН2О); 3.71 (т, 2 Н, CH2CH2N, J=5.9 Гц); 3.84 (м, 2 Н, CH2CH2OAr); 4.17 (м, 2 Н, CH2OAr); 4.19 (с, 3 Н, MeN+); 6.85 (д, 1 Н, Н(17), J=8.2 Гц); 7.21 (д.д, 1 Н, Н(18), J=8.2 Гц, J=1.4 Гц); 7.29 (д, 1 Н, Н(20), J=1.4 Гц); 7.30 (д, 1 Н, CH=CHPy, 3Jтранс=16.4 Гц); 7.89 (д, 1 Н, CH=CHPy, 3Jтранс=16.4 Гц); 8.07 (д, 2 Н, Н(3), Н(5), J=6.8 Гц); 8.73 (д, 2 Н, Н(2), Н(6), J=6.8 Гц). Спектр ЯМР 13С (125 МГц, в ДМСО-d6, 30°С): 40.08 (MeN); 46.42 (MeN+); 53.82 (CH2N); 67.37 (CH2OAr); 68.78 (CH2CH2OAr); 69.23 (CH2O); 69.37 (CH2CH2N); 69.61 (CH2O); 69.82 (2 CH2O); 70.10 (CH2O), 70.31 (CH2O); 110.68 (С(20)); 116.30 (С(17)); 119.16 (CH=CHPy); 122.37 (С(3), С(5)); 123.36 (С(18)); 126.54 (С(19)); 141.24 (CH=CHPy); 143.94 (С(16а)); 144.42 (С(2), С(6)); 149.48 (С(20а)); 152.92 (С(4)). УФ-спектр (ацетонитрил), нм: 459 ( Найдено, %: С 55.39; Н 6.58; N 5.18. C25H35CIN2O9. Вычислено, %: С 55.30; Н 6.50; N 5.16. Пример 9. Перхлорат 4-[(E)-2-(16-Метил-2,3,5,6,8,9,11,12,15,16-декагидро-14H-1,4,7,10,13,16-бензопентаоксаазациклооктадецин-19-ил)винил]-1-октадецилпиридиния. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 26 мг (0.06 ммоля) перхлората 4-метил-1-октадецилпиридиния, 25 мг (0.07 ммоль) формильного производного N-метилбензоаза-18-краун-6-эфира, 0.02 мл пирролидина и 4 мл абс. этанола. Реакционную смесь нагревают при кипении на масляной бане в темноте в атмосфере аргона течение 25 ч и охлаждают до -10°С. Образовавшийся осадок отфильтровывают, четырежды промывают холодным абс. этанолом и высушивают на воздухе. Получают 24 мг (выход 52%) красителя в виде темно-красных кристаллов, т.пл. 92-94°С. Спектр ЯМР 1H (500 МГц, в ДМСО-d6, 30°С): 2.89 (т, 3 Н, MeN, J=7.0 Гц); 1.22 (м, 30 Н, 15 СН2); 1.88 (м, 2 Н, MeCH2); 3.40 (т, 2 Н, CH2N, J=6.2 Гц); 3.53 (м, 4 Н, 2 CH2O); 3.54 (м, 4 Н, 2 CH2O); 3.61 (м, 4 Н, 2 CH2O); 3.71 (т, 2 Н, CH2CH2N, J=6.1 Гц); 3.84 (м, 2 Н, CH2CH2OAr); 4.16 (м, 2 Н, CH2OAr); 4.42 (т, 2 Н, CH2N+, J=7.3 Гц); 6.85 (д, 1 Н, Н(17), J=8.2 Гц); 7.22 (д.д, 1 Н, Н(18), J=8.2 Гц, J=1.4 Гц); 7.29 (уш.с, 1 Н, Н(20)); 7.31 (д, 1 Н, CH=CHPy, 3Jтранс=15.9 Гц); 7.91 (д, 1 Н, CH=CHPy, 3Jтранс=15.9 Гц); 8.09 (д, 2 Н, Н(3), Н(5), J=6.8 Гц); 8.81 (д, 2 Н, Н(2), Н(6), J=6.8 Гц). УФ-спектр (ацетонитрил), нм: 459 ( Найдено, %: С 64.68; Н 8.98; N 3.69. C42H69ClN2O9. Вычислено, %: С 64.55; Н 8.90; N 3.58. Остальные соединения были получены способами, аналогичными примерам 1, 3 или 5-9. Изучены комплексообразующие, ионохромные и ионофлуорохромные свойства полученных азакраунсодержащих стириловых красителей (I) из примеров 1 (1a), 2 (1b), 4 (2), 5 (3) и 8 (4) в ацетонитрильных растворах. Методом ЯМР 1Н-титрования измерены константы устойчивости комплексов красителей 1b и 2 с биогенными катионами Na+, K+, Mg2+ и Ca2+ в ацетонитриле-d3 (содержание воды <0.05%). В таблице 1 приведены значения констант устойчивости комплексов состава 1:1, которые указывают на очень высокую селективность связывания 1b и 2 с катионами кальция (коэффициенты селективности Ca2+/Mm+ (m=1,2)>103).
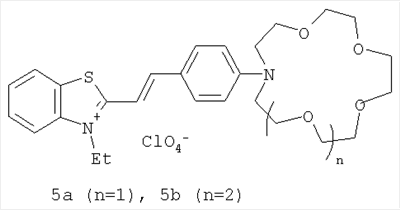
В таблице 2 приведены основные абсорбционные и люминесцентные характеристики красителей 1a,b и 2-4 и их комплексов состава 1:1 с катионами щелочных и щелочноземельных металлов. Константы устойчивости комплексов красителей 1a,b и 2, измеренные методом спектрофотометрического титрования, даны в таблице 3. Для сравнения в таблице 4 приведены основные абсорбционные характеристики и константы устойчивости комплексов с катионами металлов для стириловых красителей 5a,b, отличающихся от красителей 1a,b тем, что вместо фрагмента N-метилбензоазакраун-эфира содержат соответствующий по размеру фрагмент N-фенилазакраун-эфира [Ушаков Е.Н., Громов С.П., Федорова О.А., Алфимов М.В., Изв. АН. Сер. хим., 1997, 484; Насимова И.Р., Ушаков Е.Н., Махаева Е.Е., Федорова О.А., Громов С.П., Алфимов М.В., Хохлов А.Р., Высокомол. соединения. Сер. А, 2002, 44, 2171; Ушаков Е.Н., Дисс. док. хим. наук, ИПХФ РАН, Черноголовка, 2006]. Количественные данные, приведенные в таблицах 2-4, убедительно свидетельствуют о том, что новые хромогенные бензоазакраун-эфиры 1a,b и 2-4 значительно превосходят аналогичные хромогенные N-фенилазакраун-эфиры 5a,b как по термодинамической устойчивости комплексов с катионами щелочных и щелочноземельных металлов, так и по величине ионохромного эффекта. Краситель 1а в сравнении с ранее известными донорно-акцепторными хромоионофорами на основе краун-эфиров [Ушаков Е.Н., Алфимов М.В., Громов С.П. Успехи химии, 2008, 77, 39] демонстрирует рекордные величины ионохромного эффекта для ионов Li+ и Na+ (105 и 95 нм, соответственно). Красители 1b и 2 характеризуются очень высокими коэффициентами селективности Ca2+/Mg2+ (>105) в сочетании с большими величинами ионохромного эффекта для Ca2+ (127 и 117 нм, соответственно). Кроме того, красители 1b-4 способны действовать не только как колориметрические молекулярные сенсоры, но и как «включающиеся» люминесцентные сенсоры. Например, при комплексообразовании красителя 4 с ионом Ва2+ квантовый выход люминесценции возрастает в 60 раз.
Таким образом, предварительные результаты исследования красителей общей формулы (I) показали, что в апротонной среде они способны селективно и с хорошим оптическим откликом связывать катионы щелочных и щелочноземельных металлов, то есть проявляют свойства оптических молекулярных сенсоров. Эти свойства сохраняются в полимерных композитных пленках, что позволяет создать на основе полученных красителей оптические хемосенсорные материалы. Композитные материалы, заявляемые в данном изобретении, получают методом спин-коатинга из растворов в органическом растворителе, содержащих полимер, пластификатор, ионофор и краунсодержащий краситель общей формулы (I). Способ получения пленочного материала на кварцевой подложке технологически прост и доступен как в лабораторной практике, так и в процессе производства и является оптимальным для целей, указанных в данном изобретении. Важным достоинством этого метода получения пленок является возможность получения тонких пленок (толщиной менее микрона) и то, что процесс проводится при сравнительно низкой температуре, благодаря чему возможно введение нетермостойких добавок, например красителей, определяющих дальнейшее применение пленки. Однако стириловые красители ранее не вводились в полимерные пленки или композитные материалы указанным способом. Для получения хемосенсорных композитных материалов использовали следующие полимеры: целлюлозы ацетатфталат, целлюлозы ацетатгидрофталат, поливинилбутираль, полистирол и поливинилхлорид. В качестве пластификаторов использовали диоктиловый эфир себациновой кислоты, диоктилфталат, O-трифторметилоктиловый эфир. В качестве ионофора использовали дицетилфосфат натрия. В качестве ионофлуорофоров были взяты красители общей формулы (I) из примеров 7 и 8. Растворы полимеров, пластификаторов, ионофора и красителей готовили в следующих растворителях: хлороформе, метиленхлориде, дихлорэтане, тетрагидрофуране. Пленкообразующий раствор содержал в 1 мл растворителя (например, ТГФ) 30 мг полимера (например, поливинилхлорида), 50-60 мкл пластификатора (например, диоктилового эфира себациновой кислоты), 1 ммоль·л-1 дицетилфосфата натрия, 16 мг красителя общей формулы (I) с противоионами I– или ClO4 В качестве подложки для приготовления пленок использовали кварцевые пластины размерами 20×13×1.3 мм. Пластины отмывали свежеприготовленной хромовой смесью с последующим многократным промыванием бидистиллированной водой. На подготовленную поверхность пластины, вращающейся на горизонтальном роторе центрифуги со скоростью 2000 об/мин, наносили 50 мкл пленкообразующего раствора в течение не более 0.5 с. Образовавшуюся пленку высушивали на воздухе в течение 30 мин. Дальнейшее увеличение времени высушивания не приводило к изменению параметров пленки. Толщина пленки, измеренная путем взвешивания, составляла 1-2 мкм. Полученные пленки, содержащие заявленные красители общей формулы (I), были исследованы в качестве ион-селективных оптических материалов для определения ионов Ca2+. Определение катионов кальция проводили методами флуоресценции и спектрофотометрии. В случае флуоресцентной регистрации кварцевую пластину с нанесенной пленкой помещали в стандартную флуорометрическую кювету с длиной оптического пути 10 мм по диагонали. Кювету располагали в держателе таким образом, чтобы угол падения возбуждающего луча составлял 60 градусов с поверхностью пленки, при этом пленка находилась на стороне пластины, обращенной в направлении возбуждающего света. В кювету вводили раствор соли кальция в концентрации, соответствующей физиологической концентрации кальция в плазме крови – 2.5 ммоль·л-1 и в меньших концентрациях в диапазоне 0.25-2.5 ммоль·л-1. После добавления исследуемого раствора через определенные интервалы времени записывали спектры флуоресценции при возбуждении на длине волны 403 нм. В отсутствие катионов кальция наблюдается флуоресценция от хемосенсорной пленки с максимумом около 610 нм. В присутствии катионов кальция происходит коротковолновый сдвиг максимума флуоресценции, достигающий 60 нм при концентрации 2.5 ммоль·л-1. Выход на стационарное значение спектров флуоресценции и поглощения происходит экспоненциально с характерным временем 15 мин. При уменьшении концентрации катионов кальция спектр флуоресценции становится асимметричным вследствие того, что он состоит из двух сигналов: свободного (не связанного в комплекс) красителя и комплексов красителя с катионами кальция. Разложение этого сигнала на составляющие позволяет определить долю комплекса и тем самым концентрацию комплексов в растворе. Калибровочные зависимости величины сдвигов максимумов поглощения и флуоресценции от концентрации катионов кальция позволяют определять эти ионы в интервале концентраций 0.25-2.5 ммоль·л-1. Таким образом, получен новый тип азакраунсодержащих стириловых красителей – N-алкилазакраунсодержащие стириловые красители, содержащие неизвестное ранее сочетание фрагментов стирилового красителя и моноазакраун-эфира, конденсированных таким образом, что атом азота макрогетероцикла находится в сопряжении с бензольным циклом и в пара-положении к этиленовой группе и обнаружена их ярко выраженная способность к селективному связыванию катионов щелочных и щелочноземельных металлов как в апротонной, так и в водной среде, в том числе в составе полимерных матриц, характеризующаяся существенными изменениями в спектрах поглощения и испускания. Эти свойства позволяют использовать заявленные соединения в составе оптических хемосенсоров для колориметрического и люминесцентного определения катионов щелочных и щелочноземельных металлов, например, в составе полимерных пленок, мембран и ультратонких пленок для определения микроколичеств указанных ионов в биологических жидкостях, в том числе в плазме крови, а также для определения микроколичеств указанных ионов в промышленных водах и стоках, в том числе для мониторинга окружающей среды. Разработан также способ получения заявленных соединений высокой степени чистоты и с хорошими выходами (до 89%).
Формула изобретения
1. N-Алкилазакраунсодержащие стириловые красители общей формулы I 2. Способ получения азакраунсодержащих стириловых красителей формулы (I) по п.1, отличающийся тем, что он включает взаимодействие четвертичных солей метильных производных гетероциклических оснований формул (V) или (VI): 3. Способ по п.2, отличающийся тем, что процесс проводят в присутствии органического основания. 4. Композитные пленочные материалы, проявляющие оптические хемосенсорные свойства по отношению к катионам щелочных и щелочноземельных металлов, включающие полимерную матрицу, пластификатор, ионофор и азакраунсодержащий стириловый краситель, отличающиеся тем, что в качестве красителя они содержат азакраунсодержащий стириловый краситель формулы (I) по п.1.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

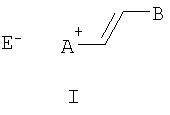
 9; Громов С.П., Алфимов М.В., Изв. АН. Сер. хим., 1997, 641; Громов С.П., Федорова О.А., Ведерников А.И., Ещеулова О.В., Федоров Ю.В., Алфимов М.В., Патент 2176256 РФ, Бюл. изобр., 2001,
9; Громов С.П., Алфимов М.В., Изв. АН. Сер. хим., 1997, 641; Громов С.П., Федорова О.А., Ведерников А.И., Ещеулова О.В., Федоров Ю.В., Алфимов М.В., Патент 2176256 РФ, Бюл. изобр., 2001, 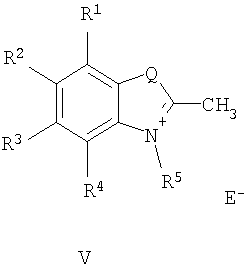
 =42000).
=42000).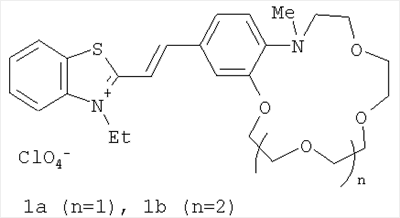
 max, б)
max, б)
 max,д) нм
max,д) нм