Патент на изобретение №2398768
|
||||||||||||||||||||||||||||
(54) ИНГИБИРУЮЩИЕ ВИЧ ПРОИЗВОДНЫЕ 2-(4-ЦИАНОФЕНИЛАМИНО)-ПИРИМИДИН-ОКСИДА
(57) Реферат:
Изобретение относится к новым производным 2-(4-цианофениламино)-пиримидин-оксида, обладающими активностью в отношении ВИЧ формулы (I):
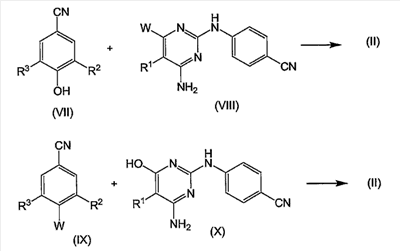
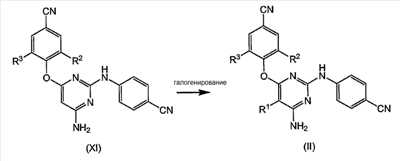
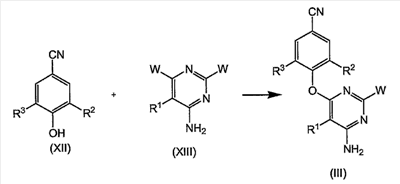
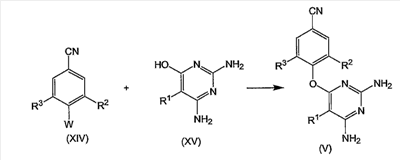
Настоящее изобретение относится к производным пиримидин-оксида, обладающим свойствами ингибирования репликации ВИЧ (Вируса Иммунодефицита Человека), к их получению и к фармацевтическим композициям, содержащим указанные соединения. Устойчивость ВИЧ к доступным в настоящее время лекарствам против ВИЧ продолжает быть основной причиной неудач при лечении. Это привело к введению комбинированной терапии двумя или более анти-ВИЧ агентами, обычно имеющими различный профиль активности. Значительный прогресс был достигнут за счет введения ВААРТ (Высоко Активная Анти-Ретровирусная Терапия, HAART Highly Active Anti-Retroviral Therapy), которая привела к существенному снижению заболеваемости и смертности среди больных ВИЧ, подвергшихся такому лечению. ВААРТ включает различные комбинации нуклеозидных ингибиторов обратной транскриптазы (NRTI), ненуклеозидных ингибиторов обратной транскриптазы (NNRTI) и ингибиторов протеазы (PI). Современные руководства по антивирусной терапии рекомендуют такую тройную комбинированную схему лечения даже в случае начального лечения. Однако такое полилекарственное лечение не всегда эффективно и никогда полностью не излечивает ВИЧ. Сообщается, что половина пациентов, получающих комбинированное анти-ВИЧ лечение, реагирует на лечение не полностью главным образом из-за устойчивости вируса к одному или нескольким используемым лекарствам. Переход на альтернативные комбинации обычно дает временное облегчение, но любая форма долговременного лечения будет в итоге неудачной, так как развивается полилекарственная устойчивость. Более того, показано, что устойчивый вирус переносится к вновь инфицированным индивидуумам, что приводит к сильно ограниченным возможностям лечения в случае нечувствительных к лекарствам больных. Таким образом, остается потребность в новых лекарственных комбинациях, которые эффективны против ВИЧ. В таких новых комбинациях необходимы новые типы ингибиторов ВИЧ, отличающиеся по химической структуре и профилю активности. Следовательно, обнаружение таких новых активных ингредиентов является весьма желательным. Настоящее изобретение предлагает заслуживающие особого внимания новые серии производных бисарил-замещенного пиримидина, которые могут найти применение при лечении ВИЧ, в особенности в качестве нового компонента лекарственных комбинаций. В публикации WO 00/27825 описаны отдельные бисарил-замещенные пиримидины, обладающие свойствами ингибирования репликации ВИЧ. Соединения настоящего изобретения ведут себя превосходно с точки зрения ингибирования репликации ВИЧ и проявляют улучшенную способность ингибировать репликацию мутантных штаммов, в особенности штаммов, которые стали устойчивыми к одному или нескольким известным NNRTI, и такие штаммы называют штаммами, устойчивыми к лекарству или множеству лекарствам. Настоящее изобретение относится к соединениям формулы: к фармацевтически приемлемым аддитивным солям или к их стереохимически изомерным формам, где R1 представляет собой атом галогена; R2 и R3 каждый независимо друг от друга представляет собой С1-6-алкил. Как используется в данном случае, определение «С1-4-алкил» означает линейные или разветвленные насыщенные углеводородные радикалы, содержащие от 1 до 4 атомов углерода, такие как метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-1-пропил и т.д.; «С1-6-алкил» охватывает С1-4-алкильные радикалы и их высшие аналоги, содержащие 5 или 6 атомов углерода, такие как 1-пентил, 2-пентил, 3-пентил, 1-гексил, 2-гексил, 2-метил-1-бутил, 2-метил-1-пентил и т.д. Предпочтительными из С1-6-алкилов являются С1-4-алкильные радикалы. Определение «галоген» охватывает атомы фтора, хлора, брома и йода. Соединения настоящего изобретения содержат N-оксидную связь, которая может быть представлена с помощью NO, N=O или N+-O– или, как преимущественно используется в данной заявке и в формуле изобретения, N В случае терапевтического применения соли соединения формулы (I) представляют собой соли, где противоион является фармацевтически приемлемым. Однако соли, которые являются фармацевтически неприемлемыми, также могут найти применение, например, при получении или при очистке фармацевтически приемлемого соединения. Все соли, независимо от того, являются ли они фармацевтически приемлемыми или нет, входят в объем настоящего изобретения. Определение «фармацевтически приемлемые аддитивные соли», используемое в данном описании, охватывает терапевтически активные нетоксичные кислотно-аддитивные солевые формы, которые способны образовывать соединения формулы (I). Солевые формы обычно могут быть получены обработкой основной формы подходящими кислотами, такими как неорганические кислоты, например галогенводородная кислота, то есть хлористоводородная, бромистоводородная кислота и т.д.; серная кислота; азотная кислота; фосфорная кислота и т.д.; или органические кислоты, например, уксусная, пропановая, гидроксиуксусная, 2-гидрокси-пропановая, 2-оксопропановая, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, 2-гидрокси-1,2,3-пропантрикарбоновая, метансульфоновая, этансульфоновая, бензолсульфоновая, 4-метилбензолсульфоновая, циклогексансульфаминовая, 2-гидроксибензойная, 4-амино-2-гидроксибензойная и подобные кислоты. И наоборот, солевая форма может быть превращена обработкой щелочью в свободную основную форму. Соединения формулы (I), содержащие кислые протоны, могут быть превращены в их терапевтически активные нетоксичные аддитивные солевые формы металлов и аминов обработкой соответствующими органическими и неорганическими основаниями. Определение аддитивная соль также включает гидраты и аддитивные формы с растворителем, которые способны образовывать соединения формулы (I). Примерами таких форм являются гидраты, алкоголяты и др. Некоторые соединения формулы (I) и их аддитивные соли могут содержать один или несколько хиральных центров и могут существовать в виде стереохимически изомерных форм. Стереоизомерия может существовать, когда R2 и R3 представляют собой С4-6-алкил. Определение «стереохимически изомерные формы», используемое в данном описании, определяет все возможные стереоизомерные формы, которыми соединения формулы (I) и их аддитивные соли могут обладать. Подразумевается, что стереохимически изомерные формы соединений формулы (I) входят в объем настоящего изобретения. Предпочтительными подгруппами соединений являются соединения формулы (I), которые определены выше, или любая подгруппа соединений формулы (I), определенной в данном описании, где R1 представляет собой атом хлора или брома, более предпочтительно, где R1 представляет собой атом брома. Другими предпочтительными подгруппами соединений являются соединения формулы (I), определенной выше, или любая подгруппа соединений формулы (I), определенной в данном описании, где R2 и R3 представляет собой С1-4-алкил, более предпочтительно, где R2 и R3 представляют собой С1-2-алкил, еще более предпочтительно, где R2 и R3 представляют собой метил. Особого внимания заслуживают соединения формулы (I), где R1 представляет собой бром и R3 представляет собой метил. В общем случае соединения формулы (I) могут быть получены путем N-окисления соответствующих соединений формулы (II) с использованием известных в данной области методик превращения третичного атома азота в его N-оксидную форму. Реакция N-окисления с целью получения соединений формулы (I) может быть проведена путем введения в реакцию исходного материала формулы (II) с соответствующим органическим или неорганическим пероксидом. Подходящими неорганическими пероксидами являются, например, пероксид водорода, пероксид щелочного металла или щелочноземельного металла, например, пероксид натрия, пероксид калия; подходящими органическими пероксидами могут быть надкислоты, такие как, например, надбензойная кислота или галоген-замещенная надбензойная кислота, например 3-хлорнадбензойная кислота; пероксо-алкановые (надалкановые) кислоты, например надуксусная кислота; алкилгидропероксиды, например, трет-бутилгидро-пероксид. Предпочтительной является 3-хлорнадбензойная кислота (м-ХНБК). Реакцию N-окисления обычно проводят в подходящем растворителе, таком как, например, вода; низший спирт, например этанол и др.; углеводород, например толуол; кетон, например ацетон или 2-бутанон; галогенированный углеводород, например дихлорметан или хлороформ; а также любые смеси таких растворителей. Предпочтительными являются галогенированные углеводороды, в особенности дихлорметан. Конечные продукты могут быть очищены с использованием способов, в целом известных в данной области техники, таких как экстракция, кристаллизация, растирание и хроматография. Исходные соединения формулы (II) являются известными соединениями, которые могут быть получены в соответствии с методиками, описанными в публикации WO 00/27825. Они могут быть получены реакцией промежуточного соединения формулы (III) или (V) с промежуточным соединением формулы (IV) или (VI), как показано на приведенной ниже реакционной схеме, где заместители R1, R2 и R3 имеют значения, которые определены для соединений формулы (I) или любой их подгруппы, а W представляет собой подходящую уходящую группу, такую как, например, атом хлора и др. Реакцию производного пиримидина (III) и, соответственно, (V) с цианоанилином (IV) и, соответственно, с цианофенильным производным (VI) предпочтительно проводят в подходящем растворителе, таком как, например, спирт, такой как, например, метанол, этанол, 2-пропанол; N,N-диметилформамид; N,N-диметилацетамид; 1-метил-2-пирролидинон; 1,4-диоксан; монометиловый эфир пропиленгликоля; ацетонитрил. Реакция может быть проведена в кислых условиях, которые могут быть получены путем добавления подходящей кислоты, например камфорсульфоновой кислоты, к подходящему растворителю, такому как, например, тетрагидрофуран или спирт, например, этанол, 1- или 2-пропанол, или путем использования подкисленных растворителей, например, хлористоводородной кислоты, растворенной в алканоле, таком как этанол, 1- или 2-пропанол. Соединения формулы (II) могут быть также получены реакцией цианофенильного производного (VII) с производным пиримидина (VIII) или реакцией цианофенильного производного (IX) с производным пиримидина (Х), как показано на приведенных ниже схемах. На приведенных схемах реакции R1, R2 и R3 имеют значения, определенные выше для соединений формулы (I) или любой их подгруппы, а W представляет собой подходящую уходящую группу, такую как, например, атом галогена, например, атом хлора и т.д. Указанные реакции предпочтительно проводят в подходящем растворителе, в частности в любом растворителе, упомянутом выше в связи с реакцией (III) c (IV). Еще один путь получения соединений формулы (II) состоит в галогенировании исходного материала (XI) свободным галогеном, например, хлором или бромом, или донором галогена, таким как N-бром- или N-хлорсукцинимид. Указанную реакцию галогенирования предпочтительно проводят в подходящем инертном для реакции растворителе, таком как простой эфир, в особенности в ТГФ. N-бром или N-хлорсукцинимид могут быть использованы в присутствии уксусной кислоты. Соединения формулы (I) также могут быть получены путем превращения соединений формулы (I) друг в друга в соответствии с известными в данной области реакциями трансформации группы. Например, хлорированные аналоги могут быть превращены в соответствующие бромированные аналоги или, наоборот, реакцией обмена галогена. Соединения формулы (I) также могут быть получены с использованием любых методик, известных или описанных в данной работе для получения соединений формулы (II), но заменяя, где это возможно, пиримидиновые исходные материалы соответствующими пиримидин-оксидами. Последние соединения могут быть получены аналогичной реакцией N-окисления, которая описана для превращения (II) в (I). Некоторые соединения формулы (I) и некоторые предшествующие им промежуточные соединения могут содержать асимметричный атом. Чистые стереохимически изомерные формы указанных соединений и указанных промежуточных соединений могут быть получены путем применения известных в данной области методик. Синтез некоторых промежуточных соединений, используемых в предыдущих реакционных схемах, описан далее, где на приведенных ниже реакционных схемах R1, R2 и R3 имеют значения, определенные выше для соединений формулы (I) или любой их подгруппы, а W представляет собой подходящую уходящую группу, в особенности атом хлора или брома. Радикал R1 представляет собой атом галогена, но на приведенных ниже реакционных схемах он также может представлять собой предшественник галогена, например, гидроксигруппу или защищенную гидроксигруппу (например, бензилоксигруппу), которые могут быть превращены в галоген с помощью галогенирующего агента, такого как POCl3 или POBr3. Это может быть предпочтительным для исключения побочных реакций. Промежуточные соединения формулы (III) могут быть получены реакцией производного фенола (XII) с производным пиримидина (XIII), как это описано на приведенной ниже схеме реакции. Аналогично промежуточные соединения (V) могут быть получены, исходя из пиримидина (XV), как это описано на приведенной далее схеме: В приведенной выше реакции аминогруппа может быть защищена или не защищена подходящей защитной группой. Промежуточные соединения (Х) могут быть получены конденсацией производного пиримидина (XVI) с 4-аминобензонитрилом, как показано на приведенной ниже схеме. Если желательно исключить побочные реакции, ОН- и/или аминогруппа могут быть защищены, а R1 может быть предшественником галогена, как описано выше. Промежуточные соединения формулы (XI) могут быть получены, как описано на реакционной схеме, приведенной ниже. Вначале 4-аминобензонитрил вводят в реакцию с цианамидом с получением 4-цианофенилгуанидина (XVII). Указанную реакцию можно проводить в воде в присутствии сильной кислоты, например хлористоводородной кислоты, при повышенной температуре, например приблизительно при температуре от 50 до 70°С, например, приблизительно при 60°С. Последнее соединение вводят в реакцию с ди-С1-6-алкил-малоновым эфиром формулы (XVIII), где каждый заместитель R независимо представляет собой С1-6-алкил, предпочтительно каждый R представляет собой метил. Указанная реакция может быть проведена в подходящем растворителе, например в спирте, таком как метанол, в присутствии сильного основания, такого как алкоксид щелочного металла, например метоксид натрия, при повышенной температуре, такой как температура кипения с обратным холодильником. Полученный в результате 4,6-дигидроксипиримидин (XIX) превращают в производное пиримидина (ХХ), где W представляет собой уходящую группу и в особенности атом галогена, предпочтительно атом хлора или брома. Такое превращение может быть осуществлено с использованием подходящего галогенирующего агента, такого как POCl3 или POBr3, в подходящем растворителе, в частности в полярном апротонном растворителе, например, в ДМФА, ДМА, ГМФА, N-метилпирролидоне, ДМСО и др., предпочтительно в ацетонитриле. Другие уходящие группы могут быть введены по известным в данной области реакциям превращения спирта в уходящую группу. Производное пиримидина (ХХ) затем вводят в реакцию с 4-замещенным бензонитрилом (XXI) с получением желаемых промежуточных соединений (XXI). Реакцию (ХХ) с (XXI) можно провести в подходящем растворителе, таком как простой эфир, например, ТГФ, галогенированный углеводород, например, CH2Cl2, CHCl3, и в частности в полярном апротонном растворителе, например, в ДМФА, ДМА, ГМФА, ацетонитрил, ДМСО и др., и предпочтительно в N-метилпирролидоне. Для связывания кислоты, которая высвобождается в процессе реакции, может быть добавлено основание, например, карбонат щелочного металла, такой как карбонат калия. Соединения формулы (I) проявляют противовирусные свойства (свойства ингибирования обратной транскриптазы), в частности они активны против ВИЧ, который является этиологическим агентом синдрома приобретенного иммунодефицита (СПИД) у человека. ВИЧ преимущественно инфицирует Т-4 клетки человека и затем разрушает их или изменяет их нормальную функцию, особенно координирование иммунной системы. В результате инфицированный пациент имеет постоянно пониженное число Т-4 клеток, которые, кроме того, ведут себя аномально. Следовательно, иммунная защитная система неспособна бороться с инфекцией и опухолями, и ВИЧ-инфицированный субъект обычно умирает от оппортунистических инфекций, таких как пневмония, или от рака. Другие состояния, связанные с ВИЧ инфекцией, включают тромбоцитопению, саркома Капоши и инфекцию центральной нервной системы, характеризующуюся прогрессивной демиелинизацией, приводящей к слабоумию и к таким симптомам, как прогрессирующая дизартрия, атаксия и дезориентация. ВИЧ инфекция также ассоциируется с периферической невропатией, прогрессирующей генерализованной лимфаденопатией (ПГЛ, PGL) или со СПИД-ассоциированным комплексом (ССК, ARC). Соединения настоящего изобретения также проявляют активность против мутированных штаммов ВИЧ, включая также единожды, дважды, трижды и многократно мутированные штаммы. Соединения настоящего изобретения активны против штаммов ВИЧ, устойчивых ко многим лекарствам, в частности против устойчивых к многим лекарствам штаммов ВИЧ-1, более предпочтительно рассматриваемые соединения проявляют активность против штаммов ВИЧ, особенно штаммов ВИЧ-1, которые имеют приобретенную устойчивость к одному или нескольким известным в данной области ненуклеозидным ингибиторам обратной транскриптазы. Известные ненуклеозидные ингибиторы обратной транскриптазы представляют собой ненуклеозидные ингибиторы обратной транскриптазы, отличные от рассматриваемых соединений и известные специалистам в данной области, в частности находящиеся в продаже ненуклеозидные ингибиторы обратной транскриптазы. Соединения настоящего изобретения имеют незначительную аффинность связывания или не имеют аффинности связывания к человеческому Благодаря антиретровирусным свойствам, в особенности анти-ВИЧ свойствам, особенно анти-ВИЧ-1 активности, соединения формулы (I), их фармацевтически приемлемые аддитивные соли и стереохимически изомерные формы полезны при лечении индивидуумов, инфицированных ВИЧ, и для профилактики указанных инфекций. В общем случае соединения настоящего изобретения могут быть использованы при лечении теплокровных животных, инфицированных вирусами, существование которых опосредуется или зависит от фермента обратной транскриптазы. Состояния, которые могут быть предупреждены или вылечены с помощью соединений настоящего изобретения, особенно состояния, связанные с ВИЧ и другими патогенными ретровирусами, включают СПИД, СПИД-ассоциированный комплекс (ARC), прогрессирующую генерализованную лимфаденопатию (ПГЛ), а также хронические заболевания центральной нервной системы, вызванные ретровирусами, такие как, например, опосредуемое ВИЧ слабоумие и рассеянный склероз. Таким образом, соединения настоящего изобретения или любая их подгруппа могут быть использованы в качестве лекарственных средств против названных выше состояний. Указанное применение в качестве лекарственного средства или способ лечения включает введение ВИЧ-инфицированному субъекту количества соединения, эффективного для борьбы с состояниями, связанными с ВИЧ и другими патогенными ретровирусами, в особенности с ВИЧ-1. В частности, соединения формулы (I) могут быть использованы при производстве лекарственного средства для лечения или предупреждения ВИЧ-инфекций. В еще одном аспекте настоящее изобретение предлагает способ лечения теплокровных животных, включая человека, страдающих от вирусных инфекций, или способ предупреждения теплокровных животных, включая человека, от вирусных инфекций, в особенности от ВИЧ инфекций. Указанный способ включает введение, предпочтительно пероральное введение, эффективного количества соединения (I), его фармацевтически приемлемой аддитивной соли или его возможной стереохимической формы теплокровным животным, включая человека. По другому аспекту соединения формулы (I) или любая из их подгрупп могут быть использованы в способе предупреждения, лечения или борьбы с инфекцией или заболеванием, связанным с инфицированием млекопитающего мутантным вирусом ВИЧ, который включает введение указанному млекопитающему эффективного количества соединения формулы (I) или любой его подгруппы. В другом аспекте соединения формулы (I) или любая их подгруппа могут быть использованы в способе предупреждения, лечения или борьбы с инфекцией или заболеванием, связанным с инфицированием млекопитающих вирусом ВИЧ с множественной лекарственной устойчивостью, который включает введение указанному млекопитающему эффективного количества соединения формулы (I) или любой его подгруппы. В еще одном аспекте соединения формулы (I) или любая их подгруппа могут быть использованы в способе ингибирования репликации ВИЧ, в частности ВИЧ, имеющего мутантную обратную транскриптазу ВИЧ, более предпочтительно мутантную обратную транскриптазу ВИЧ с множественной лекарственной устойчивостью, который включает введение указанному млекопитающему эффективного количества соединения формулы (I) или любой его подгруппы. Предпочтительно млекопитающим, которое упоминается в настоящем изобретении, является человек. Настоящее изобретение также предлагает композиции для лечения вирусной инфекции, содержащие терапевтически эффективное количество соединения формулы (I), и фармацевтически приемлемый носитель или разбавитель. Соединения настоящего изобретения или любая их подгруппа для целей введения могут быть получены в различных фармацевтических формах. В качестве подходящих композиций можно назвать все композиции, обычно используемые для систематического введения лекарств. Для получения фармацевтических композиций настоящего изобретения эффективное количество конкретного соединения, необязательно в кислотно-аддитивной форме, в качестве активного ингредиента смешивают в однородную смесь с фармацевтически приемлемым носителем, и этот носитель может иметь широкое разнообразие форм в зависимости от формы препарата, необходимой для введения. Такие фармацевтические композиции желательны в единичной дозированной форме, приемлемой предпочтительно для введения перорально, ректально, подкожно или путем парентеральной инъекции. Например, при получении композиции в пероральной дозированной форме может быть использована любая обычная фармацевтическая среда, такая как, например, вода, гликоли, масла, спирты и т.д., в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, лутриканты, связующие вещества, дезинтегрирующие агенты и т.д., в случае порошков, пилюль, капсул и таблеток. Вследствие простоты введения таблетки и капсулы являются наиболее предпочтительными пероральными единичными дозированными формами, в которых, конечно, используются твердые фармацевтические носители. В случае парентеральных композиций носитель обычно будет представлять собой стерильную воду, по меньшей мере, в большей части, хотя могут быть включены другие ингредиенты, например, для содействия растворимости. Могут быть приготовлены, например, инъецируемые растворы, в которых носитель представляет собой физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Могут быть также приготовлены инъецируемые суспензии, в которых могут быть использованы подходящие жидкие носители, суспендирующие агенты и т.д. Кроме того, существуют препараты твердых форм, которые, как подразумевается, непосредственно перед применением переводят в препараты жидких форм. В композициях, подходящих для подкожного введения, носитель необязательно содержит агент, усиливающий проникание, и/или подходящий смачивающий агент, необязательно смешанные с подходящими добавками любой природы в небольших количествах, и такие добавки не оказывают сильного отрицательного влияния на кожу. Указанные добавки могут облегчать нанесение на кожу и/или могут способствовать получению необходимой композиции. Такие композиции могут быть введены любыми путями, например, в виде трансдермального пластыря, в виде наклейки, в виде мази. Соединения настоящего изобретения могут быть введены посредством ингаляции или путем вдувания с помощью способов и препаратов, используемых в данной области для введения таким образом. Следовательно, в общем случае соединения настоящего изобретения могут быть введены в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухих порошков посредством пероральных или назальных ингаляции или вдувания, подходит для введения рассматриваемых соединений. Для содействия растворимости соединений формулы (I) в композицию могут быть добавлены соответствующие ингредиенты, например циклодекстрины. Подходящими циклодекстринами являются Определение «смешанные простые эфиры» означает производные циклодекстрина, в которых, по меньшей мере, две гидрокси-группы циклодекстрина этерифицированы разными группами, например, гидроксипропилом и гидроксиэтилом. Среднее молярное замещение (М.З.) используется как мера среднего числа молей алкокси-звеньев на моль глюкозных остатков. Степень среднего замещения (С.З.) относится к среднему числу замещенных гидроксилов на моль глюкозных остатков. Значения М.З. и С.З. могут быть определены c помощью различных аналитических методов, таких как ядерный магнитный резонанс (ЯМР), масс-спектрометрия (МС) и инфракрасная спектрометрия (ИК). В зависимости от используемого метода могут наблюдаться несколько разные значения, полученные для одного данного производного циклодекстрина. Предпочтительно при измерении с помощью масс-спектрометрии значения М.З. находятся в интервале от 0,125 до 10 и значения С.З. находятся в интервале от 0,125 до 3. Другие подходящие композиции для перорального или ректального введения включают частицы, состоящие из твердой дисперсии, содержащей соединение формулы (I) и один или несколько соответствующих фармацевтически приемлемых растворимых в воде полимеров. Определение «твердая дисперсия», используемое в данном описании, означает систему в твердом состоянии (в отличие от жидкого или газообразного состояния), содержащую, по меньшей мере, два компонента, то есть соединение формулы (I) и растворимый в воде полимер, где один компонент распределен более или менее равномерно по всему другому компоненту или компонентам (в случае, когда включены дополнительные фармацевтически приемлемые рецептурные агенты, известные в данной области, такие как пластификаторы, консерванты и т.д.). Когда указанная дисперсия компонентов такова, что система химически и физически однородна или гомогенна на всем протяжении или состоит из одной фазы, как определяется в термодинамике, то такую дисперсию называют «твердым раствором». Твердые растворы являются предпочтительными физическими системами, так как компоненты в них обычно легко биодоступны для организмов, в которые они введены. Определение «твердая дисперсия» также включает дисперсии, которые являются в меньшей степени гомогенными по всему объему, чем твердые растворы. Такие дисперсии не являются химически и физически однородными по всему объему или содержат более одной фазы; например, системы, имеющие домены или небольшие области, где аморфное, микрокристаллическое или кристаллическое соединение формулы (I) или аморфный, микрокристаллический или кристаллический растворимый в воде полимер, или оба распределены более или менее равномерно в другой фазе, содержащей растворимый в воде полимер или соединение формулы (I), или твердый раствор, содержащий соединение формулы (I) и растворимый в воде полимер. Указанные домены представляют собой области в пределах твердой дисперсии, отчетливо отмеченные некоторым физическим признаком, небольшие по размеру и равномерно и статистически распределенные по всей твердой дисперсии. Существуют различные методы получения твердых дисперсий, в том числе экструзия из расплава, распылительная сушка и растворение-упаривание. После получения твердых дисперсий полученные продукты необязательно могут быть измельчены и просеяны. Твердая дисперсия может быть подвергнута помолу или измельчению до частиц, имеющих размер менее чем 600 мкм, предпочтительно менее чем 400 мкм и наиболее предпочтительно менее чем 125 мкм. Полученные частицы, которые описаны выше, затем могут быть превращены с помощью обычных методов в фармацевтические дозированные формы, такие как таблетки или капсулы. Растворимые в воде полимеры в частицах представляют собой полимеры, имеющие кажущуюся вязкость при растворении при 20°С в водном растворе при концентрации 2% (мас./об.), от 1 до 5000 мПа·сек, более предпочтительно от 1 до 700 мПа·сек и наиболее предпочтительно от 1 до 100 мПа·сек. Например, подходящие растворимые в воде полимеры представляют собой алкилцеллюлозы, гидроксиалкилцеллюлозы, гидроксиалкилалкилцеллюлозы, карбоксиалкилцеллюлозы, соли щелочных металлов карбоксиалкилцеллюлоз, карбоксиалкилалкилцеллюлозы, сложные эфиры карбоксиалкилцеллюлозы, крахмалы, пектины, производные хитина, ди-, олиго- и полисахариды, такие как трегалоза, альгиновая кислота или ее соли с щелочным металлом или аммонийные соли, каррагенаны, галактоманнаны, трагакант, агар-агар, аравийская камедь и ксантановая камедь, полиакриловые кислоты и их соли, полиметакриловые кислоты и их соли, сополимеры метакрилата, поливиниловый спирт, поливинилпирролидон, сополимеры поливинилпирролидона с винилацетатом, комбинации поливинилового спирта и поливинилпирролидона, полиалкиленоксиды и сополимеры этиленоксида и пропиленоксида. Предпочтительными растворимыми в воде полимерами являются гидроксипропилметилцеллюлозы. Кроме того, один или несколько циклодекстринов могут быть использованы в качестве растворимого в воде полимера при получении описанных выше частиц, как раскрыто в публикации WO 97/18839. Указанные циклодекстрины включают фармацевтически приемлемые незамещенные и замещенные циклодекстрины, известные в данной области, более конкретно, Замещенные циклодекстрины, которые могут быть использованы для получения описанных выше частиц, включают простые полиэфиры, описанные в патенте США Отношение соединения формулы (I) к растворимому в воде полимеру может меняться в широких пределах. Например, могут быть использованы отношения от 1:100 до 100:1. Представляющие интерес отношения соединения формулы (I) к циклодекстрину находятся в интервале приблизительно от 1:10 до 10:1. Более предпочтительно отношения находятся в интервале от 1:5 до 5:1. Кроме того, также удобно составлять в композиции соединения формулы (I) в виде наночастиц, которые имеют модификатор поверхности, адсорбированный на их поверхности в количестве, достаточном для сохранения эффективного среднего размера частиц менее чем 1000 нм. Полезными модификаторами поверхности, как полагают, являются модификаторы, которые физически прикрепляются к поверхности соединения формулы (I), но химически не связываются с указанным соединением и могут быть выбраны из известных органических и неорганических фармацевтических эксципиентов. Такими эксципиентами являются различные полимеры, низкомолекулярные олигомеры, природные продукты и поверхностно-активные вещества. Предпочтительными модификаторами поверхности являются неионные и анионные поверхностно-активные вещества. Еще один представляющий интерес способ приготовления препаратов соединений формулы (I) включает фармацевтическую композицию, посредством которой соединения формулы (I) вводят в гидрофильные полимеры, и нанесение этой смеси в качестве покрывающей пленки поверх множества небольших шариков; в результате получают композицию, которая может быть удобно произведена и которая подходит для получения фармацевтических дозированных форм для перорального введения. Такие шарики имеют центральную, закругленную или сферическую сердцевину, покрывающую пленку гидрофильного полимера и соединения формулы (I) и необязательно изолирующий покрывающий слой. Материалы, подходящие для использования в качестве сердцевины в шариках, являются разными, при условии, что указанные материалы фармацевтически приемлемы и имеют подходящие размеры и твердость. Примерами таких материалов служат полимеры, неорганические вещества, органические вещества и сахариды, и их производные. Особенно предпочтительно получать названные фармацевтические композиции в единичных дозированных формах для простоты введения и равномерности дозирования. Единичной дозированной формой в данном описании называются физически дискретные элементы, подходящие в качестве разовых дозировок, причем каждый элемент содержит предопределенное количество активного ингредиента, рассчитанное так, чтобы получить желаемый терапевтический эффект, в сочетании с требуемым фармацевтическим носителем. Примерами таких единичных дозированных форм являются таблетки (в том числе таблетки с насечкой или с покрытием), капсулы, пилюли, пакетики с порошками, облатки, свечи, инъецируемые растворы или суспензии и т.д., и их отдельные составные структуры. Специалист в области лечения ВИЧ инфекции может определить эффективное ежедневное количество из представленных в описании результатов испытания. В целом подразумевается, что эффективное ежедневное количество может составлять от 0,01 до 50 мг/кг массы тела, более предпочтительно от 0,1 до 10 мг/кг массы тела. Может быть приемлемым вводить требуемую дозу в виде двух, трех, четырех или более суб-доз через соответствующие интервалы в течение всего дня. Указанные суб-дозы могут быть приготовлены в виде единичных дозированных форм, например, содержащих от 1 до 1000 мг, и в частности от 5 до 200 мг активного ингредиента на единичную дозированную форму. Точная дозировка и частота введения зависят от конкретного используемого соединения формулы (I), конкретного состояния, подвергающегося лечению, серьезности состояния, подвергающегося лечению, возраста, массы и общего физического состояния конкретного больного, а также других лекарственных средств, которые индивидуум может принимать, что хорошо известно специалистам в данной области. Более того, очевидно, что указанное эффективное ежедневное количество может быть уменьшено или увеличено в зависимости от реакции подвергающегося лечению субъекта и/или в зависимости от оценки врача, прописывающего соединения настоящего изобретения. Следовательно, диапазоны эффективного ежедневного количества, упомянутые выше, являются только справочными и ни в коей мере не предназначены для ограничения объема изобретения или его применения. Рассматриваемые соединения формулы (I) могут быть использованы отдельно или в комбинации с другими терапевтическими агентами, такими как противовирусные средства, антибиотики, иммуномодуляторы или вакцины для лечения вирусных инфекций. Они могут быть также использованы отдельно или в комбинации с другими профилактическими агентами для предупреждения вирусных инфекций. Соединения настоящего изобретения могут быть использованы в вакцинах и способах защиты индивидуума от вирусных инфекций в течение продолжительного периода времени. Соединения могут быть использованы в таких вакцинах или отдельно, или вместе с другими соединениями настоящего изобретения, или вместе с другими противовирусными агентами в соответствии с обычной практикой применения ингибиторов обратной транскриптазы в вакцинах. Следовательно, соединения могут быть объединены с фармацевтически приемлемыми адъювантами, обычно используемыми в вакцинах, и введены в профилактически эффективных количествах для защиты индивидуума от ВИЧ инфекции в течение продолжительно периода времени. Кроме того, в качестве лекарственными средствами можно использовать одно или несколько дополнительных противовирусных соединений и соединение формулы (I). Следовательно, настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) одно или несколько дополнительных противовирусных соединений, в виде комбинированного препарата для одновременного, раздельного или последовательного применения при лечении ВИЧ. Различные лекарства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. Указанные другие противовирусные соединения могут представлять собой любые известные противовирусные соединения, такие как сурамин, пентамидин, тимопентин, кастаноспермин, декстран (декстран-сульфат), фоскарнет-натрий (тринатрийфосфоноформиат); нуклеозидные ингибиторы обратной транскриптазы (NRTI), например, зидовудин (AZT), диданозин (ddI), зальцитабин (ddC), ламивудин (3ТС), ставудин (d4T), эмтрицитабин (FTC), абакавир (АВС), D-D4FC (ReversetTM), аловудин (MIV-310), амдоксовир (DAPD), элвуцитабин (АСН-126443) и т.д.; ненуклеозидные ингибиторы обратной транскриптазы (NNRTI), такие как деларвидин (DLV), эфавиренз (EFV), невирапин (NVP), каправирин (CPV), каланолид А, ТМС120, этравирин (ТМС125), ТМС278, BMS-561390, DPC-083 и т.д.; нуклеотидные ингибиторы обратной транскриптазы (NtRTI), например тенофовир (TDF) и фумарат тенофовир-дисопроксила и т.д.; соединения TIBO (тетрагидроимидазо[4,5,1-jk][1,4]-бензодиазепин-2-(1Н)-онового и -тионового) типа, например, (S) 8-хлор-4,5,6,7-тетрагидро-5-метил-6-(3-метил-2-бутенил)имидазо-[4,5,1-jk][1,4]бензодиазепин-2(1Н)-тион; соединения Путем введения соединений настоящего изобретения с другими противовирусными агентами, которые нацелены на различные события в цикле развития вируса, может быть потенцирован терапевтический эффект этих соединений. Комбинированное лечение, которое описано выше, оказывает синергетический эффект при ингибировании репликации ВИЧ, так как каждый компонент комбинации действует на различные сайты репликации ВИЧ. Применение указанных комбинаций может уменьшить дозировку данного обычного противовирусного агента, которая потребовалась бы для достижения желаемого терапевтического или профилактического эффекта по сравнению с тем, когда этот агент вводится при монотерапии. Такие комбинации могут уменьшить или исключить побочные эффекты обычной отдельной анти-ретровирусной терапии, не мешая при этом противовирусной активности агентов. Такие комбинации снижают потенциальную устойчивость к лечению одним агентом, при этом сводя любую сопутствующую токсичность к минимальной. Указанные комбинации также могут повышать эффективность обычных агентов без повышения сопутствующей токсичности. Кроме того, соединения настоящего изобретения могут быть введены в комбинации с иммуномодулирующими агентами, такими как левамизол, бропиримин, антитело против человеческого альфа-интерферона, интерферон-альфа, интерлейкин 2, метионин-энкефалин, диэтилдитиокарбамат, фактор некроза опухоли, налтрексон и т.д.; с антибиотиками, такими как пентамидина изетиорат и т.д.; с холинергическими агентами, такими как такрин, ривастигмин, донерезил, галантамин и т.д.; с блокаторами NMDA канала, такими как мемантин; для предупреждения или искоренения инфекции и заболеваний или симптомов, сопутствующих ВИЧ инфекции, таких как СПИД и ARC, например, слабоумия. Соединения формулы (I) также могут быть объединены с другими соединениями формулы (I). Хотя настоящее изобретение нацелено на применение рассматриваемых соединений для предупреждения или лечения ВИЧ инфекции, рассматриваемые соединения также могут быть использованы в качестве ингибирующих агентов для других вирусов, которые зависят от подобных обратных транскриптаз при их репродуцировании. Следующие примеры предназначены для иллюстрации настоящего изобретения и не ограничивают его объем. ПРИМЕРЫ Пример 1: Синтез N-оксида 4-[[6-амино-5-бром-2-[(4-цианофенил)амино]-4-пиримидинил]окси]-3,5-диметилбензонитрила Смесь 4-[[6-амино-5-бром-2-[(4-цианофенил)амино]-4-пиримидинил]окси]-3,5-диметилбензонитрила (промежуточное соединение 1; 5,00 г; 11,5 ммоль) и м-ХНБК (3 экв., 34,5 ммоль, 8,50 г, 70 мас.%) кипятят с обратным холодильником в дихлорметане (100 мл). Через 10 минут образуется прозрачный раствор, а еще через 5 минут образуется осадок. Смесь кипятят с обратным холодильником еще 15 минут, охлаждают до комнатной температуры, и белое твердое вещество отфильтровывают и промывают дихлорметаном. Твердое соединение перемешивают в уксусной кислоте в течение 1 часа, фильтруют и сушат, получают 1,7 г (33%) соединения 1. Физические характеристики: т.пл. 271°С (АсОН); Спектр 1Н ЯМР (300 МГц, ДМСО) Данные анализа ЖХ-МС (линейный градиент 1 мл/мин от t0 95% 10 мМ водной НСООН/ацетонитрил до t15 5% 10 мМ водной НСООН/ацетонитрил, UV-DAD): чистота 95%, t=9,49 мин, масс-спектр m/z 449, 451 [М-Н]–. Пример 2: Формы фармацевтических композиций Капсулы Соединение 1, описанное в примере 1, растворяют в органическом растворителе, таком как этанол, метанол или метиленхлорид, предпочтительно в смеси этанола и метиленхлорида. Полимеры, такие как сополимер поливинил-пирролидона с винилацетатом (ПВП-ВА) или гидроксипропилметил-целлюлоза (ГПМЦ), обычно с вязкостью 5 мПа·сек, растворяют в органических растворителях, таких как этанол, метанол, метиленхлорид. Соответствующий полимер растворяют в этаноле. Растворы полимера и соединения смешивают и затем подвергают распылительной сушке. Соотношение соединение/полимер выбирают от 1:1 до 1:6. Промежуточные соотношения могут составлять 1:1,5 и 1:3. Подходящим соотношением может быть 1:6. Высушенным распылительной сушкой порошком, твердой дисперсией, затем заполняют капсулы, предназначенные для введения. Загрузка лекарства на одну капсулу находится в интервале от 50 до 100 мг в зависимости от размера используемой капсулы. Таблетки с пленочным покрытием Получение ядра таблетки Смесь 100 г соединения 1, 1,750 г лактозы и 200 г крахмала тщательно смешивают и затем увлажняют раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона приблизительно в 200 мл воды. Влажную порошковую смесь просеивают, сушат и снова просеивают. Затем добавляют 100 г микрокристаллической целлюлозы и 15 г гидрированного растительного масла. Всю смесь тщательно смешивают и прессуют в таблетки, получают 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента. Нанесение покрытия К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. Плавят 10 г полиэтиленгликоля и растворяют в 75 мл дихлорметана. Последний раствор добавляют к первому, и затем добавляют 2,5 г октадеканоата магния, 5 г поливинил-пирролидона и 30 мл концентрированной суспензии красителя, и затем все гомогенизируют. Ядра таблеток покрывают полученной смесью в устройстве для нанесения покрытия. Пример 3: Спектр противовирусной активности Вследствие возрастающего появления устойчивых к лекарствам штаммов ВИЧ рассматриваемые соединения испытаны на их потенциальную активность против клинически выделенных штаммов ВИЧ, накопивших несколько мутаций. Такие мутации сопровождаются устойчивостью к ингибиторам обратной транскриптазы и приводят к вирусам, которые проявляют различные степени фенотипической перекрестной устойчивости к современным коммерчески доступным лекарствам, таким как AZT и делавирдин. Противовирусную активность соединения настоящего изобретения оценивают в присутствии дикого типа ВИЧ и ВИЧ-мутантов, несущих мутации в гене обратной транскриптазы. Активность соединений оценивают с использованием клеточного анализа, и остаточную активность выражают в значения рЕС50. В таблице в столбцах IIIB и A-G перечислены значения рЕС50 против различных штаммов IIIB, A-G. Штамм IIIB представляет собой штамм ВИЧ-LAI дикого типа, Штамм А содержит мутацию Y181C в обратной транскриптазе ВИЧ, Штамм В содержит мутацию K103N в обратной транскриптазе ВИЧ, Штамм C содержит мутацию L100I в обратной транскриптазе ВИЧ, Штамм D содержит мутации Y1881L и S162K в обратной транскриптазе ВИЧ, Штамм Е содержит мутации L100I и K103N в обратной транскриптазе ВИЧ, Штамм F содержит мутации K101E и K103N в обратной транскриптазе ВИЧ.
Соединение А является соединением сравнения, представляет собой соединение, называемое в примере 1 «промежуточным соединением 1», и описано в публикации WO 00/27825.
Формула изобретения
1. Соединение формулы 2. Соединение по п.1, где R2 и R3 представляют собой метил. 3. Фармацевтическая композиция, обладающая активностью в отношении ВИЧ, содержащая фармацевтически приемлемый носитель и в качестве активного ингредиента терапевтически эффективное количество соединения по любому из пп.1 и 2. 4. Способ получения фармацевтической композиции по п.3, включающий тщательное смешение активного ингредиента и носителя.
|
||||||||||||||||||||||||||||

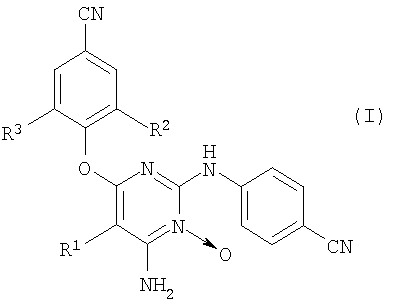 , где R1 представляет собой атом брома; R2 и R3 каждый независимо друг от друга представляет собой C1-6-алкил, а также к их фармацевтически приемлемым аддитивным солям. Изобретение также относится к фармацевтической композиции и способу получения фармацевтической композиции. 3 н. и 1 з.п. ф-лы, 1 табл.
, где R1 представляет собой атом брома; R2 и R3 каждый независимо друг от друга представляет собой C1-6-алкил, а также к их фармацевтически приемлемым аддитивным солям. Изобретение также относится к фармацевтической композиции и способу получения фармацевтической композиции. 3 н. и 1 з.п. ф-лы, 1 табл.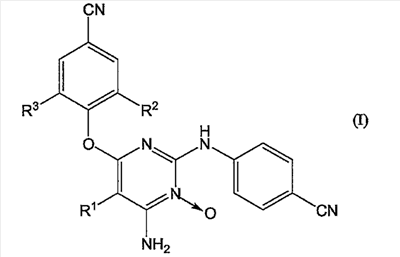
 O.
O.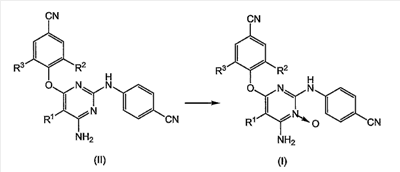
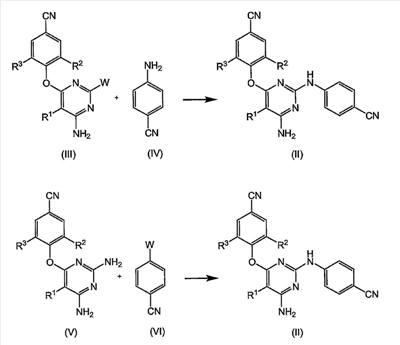
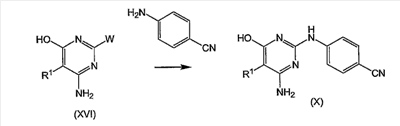
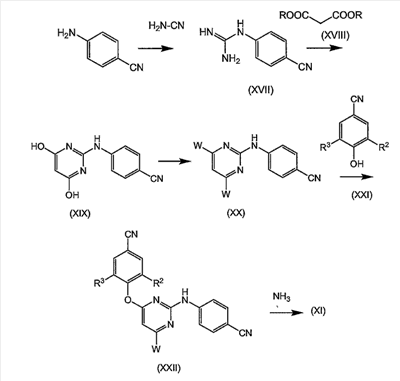
 -1 кислому гликопротеину; человеческий
-1 кислому гликопротеину; человеческий  -циклодекстрины или простые эфиры и смешанные простые эфиры, где одна или несколько гидроксильных групп глюкозных звеньев циклодекстрина замещены С1-6-алкилом, особенно метилом, этилом или изопропилом, например, произвольно метилированный
-циклодекстрины или простые эфиры и смешанные простые эфиры, где одна или несколько гидроксильных групп глюкозных звеньев циклодекстрина замещены С1-6-алкилом, особенно метилом, этилом или изопропилом, например, произвольно метилированный  -циклодекстрины или их фармацевтически приемлемые производные.
-циклодекстрины или их фармацевтически приемлемые производные. 3459731. Кроме того, замещенные циклодекстрины представляют собой циклодекстрины, описанные в качестве агентов, которые способствуют растворимости соединений формулы (I).
3459731. Кроме того, замещенные циклодекстрины представляют собой циклодекстрины, описанные в качестве агентов, которые способствуют растворимости соединений формулы (I).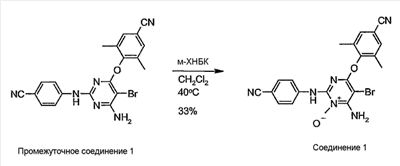
 м.д.: 1,90 (с, 2,25Н, АсОН), 2,12 (с, 6Н), 7,39 (д, 2Н), 7,40 (д, 2Н), 7,76 (с, 2Н), 7,95 (уш. с, 1Н), 10,2 (уш. с, 1Н). Продукт содержит 0,75 эквивалентов уксусной кислоты.
м.д.: 1,90 (с, 2,25Н, АсОН), 2,12 (с, 6Н), 7,39 (д, 2Н), 7,40 (д, 2Н), 7,76 (с, 2Н), 7,95 (уш. с, 1Н), 10,2 (уш. с, 1Н). Продукт содержит 0,75 эквивалентов уксусной кислоты.