|
|
(21), (22) Заявка: 2007109518/04, 18.08.2005
(24) Дата начала отсчета срока действия патента:
18.08.2005
(30) Конвенционный приоритет:
18.08.2004 GB 0418414.9
14.03.2005 US 11/079,795
(43) Дата публикации заявки: 27.09.2008
(46) Опубликовано: 10.08.2010
(56) Список документов, цитированных в отчете о
поиске:
WO 03/091429 A1, 06.11.2003. US 2003/087827 A1, 08.05.2003. WO 98/40401 A2, 17.09.1998. RU 2183643 C1, 20.06.2002. HAYNIE S L; CRUM G A; DOELE В A “Antimicrobial Activities jf Amphiphilic Peptides Covalently Bonded to a Water-Insoluble Resin”, ANTIMICROBIAL AGENTS AND CHEMOTHERAPY, 1995 Vol:39, Nr:2, Page(s):301-307. MILLER С Т; ЕТ AL “Thesynthesis and screening of 1,4,5,8-naphthalenetetracarboxylic diimide-peptide conjugates with antibacterial activity” BIOORGANIC & MEDICINAL CHEMISTRY, 2001 Vol:9, Nr:8, Page(s): 2015-2024. BESSALLE R; ET AL ANTIMICROBIAL AGENTS AND CHEMOTHERAPY, 1992 Vol:36, Nr:2, Page(s): 313-317. ZASLOFF M Antimicrobial peptides of multicellular organisms NATURE, 2002 Vol:415, Nr:6870, Page(s): 389-395.
(85) Дата перевода заявки PCT на национальную фазу:
19.03.2007
(86) Заявка PCT:
GB 2005/003245 20050818
(87) Публикация PCT:
WO 2006/018652 20060223
Адрес для переписки:
191036, Санкт-Петербург, а/я 24, “НЕВИНПАТ”, пат.пов. А.В.Поликарпову
|
(72) Автор(ы):
О’НИЛ Дебора (GB)
(73) Патентообладатель(и):
НоваБиотикс Лимитед (GB)
|
(54) ПРОТИВОМИКРОБНЫЕ ПЕПТИДЫ, СОДЕРЖАЩИЕ АРГИНИН- И ЛИЗИНСОДЕРЖАЩИЙ МОТИВ
(57) Реферат:
Настоящее изобретение относится к применению пептида формулы (I): ((X)l(Y)m)n, где пептид содержит от 3 до 200 аминокислот и где 1, m и n представляют собой целые числа от 0 до 10; Х и Y, которые могут быть одинаковыми или разными, представляют собой катионные аминокислоты, выбранные из аргинина и лизина, в изготовлении лекарственных средств для лечения грибковой инфекции. 2 н. и 24 з.п. ф-лы, 19 ил., 2 табл.
В настоящем изобретении предложены противомикробные пептиды. Кроме того, изобретение относится к фармацевтическим композициям, содержащим эти противомикробные пептиды, и к применению этих пептидов при лечении, среди прочего, микробных инфекций.
Одно большое семейство эндогенных антибактериальных пептидов, бета-дефензины, секретируется эпителиальными клетками, которые выстилают пищеварительный тракт, дыхательные и мочеполовые пути высших млекопитающих. Они также продуцируются кератиноцитами в коже. Их основная роль состоит в обеспечении необходимой первой линии защиты против инфекции через эти пути патогенными организмами.
Дефензины являются одним из наиболее изученных классов противомикробных пептидов. Этот класс состоит из богатых цистеином молекул с тремя дисульфидными мостиками. Они обнаружены в растениях, насекомых и различных млекопитающих. У людей обнаружено два класса дефензинов, которые отличаются друг от друга в отношении пространственного распределения и связей между шестью цистеиновыми остатками. Первый из трех классов составляют альфа-дефензины (шесть типов), которые выделены из нейтрофилов (HNP1-4, человеческий нейтрофильный пептид) и в клетках Панета желудочно-кишечного тракта (альфа-дефензины 5 и 6). Второй класс, бета-дефензины, являются более длинными, более основными и экспрессируются во всех слизистых оболочках в эпителиальных клетках и кератиноцитах, которые выстилают, и/или содержатся, и/или присутствуют в пищеварительном тракте, дыхательных и мочеполовых путях и коже. hBD1 (человеческий бета-дефензин 1) секретируется конститутивно, а человеческие бета-дефензины 2, 3 и 4 (hBD2, hBD3 и hBD4) продуцируются в ответ на инфекцию или воспаление. Экспрессия и секреция hBD2 запускается бактериальной стимуляцией, в частности, жгутиковыми бактериями (Harder et al, Nature 1997; 387: 861) и IL1 [альфа] и IL1 [бета] (интерлейкином 1) (Liu et al. J Invest Dermatol. 2002; 118; 275-281). В некоторых участках ткани фактор некроза опухоли альфа (TNF-альфа) и липополисахарид (LPS) также могут играть роль в индукции экспрессии hBD2. В экспериментах in vitro выявлено, что hBD2 активен против грамотрицательных бактерий, таких как Escherichia coli (Е.coli), и в меньшей степени против грамположительных бактерий, таких как Streptococcus pneumoniae (Str. pneumoniae). Также продемонстрирована киллерная активность hBD2 in vitro против дрожжей Candida albicans. Экспрессия и секреция hBD3 индуцируется бактериальной стимуляцией, TNF-альфа и особенно интерфероном-гамма (IFN ), который также обладает общим свойством молекул, вовлеченных в воспалительные процессы. ), который также обладает общим свойством молекул, вовлеченных в воспалительные процессы.
В дополнение к эффективной, конститутивной и регулируемой природной противомикробной защите широкого спектра действия, которую обеспечивают бета-дефензины, эти молекулы, в частности hBD2, также обладают способностью к мобилизации адаптивной ветви иммунного ответа посредством хемотaксических эффектов в отношении незрелых дендритных клеток и Т-лимфоцитов памяти (Yang et al. Science. 1999; 286: 525-528).
Важно, что было обнаружено, что бета-дефензины не только обеспечивают защиту против инфекции, вызванной патогенными микробами, но также являются ключевыми в регуляции и поддержании оптимальной плотности и разнообразия существенных для организма комменсальных микробных экосистем, например, на коже и в желудочно-кишечном тракте и половых путях (Ganz. Т. Nat Rev Immunol. 2003 3(9): 710-20).
Механизм действия бета-дефензинов состоит в том, что они в основном являются нетоксичными для клеток-хозяев при активных концентрациях. Поэтому бета-дефензины вовлечены в качестве потенциальных мишеней для терапевтических средств для широкого диапазона инфекций. Однако природные формы дефензинов технически трудно получать в рекомбинантных системах, приводящих к низким выходам. Кроме того, растет количество данных, позволяющих предположить, что благодаря своим хемотaксическим действиям бета-дефензины являются сильными воспалительными соединениями (Yang et al. Science. 1999; 286: 525-528; Van Wetering et al. Inflamm Res. 2002; 51(1): 8-15; Niyonsaba et al. Curr Drug Targets Inflamm Allergy. 2003; 2(3): 224-231). Взятые вместе эти факторы делают природные дефензины непригодными для терапевтических применений.
Бета-дефензины также высокочувствительны к соли (Porter et al. Infect. Immun. 1997; 65(6): 2396-401; Bals et al. J Clin Invest. 1998; 102(5); 874-80; Valore et al. J Clin Invest. 1998; 101(8): 1633-42; Goldmann et al. Cell. 1997; 88(4): 553-609; Singh et al. Proc Natl Acad Sci USA 95(25): 14961-6). По этой причине бета-дефензины не могут обеспечить противомикробную защиту при состояниях, таких как муковисцидоз, где, хотя респираторный эпителий обильно продуцирует бета-дефензины в ответ на хронические бактериальные инфекции, ассоциированные с этим состоянием, они являются неактивными вследствие дисбаланса в ионном транспорте через мембраны респираторного эпителия, который приводит к повышенной ресорбции катионов (в частности, Na+) и повышенной секреции хлорида (Donaldson SH and Boucher RC Curr. Opin. Pulm. Med. 2003, Nov; 9(6): 486-91; Davies JC Pediatr Pulmonol Suppl. 2004; 26: 147-8).
Таким образом, существует необходимость в дополнительных агентах, которые можно использовать для лечения микробных инфекций.
Авторы настоящего изобретения идентифицировали пептиды, которые неожиданно обладают более высокой противомикробной активностью по сравнению с природными дефензинами.
Согласно первому аспекту изобретения предложен пептид, содержащий от 3 до примерно 200 D- и/или L-аминокислот, которые могут быть одинаковыми или разными, где эти аминокислоты выбраны из группы, состоящей из гидрофобных аминокислот и/или катионных аминокислот. Этот пептид может содержать от 3 до примерно 100 D- и/или L-аминокислот, например от 3 до 50 аминокислот D- и/или L-аминокислот, включая от 4 до примерно 50 D- и/или L-аминокислот.
Пептиды по изобретению полезны, среди прочего, в лечении или предупреждении микробных инфекций.
В следующем аспекте изобретения предложен пептид, содержащий аминокислоты формулы I:
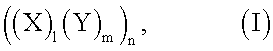
где l и m представляют собой целые числа от 0 до 10, например от 0 до 5; n представляет собой целое число от 0 до 10; Х и Y, которые могут быть одинаковыми или разными, представляют собой аминокислоту, выбранную из группы, состоящей из гидрофобных аминокислот и/или катионных аминокислот.
В предпочтительном аспекте изобретения пептид содержит от 3 до 200 аминокислот, например от 3, 4, 5, 6 или 7 вплоть до 100 аминокислот, включая от 3, 4, 5, 6 или 7 вплоть до 20, 25, 30, 35, 40 или 42 аминокислот.
Пептид по изобретению может содержать от 100 до 200 аминокислот, от 27 до 100 аминокислот, от 28 до 86 аминокислот, от 7 до 27 аминокислот или от 3 до 14 аминокислот.
Предпочтительно, пептиды содержат от 3 до 15 аминокислот, например от 3 до 7 аминокислот.
В следующем предпочтительном аспекте пептиды содержат один или более чем один цистеиновый остаток, например вплоть до 6 цистеиновых остатков, например 1, 2, 3, 4, 5 или 6 цистеиновых остатков.
В предпочтительном аспекте изобретения предложен пептид, содержащий аминокислоты формулы II:
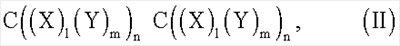
где С представляет собой цистеин, l, n и m представляют собой целые числа от 0 до 10; и Х и Y, которые могут быть одинаковыми или разными, представляют собой аминокислоту, выбранную из группы, состоящей из гидрофобных аминокислот и/или катионных аминокислот.
В следующем предпочтительном аспекте изобретения предложен пептид, содержащий аминокислоты формулы III:
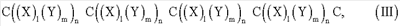
где С, X, Y, l, m и n являются такими, как определено в данном описании.
Еще в одном предпочтительном аспекте изобретения предложен пептид, содержащий аминокислоты формулы IV:
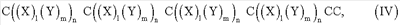
где С, X, Y, l, m и n являются такими, как определено в данном описании.
Поскольку пептиды по изобретению являются более простыми по структуре, чем природные бета-дефензины, они просты и эффективны для получения. Эти пептиды также по существу нечувствительны к соли и не являются гепатотоксичными. Кроме того, механизм их действия, являющийся скорее физическим, чем метаболическим (то есть непосредственный разрыв мембраны скорее, чем воздействие на компоненты жизненно важных метаболических путей), минимизирует, если не исключает, возможность, что у микроорганизмов-мишеней может развиться устойчивость к этим противомикробным агентам.
Как известно специалистам в данной области, аминокислоты могут быть помещены в различные классы в зависимости, прежде всего, от химических и физических свойств аминокислотной боковой цепи. Например, некоторые аминокислоты обычно считаются гидрофильными или полярными аминокислотами, а другие считаются гидрофобными или неполярными аминокислотами. Используемые в данном описании термины “гидрофобный” и “катионный” могут относиться к аминокислотам, обладающим гидрофобностью, которая больше или равна – 1,10, и/или суммарным зарядом, который больше или равен 0, как описано в Fauchere and Pliska Eur. J. Med Chem. 10: 39 (1983). Гидрофобная или неполярная аминокислота может также относиться к аминокислоте, имеющей боковую цепь, которая является незаряженной при физиологическом pH, которая является неполярной и которая, как правило, отталкивается водным раствором.
В предпочтительном аспекте изобретения Х и/или Y выбраны из группы гидрофобных аминокислот, состоящей из глицина, лейцина, фенилаланина, пролина, аланина, триптофана, валина, изолейцина, метионина, тирозина и треонина, и/или из группы катионных аминокислот, состоящей из орнитина, гистидина, аргинина и лизина. Х и/или Y могут представлять собой D- или L-аминокислоты. Кроме того, Х и/или Y могут представлять собой чередующиеся аминокислоты.
Изобретение также включает известные изомеры (структурные, стерео-, конформационные и конфигурационные) и структурные аналоги вышеуказанных аминокислот, а также те, которые являются модифицированными либо от природы (например посттрансляционная модификация), либо химическим путем, включая, но не исключительно, фосфорилирование, гликозилирование, сульфонилирование и/или гидроксилирование.
Как правило, пептиды по изобретению не включают аминокислоты: аспарагиновую кислоту, глутаминовую кислоту, аспарагин, глутамин или серин, но некоторые пептиды по изобретению могут обладать активностью, даже если эти аминокислоты присутствуют.
Пептиды по изобретению могут включать в себя один или более чем один дополнительный аминокислотный остаток, смежный с одним или с обоими концевыми цистеиновыми остатками формулы II, III или IV, например пептиды могут содержать вплоть до 10 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10) дополнительных аминокислотных остатков. Предпочтительно, дополнительные аминокислоты представляют собой нецистеиновые остатки. Более предпочтительно, дополнительные аминокислоты представляют собой Х и/или Y.
Кроме того, аминокислотная последовательность пептида может быть модифицирована, результатом чего является пептидный вариант, который включает замену по меньшей мере одного аминокислотного остатка в пептиде другим аминокислотным остатком, включая замены, в которых используют D-, а не L-форму.
Один или более чем один из остатков пептида может быть заменен на другой для изменения, усиления или сохранения биологической активности пептида. Такой вариант может обладать, например, по меньшей мере примерно 10% биологической активности соответствующего невариантного пептида. Часто используют консервативные аминокислоты, то есть замены аминокислот с похожими химическими и физическими свойствами, как описано выше.
Следовательно, например, консервативные аминокислотные замены могут включать замену лизина на аргинин, орнитин или гистидин; замену одной гидрофобной аминокислоты на другую. После введения замен варианты подвергают скринингу на биологическую активность.
Пептид может содержать по меньшей мере 4 аминокислоты, например от 4 до 50 аминокислот, или 4 и 50 аминокислот, например от 20 до 45 аминокислот, например 20, 25, 30, 35, 40, 42 или 45 аминокислот.
В предпочтительном аспекте изобретения Х и Y являются одинаковыми и представляют собой лейцин или глицин.
В следующем предпочтительном аспекте изобретения Х представляет собой лейцин, и Y представляет собой глицин.
В предпочтительном аспекте изобретения Х и Y являются одинаковыми и представляют собой лизин или аргинин. Таким образом, в изобретении предложены пептиды, выбранные из поли-L-лизина, поли-D-лизина, поли-L-аргинина и поли-D-аргинина.
Еще в одном предпочтительном аспекте изобретения Х представляет собой лизин, и Y представляет собой аргинин.
В пептиде по изобретению l и m могут быть равны 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, и n может быть равно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
В пептиде по изобретению l может быть равно 1, n может быть равно 1, и m может находиться между 4 и 9, например m может быть равно 3, 4, 5, 6, 7, 8 или 9.
В пептиде по изобретению l, n и/или m могут находиться между 1 и 5, например 1, 2, 3, 4 или 5.
Предпочтительно, пептид является ациклическим. Пептид может быть с прямой цепью, то есть линейным, или разветвленным.
Термин “пептид”, используемый в данном описании, означает в общем смысле множество аминокислотных остатков, соединенных вместе пептидными связями. Он используется взаимозаменяемо и означает то же самое, что полипептид и белок.
В одном воплощении изобретения пептид содержит аминокислотную последовательность, выбранную из группы, состоящей из:
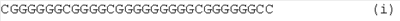
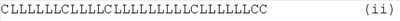
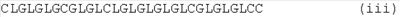
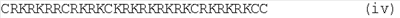




В следующем аспекте изобретения пептид содержит по меньшей мере одну из аминокислотных последовательностей (i)-(viii) и дополнительные аминокислотные остатки, смежные с одним или с обоими из концевых остатков цистеина. Таким образом, в следующем воплощении изобретения предложен пептид, содержащий аминокислотную последовательность, выбранную из аминокислотных последовательностей, представленных на Фиг.1.
Пептиды по изобретению, как правило, представляют собой синтетические пептиды. Эти пептиды могут представлять собой выделенные, очищенные пептиды или их варианты, которые могут быть синтезированы in vitro, например, способом твердофазного пептидного синтеза, пептидного синтеза, катализируемого ферментами, либо с помощью технологии рекомбинантных ДНК.
Для идентификации активных пептидов, которые имеют небольшую нежелательную токсичность или не токсичны для клеток млекопитающих, могут быть получены индивидуальные пептиды или пептидные библиотеки, и индивидуальные пептиды или пептиды из этих библиотек могут быть подвергнуты скринингу на противомикробную активность и токсичность, включая, но не ограничиваясь этим, противогрибковую, антибактериальную, антивирусную, антипротозойную, противопаразитарную активность и токсичность.
Пептиды по изобретению могут существовать в различных формах, таких как свободные кислоты, свободные основания, сложные эфиры и другие пролекарства, соли и таутомеры, например, и в изобретение включены все вариантные формы этих соединений.
Таким образом, изобретение охватывает соль или пролекарство пептида или пептидного варианта по изобретению.
Пептиды по изобретению можно вводить в форме фармацевтически приемлемых солей. Фармацевтически приемлемые соли по настоящему изобретению можно синтезировать из исходного пептида, который содержит основную или кислотную группировку, стандартными химическими способами. Как правило, такие соли могут быть получены путем взаимодействия форм свободной кислоты или основания этих пептидов со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе, либо в смеси этих двух растворителей; как правило, предпочтительными являются неводные среды, такие как этиловый эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечни пригодных солей находятся в Remington’s Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., US, 1985, p.1418, описание которого включено в данное изобретение путем ссылки; см. также Stahl et al, Eds, “Handbook of Pharmaceutical Salts Properties Selection and Use”, Verlag Helvetica Chimica Acta and Wiley-VCH, 2002.
В изобретение, таким образом, включены фармацевтически приемлемые соли описанных пептидов, где исходное соединение модифицировано посредством получения его кислотных или основных солей, например традиционных нетоксичных солей или солей четвертичного аммония, которые образуются, например, из неорганических или органических кислот или оснований. Примеры таких солей присоединения кислот включают в себя ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, лактат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, пальмоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат. Соли оснований включают в себя соли аммония, соли щелочных металлов, такие как соли натрия и калия, соли щелочноземельных металлов, такие как соли кальция и магния, соли с органическими основаниями, такие как соли дициклогексиламина, N-метил-D-глутамина, и соли с аминокислотами, такими как аргинин, лизин и т.д. Основные азотсодержащие группы также могут быть кватернизированы такими агентами, как низшие алкилгалогениды, такие как метил-, этил-, пропил- и бутилхлориды, бромиды и йодиды; диалкилсульфаты, такие как диметил-, диэтил-, дибутил- и диамилсульфаты; длинноцепочечные галогениды, такие как децил-, лаурил-, миристил- и стеарилхлориды, бромиды и йодиды, аралкилгалогениды, такие как бензил- и фенетилбромиды, и другие.
Соли карбоксильных групп пептида или пептидного варианта по изобретению могут быть получены обычным способом путем приведения пептида в контакт с одним или более эквивалентами желаемого основания, такого как, например, основание, представляющее собой гидроксид металла, например гидроксид натрия; карбонат или бикарбонат металла, такой как, например, карбонат или бикарбонат натрия; либо аминное основание, такое как, например, триэтиламин, триэтаноламин и тому подобное.
N-ацильные производные аминогруппы пептида или пептидных вариантов по изобретению могут быть получены путем использования N-ацилзащищенной аминокислоты для конечной конденсации либо путем ацилирования защищенной или незащищенной аминокислоты. O-ацильные производные могут быть получены, например, путем ацилирования свободного гидроксипептида или пептидной смолы. Любое ацилирование можно проводить, используя стандартные ацилирующие реагенты, такие как ацилгалогениды, ангидриды, ацилимидазолы и тому подобное.
В изобретение включены пролекарства для активных фармацевтических видов описанных пептидов, например, в которых одна или более функциональных групп защищены или преобразованы, но могут превращаться in vivo в функциональную группу, как в случае сложных эфиров карбоновых кислот, превращаемых in vivo в свободную кислоту или, в случае защищенных аминов, в свободную аминогруппу. Термин “пролекарство”, используемый в данном описании, представлен в конкретных структурах, которые быстро трансформируются in vivo в исходную структуру, например, посредством гидролиза в крови. Подробное обсуждение приведено в Т. Higuchi and V. Stella, Pro-drugs as Novel Delivery Systems, Vol.14 of the ACS Symposium Series, Edward B. Roche, ed., Bioreversible Carriers in Drug Design, American Pharmaceutical Association and Pergamon Press, 1987; H. Bundgaard, ed., Design of Prodrugs, Elsevier, 1985; and Judkins, et al. Synthetic Communications, 26 (23), 4351-4367 (1996), где каждая из публикаций включена в данное описание путем ссылки.
Таким образом, пролекарства включают в себя лекарственные средства, имеющие функциональную группу, которая трансформирована в ее обратимое производное. Типично, такие пролекарства превращаются в активное лекарственное средство посредством гидролиза. В качестве примеров можно упомянуть следующее:
| Функциональная группа |
Обратимое производное |
| Карбоновая кислота |
Сложные эфиры, включая, например, ацилоксиалкиловые эфиры, амиды |
| Спирт |
Сложные эфиры, включая, например, сульфаты и фосфаты, а также сложные эфиры карбоновых кислот |
| Амин |
Амиды, карбаматы, имины, энамины |
| Бороновая кислота |
Сложный эфир диола |
| Карбонил (альдегид, кетон) |
Имины, оксимы, ацетали/кетали, сложные енольные эфиры, оксазолидины и тиазоксолидины |
Пролекарства также включают в себя соединения, превращаемые в активное лекарственное средство путем окислительной или восстановительной реакции. В качестве примеров можно упомянуть:
Окислительная активация
– N-и O-дезалкилирование
– Окислительное дезаминирование
– N-окисление
– Эпоксидирование
Восстановительная активация
– Азовосстановление
– Сульфоксидное восстановление
– Дисульфидное восстановление
– Биовосстановительное алкилирование
– Нитровосстановление
В качестве метаболической активации пролекарств следует также упомянуть нуклеотидную активацию, активацию фосфорилированием и активацию декарбоксилированием.
Использование защитных групп полностью описано в ‘Protective Groups in Organic Chemistry’, edited by J W F McOmie, Plenum Press (1973), и в ‘Protective Groups in Organic Synthesis’, 2nd edition, Т W Greene & P G M Wutz, Wiley-Interscience (1991).
Таким образом, специалистам в данной области следует понимать, что, хотя защищенные производные описанных пептидов могут не обладать фармакологической активностью как таковые, их можно вводить, например, парентерально или перорально, после чего они метаболизируются в организме с образованием соединений, которые являются фармакологически активными. Такие производные, таким образом, являются примерами “пролекарств”. Все пролекарства описанных соединений включены в объем изобретения.
В следующем аспекте изобретения предложена фармацевтическая композиция, содержащая фармацевтически эффективное количество по меньшей мере одного из пептидов по изобретению или двух или более чем двух различных пептидов по изобретению.
Эти пептиды также включают фармацевтически приемлемый носитель, эксципиент или разбавитель. Выражение “фармацевтически приемлемый” используют в данном описании относительно соединений, веществ, композиций и/или лекарственных форм, которые являются, в пределах объема суждения специалистов в области медицины, пригодными для применения в контакте с тканями людей или, возможно, животного без чрезмерной токсичности, раздражения, аллергических реакций или других проблем или осложнений в соответствии с разумным соотношением пользы/риска.
Пептиды по изобретению полезны, среди прочего, в качестве противомикробных пептидов, например, против бактерий, грибков, дрожжей, паразитов, простейших и вирусов. Термин “противомикробный пептид” можно использовать в данном описании для определения любого пептида, который обладает бактерицидной и/или бактериостатической активностью и охватывает, не исключительно, любой пептид, описанный как обладающий антибактериальными, противогрибковыми, антимикозными, противопаразитарными, антипротозойными, антивирусными, противоинфекционными, антисептическими и/или гермицидными, альгицидными, амебоцидными, противомикробными, бактерицидными, фунгицидными, паразитицидными, протозоицидными свойствами.
Таким образом, в изобретении дополнительно предложен пептид по изобретению для применения в качестве лекарственного средства. Пептиды по изобретению могут иметь применение в качестве противомикробных агентов как in vivo, так и ex vivo.
В предпочтительном аспекте в изобретении предложено применение пептида по изобретению в изготовлении лекарственного средства для лечения микробной инфекции.
Под “микробной инфекцией” подразумевают инфекцию, вызванную бактериальным, паразитическим, простейшим, вирусным или грибковым патогеном. “Патоген” в целом определяют как любой организм, вызывающий заболевание.
Бактериальный патоген может происходить от видов бактерий, выбранных из группы, состоящей из: Staphylococcus spp., например Staphylococcus aureus, Staphylococcus epidermidis; Enterococcus spp., например Enterococcus faecalis; Streptococcus pyogenes; Listeria spp.; Pseudomonas spp.; Mycobacterium spp., например Mycobacterium tuberculosis; Enterobacter spp.; Campylobacter spp.; Salmonella spp.; Streptococcus spp., например Streptococcus группы А или В, Streptococcus pneumoniae; Helicobacter spp., например Helicobacter pylori; Neisseria spp., например Neisseria gonorrhea, Neisseria meningitidis; Borrelia burgdorferi; Shigella spp., например Shigella flexneri; Escherichia coli; Haemophilus spp., например Haemophilus influenzae; Chlamydia spp., например Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci; Francisella tularensis; Bacillus spp., например Bacillus anthracis; Clostridia spp., например Clostridium botulinum; Yersinia spp., например Yersinia pestis; Treponema spp.; Burkholderia spp.; например Burkholderia mallei и В pseudomallei.
Вирусный патоген может происходить от вируса, выбранного из группы, состоящей из: вируса иммунодефицита человека (ВИЧ1 и 2); вируса Т-клеточного лейкоза человека (HTLV 1 и 2); вируса Эбола; вируса папилломы человека (например, HPV-2, HPV-5, HPV-8, HPV-16, HPV-18, HPV-31, HPV-33, HPV-52, HPV-54 и HPV-56); паповавируса; риновируса; полиовируса; герпесвируса; аденовируса; вируса Эпштейна-Барр; вируса гриппа, вирусов гепатита В и С, вируса оспы человека, ротавируса или коронавируса SARS (тяжелого острого респираторного синдрома).
Паразитический патоген может происходить от паразитического патогена, выбранного из группы, состоящей из Trypanosoma spp. (Trypanosoma cruzi, Trypansosoma brucei), Leishmania spp., Giardia spp., Trichomonas spp., Entamoeba spp., Naegleria spp., Acanthamoeba spp., Schistosoma spp., Ptasmodium spp., Crytosporidium spp., Isospora spp., Balantidium spp., Loa Loa, Ascaris lumbricoides, Dirofilaria immitis, Toxoplasma ssp., например Toxoplasma gondii.
Грибковый патоген может происходить от грибкового патогена из рода Candida spp. (например, C.albicans), Epidermophyton spp., Exophiala spp., Microsporum spp., Trichophyton spp. (например, T.rubrum и T.interdigitale), Tinea spp., Aspergillus spp., Blastomyces spp., Blastoschizomyces spp., Coccidioides spp., Cryptococcus spp., Histoplasma spp., Paracoccidiomyces spp., Sporotrix spp., Absidia spp., Cladophialophora spp., Fonsecaea spp., Phialophora spp., Lacazia spp., Arthrographis spp., Acremonium spp., Actinomadura spp., Apophysomyces spp., Emmonsia spp., Basidiobolus spp., Beauveria spp., Chrysosporium spp., Conidiobolus spp., Cunninghamella spp., Fusarium spp., Geotrichum spp., Graphium spp., Leptosphaeria spp., Malassezia spp., Mucor spp., Neotestudina spp., Nocardia spp., Nocardiopsis spp., Paecilomyces spp., Phoma spp., Piedraia spp., Pneumocystis spp., Pseudallescheria spp., Pyrenochaeta spp., Rhizomucor spp., Rhizopus spp., Rhodotorula spp., Saccharomyces spp., Scedosporium spp., Scopulariopsis spp., Sporobolomyces spp., Syncephalastrum spp., Trichoderma spp., Trichosporon spp., Ulocladium spp., Ustilago spp., Verticillium spp., Wangiella spp.
Микробные инфекции, подлежащие лечению пептидами по настоящему изобретению, могут быть выбраны из любых человеческих бактериальных, грибковых, паразитических, оболочечных вирусных патогенов, представленных в Таблице 1.
Таким образом, в изобретении предложено применение пептида по изобретению в изготовлении лекарственного средства для лечения микробной инфекции, где микробная инфекция представляет собой системную, местную, подкожную, кожную грибковую инфекцию или грибковую инфекцию слизистой оболочки.
Грибковые инфекции можно классифицировать как системные, что означает, что инфекция является глубокой и поражает внутренние органы или переносится кровью, либо местные (дерматофитные), что означает, что инфекция является поверхностной и наблюдается на коже. Кроме того, дрожжевые инфекции могут поражать слизистые оболочки организма. Дрожжевые инфекции также могут быть системными (например, кандидемия и другие часто смертельные заболевания). Грибковые инфекции на коже обычно лечат кремами или мазями (местные противогрибковые лекарственные средства). Однако системные инфекции, дрожжевые инфекции или местные инфекции, которые не устраняются после лечения кремами или мазями, может быть необходимо лечить системными противогрибковыми лекарственными средствами (перорально или в/в). Эти лекарственные средства применяют, например, для лечения распространенных грибковых инфекций, таких как дерматофития (дерматомикоз), который встречается на коже, или кандидоз (дрожжевая инфекция, также известная как молочница), который может встречаться в горле, во влагалище или в других частях организма. Системные противогрибковые лекарственные средства также применяют для лечения других глубоких грибковых инфекций, таких как гистоплазмоз, бластомикоз и аспергиллез, которые могут поражать легкие и другие органы. Иногда их применяют для предупреждения или лечения грибковых инфекций у людей, иммунная система которых ослаблена, таких как пациенты после пересадки костного мозга или органа и люди с ВИЧ-СПИД.
Местные или дерматофитные грибковые инфекции, хотя типично не являются причиной смерти или серьезного заболевания, являются распространенными и экономически значимыми, поскольку их лечение может быть дорогостоящим. Местные или поверхностные грибковые инфекции могут включать в себя инфекции кожи, тонкой пластинки, рогового слоя, ногтей и волос. Кожные инфекции представляют собой инфекции кожи, ногтей пальцев рук и ног.
В предпочтительном аспекте изобретения грибковая инфекция представляет собой онихомикоз. Онихомикоз может быть вызван грибком из рода Trichophyton spp., например этот грибок может представлять собой Trichophyton interdigitale или Trichophyton rubrum, но не ограничивается этим.
Термин “онихомикоз” включает, но не ограничивается этим, дистальный латеральный подногтевой, поверхностный белый, проксимальный белый подногтевой, вторичный дистрофический, первичный дистрофический, внутриногтевой, кандидальный (например онихомикоз и хроническое кожно-слизистое заболевание) типы онихомикоза. Показано, что онихомикоз является значимым фактором риска для многих серьезных клинических осложнений, таких как острый бактериальный целлюлит руки/ноги и другие вторичные бактериальные инфекции, таким образом, настоящее изобретение охватывает эти инфекции.
Пептиды по изобретению являются эффективными противомикробными пептидами для широкого разнообразия патогенов. Однако пептиды по изобретению могут быть также полезны в лечении других состояний, включая, но не ограничиваясь этим, муковисцидоз и другие состояния, ассоциированные с инфекциями слизистых оболочек, например желудочно-кишечными, мочеполовыми или респираторными инфекциями.
Пептиды по изобретению могут быть также полезны в лечении или предупреждении, среди прочего, ран, язв и поражений, например кожных ран, таких как порезы или ожоги, и состояний, ассоциированных с ними.
Термин “лечение” относится к эффектам пептидов, описанных в данном изобретении, то есть к оказанию помощи пациентам, пораженным (инфекционным) заболеванием, включая улучшение состояния пациента или замедление развития заболевания.
Используемый в данном описании термин “лечение раны” может включать заживление раны и ассоциированных с ней состояний и терапию, которая стимулирует, способствует или ускоряет заживление тканей и включает послеоперационные рубцы, ожоги, псориаз, ускорение ремоделирования ткани, например, после косметической операции и трансплантации органа.
Таким образом, в следующем аспекте изобретения предложен субстрат, на который наносят или к которому присоединяют пептид по изобретению. Предпочтительно, этот субстрат является пригодным для наложения на раны или доставки в места ранения. Предпочтительно, этот субстрат позволяет переносить пептиды по изобретению из субстрата в раневое ложе для достижения их антибиотического эффекта. Субстрат может представлять собой перевязочный материал, например перевязочный материал для раны. Этот перевязочный материал может содержать текстильный материал, или он может представлять собой коллагеноподобный материал.
Пептиды по изобретению также могут находить применение в качестве дезинфицирующего средства/в дезинфицирующем средстве. В данном контексте пептид или фармацевтические композиции по изобретению могут быть использованы либо отдельно, либо в комбинации с другими дезинфицирующими агентами на поверхности, подлежащей обработке. Как использовано в данном описании, “поверхность, подлежащая обработке” может представлять собой субстрат, как определено в данном описании, или медицинское устройство.
В следующем аспекте в изобретении предложен способ лечения или предупреждения микробной инфекции у субъекта, включающий введение указанному субъекту терапевтически эффективного количества пептида по изобретению.
В предпочтительном способе по изобретению микробная инфекция представляет собой грибковую инфекцию. В способе по изобретению пептид можно наносить на кожу или ногти указанного субъекта.
Млекопитающих, птиц и других животных можно лечить пептидами, композициями или способами, описанными в данном изобретении. Такие млекопитающие и птицы включают в себя людей, собак, кошек и домашний скот, такой как лошади, крупный рогатый скот, овцы, козы, куры и индюки и тому подобное. Кроме того, растения также можно обрабатывать пептидами, композициями или способами по изобретению.
В тех случаях когда субъект представляет собой животное, способ по изобретению можно использовать для ногтеподобных структур, включая, но не исключительно, копыта, когти и копытца.
Способ по изобретению может включать, кроме пептидной терапии, терапии, которые могут усиливать проникновение пептидов в ногти. Этот процесс можно усиливать химическими или физическими средствами. Физические терапии, такие как отслаивание ногтей или шлифовка дорзального слоя ногтя, могут усиливать проникание пептидов по изобретению. Химическое усиление проницаемости ногтя для пептидов по изобретению может быть достигнуто путем разрушения физических или химических связей внутри кератина ногтевой пластинки. Агенты, смягчающие ногти, включающие, но не исключительно, мочевину и салициловую кислоту, повышают гидратацию ногтя с уменьшением плотности ногтя и, следовательно, могут повысить его проницаемость для пептидов по изобретению. Соединения, содержащие сульфгидрильные группы, будут расщеплять дисульфидные связи в кератине ногтя и могут привести к дестабилизации и повышенному прониканию лекарственных средств. Соединения, включающие, но не исключительно, производные ацетилцистеина и меркаптоэтанола, можно использовать в комбинации с пептидами по изобретению. Другие известные эксципиенты/адъюванты для проницаемости ногтей, которые можно использовать в комбинации с пептидами по изобретению, включают в себя метилсульфонилметан, мочевину, полиэтиленгликоль, N-(2-меркаптопропионил)глицин, диметилсульфон и 2-н-нонил-1,3-диоксолан.
В следующем аспекте в изобретении предложен способ лечения раны у субъекта, включающий нанесение на рану терапевтически эффективного количества пептида или субстрата по изобретению.
Пептиды по изобретению, включая их соли, вводят таким образом, чтобы достичь уменьшения по меньшей мере одного симптома, ассоциированного с инфекцией, показанием или заболеванием, либо снижения количества антитела, связанного с показанием или заболеванием.
Для достижения желаемого(ых) эффекта(ов) пептид, его вариант или их комбинацию можно вводить в виде однократной или разделенных доз, например по меньшей мере от примерно 0,01 мг/кг до примерно 500-750 мг/кг, по меньшей мере от примерно 0,01 мг/кг до примерно 300-500 мг/кг, по меньшей мере от примерно 0,1 мг/кг до примерно 100-300 мг/кг или по меньшей мере от примерно 1 мг/кг до примерно 50-100 мг/кг массы тела или по меньшей мере от примерно 1 мг/кг до примерно 20 мг/кг массы тела, хотя другие дозировки могут обеспечить благоприятные результаты. Вводимое количество будет варьировать в зависимости от различных факторов, включая, но не ограничиваясь этим, выбранный пептид и его клинические эффекты, заболевание, массу, физическое состояние, состояние здоровья, возраст млекопитающего, должно быть достигнуто предупреждение или лечение, и является ли пептид химически модифицированным. Такие факторы могут быть легко определены врачом при исследовании эмпирических данных клинических испытаний и изучении доклинических результатов на животных моделях или других тест-системах, которые доступны в данной области.
Введение терапевтических агентов в соответствии с настоящим изобретением можно осуществлять в однократной дозе, в многократных дозах, в непрерывном или чередующемся режиме в зависимости, например, от физиологического состояния реципиента, от того, является ли цель введения терапевтической или профилактической, и от других факторов, известных практикующим специалистам в данной области. Введение пептидов по изобретению может быть по существу непрерывным в течение предварительно выбранного периода времени, либо его можно проводить в виде серии разделенных доз. Рассматривают как местное, так и системное введение.
Для приготовления композиции пептиды синтезируют или получают иным путем, очищают, насколько это необходимо или желательно, а затем лиофилизируют и стабилизируют. Затем пептид может быть доведен до подходящей концентрации и возможно объединен с другими агентами. Абсолютная масса данного пептида, включенного в стандартную дозу, может широко варьировать. Например, можно вводить от примерно 0,01 до примерно 2 г или от примерно 0,01 до примерно 500 мг по меньшей мере одного пептида по изобретению либо множества пептидов, специфичных для конкретного типа клеток. Альтернативно, стандартная дозировка может варьировать от примерно 0,01 г до примерно 50 г, от примерно 0,01 г до примерно 35 г, от примерно 0,01 г до примерно 25 г, от примерно 0,5 г до примерно 12 г, от примерно 0,5 г до примерно 8 г, от примерно 0,5 г до примерно 4 г или от примерно 0,5 г до примерно 2 г.
Суточные дозы пептидов по изобретению также могут варьировать. Такие суточные дозы могут находиться в интервале, например, от примерно 0,001 г/сутки до примерно 100 или 50 г/сутки, от примерно 0,1 г/сутки до примерно 25 г/сутки, от примерно 0,1 г/сутки до примерно 12 г/сутки, от примерно 0,1 г/сутки до примерно 5 г/сутки, от примерно 0,1 г/сутки до примерно 2,5 г/сутки, от примерно 0,1 г/сутки до примерно 2 г/сутки, от примерно 0,5 г/сутки до примерно 8 г/сутки, от примерно 0,5 г/сутки до примерно 4 г/сутки, от примерно 0,5 г/сутки до примерно 2 г/сутки и от примерно 0,5 г/сутки до примерно 1 г/сутки.
Таким образом, одну или более чем одну подходящую стандартную лекарственную форму, содержащую терапевтические пептиды по изобретению, можно вводить многими путями, включая пероральный, парентеральный (включая подкожный, внутривенный, внутримышечный и внутрибрюшинный), ректальный, кожный, трансдермальный, внутригрудной, внутрилегочный и интраназальный (респираторный) пути. Терапевтические пептиды могут быть приготовлены в виде жидкого препарата или для пролонгированного высвобождения (например, с использованием микроинкапсуляции, см. WO 94/07529 и патент США  4962091). Препараты могут быть, если это целесообразно, удобно представлены в дискретных стандартных лекарственных формах, и их можно приготавливать любым из способов, хорошо известных в области фармацевтики. Такие способы могут включать стадию смешивания терапевтического агента с жидкими носителями, твердыми матриксами, полутвердыми носителями, тонко измельченными твердыми носителями или их комбинациями, а затем, при необходимости, введения или формования продукта в желаемую систему доставки. 4962091). Препараты могут быть, если это целесообразно, удобно представлены в дискретных стандартных лекарственных формах, и их можно приготавливать любым из способов, хорошо известных в области фармацевтики. Такие способы могут включать стадию смешивания терапевтического агента с жидкими носителями, твердыми матриксами, полутвердыми носителями, тонко измельченными твердыми носителями или их комбинациями, а затем, при необходимости, введения или формования продукта в желаемую систему доставки.
Когда терапевтические пептиды по изобретению приготавливают для перорального введения, их обычно объединяют с фармацевтически приемлемым носителем, разбавителем или эксципиентом с образованием фармацевтического препарата или стандартной лекарственной формы. Для перорального введения пептиды могут быть представлены в виде порошка, гранулированного препарата, раствора, суспензии, эмульсии либо в природном или синтетическом полимере или смоле для проглатывания активных ингредиентов из жевательной резинки. Активные пептиды могут быть также представлены в виде болюса, электуария или пасты. Перорально вводимые терапевтические пептиды по изобретению могут быть также приготовлены в виде препаратов для пролонгированного высвобождения, например эти пептиды могут быть покрыты оболочкой, подвергнуты микроинкапсулированию или иным способом помещены в устройство для пролонгированной доставки. Суммарные активные ингредиенты в таких препаратах составляют от 0,1 до 99,9 мас.%/мас. препарата.
Фармацевтические препараты, содержащие терапевтические пептиды по изобретению, могут быть приготовлены с помощью методик, известных в данной области, с использованием хорошо известных и легкодоступных ингредиентов. Например, пептид может быть приготовлен в виде препарата с обычными эксципиентами, разбавителями или носителями и в форме таблеток, капсул, растворов, суспензий, порошков, аэрозолей или тому подобного. Примеры эксципиентов, разбавителей и носителей, которые являются пригодными для таких препаратов, включают в себя буферы, а также наполнители и разбавители, такие как крахмал, целлюлоза, сахара, маннит и производные кремния. Могут быть включены также связующие агенты, такие как карбоксиметилцеллюлоза, гидроксиметилцеллюлоза, гидроксипропилметилцеллюлоза и другие производные целлюлозы, альгинаты, желатин и поливинилпирролидон. Могут быть включены увлажняющие агенты, такие как глицерин, разрыхлители, такие как карбонат кальция и бикарбонат натрия. Могут быть включены также агенты, замедляющие растворение, такие как вазелин. Могут быть включены также ускорители резорбции, такие как соединения четвертичного аммония. Могут быть включены поверхностно-активные агенты, такие как цетиловый спирт и глицерина моностеарат. Могут быть добавлены агенты адсорбции, такие как каолин и бентонит. Могут быть включены также смазывающие агенты, такие как тальк, стеарат кальция и магния и твердые полиэтиленгликоли. Могут быть добавлены также консерванты. Композиции по изобретению также могут содержать загустители, такие как целлюлоза и/или производные целлюлозы. Они также могут содержать смолы, такие как ксантановая, гуаровая или карбосмола или аравийская камедь, либо, альтернативно, полиэтиленгликоли, бентоны и монтмориллониты и тому подобное.
Например, таблетки или каплеты, содержащие пептиды по изобретению, могут включать в себя буферные агенты, такие как карбонат кальция, оксид магния и карбонат магния. Подходящие буферные агенты также могут включать в себя уксусную кислоту в соли, лимонную кислоту в соли, борную кислоту в соли и фосфорную кислоту в соли. Каплеты и таблетки также могут включать в себя неактивные ингредиенты, такие как целлюлоза, прежелатинизированный крахмал, диоксид кремния, гидроксипропилметилцеллюлоза, стеарат магния, микрокристаллическая целлюлоза, крахмал, тальк, диоксид титана, бензойная кислота, лимонная кислота, кукурузный крахмал, минеральное масло, полипропиленгликоль, фосфат натрия, стеарат цинка и тому подобное. Твердые или мягкие желатиновые капсулы, содержащие по меньшей мере один пептид по изобретению, могут содержать неактивные ингредиенты, такие как желатин, микрокристаллическая целлюлоза, лаурилсульфат натрия, крахмал, тальк, диоксид титана и тому подобное, а также жидкие растворители, такие как полиэтиленгликоли (ПЭГ) и растительное масло. Кроме того, каплеты или таблетки, покрытые энтеросолюбильным покрытием, содержащие один или более пептидов по изобретению, предназначены для противодействия распаду в желудке и растворению в более нейтральной-щелочной среде двенадцатиперстной кишки.
Терапевтические пептиды по изобретению могут быть также приготовлены в виде эликсиров или растворов для удобного перорального введения или в виде растворов, пригодных для парентерального введения, например, внутримышечным, подкожным, внутрибрюшинным или внутривенным путями. Фармацевтические препараты терапевтических пептидов по изобретению также могут принимать форму водного или безводного раствора или дисперсии либо, альтернативно, форму эмульсии, или суспензии, или мази.
Таким образом, терапевтические пептиды могут быть приготовлены в виде препаратов для парентерального введения (например, путем инъекции, например болюсной инъекции или непрерывной инфузии) и могут быть представлены в форме стандартной дозы в ампулах, предварительно заполненных шприцах, инфузионных контейнерах малого объема или в многодозовых контейнерах. Как указано выше, могут быть добавлены консерванты для поддержания срока хранения лекарственной формы. Активные пептиды и другие ингредиенты могут образовать суспензии, растворы или эмульсии в масляных или водных носителях и могут содержать такие агенты для приготовления препаратов, как суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активные пептиды и другие ингредиенты могут находиться в порошковой форме, полученной путем асептического выделения стерильного твердого вещества или путем лиофилизации из раствора для разведения подходящим растворителем, например стерильной апирогенной водой перед применением.
Эти препараты могут содержать фармацевтически приемлемые носители, растворители и адъюванты, которые хорошо известны в данной области. Возможно, например, приготавливать растворы, используя один или более чем один органический растворитель, который является приемлемым с физиологической точки зрения, выбранный, кроме воды, из растворителей, таких как ацетон, уксусная кислота, этанол, изопропиловый спирт, диметилсульфоксид, эфиры гликоля, такие как продукты, продаваемые под названием “Dowanol”, полигликоли и полиэтиленгликоли, С1-С4алкиловые эфиры короткоцепочечных кислот, этил- или изопропиллактат, триглицериды жирных кислот, такие как продукты, продаваемые под названием “Miglyol”, изопропилмиристат, животные, минеральные и растительные масла и полисилоксаны.
Предпочтительно, фармацевтические препараты терапевтических пептидов по изобретению также могут принимать форму растворителя или разбавителя, содержащего пептид. Растворители или разбавители могут включать в себя растворы кислот, диметилсульфон, N-(2-меркаптопропионил)глицин, 2-н-нонил-1,3-диоксолан и этиловый спирт. Предпочтительно, растворитель/разбавитель представляет собой кислотный растворитель, например уксусную кислоту, лимонную кислоту, борную кислоту, молочную кислоту, пропионовую кислоту, фосфорную кислоту, бензойную кислоту, масляную кислоту, яблочную кислоту, малоновую кислоту, щавелевую кислоту, янтарную кислоту или винную кислоту.
Более предпочтительно, растворитель представляет собой раствор уксусной кислоты. Растворитель, например раствор уксусной кислоты, может присутствовать в композиции в концентрации менее 1%, 0,5%, 0,25%, 0,1%, 0,05% или 0,01% кислоты, например уксусной кислоты.
В следующем аспекте настоящего изобретения предложено применение кислоты в изготовлении лекарственного средства для лечения микробной инфекции, в частности грибковой инфекции. Эта грибковая инфекция может представлять собой онихомикоз. Онихомикоз может быть вызван грибком из рода Trichophyton spp., но не ограничивается этим, например этот грибок может представлять собой Trichophyton interdigitale или Trichophyton rubrum. Кислота может быть такой, как описано в данном изобретении выше. Предпочтительно, кислота представляет собой уксусную кислоту. Еще предпочтительно, чтобы кислота присутствовала в растворе в концентрации менее 1%, 0,5%, 0,25%, 0,1%, 0,05% или 0,01% кислоты, например уксусной кислоты. Типично это лекарственное средство адаптировано для местного введения для лечения, например, ногтей.
Как используют в данном описании далее, термин “активный агент” охватывает единичный пептид по изобретению или комбинацию пептидов, как описано в данном изобретении. Термин “активный агент” может также охватывать фармацевтически эффективное количество кислоты, как описано в данном изобретении. Активные агенты можно вводить одновременно, последовательно или раздельно. В целом предпочтительно, чтобы такое введение было местным.
Активные агенты можно вводить в синергически эффективных количествах. Таким образом, изобретение включает: применение синергически эффективных количеств активных агентов, например пептида по изобретению и фармацевтически эффективного количества кислоты, как описано в данном изобретении, для изготовления продукта, например лекарственного средства, для одновременного, раздельного или последовательного введения указанных агентов при лечении микробной инфекции.
Возможно добавлять, если необходимо, адъювант, выбранный из антиоксидантов, сурфактантов, других консервантов, пленкообразующих, кератолитических или комедолитических агентов, ароматизаторов, корригентов и красителей. Могут быть добавлены антиоксиданты, такие как трет-бутилгидрохинон, бутилированный гидроксианизол, бутилированный гидрокситолуол и  -токоферол и их производные. -токоферол и их производные.
Также рассматриваются комбинированные продукты, которые включают один или более пептидов по настоящему изобретению и один или более других противомикробных или противогрибковых агентов, например полиенов, таких как амфотерицин В, липидный комплекс амфотерицина В (ABCD), липосомный амфотерицин В (L-AMB) и липосомный нистатин, азолы и триазолы, такие как вориконазол, флуконазол, кетоконазол, итраконазол, позаконазол и тому подобное; ингибиторов глюкансинтазы, таких как каспофунгин, микафунгин (FK463) и V-эхинокандин (LY303366); гризеофульвина; аллиламинов, таких как тербинафин; флуцитозина или других противогрибковых агентов, включая описанные в данном изобретении. Кроме того, предусматривают, что пептиды можно комбинировать с местными противогрибковыми агентами, такими как циклопирокс оламин, галопрогин, толнафтат, ундециленат, местный нистатин, аморолфин, бутенафин, нафтифин, тербинафин и другие местные агенты.
Кроме того, пептиды хорошо подходят для изготовления лекарственных форм с пролонгированным высвобождением и тому подобных. Эти препараты могут иметь такой состав, что они высвобождают активный пептид, например, в конкретном участке кишечного тракта или дыхательных путей, возможно, в течение некоторого периода времени. Покрытия, оболочки и защитные матриксы могут быть изготовлены, например, из полимерных веществ, таких как полилактид-гликолаты, липосомы, микроэмульсии, микрочастицы, наночастицы или воски. Эти покрытия, оболочки и защитные матриксы полезны для покрытия постоянных устройств, например стентов, катетеров, трубок для перитонеального диализа, дренажных устройств и тому подобного.
Для местного введения активные агенты могут быть приготовлены в виде препаратов, как известно в данной области, для непосредственного нанесения на целевую область. Формы, главным образом приспособленные для местного применения, имеют форму, например, кремов, молочка, гелей, порошков, дисперсии или микроэмульсий, лосьонов, сгущенных в большей или меньшей степени, импрегнированных подушечек, мазей или палочек, аэрозольных препаратов (например, спреев или пен), мыла, детергентов, лосьонов или кусков мыла. Другие традиционные формы для данной цели включают в себя перевязочный материал для ран, покрытые бандажи или другие полимерные покрытия, мази, кремы, лосьоны, пасты, желе, спреи и аэрозоли. Таким образом, терапевтические пептиды по изобретению можно доставлять посредством пластырей или бандажей для кожного введения. Альтернативно, пептид может быть приготовлен в виде препарата, являющегося частью адгезивного полимера, такого как полиакрилат или сополимер акрилата/винилацетата. Для долговременных применений может быть желательно использовать микропористые и/или воздухопроницаемые подстилающие слоистые материалы, чтобы можно было минимизировать гидратацию или мацерацию кожи. Подстилающий слой может иметь любую подходящую толщину, которая будет обеспечивать желаемые защитные и поддерживающие функции. Подходящая толщина будет составлять, как правило, от примерно 10 до примерно 200 микрон.
Местное введение можно осуществлять в форме покрытия или лака для ногтей. Например, противогрибковые пептиды могут быть приготовлены в виде раствора для местного введения, который содержит этилацетат (NF, национальный формуляр), изопропиловый спирт (USP, Фармакопея США) и бутиловый моноэфир поли[метилвиниловый эфир/малеиновая кислота] в изопропиловом спирте.
Фармацевтические препараты для местного введения могут содержать, например, физиологически приемлемый забуференный солевой раствор, содержащий от примерно 0,001 мг/мл до примерно 100 мг/мл, например от 0,1 мг/мл до 10 мг/мл одного или более пептидов по настоящему изобретению, специфичных для показания или заболевания, подлежащего лечению.
Мази и кремы могут быть приготовлены, например, в виде препаратов с водной или масляной основой с добавлением подходящих загущающих и/или желирующих агентов. Лосьоны могут быть приготовлены в виде препаратов с водной или масляной основой, и они будут, как правило, также содержать один или более эмульгирующих агентов, стабилизирующих агентов, диспергирующих агентов, суспендирующих агентов, загущающих агентов или красящих агентов. Активные пептиды также могут доставляться посредством ионтофореза, например, как раскрыто в патентах США  4140122; 4383529 или 4051842. Процент массы терапевтического агента по изобретению, присутствующего в местном препарате, будет зависеть от различных факторов, но обычно будет составлять от 0,01% до 95% суммарной массы препарата и типично 0,1-85% по массе. 4140122; 4383529 или 4051842. Процент массы терапевтического агента по изобретению, присутствующего в местном препарате, будет зависеть от различных факторов, но обычно будет составлять от 0,01% до 95% суммарной массы препарата и типично 0,1-85% по массе.
Капли, такие как глазные капли или капли в нос, могут быть приготовлены в виде препаратов с одним или более терапевтическими пептидами в водной или неводной основе, также содержащей один или более диспергирующих агентов, солюбилизирующих агентов или суспендирующих агентов. Жидкие спреи могут нагнетаться насосом или удобно доставляться из упаковок под давлением. Капли могут доставляться с помощью простой бутылочки, закрытой капельницей, пластиковой бутылочки, приспособленной для капельной доставки жидкого содержимого, или с помощью колпачка специальной формы.
Кроме того, терапевтический пептид может быть приготовлен в виде препарата для местного введения в рот или горло. Например, препараты активных ингредиентов могут быть приготовлены в виде лепешки, дополнительно содержащей корригирующую основу, обычно сахарозу, и аравийскую камедь или трагакант; пастилок, содержащих композицию в инертной основе, такой как желатин и глицерин или сахароза и аравийская камедь; и полосканий для рта, содержащих композицию по настоящему изобретению в подходящем жидком носителе.
Фармацевтические препараты по настоящему изобретению могут включать в качестве возможных ингредиентов фармацевтически приемлемые носители, разбавители, солюбилизирующие или эмульгирующие агенты и соли типа, который доступен в данной области. Примеры таких веществ включают в себя нормальные солевые растворы, такие как физиологически забуференные солевые растворы и вода. Конкретные неограничивающие примеры носителей и/или разбавителей, которые полезны в фармацевтических препаратах по настоящему изобретению, включают в себя воду и физиологически приемлемые забуференные солевые растворы, такие как фосфатно-солевые буферные растворы, рН 7,0-8,0.
Пептиды по изобретению можно также вводить в дыхательные пути. Таким образом, в настоящем изобретении также предложены аэрозольные фармацевтические препараты и лекарственные формы для применения в способах по изобретению. Как правило, такие лекарственные формы содержат количество по меньшей мере одного из агентов по изобретению, эффективное для лечения или предупреждения клинических симптомов конкретной инфекции, показания или заболевания. Любое статистически значимое ослабление одного или более симптомов инфекции, показания или заболевания, которое лечили согласно способу по настоящему изобретению, рассматривают как лечение такой инфекции, показания или заболевания в пределах объема изобретения.
Альтернативно, для введения путем ингаляции или инсуффляции композиция может принимать форму сухого порошка, например порошковой смеси терапевтического агента и подходящей порошковой основы, такой как лактоза или крахмал. Порошковая композиция может быть представлена в стандартной лекарственной форме, например, в капсулах или картриджах либо, например, в желатиновых или блистерных упаковках, из которых порошок можно вводить с помощью ингалятора, инсуффлятора или дозированного ингалятора (см., например, дозированный ингалятор под давлением (MDI) и ингалятор сухого порошка, раскрытый в Newinan, S.P. in Aerosols and the Lung, Clarke, S.W. and Davia, D. eds., p.197-224, Butterworths, London, England, 1984).
Терапевтические пептиды по настоящему изобретению можно также вводить в водном растворе при введении в форме аэрозоля или в ингаляционной форме. Таким образом, другие аэрозольные фармацевтические препараты могут содержать, например, физиологически приемлемый забуференный солевой раствор, содержащий от примерно 0,001 мг/мл до примерно 100 мг/мл одного или более пептидов по настоящему изобретению, специфичных для показания или заболевания, подлежащего лечению. Сухой аэрозоль в форме тонко измельченных твердых частиц пептида или нуклеиновой кислоты, которые не растворяются или не суспендируются в жидкости, также полезны в практике настоящего изобретения. Препараты пептидов по настоящему изобретению могут быть приготовлены в виде присыпок и могут содержать тонко измельченные частицы, имеющие средний размер частиц от примерно 1 до 5 мкм, альтернативно от 2 до 3 мкм. Тонко измельченные частицы могут быть получены путем пульверизации и фильтрования через сито с использованием методик, хорошо известных в данной области. Эти частицы можно вводить путем ингаляции заданного количества тонко измельченного вещества, которое может находиться в форме порошка. Следует понимать, что стандартное содержание активного ингредиента или ингредиентов, содержащихся в индивидуальной дозе аэрозоля каждой лекарственной формы, не обязательно должно составлять эффективное количество для лечения конкретной инфекции, показания или заболевания, поскольку необходимое эффективное количество может быть достигнуто путем введения множества стандартных доз. Кроме того, эффективное количество может быть достигнуто с использованием меньшей дозы, чем в стандартной лекарственной форме, либо индивидуально, либо в серии введений.
Что касается введения в верхние (носовые) или нижние дыхательные пути путем ингаляции, то терапевтические пептиды по изобретению удобно доставлять из небулайзера, или упаковки под давлением, или других удобных средств доставки аэрозольного спрея. Упаковки под давлением могут содержать подходящий пропеллент, такой как дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой подходящий газ. В случае аэрозоля под давлением стандартная доза может быть определена путем обеспечения клапана для доставки отмеренного количества. Небулайзеры включают в себя, но не ограничиваются этим, небулайзеры, описанные в патентах США  4624251; 3703173; 3561444 и 4635627. Аэрозольные системы доставки такого типа, как раскрыто в данном изобретении, доступны из различных коммерческих источников, включая Fisons Corporation (Bedford, Mass.), Schering Corp. (Kenilworth, NJ) и American Pharmoseal Co. (Valencia, CA). Что касается интраназального введения, то терапевтический агент можно также вводить посредством капель в нос, жидкого спрея, например, с помощью пульверизатора, представляющего собой пластиковую бутылочку, или дозированного ингалятора. Типы пульверизаторов представляют собой Mistometer (Wintrop) и Medihaler (Riker). 4624251; 3703173; 3561444 и 4635627. Аэрозольные системы доставки такого типа, как раскрыто в данном изобретении, доступны из различных коммерческих источников, включая Fisons Corporation (Bedford, Mass.), Schering Corp. (Kenilworth, NJ) и American Pharmoseal Co. (Valencia, CA). Что касается интраназального введения, то терапевтический агент можно также вводить посредством капель в нос, жидкого спрея, например, с помощью пульверизатора, представляющего собой пластиковую бутылочку, или дозированного ингалятора. Типы пульверизаторов представляют собой Mistometer (Wintrop) и Medihaler (Riker).
Кроме того, активные ингредиенты могут быть использованы также в комбинации с другими терапевтическими агентами, например болеутоляющими средствами, противовоспалительными агентами, антигистаминными агентами, бронходилататорами и тому подобным, либо для описанных состояний, либо какого-либо другого состояния.
В настоящем изобретении также предложен скрининговый анализ пептидов, которые обладают низкой токсичностью в отношении нормальных человеческих или других животных клеток, но обладают желательными противомикробными, например противогрибковыми, свойствами (пермеабилизация мембран клеток грибков, лизис или иной путь уничтожения или ингибирование роста грибков).
Кандидатные пептиды могут быть получены из библиотек пептидов по изобретению, как описано в данном изобретении. Пептиды могут быть также индивидуально или рационально сконструированы как обладающие конкретными структурными признаками.
Ниже изобретение будет описано только с помощью примера со ссылкой на следующие фигуры:
на Фиг.1 показаны аминокислотные последовательности четырех пептидов по изобретению;
на Фиг.2 представлена гистограмма, демонстрирующая рост грибка Т. interdigitale через (а) 4 суток и (б) 7 суток после обработки пептидами из Фиг.1;
на Фиг.3 представлена гистограмма, демонстрирующая рост грибка Т. rubrum через (а) 4 суток и (б) 7 суток после обработки пептидами из Фиг.1;
на Фиг.4 представлена гистограмма, демонстрирующая рост грибка Candida albicans через (а) 24 часа и (б) 48 часов после обработки пептидами из Фиг.1;
на Фиг.5 представлена гистограмма, демонстрирующая результаты дозозависимого эксперимента для пептида 1 (показанного на Фиг.1) на выживаемость Candida albicans через 24 часа после обработки;
на Фиг.6 представлен график, показывающий выживаемость Candida spp. через 24 часа в присутствии ряда доз пептида 4, как показано на Фиг.1;
на Фиг.7 представлен график, показывающий выживаемость 3 различных штаммов бактерий через 24 часа в присутствии ряда доз пептида 4, как показано на Фиг.1;
на Фиг.8 представлена гистограмма, демонстрирующая синергическое влияние 0,01% уксусной кислоты на противогрибковую активность (против Т. rubrum) пептида 4 (1 мг/мл) на сутки 3 роста;
на Фиг.9 представлена гистограмма, демонстрирующая ингибирование Т. interdigitale и T. rubrum пептидом 4;
на Фиг.10 представлена гистограмма, демонстрирующая эффекты пептида 3 и 4 на Т. interdigitale;
на Фиг.11 представлена гистограмма, демонстрирующая эффект уксусной кислоты на рост Т. interdigitale;
на Фиг.12 представлена гистограмма, демонстрирующая эффект полилизина на рост T. interdigitale;
на Фиг.13 представлена гистограмма, демонстрирующая эффекты полилизина и полиаргинина на рост T. rubrum;
на Фиг.14 представлена гистограмма, демонстрирующая ингибирование Т. interdigitale и Т. rubrum поли-L-аргинином;
на Фиг.15 представлена гистограмма, демонстрирующая эффект пониженной концентрации полиаргинина на Т. rubrum и Т. interdigitale;
на Фиг.16 представлена гистограмма, демонстрирующая эффект тримеров на рост Т. rubrum;
на Фиг.17 представлена гистограмма, демонстрирующая эффект пептида 4 и NaCl на рост Т. Interdigitale;
на Фиг.18 представлен график, показывающий эффект пептида 4 на Candida albicans при повышенных концентрациях соли;
на Фиг.19 представлена гистограмма, демонстрирующая эффекты полилизина и полиаргинина на выживаемость Candida albicans.
В Таблице 1 перечислены человеческие бактериальные, грибковые, паразитические и оболочечные вирусные патогены, подлежащие лечению пептидами по изобретению.
В Таблице 2 подробно описаны пептиды, которые соответствуют аминокислотным полимерным кодам, показанным в Результатах и Фигурах.
Ниже изобретение будет описано путем ссылки только на следующие примеры.
ПРИМЕРЫ
Материалы и методы, реагенты
Все пептиды получали либо путем твердофазного синтеза по контракту с Invitrogen-Evoquest, Carlsbad, CA, USA, либо получали от фирмы-поставщика пептидов NeoMPS SA (Strasbourg, France) или Sigma-Aldrich Chemical Company Ltd. (Poole, UK). Что касается тестов с грибками, то лиофилизированный пептид приготавливают в виде исходного раствора 1000 мкг/мл в буфере для анализа. В тех случаях когда ясно показано в экспериментах, на основании которых получены Фиг.2-8 и Фиг.11, уксусную кислоту добавляли в качестве растворителя до конечной концентрации 0,5%.
Патогены
Штаммы Trichophyton interdigitale (NCPF 117) и Trichophyton rubrum (NCPF 335) были получены из Национальной Коллекции патогенных грибов в Бристоле и поддерживались в культуре путем пересева приблизительно с месячными интервалами на скошенный агар Сабуро (Sabuoraud) и картофельный декстрозный агар при 30°С. Candida albicans штамм 3179 (полученный из Национальной Коллекции типовых культур [NCTC], Колиндейл) поддерживали в бульоне Мюллера-Хинтона (Mueller Hinton) фирмы Oxoid при 37°С. Streptococcus pyogenes штамм 8198, Staphylococcus aureus штамм 10642 (метициллин-устойчивый) и E. coli 0157 штамм 12900 были получены из NCTC в Колиндейле и поддерживались в бульоне Мюллера-Хинтона фирмы Oxoid при 37°С.
Анализы чувствительности роста грибков
Чтобы определить чувствительность грибковых штаммов к каждому из тестируемых пептидов, их воздействие на рост грибков оценивали следующим образом. Суспензии конидий и фрагментов гиф Т. interdigitale и Т. rubrum приготавливали путем добавления 10 мл свежего питательного глюкозного бульона (Nutrient Glucose Broth, NGB) (питательный бульон фирмы Oxoid, содержащий 2 мас.%/об. глюкозы) к культуре на скошенном агаре и перемешивали шпателем. Полученную в результате суспензию фрагментов конидий/гиф фильтровали через 2 слоя стерильной хирургической марли для удаления больших пленок гиф и кусочков агара. 20 мкл этой суспензии (поглощение при 540 нм примерно 0,1, что соответствует примерно 106 ростков/мл) инокулировали в каждую лунку стерильных 96-луночных микротитрационных планшетов, в которую заранее добавляли суммарный объем 80 мкл питательной среды (NGB) и соответствующее количество раствора пептида. Контрольные лунки представляли собой лунки, в которых конечный объем буфера для анализа, равный 100 мкл, доводили одной средой NGB плюс растворитель (если его использовали, и в такой же концентрации, что и в образцах пептидов). Мониторинг роста грибков в планшетах проводили на основании поглощения при 540 нм в считывающем устройстве для планшетов Microtek после 24 ч, 4 суток и 7 суток инкубации при 30°С.
Анализы на выживаемость Candida albicans
Чтобы определить чувствительность штаммов грибков к каждому из тестируемых пептидов, их воздействие на выживаемость Candida оценивали следующим образом. Культуры С. albicans выращивали в течение 18-24 ч, затем хранили при 4°С до использования. Свежие ночные культуры центрифугировали при 2000×g в течение 10 мин и промывали свежим бульоном Мюллера-Хинтона, доводя количество жизнеспособных клеток до значения между 5×106 и 1×107/мл. Буфер для анализа приготавливали путем добавления 100 мкл среды NGB к 6,9 мл 10 мМ натрий-фосфатного буфера, pH 7,7. 35 мкл буфера для анализа без пептидов или с рядом концентраций пептидов добавляли в стерильный полипропиленовый флакон с завинчивающейся крышкой и добавляли 15 мкл инокулята Candida albicans, описанного выше. Флаконы инкубировали при 37°С в водяной бане в течение 2 ч и количество выживших Candida spp. определяли путем серийного разведения в стерильном фосфатно-солевом буфере (ФСБ) и высевали на 9 см чашки Петри, содержащие агар Сабуро фирмы Oxoid (20 мл). Подсчет проводили после инкубации этих чашек при 37°С в течение 18-24 ч.
Анализы выживаемости бактерий
Streptococcus pyogenes штамм 8198, Staphylococcus aureus штамм 10642 (метициллин-устойчивый) и Е. coli 0157 штамм 12900 (все получены из NCTC, Колиндейл) выращивали в течение 18-24 ч, затем хранили при 4°С до использования. Свежие ночные культуры центрифугировали при 2000×g в течение 10 мин и промывали свежим бульоном Мюллера-Хинтона. Чувствительность к каждому из четырех пептидов анализировали, как описано выше для С. albicans. Для Е. coli и S. aureus исходное количество клеток для анализа чувствительности к пептиду составляло 108/мл, и среда, используемая для подсчета, представляла собой питательный агар (Oxoid). Str. pyogenes рос хуже, чем другие штаммы, на агаре Мюллера-Хинтона, и поэтому исходное количество клеток для этих анализов было ниже, чем для других штаммов, при 106/мл. Выживаемость Str. pyogenes определяли, используя триптозно-соевый агар Oxoid вместо питательного агара.
Результаты
Ингибирование роста Trichophtyon spp. пептидами 1-4
Два клинически релевантных кожных патогенных грибка Trichopyton rubrum и Trichopyton interdigitale культивировали, как описано выше в разделе Материалы и Методы, только в ростовой среде (контрольные культуры) или в ростовой среде, содержащей 50 мкг/мл пептида 1, 2, 3 или 4 (показано на Фиг.1). Рост Т. interdigitale и Т. rubrum оценивали путем измерения оптической плотности (поглощение при 540 нм) после 4 и 7 суток в культуре. По сравнению с контрольными необработанными образцами каждый тестируемый пептид значительно ингибировал рост Т. interdigitale (Фиг.2) и Т. rubrum (Фиг.3) на 4 и 7 сутки. Контрольные культуры каждого тестируемого штамма продолжали расти, на что указывает повышение считываний OD между 4 и 7 сутками.
Ингибирование роста и выживаемости Candida spp. пептидами 1-4
Дрожжи Candida albicans культивировали, как описано выше в разделе Материалы и Методы, только в ростовой среде (контрольные культуры) или в ростовой среде, содержащей 50 мкг/мл или 100 мкг/мл и 300 мкг/мл или 500 мкг/мл пептида 1, 2, 3 или 4. Рост С. albicans оценивали на основании измерения оптической плотности (поглощение при 540 нм) после 24 ч (Фиг.4а) и 48 ч (Фиг.4б) в культуре. По сравнению с контрольными необработанными образцами каждый тестируемый пептид значительно ингибировал рост С. albicans время- и дозозависимым образом. Зависимость ингибирования роста от дозы дополнительно подтверждали в экспериментах, в которых рост С. albicans оценивали оптически после 24 ч в культуре в контрольных условиях (только ростовая среда) или в присутствии ряда концентраций пептида 1, от 50 мкг/мл до 500 мкг/мл (Фиг.5). В отдельном эксперименте выживаемость С. albicans оценивали после 18-24 ч в культурах, выращенных только в среде (контроли) или включающих ряд концентраций пептида 4 с интервалом от 1 мкг/мл до 1000 мкг/мл (Фиг.6). Выживаемость организмов С. albicans, как оценивали на основании подсчетов выживаемости после 24 ч в культуре, снижалась дозозависимым образом (Фиг.6).
Ингибирование выживаемости бактерий пептидом 4
Три клинически релевантных патогенных бактерии, E. coli 0157, метициллин-устойчивый Staphylococcus aureus (MRSA) и Streptococcus pyogenes подвергали воздействию, как описано выше в разделе Материалы и Методы, серии, содержащей ряд концентраций пептида 4. Через 3 ч образцы каждой бактериальной культуры переносили на чашки с подходящей твердофазной ростовой средой и количество жизнеспособных колоний в контрольных (только ростовая среда) и обработанных (ростовая среда, содержащая пептид 4) образцах оценивали через 18-24 ч. После 3 ч воздействия пептид 4 значительно ингибировал выживаемость каждого бактериального штамма (Фиг.7) по сравнению с контрольными необработанными культурами дозозависимым образом.
Уксусная кислота усиливает противогрибковую активность пептида 4
Поскольку как контрольная (без пептида), так и тестируемая (содержащая пептид 1, 2, 3 или 4) среда в экспериментах, показанных на Фиг.2 и 3, содержала 0,5% уксусной кислоты в качестве растворителя пептида (подробности в разделе Материалы и Методы), был поставлен отдельный эксперимент, чтобы выяснить, может ли сама уксусная кислота играть роль в активности пептида и/или выживаемости грибков. С этой целью были поставлены эксперименты в отношении роста Т. rubrum, как в разделе Материалы и Методы, только с ростовой средой, с ростовой средой, содержащей только 0,01% уксусной кислоты, с ростовой средой, содержащей 1 мг/мл пептида 4, и с ростовой средой, содержащей 1 мг/мл пептида 4 плюс 0,01% уксусной кислоты. Рост грибка определяли по OD, как описано выше, после 3 суток в культуре. Как ожидали, пептид 4 ингибировал рост Т. rubrum. Только 0,01% уксусной кислоты не оказывал значительного воздействия на рост Т. rubrum (Фиг.8), но при включении в среду с пептидом 4 присутствие 0,01% уксусной кислоты значительно ингибировало рост Т. rubrum больше, чем 1 мг/мл одного пептида 4.
Ингибирование роста Т. interdigitale и Т. rubrum пептидом 4
Ингибиторные эффекты пептида 4 на рост Trichophyton spp. определяли путем анализа роста грибка, как в Материалах и Методах. Т. rubrum и Т. interdigitale культивировали в одной среде или в среде, содержащей 3 различных концентрации пептида 4. Уксусная кислота не присутствовала ни в одном из образцов. Контроли с одной средой использовали для иллюстрации фонового поглощения среды. Рост грибка определяли по OD, как описано выше, после 96 часов инкубации при 30°С. Как показано на Фиг.9, эти анализы подтвердили ингибиторный эффект пептида 4 на рост обоих видов грибков, причем Т. interdigitale постоянно более чувствителен к ингибиторным эффектам обработки пептидом 4, чем Т. rubrum. Рост Т. interdigitale ингибировали при концентрациях пептида 0,55 мг/мл.
Эффекты пептидов 3 и 4 на рост Т. interdigitale
Оценивали противогрибковый потенциал пептида 3 и пептида 4 в отношении Т. interdigitale. Анализы ингибирования роста проводили, как в Материалах и Методах, в отсутствие уксусной кислоты. Поскольку пептиды 1-3 являются высокогидрофобными и, следовательно, нерастворимыми, ранее тестировали только против Trichophyton spp. в уксусной кислоте в качестве растворителя. Когда культуры Т. interdigitale выращивали в течение 7 суток в присутствии пептида 3, пептида 4 или одной среды без растворителя уксусной кислоты и измеряли рост по OD, наблюдали, что пептид 4 значительно ингибировал рост грибка (Фиг.10), тогда как пептид 3 не проявлял ингибиторной активности (Фиг.10). Эта повышенная активность катионного пептида 4 по сравнению с гидрофобным пептидом 3 в отсутствие 0,5% уксусной кислоты позволяет предположить значительный вклад уксусной кислоты в активность, наблюдавшуюся ранее для гидрофобных пептидов.
Эффект уксусной кислоты на рост Т. interdigitale
Ингибирование роста Т. interdigitale уксусной кислотой оценивали с помощью экспериментов, определяющих рост грибков, согласно разделу Материалы и Методы. Культуры Т. interdigitale выращивали либо необработанными, либо обработанными 3 различными концентрациями уксусной кислоты при 30°С в течение 96 часов (Фиг.11). Это иллюстрирует отсутствие значительного эффекта 0,5% уксусной кислоты, такой же концентрации, как использовали ранее для пептидов 1-4 в качестве растворителя. Данный эксперимент вместе с отсутствием активности пептида 3 в отсутствие уксусной кислоты позволяет предположить, что пептид 4 является наиболее активным соединением против Trichophyton spp.
Эффект поли-L-лизина на рост Т. interdigitale
Поскольку пептид 4 является высококатионным пептидом, содержащим остатки лизина и аргинина, противогрибковую активность поли-L-форм этих аминокислот тестировали против Т. interdigitale с использованием анализов ингибирования роста, как подробно описано в Материалах и Методах, в отсутствие уксусной кислоты. Получали контрольные необработанные культуры Т. interdigitale и культуры, содержащие от 1 мг/мл до 50 мкг/мл молекул поли-L-лизина, варьирующих по длине 27-100 остатков и 100-200 остатков. Рост Т. interdigitale в каждой культуре оценивали после 96 часов при 30°С. Молекулы поли-L-лизина обоих размеров ингибировали рост T. interdigitale (Фиг.12), но, хотя молекула большего размера ингибировала рост при всех тестируемых концентрациях, ингибиторную активность с молекулой длины 27-100 аминокислот наблюдали только при более высоких концентрациях (Фиг.12). Это позволяет предположить, что ростингибирующие эффекты лизина на Trichophyton spp. зависят как от размера, так и от дозы.
Эффекты поли-L-аргинина и поли-L-лизина на рост Т. rubrum
Противогрибковую активность поли-L-аргинина в сравнении с поли-L-лизином затем тестировали против Т. rubrum. Ингибирование роста определяли, как в Материалах и Методах, в отсутствие уксусной кислоты. Т. rubrum культивировали в одной среде, в среде, содержащей поли-L-аргинин (длина 28-86 аминокислот) и поли-L-лизин (длина 100-200 аминокислот). Также ставили контроль с одной средой без инокулята. Культуры поддерживали и мониторинг роста проводили в течение 96 часов при 30°С. Как поли-L-аргинин, так и поли-L-лизин ингибировали рост Т. rubrum (Фиг.13). Поли-L-аргинин был более активным в своем ингибиторном воздействии против T. rubrum, чем поли-L-лизин при тестировании в эквивалентных дозах, суммарно ингибирующих рост при 1 мг/мл (Фиг.13).
Ингибирование T. interdigitale и Т. rubrum поли-L-аргинином
Ингибирование роста Trichophyton spp. поли-L-аргинином тестировали с помощью экспериментов, определяющих рост грибка, согласно разделу Материалы и Методы. Культуры Т. rubrum и Т. interdigitale выращивали либо в одной среде, либо в среде, содержащей 3 различные концентрации поли-L-аргинина. Уксусная кислота не присутствовала ни в одном из образцов. Контроли среды использовали для иллюстрации фонового поглощения среды. Рост грибка определяли по OD, как описано выше, после 96 часов инкубации при 30°С (Фиг.14). Видно, что полиаргинин более активен против обоих видов грибков вплоть до 0,55 мг/мл (Фиг.14).
Эффект сниженной концентрации (100 мкг/мл) полиаргинина в отношении Т. rubrum и Т. interdigitale
Ингибирование роста Trichophyton spp. поли-L-аргинином тестировали с помощью экспериментов, определяющих рост грибка, согласно разделу Материалы и Методы. Культуры Т. rubrum и Т. interdigitale выращивали либо необработанными, либо обработанными одной концентрацией полиаргинина (100 мкг/мл), причем уксусная кислота не присутствовала ни в одном из образцов. Контроли среды использовали для иллюстрации фонового поглощения среды. Рост грибка определяли по OD, как описано выше, после 96 часов инкубации при 30°С (Фиг.15). Сниженная концентрация приводит к потере активности, что иллюстрирует дозовый эффект полиаргинина на Trychophyton spp.
Эффект пептидных тримеров (3 аминокислоты) на рост Т. rubrum
Тестировали активность пептидных тримеров поли-L-лизина, поли-L-аргинина, поли-L-гистидина и поли-L-триптофана на рост Т. rubrum. Ингибирование роста проводили, как в Материалах и Методах, и Т. rubrum оставляли либо необработанным, либо подвергали воздействию 2 мг/мл каждого из тримеров. Культуры поддерживали в течение 96 часов при 30°С. Рост грибков измеряли по OD и результаты выражали в процентах роста в необработанной культуре (Фиг.16). Поли-L-аргинин был наиболее активным пептидом против T. rubrum, причем требовался только 3-аминокислотный полипептид, чтобы вызвать значительное снижение роста Т. rubrum.
Эффект пептида 4 (1.2 мг/мл) и NaCl на рост Т. interdigitale
Исследовали воздействие различных концентраций соли на противогрибковую активность пептида 4 в отношении Т. interdigitale. Анализы ингибирования роста T. interdigitale осуществляли, как в Материалах и Методах, в отсутствие уксусной кислоты. Культуры оставляли необработанными или подвергали воздействию пептида 4 плюс ряда концентраций NaCl от 100 мМ до 500 мМ. Культуры Т. interdigitale поддерживали в течение 96 часов при 30°С и рост оценивали по OD, как описано выше (Фиг.17). На противогрибковую активность пептида 4 не оказывали воздействия концентрации соли, близкие к физиологическим условиям или превышающие их (Фиг.17). Противомикробные активности эндогенных  -дефензинов хорошо описаны как ингибируемые даже низкими концентрациями соли. -дефензинов хорошо описаны как ингибируемые даже низкими концентрациями соли.
Эффект пептида 4 против Candida albicans при высоких концентрациях соли
Выживаемость С. albicans оценивали, как подробно описано в Материалах и Методах, после 2 ч инкубации при 37°С с рядом концентраций пептида 4. Две концентрации NaCl вводили в ростовую среду, чтобы убедиться в воздействии физиологических и очень высоких концентраций соли (известных как ингибирующие пептидную активность эндогенных  -дефензинов). Значительную киллерную активность пептида 4 наблюдали даже при очень высоких концентрациях соли (Фиг.18). По мере повышения концентрации пептида 4 видно, что воздействие более высокой концентрации соли уменьшается (Фиг.18). Следовательно, фунгицидная активность пептида 4 не ингибируется солями. -дефензинов). Значительную киллерную активность пептида 4 наблюдали даже при очень высоких концентрациях соли (Фиг.18). По мере повышения концентрации пептида 4 видно, что воздействие более высокой концентрации соли уменьшается (Фиг.18). Следовательно, фунгицидная активность пептида 4 не ингибируется солями.
Активность поли-L-лизина, поли-D-лизина и поли-D-аргинина против Candida albicans
Противогрибковую активность поли-L-аргинина по сравнению с лизином и поли-L- по сравнению с поли-D-лизином оценивали, чтобы определить, какой из этих пептидных вариантов демонстрирует повышенную активность против Candida albicans. Candida spp. инкубировали, как описано в разделе Материалы и Методы, в течение 2 часов при 37°С в присутствии 100 мкг/мл, 1 мг/мл и 10 мг/мл поли-D-лизина, поли-L-лизина и поли-L-аргинина. Выживаемость оценивали, как подробно описано выше, и продемонстрировали повышенную противогрибковую активность поли-L-аргинина по сравнению с поли-L-лизином (Фиг.19). Также продемонстрировали, что поли-D-лизин имеет очень похожую противогрибковую активность с поли-L-лизином.
| Таблица 1 (продолжение) |
| Неисчерпывающий перечень оболочечных вирусных патогенов человека |
| Оболочечный вирус: вирус, имеющий наружный липопротеиновый бислой, приобретенный в результате отпочкования от мембраны клетки хозяина |
| Вирус |
Заболевание |
Примечания |
| ТОГАВИРУСЫ |
 |
 |
| Альфавирусы: |
 |
 |
| Восточный энцефаломиелит лошадей |
Лихорадка, недомогание, головные боли, энцефалит |
 |
| Западный энцефаломиелит лошадей |
Лихорадка, недомогание, головные боли, энцефалит |
 |
| Венесуэльский энцефаломиелит лошадей |
Лихорадка, недомогание, головные боли, энцефалит |
Включает вирус/лихорадку Мукамбо, Эверглейдс, Tonate, Пиксуна, Cabassou |
| Реки Росс |
Лихорадка, сыпь, артралгия |
 |
| Чикунгунья |
Лихорадка, сыпь, артралгия, артрит |
 |
| Майяро |
Лихорадка, сыпь, артралгия |
 |
| О’Ньонг-Ньонг |
Лихорадка, сыпь, артралгия |
 |
| Синдбис |
Лихорадка, сыпь, артралгия |
Лихорадки Оскелбо, карельская и Погоста |
| Ндуму |
 |
 |
| Миддельбург |
 |
 |
| Бебару |
 |
 |
| Сагияма |
 |
 |
| Леса Семлики |
 |
 |
| Гета |
 |
 |
| Рубивирусы: |
 |
 |
| Краснуха |
Корь германская |
 |
| Шотландский энцефаломиелит овец |
 |
Клещевой |
| Негиши |
 |
Клещевой |
| Омский вирус |
 |
Клещевой |
 |
 |
 |
| БУНЬЯВИРУСЫ |
 |
 |
| Банги |
Лихорадка, сыпь |
 |
| Бханджа |
Лихорадка, энцефалит |
 |
| Иссык-Куль |
Лихорадка |
 |
| Касокеро |
Лихорадка |
 |
| Ньяндо |
Лихорадка |
 |
| Тамди |
Лихорадка |
 |
| Татагине |
Лихорадка |
 |
| Вановри |
Лихорадка, геморрагия |
 |
 |
 |
 |
| Буньявирусы: |
 |
 |
| Акабане |
 |
 |
| Буньямвера |
Лихорадка |
Буньямвера, Джермистон, Илеша, Shokwe, Тенсо, Вьеомия |
| Бвамба |
Лихорадка |
Бвамба, Понгола |
| С |
Лихорадка |
Апеу, Карапару, Итаки, Мадрид, Маритуба, Мурутуку, Непуйо, Орибока, Осса, Рестан |
 |
 |
 |
| Калифорнийский |
Лихорадка или энцефалит |
Калифорнийский энцефалит, Гуароа, Inkoo, La Crosse, зайцев-беляков, Джеймстаун-Каньон, Tahyna |
| Гуама |
Лихорадка |
Кату, Гуама |
| Симбу |
Лихорадка |
Шуни, Оропуш |
 |
 |
 |
| Флебовирусы: |
 |
 |
| Флеботомная лихорадка |
Лихорадка |
Alenquer, Кандину, Чагрес, Неаполь, Punto Toro, лихорадка долины Рифт, Сицилийский, Тоскана |
| Москитная лихорадка |
 |
 |
 |
 |
 |
 |
 |
 |
| Найровирусы: |
 |
 |
| Крымско-конголезская лихорадка |
Геморрагическая лихорадка |
 |
| Найробская геморрагическая лихорадка |
Лихорадка |
 |
| Хазара |
 |
 |
 |
 |
 |
| Хантавирусы: |
 |
 |
| Хантаан |
Геморрагическая лихорадка с почечным синдромом или хантавирусным легочным синдромом |
Хантаан (Корейская геморрагическая лихорадка), Пуумала, Сеул, Sin Nombre (Каньона Муэрто), Нью-Йорк, Black Creek Canal |
| Белград (Добрава) |
 |
 |
| Prospect Hill |
 |
 |
 |
 |
 |
| АРЕНАВИРУСЫ |
 |
 |
| LCM-Ласса-вирусный комплекс (аренавирусы Старого Света) |
 |
Ippy, лихорадка Ласса, лимфатический хориоменингит, Мобала, Мобейа |
| Такарибе-вирусный комплекс |
 |
Ампари, Flexal, Гуанарито, Хунин, Латино, Мачупо, Парана, Пичинде, Сабиа, Тамиами |
 |
 |
 |
   
Формула изобретения
1. Применение пептида или его фармацевтически приемлемой соли формулы I:
 , ,
где этот пептид содержит от 3 до 200 аминокислот, и где l и m представляют собой целые числа от 0 до 10; n представляет собой целое число от 1 до 10; Х и Y, которые могут быть одинаковыми или разными, представляют собой катионные аминокислоты, выбранные из аргинина и лизина, в изготовлении лекарственного средства для лечения грибковой инфекции.
2. Применение по п.1, где Х и/или Y представляет собой D или L-аминокислоты.
3. Применение по п.1, где Х и Y представляют собой чередующиеся аминокислоты.
4. Применение по п.1, где Х и Y являются одинаковыми.
5. Применение по п.1, где Х представляет собой лизин и Y представляет собой аргинин.
6. Применение по п.1, где пептид содержит от 3 до примерно 100 аминокислот.
7. Применение по п.1, где пептид содержит от 3 до 50 аминокислот.
8. Применение по п.7, где пептид содержит от 3 до 15 аминокислот.
9. Применение по п.8, где пептид содержит от 3 до 7 аминокислот.
10. Применение по п.1, пептид состоит из от 3 до 200 аминокислот.
11. Применение по п.1, где грибковая инфекция выбрана из группы, состоящей из дерматофитии, гистоплазмоза, бластомикоза и аспергиллеза.
12. Применение по п.1, где грибковая инфекция является недерматофитной инфекцией.
13. Применение по п.12, где грибковая инфекция представляет собой дрожжевую инфекцию.
14. Применение по п.13, где грибковая инфекция вызвана грибковым патогенном из рода Candida spp.
15. Применение по п.1, где грибковая инфекция является дерматофитной инфекцией.
16. Применение по п.15, где инфекция вызвана грибковым патогеном рода Trichophyton spp.
17. Применение по п.16, где грибковый патоген представляет собой Trichophyton interdigitale.
18. Применение по п.16, где патоген представляет собой Trichophyton rubrum.
19. Применение по п.15, где грибковая инфекция представляет собой кожную инфекцию.
20. Применение по п.19, где инфекция представляет собой онихомикоз.
21. Противогрибковая композиция, содержащая фармацевтически эффективное количество одного или более пептидов или их фармацевтически приемлемых солей и фармацевтически приемлемый носитель, эксципиент или разбавитель, где указанный пептид соответствует формуле I:
 , ,
где этот пептид содержит от 3 до 200 аминокислот, и где l и m представляют собой целые числа от 0 до 10; n представляет собой целое число от 1 до 10; Х и Y, которые могут быть одинаковыми или разными, представляют собой катионные аминокислоты, выбранные из аргинина и лизина.
22. Противогрибковая композиция по п.21, содержащая по меньшей мере два пептида формулы I, где эти пептиды являются разными.
23. Противогрибковая композиция по п.21, где эксципиент или разбавитель выбран из группы, состоящей из кислоты, диметилсульфона, N-(2-меркаптопропионил)глицина, 2-н-нонил-1,3-диоксолана и этилового спирта.
24. Противогрибковая композиция по п.23, где эксципиент или разбавитель представляет собой кислоту, выбранную из группы, состоящей из уксусной кислоты, лимонной кислоты, борной кислоты, молочной кислоты, пропионовой кислоты, фосфорной кислоты, бензойной кислоты, масляной кислоты, малоновой кислоты, яблочной кислоты, щавелевой кислоты, янтарной кислоты или винной кислоты.
25. Противогрибковая композиция по п.24, где кислота представляет собой уксусную кислоту.
26. Противогрибковая композиция по п.25, где уксусная кислота представлена в композиции в концентрации менее 1, 0,5, 0,25, 0,1, 0,05 или 0,01% уксусной кислоты.
РИСУНКИ
|
|