Патент на изобретение №2396207
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ MRI-КОНТРАСТИРУЮЩЕГО АГЕНТА
(57) Реферат:
Изобретение может быть использовано для получения высокоэффективных магниторелаксационных систем, а именно водорастворимых эндометаллофуллеренов, применяемых в ЯМР-томографии. Фуллереносодержащую сажу предварительно экстрагируют растворителем из класса ароматических углеводородов или сероуглеродом. Затем селективной экстракцией диметилформамидом получают твердую высокообогащенную по металлофуллеренам гадолиния смесь пустых фуллеренов и металлофуллеренов гадолиния Gd@C82. Смесь подвергают гидроксилированию перекисью водорода в один этап с получением Gd@C82(OH)x, где х больше или равен 20, представляющего собой водорастворимую гидроксилированную смесь пустых фуллеренов и металлофуллеренов гадолиния Gd@C82(OH)x. Полученный целевой продукт выделяют осаждением избытком спирта с последующим центрифугированием и отделяют от избытка перекиси водорода промывкой спиртом. 2 ил.
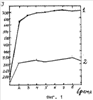
Изобретение относится к химии фуллеренов, а именно к методам получения высокоэффективных магниторелаксационных систем для ЯМР-томографии на основе водорастворимых эндометаллофуллеренов. Важнейшими материалами, улучшающими разрешение ЯМР изображения тканей, являются контрастирующие агенты, уменьшающие время релаксации протонов воды в исследуемой ткани. В настоящее время для этих целей используются различные органические комплексы гадолиния (хелаты), например Gd – диэтилентриаминиептаацетат (GD-ДТРА). Этот препарат коммерчески выпускается и используется для проведения ЯМР-томографии. Однако его недостатком является токсичность, связанная с возможным появлением в организме свободного иона гадолиния. В России магнитоконтрастирующие препараты не производятся. В настоящее время поиски ученых идут в направлении использования с этой целью эндометаллофуллеренов, обладающих способностью уменьшать время магнитной релаксации протонов воды и биологических жидкостей по сравнению с протонами тканей: [1] Патент JP 2001114713, A61K 49/00, G01N 30/00 (Gadolinium-Included Fullerol and its Use as Contrast Medium); [2] Патент US 20060088474, C07F 5/00 (Endohedral Metallofullerene Contrast Agent). Преимуществом эндометаллофуллеренов является то, что инкапсулированный в углеродную оболочку фуллерена ион металла защищен от химической атаки и потому не проявляет токсичности, характерной для тяжелых металлов. Другим важным в перспективе свойством эндометаллофуллернов является возможность присоединения к фуллереновой оболочке определенных функциональных групп, определяющих маршрут молекулы в организме и доставку ее в определенный орган/ткань при определенных методах администрирования. В качестве аналога нами рассмотрен способ получения гидроксилированного металлофуллерена гадолиния Gd@C82(ОН)2, описанный в работе [3] (Chemistry Letters., Soc, 2005, 34, Полученный гидроксилированный металлофуллерен не растворим в воде, поэтому не может быть использован в качестве контрастирующего агента. Наиболее близким к заявляемому способу получения MRI-констрастирующего агента является способ, описанный в работе [4]: Nano Letters, 5 (10), 2050-2057, 2005 – прототип. Способ заключается в следующем: MPI-контрастирующий агент готовится из Gd@C82. Металлофуллерены были синтезированы методом электродугового разряда и экстрагированы из фуллереносодержащей сажи (ФСС) диметилформамидом (ДМФ) с использованием высокой температуры и высокого давления. Разделение и очистка Gd@C82 была выполнена с помощью высокоэффективной жидкостной (ВЭЖХ) в сочетании с 5РВВ- и затем Buckyprep колоннами. Степень очистки доводили до 99,5%. Далее проводили гидроксилирование Gd@C82. Водорастворимый гадолиний-фуллеренол был синтезирован методом гидроксилирования по щелочной реакции. Раствор Gd@C82 в толуоле смешивают с водным раствором, содержащим 50% NaOH. Затем в реакционную систему добавляется несколько капель катализатора 40% ТВАН (тетрабутиламмоний гидроксид). Смесь растворов перемешивается при комнатной температуре. Выпавший осадок коричневого цвета отделяется, к нему добавляется вода, после чего он перемешивается в течение ночи. Далее он промывается метиловым спиртом, который затем удаляется в роторном испарителе. Процедуру промывки повторяют несколько раз до полного удаления остатков ТВАН и NaOH. Окончательно коричневый осадок растворяют в деионизованной воде при постоянном перемешивании до того момента, как цвет раствора не станет прозрачным. Красновато-коричневым раствор подвергают хроматографической очистке на колонке Сефадксе G-25 при элюированнии нейтрализованной водой. Оставшиеся следы катализатора и Na-ионов полностью удаляют в этом процессе. XPS-анализ дает формулу Gd@C82(ОН)22. К недостаткам этого способа относим сложную и трудоемкую процедуру хроматографического (ВЭЖХ) выделения Gd@C82, сложность процедуры гидроксилирования металлофуллерена Gd щелочным методом и дальнейшую его очистку. Совокупность всех этих сложнейших процедур приводит к значительным потерям целевого продукта. Общие потери целевого продукта по литературным данным составляют порядка 50% [5] (Journal of Radioanalytical and Nuclear Chemistry, V.272, Задачей, решаемой в предлагаемом изобретении, является упрощение и удешевление способа получения MPI-контрастирующего агента при сохранении высоких контрастирующих характеристик и нетоксичности. Технический результат – получение MPI-контрастирующего агента, имеющего хорошие контрастирующие характеристики, сравнимые со стандартными медицинскими заграничными препаратами. Технический результат достигается тем, что в способе получения MRI-контрастирующего агента на основе Gd@C82(OH)x, где х больше или равен 20, представляющего собой водорастворимую гидроксилированную смесь пустых фуллеренов и металлофуллеренов гадолиния Gd@C82(OH)x, включающем стадии извлечения Gd@C82 диметилформамидом из фуллереносодержащей сажи, его гидроксилирование и выделение целевого продукта, новым является то, что фуллереносодержащую сажу предварительно экстрагируют растворителем из класса ароматических углеводородов или сероуглеродом, затем селективной экстракцией диметилформамидом получают твердую высокообогащенную по металлофуллеренам гадолиния смесь пустых фуллеренов и металлофуллеренов гадолиния Gd@C82, которую подвергают гидроксилированию перекисью водорода в один этап, и полученный целевой продукт выделяют осаждением избытком спирта с последующим центрифугированием и отделяют от избытка перекиси водорода промывкой спиртом. Предлагаемая совокупность операций позволяет получить гидроксилированную смесь металлофуллеренов гадолиния Gd@C82(OH)x, пригодную, в том числе по чистоте, для применения в качестве MRI-контрастирующего агента. Такая смесь обладает также практически полезными свойствами, характерными для MRI-контрастирующих агентов, а именно: способностью уменьшать время магнитной релаксации протонов воды и биологических жидкостей по сравнению с чистой водой, хорошей растворимостью в воде. Растворимость в воде и содержание активной компоненты (Gd) для полученных препаратов были не менее 5 мг/мл и 3 вес.% соответственно. Кроме того, MRI-контрастирующий эффект полученного продукта в десятки раз выше, чем препаратов, используемых в медицинской практике (хелатные комплексы гадолиния). Присутствие пустых водорастворимых фуллеренов не приводят к эффектам токсичности [6] (Chem. Comm., 1999, 663-669). Заявляемый способ отличается простотой и относительной дешевизной, т.к. исключает стадии малопроизводительной и высокозатратной ВЭЖХ при выделении Gd@C82 и многоступенчатой очистки гидроксилированного целевого продукта. На фиг.1 представлен график «интенсивность ЯМР-сигнала – время» для выделенных областей крысы, где: кривая 1 показывает изменение интенсивности сигнала в области печени; кривая 2 показывает изменение интенсивности сигнала -время в области сердца. Фиг.1 относится к стандартному ЯМР-контрастному медицинскому препарату «Гадовист» (хелатный комплекс гадолиния). Введено 200 микромоля препарата «Гадовист». На фиг.2 представлено действие заявляемого MRI-контрастирующего агента. Показан график интенсивность ЯМР-сигнала – время» для выделенных областей крысы, где: кривая 1 показывает изменение интенсивности сигнала в области печени; кривая 2 показывает изменение интенсивности сигнала – время в области сердца. Введено 4,2 микромоля заявляемого MRI-контрастирующего агента. Таким образом, использованная доза заявляемого препарата была в 47 раз меньше, чем препарата «Гадовист». Заявляемый способ включает следующие операции. Из фуллереносодержащей сажи (ФСС) получают смесь пустых фуллеренов и металлофуллеренов гадолиния, высокообогащенную металлофуллеренами гадолиния. Для этого ФСС смешивают сначала с растворителем из класса ароматических углеводородов, например орто-ксилолом, или сероуглеродом. Затем проводят селективную экстракцию диметилформамидом (ДМФ), обладающим большим электрическим дипольным моментом. В результате этого получают смесь пустых фуллеренов, обогащенную металлофуллереном Gd – (Gd@C82). Затем полученную твердую вышеуказанную смесь фуллеренов гидроксилируют путем воздействия на нее перекиси водорода. Гидроксилирование проводят в один этап. Полученный целевой продукт выделяют осаждением избытком спирта и отделяют от избытка перекиси водорода. Пример конкретной реализации ФСС, полученная электродуговым способом, имеет состав: С60 – 70-85%; С70 – 28-15%; высшие фуллерены – 1,5-2%; металлофуллерены – 1,5-0,2%. Необходимое количество ФСС смешивается с компактирующей жидкостью (орто-ксилолом) в соотношении 1,5/1,0 г/мл соответственно. Добавляется пористое стекло фракции 0,25 мм в объемном соотношении 30:70 соответственно. Все тщательно перемешивается до получения компактной механической смеси равномерно распределенных компонентов гранулированной сажи и сферических частиц пористого стекла. Такое выполнение этой операции позволяет избежать образования комков, увеличивает поверхность соприкосновения сажи с растворителем при проведении дальнейших операций. Полученная смесь загружается в фильтровальный стаканчик аппарата Сокслета, заливается орто-ксилолом в соотношении 30 мл/г сажи и проводится экстракция фуллеренов в течение 5 часов. Происходит удаление основной части пустых фуллеренов. Затем орто-ксилол заменяется на диметилформамид (ДМФ). Проводится селективная экстракция диметилформамидом ФСС с целью получения высокообогащенной по Gd смеси. В результате этого получают смесь пустых фуллеренов и металлофуллеренов гадолиния (Gd@C82) в соотношении 40:60 соответственно (смесь высокообогащенная по металлофуллеренам Gd). Далее проводят фильтрацию экстракта фуллеренов в ДМФ через фильтр зеленая лента и PTFE фильтр 0,22 мкм. Затем осуществляют перевод этого экстракта в твердую фазу на роторном испарителе при пониженном давлении. Операцию гидроксилирования проводят в один этап действием перекиси водорода на твердую вышеуказанную смесь фуллеренов. Фуллереносодержащий препарат (смесь пустых фуллеренов и металлофуллеренов гадолиния, высокообогащенная по металлофуллеренам Gd), выделенный из диметилформамидного экстракта фуллеренов перемешивается в концентрированной Н2О2 (соотношение смесь/Н2О2, мг/мл=(20÷25)/1) при температуре Примерно через 1÷1,5 часа суспензия начинает превращаться в мутную смесь темно-коричневого цвета. Наблюдается газовыделение и пенообразование. По мере протекания процесса смесь становится все более прозрачной. Прозрачный темно-коричневый раствор охлаждается до комнатной температуры (при непрерывном перемешивании) и выливается в изопропиловый спирт, взятый в 20-кратном избытке по отношению к результирующему раствору. Образовавшаяся суспензия темно-коричневого цвета перемешивается на магнитной мешалке еще не менее 6 часов, а затем центрифугируется. Жидкий спиртовой раствор после центрифугирования – практически бесцветная жидкость, что свидетельствует о полноте извлечения целевого продукта. Очистка целевого продукта: осадок коричневого цвета водорастворимых гидроксилированных фуллеренов – промывается чистым спиртом от следов перекиси водорода и сушится под разрежением при температуре 40°С. Выход целевого продукта порядка 90% относительно сухого ДМФ экстракта. Степень очистки контролировалась диализом. В заявляемом способе не требуется очень высокой степени очистки Gd@C82 от пустых фуллеренов (в прототипе она доведена до 99,5%). Как мы указывали выше, методики очистки ВЭЖХ малопроизводительны, трудоемки и высокозатратны. Заявляемый способ не требует применения ВЭЖХ, не требует сложных процедур щелочного гидроксилирования, дальнейшей сложной очистки, связанной с большими потерями (до 50%) целевого продукта, дает хороший выход нетоксичного MRJ-контрастирующего вещества. Оценка контрастирующих свойств полученного Gd@C82(OH)x в смеси с пустыми фуллеренами, где х > или =20, проводилась методом ЯМР-томографии на крысах (фиг.2). ЯМР-томография проводилась в ФГУ «НИИ Онкологии им. Н.Н.Петрова Росмедтехнологий» С.-Петербург. Для сравнения мы привели данные для препарата «Гадовист» (фиг.1). Приводим данные по пересчету. Используемая доза заявляемого препарата в 47 раз меньше, чем доза стандартного медицинского препарата «Гадовист». Рассмотрим область ROI 1 – печень. Сигнал для «Гадовиста» в пересчете на одинаковую дозу с нашим препаратом составит 7,3 МР-единиц (350:47,6). Сигнал от заявляемого MRI-агента составил 215 MR-единиц. Т.е. отношение сигнала от заявляемого MRI-агента к сигналу от препарата «Гадовист» (коэффициент усиления контраста) в расчете на равные дозы составляет 29,24 (215:7,3). Пересчет для области ROI 2 – сердце. Сигнал для заявляемого MRI-агента равен 215 MP-ед. Сигнал для «Гадовиста» равен 700 МР-ед. Доза его в 47 раз больше. Следовательно, расчетный коэффициент усиления контраста для заявляемого MRI-агента в 14,6 раз выше (215:700×47,6). Таким образом, полученный магнитоконтрастный агент в 15÷30 раз эффективнее стандартного медицинского препарата «Гадовист». В дополнительных материалах мы даем параметрическую карту крысы и данные непосредственно с ЯМР-томографа. Литература 1. Патент JP 2001114713, A61K 49/00, G01N 30/00. 2. Патент US 20060088474, C07F 5/00. 3. Chemistry Letters. Soc, 2005, 34, 4. Nano Letters, 5 (10), 2050-2057, 2005 – прототип. 5. Journal of Radioanalytical and Nuclear Chemistry, V.272, 6. Chem. Comm., 1999, 663-669.
Формула изобретения
Способ получения MRI-контрастирующего агента на основе Gd@C82(OH)x, где х больше или равен 20, представляющего собой водорастворимую гидроксилированную смесь пустых фуллеренов и металлофуллеренов гадолиния Gd@C82(OH)x, включающий стадии извлечения Gd@C82 диметилформамидом из фуллереносодержащей сажи, его гидроксилирование и выделение целевого продукта, отличающийся тем, что фуллереносодержащую сажу предварительно экстрагируют растворителем из класса ароматических углеводородов или сероуглеродом, затем селективной экстракцией диметилформамидом получают твердую высокообогащенную по металлофуллеренам гадолиния смесь пустых фуллеренов и металлофуллеренов гадолиния Gd@C82, которую подвергают гидроксилированию перекисью водорода в один этап, и полученный целевой продукт выделяют осаждением избытком спирта с последующим центрифугированием и отделяют от избытка перекиси водорода промывкой спиртом.
РИСУНКИ
|
||||||||||||||||||||||||||

 9, 1264-1265). Способ относится к получению нового производного металлофуллерена, гидроксилированного эндоэдрального Gd – металлофуллрена. Gd@C82(ОН)2 был синтезирован реакцией раствора Gd@C82 в ортодихлорбензоле с 30% перекисью водорода.
9, 1264-1265). Способ относится к получению нового производного металлофуллерена, гидроксилированного эндоэдрального Gd – металлофуллрена. Gd@C82(ОН)2 был синтезирован реакцией раствора Gd@C82 в ортодихлорбензоле с 30% перекисью водорода. 60°С в течение ~20 часов (до образования практически прозрачного окрашенного раствора).
60°С в течение ~20 часов (до образования практически прозрачного окрашенного раствора).