|
|
(21), (22) Заявка: 2008132651/15, 07.08.2008
(24) Дата начала отсчета срока действия патента:
29.04.2008
(43) Дата публикации заявки: 20.02.2010
(46) Опубликовано: 27.07.2010
(56) Список документов, цитированных в отчете о
поиске:
ГАТИНА Р.Ф. и др. ЯМР-спектры галогенидных комплексов магния и алюминия. Доклады Академии наук Таджикской ССР, 1991, т.XXXIV,  7, с.424-427. EINARSRUD M.A, ERLING R., Infrared reflection spectra of AlCl3-MCl2 (М=Mg, Са, Sr, Ва, Mn and Zn) and oxochloroaluminate melts, Proceeding-Electrochemical Society, Proc. Jt. Int. 7, с.424-427. EINARSRUD M.A, ERLING R., Infrared reflection spectra of AlCl3-MCl2 (М=Mg, Са, Sr, Ва, Mn and Zn) and oxochloroaluminate melts, Proceeding-Electrochemical Society, Proc. Jt. Int.
(62) Номер и дата подачи первоначальной заявки, из которой данная заявка выделена: 2008117304, 29.04.2008
Адрес для переписки:
420033, г.Казань, ул. Светлая, 1, ФКП “ГосНИИХП”
|
(72) Автор(ы):
Михайлов Юрий Михайлович (RU),
Гатина Роза Фатыховна (RU),
Хацринов Алексей Ильич (RU),
Климович Ольга Викторовна (RU),
Омаров Залимхан Курбанович (RU)
(73) Патентообладатель(и):
Федеральное казённое предприятие “Государственный научно-исследовательский институт химических продуктов” (ФКП “ГосНИИХП”) (RU)
|
(54) ПОЛИХЛОРАЛЮМИНАТЫ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ
(57) Реферат:
Изобретение может быть использовано в химической промышленности. Полихлоралюминаты щелочноземельных металлов получены взаимодействием хлоридов щелочноземельных металлов с хлоридом алюминия в среде диэтилового эфира и соответствуют общей химической формуле МСl2·4АlСl3·nЕt2O, в которой при М=Са n=4,5; при М=Sr n=1, 1,5; при М=Ва n=2,5. Указанные химические соединения пригодны для использования в качестве реагентов для очистки нефтепродуктов и природного газа от меркаптанов и сероводорода, катализаторов в процессах хлорметилирования и алкилирования ароматических углеводородов, исходных веществ при получении гидридов металлов. 6 табл.
Изобретение относится к получению новых соединений – полихлоралюминатов щелочноземельных металлов в среде диэтилового эфира общей формулы
МСl2·4АlСl3·nЕt2O, в которой
при М=Са n=4,5; M=Sr n=1, 1,5; при М=Ва n=2,5, которые могут быть использованы в качестве реагентов для очистки нефтепродуктов и природного газа от сероводорода и меркаптанов, катализаторов в процессах хлорметилирования и алкилирования ароматических углеводородов, исходных веществ при получении гидридов металлов.
В литературе отсутствуют сведения о хлоридных комплексах щелочноземельных металлов с хлоридами алюминия, получаемых в среде диэтилового эфира.
Задачей настоящего изобретения является получение новых соединений – полихлоралюминатов щелочноземельных металлов в среде диэтилового эфира общей формулы МСl2·4АlСl3·nЕt2O, в которой при М=Са n=4,5; M=Sr n=1, 1,5; при М=Ва n=2,5, которые могут быть использованы в качестве реагентов для очистки нефтепродуктов и природного газа от сероводорода и меркаптанов, катализаторов в процессах хлорметилирования и алкилирования ароматических углеводородов, исходных веществ при получении гидридов металлов.
Поставленная задача достигается тем, что для получения вышеназванных соединений проводят взаимодействие хлоридов алюминия с хлоридами щелочноземельных металлов в среде диэтилового эфира.
Типичный опыт заключается в следующем. К взвеси МСl2 (где М=Са, Sr, Ва) в диэтиловом эфире добавляли эфират хлорида алюминия (АlСl3·Еt2O) при перемешивании в соотношении реагентов (MCl2·Et2O):(AlCl3·Et2O)=1:1,5 и общим объемом эфира 100-150 мл.
Взаимодействие реагентов проводили в трехгорлой колбе вместимостью 250 мл при комнатной температуре и обычном перемешивании в течение 5-6 часов по схеме:
Независимо от количества исходных веществ в растворе мольное соотношение элементов в комплексах щелочноземельных металлов составляло М(Са, Sr, Ва):Аl:Сl=1:4:14.
Признаками взаимодействия служат небольшое разогревание (до 30°С) реакционной массы, резкое уменьшение объема осадка и появление в растворе ионов щелочноземельных металлов, хлориды которых нерастворимы в диэтиловом эфире. Процесс ведут до постоянства элементов в растворе. Из прозрачного эфирного послереакционного раствора путем испарения 3/4 части растворителя в вакууме при 25°С с последующим вымораживанием насыщенного раствора азотом выделяют соединения брутто-состава: МСl2·4АlСl3·nEt2O, в которой при М=Са n=4,5; M=Sr n=1, 1,5; при М=Ва n=2,5.
В таблице 1 приведены результаты опытов взаимодействия хлоридов щелочноземельных металлов с хлоридами алюминия в среде диэтилового эфира. Полученные соединения представляют собой кристаллические порошки, со временем расплывающиеся на воздухе, поэтому рекомендовано хранить их в эксикаторе или закрытой посуде. В таблице 2 приведены физико-химические характеристики полученных соединений.
Выделенные из раствора комплексные соединения реакционноспособны и легко подвержены диссоциации в растворе при обработке большим количеством диэтилового эфира. Полученные соединения стабилизированы молекулами диэтилового эфира, которые в комплексе координированы по донорно-акцепторному механизму и относятся к оксониевым соединениям.
Новые соединения были идентифицированы совокупностью физико-химических методов: рентгенографией, термографией, ИК-спектроскопией, хроматографией и методом химического анализа. Установлено, что полихлоралюминаты щелочноземельных металлов в среде диэтилового эфира отвечают индивидуальным соединениям.
При изучении термической устойчивости полихлоралюминатов щелочноземельных металлов в среде диэтилового эфира установлено, что термические кривые имеют сложный характер разложения, отличный от составляющих: АlСl3 и МСl2, где М=Са, Sr, Ba. Обнаружено, что частичная десольватация происходит при температуре 50-200°С, а разложение комплексов происходит ступенчато, с предварительным плавлением. Анализ термоэффектов показывает, что наиболее устойчивыми комплексами в среде диэтилового эфира являются бариевые комплексы.
Полученные экспериментальные данные по термической устойчивости полихлоралюминатов щелочноземельных металлов в среде диэтилового эфира позволяют предположить следующие схемы их распада:
I SrCl2·4AlCl3·1,5Et2O SrCl2·4AlCl3+1,5Et2O SrCl2·4AlCl3+1,5Et2O
II SrCl2·4AlCl3 SrCl2+4AlCl3 SrCl2+4AlCl3
Рентгенографические исследования исходных веществ АlСl3, МСl2 (где М=Са, Sr, Ва) и полихлоралюминатов щелочноземельных металлов в среде диэтилового эфира показывают, что наборы рефлексов отражения отличаются от составляющих. Исследование полученных соединений методом ИК-спектроскопии установило, что колебательные частоты полихлоралюминатов в среде диэтилового эфира отличны от спектров составляющих хлоридов металлов. Так, во всех ИК-спектрах эфиратов полихлоралюминатов встречается полоса с частотой 400 см-1, которая характерна для иона  . У эфиратов полихлоралюминатов кальция, стронция и бария полоса симметрична, что, по-видимому, указывает на увеличение ионности связи. Следует также отметить, что кроме отмеченных выше изменений, имеются сдвиги полос, отвечающих за валентные колебания С-О-С. . У эфиратов полихлоралюминатов кальция, стронция и бария полоса симметрична, что, по-видимому, указывает на увеличение ионности связи. Следует также отметить, что кроме отмеченных выше изменений, имеются сдвиги полос, отвечающих за валентные колебания С-О-С.
Полихлоралюминаты брутто-формулы MCl2·AlCl3·nEt2O, в которой при М=Са n=4,5; M=Sr n=1, 1,5; при М=Ва n=2,5, нашли применение в качестве реагентов для очистки нефти и природного газа от сероводорода и меркаптанов. Например,
CaCl2·4AlCl3·4,5Et2O+4,5H2S=CaCl2·4AlCl3·4,5H2S+4,5Et2O
CaCl2·4AlCl3·4,5Et2O+4,5RSH=CaCl2·4AlCl3·4,5RSH+4,5Et2O
Реакцию проводят при температуре 25±5°С при мольном соотношении реагентов (MCl2·AlCl3·nEt2O):nH2S (nRSH)=1:n, в котором при М=Са n=4,5; M=Sr n=1, 1,5; при М=Ва n=2,5; R – углеводородный радикал.
В таблице 3 приведены условия протекания взаимодействия комплексных соединений с молекулами сероводорода и меркаптанов на примере метил-, этил- и пропилмеркаптанов. Так, например, использование в качестве реагента эфирата полихлоралюмината кальция при вышеназванных условиях обеспечивает связывание сероводорода до 85,2%, метил-, этил- и пропилмеркаптанов до 80,1%, 76,2% и 73,5% соответственно.
Для очистки газов от сероводорода и меркаптанов используют фильтры, содержащие в себе гранулы, состоящие из мелкодисперсных комплексных соединений на субстрате (оксидах металлов d-элементов). Поверхность гранулы реагента эффективно сорбирует из потока газа сероводород и меркаптаны. Газы, не содержащие в своем составе соединений серы, на поверхности гранул не задерживаются и с комплексным соединением не реагируют. Сероводород и меркаптаны, проходя через фильтр, в процессе комплексообразования активно конкурируют с кислородсодержащими соединениями, вытесняя их из комплексного соединения.
Важным направлением очистного действия комплексными соединениями алюминия заключается в связывании или переработке сернистых соединений дистиллата. Так, сероводород, почти всегда присутствующий в крекинг-дистиллате, реагирует с соединениями алюминия с образованием соответствующих комплексных соединений. Очистка нефтяных дистиллатов необходима перед проведением каталитических процессов дегидрирования и парциального окисления, ибо сера и ее соединения являются одними из самых сильных ядов, отравляющих поверхность катализаторов.
Кроме того, при наличии небольших количеств воды в дистиллате и даже в водных растворах полихлоралюминаты щелочноземельных металлов в среде диэтилового эфира будут давать также комплексные соединения типа аквакислот, способных диссоциировать с выделением иона водорода, например,
BaCl2·4AlCl3·2,5Et2O+5H2O 4([AlCl3OH]Н)+[BaCl2OH]H+2,5Et2O 4([AlCl3OH]Н)+[BaCl2OH]H+2,5Et2O
Эти аквакислоты имеют сильные кислотные свойства, но при разбавлении водой разрушаются. Зато в концентрированных водных растворах, а также в твердом виде с содержанием небольших количеств влаги, эти аквакислоты реагируют подобно минеральной кислоте, например, серной, обладая к тому же рядом преимуществ перед ней. Так, известную в литературе очистку дистиллата серной кислотой, во избежание разрушения отдельных ценных частей дистиллата, приходится вести при низких температурах. Очистку же комплексными соединениями алюминия в диэтиловом эфире можно проводить при повышенных температурах, усиливая тем самым ее эффективность.
Полихлоралюминаты щелочноземельных металлов в среде диэтилового эфира используют в качестве катализаторов в процессах хлорметилирования и алкилирования ароматических углеводородов. Так, непредельные углеводороды, входящие в состав нефти, легко конденсируются с бензолом и его гомологами в присутствии эфиратов полихлоралюминатов щелочноземельных металлов, при этом образуются гомологи бензола предельного характера, например, с амиленом – амилбензол:
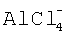
В таблице 4 приведены условия протекания данной реакции. Так, например, использование эфирата полихлоралюмината кальция, взятого в количестве 5% от массы бензола, приводит к образованию хлористого бензила с выходом 70%. Увеличение его содержания до 10% и более приводит к повышению выхода продукта до 82%. Таким образом, наиболее оптимальным количеством используемого катализатора является его 10%-ное содержание, взятое от массы бензола.
При взаимодействии бензола с муравьиным альдегидом в присутствии хлороводорода при использовании в качестве катализатора эфиратов полихлоралюминатов щелочноземельных металлов получают хлористый бензил:

Реакцию проводят при 60°С, пропуская хлористый водород через смесь бензола, параформальдегида и эфиратов полихлоралюминатов щелочноземельных металлов до прекращения абсорбции газов. В таблице 5 приведены условия проведения данной реакции. Так, использование в качестве катализатора, например, эфирата полихлоралюмината бария, взятого в количестве 10% от массы бензола, позволяет получить конечный продукт – хлористый бензил с выходом 80%; применение эфирата полихлоралюмината стронция – 87% С6Н5-СН2Сl.
Значение этой реакции велико, особенно если учитывать особенность легкого превращения группы -СН2Сl в другие, например, в группы -СН3, -CH2CN, -CHO,
-CH2NH2, -CH2OH.
Кроме того, полихлоралюминаты щелочноземельных металлов в среде диэтилового эфира используют как исходные вещества для получения алюмогидридных соединений металлов, например:


Суммируя левые и правые части уравнений 1 и 2 получаем:
CaCl2·4AlCl3·4,5Et2O+14LiAlH4 Са(AlH4)2+16AlH3+14LiCl+4,5Et2O Са(AlH4)2+16AlH3+14LiCl+4,5Et2O
Реакцию проводят при температуре 25°С в среде диэтилового эфира при мольном соотношении реагентов (MCl2·4AlCl3·nEt2O):LiAlH4=1:14 (где при М=Са n=4,5; M=Sr n=1, 1,5; при М=Ва n=2,5).
В таблице 6 приведены условия проведения данной реакции. Согласно полученным данным при использовании эфиратов полихлоралюминатов кальция, стронция и бария выход гидридов металлов составляет 80; 85 и 78% соответственно.
Таким образом, по совокупности физико-химических свойств полученные соединения – полихлоралюминаты щелочноземельных металлов в среде диэтилового эфира – являются новыми соединениями.
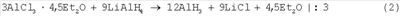 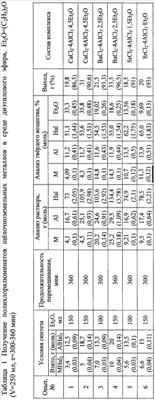
Таблица 3
Условия взаимодействия эфиратов полихлоралюминатов щелочноземельных металлов с серосодержащими соединениями |
 опыта опыта |
Формула соединения MCl2·4AlCl3·nEt2O (КС) |
Условия проведения опыта |
Получено, г(%) МСl2·4АlСl3·nН2S |
Условия проведения опыта |
Получено,г(%) MCl2·4AlCl3·nRSH |
| Взято, г (моль) |
Взято, г (моль) |
| КС |
H2S |
КС |
RSH |
| 1 |
CaCl2·4AlCl3·4,5Et2O |
489 (0,5) |
76,5 (2,25) |
320 (85,2) |
489 (0,5) |
108,0 (2,25) MM |
348,7(81,0) |
| 2 |
CaCl2·4AlCl3·4,5Et2O |
– |
– |
– |
489 (0,5) |
139,5 (2,25) ЭМ |
352,0 (76,2) |
| 3 |
CaCl2·4AlCl3·4,5Et2O |
– |
– |
– |
489 (0,5) |
171,0 (2,25) ПМ |
362,7 (73,5) |
| 4 |
SrCl2·4AlCl3·Et2O |
383,3 (0,5) |
17(0,5) |
319,7(88,0) |
383,3 (0,5) |
24,0 (0,5) MM |
303,6 (82,0) |
| 5 |
SrCl2·4AlCl3·Et2O |
– |
– |
– |
383,3 (0,5) |
31,0(0,5) ЭМ |
284,5 (75,4) |
| 6 |
SrCl2·4AlCl3·Et2O |
– |
– |
– |
383,3 (0,5) |
38,0 (0,5) ПМ |
277,5 (72,2) |
| 7 |
SrCl2·4AlCl3·1,5Et2O |
401,8(0,5) |
24 (0,75) |
310,1 (83,8) |
401,8 (0,5) |
36,0(0,75) MM |
306,6 (80,2) |
| 8 |
SrCl2·4AlCl3·1,5Et2O |
– |
– |
– |
401,8(0,5) |
46,2 (0,75) ЭМ |
290,0 (73,8) |
| 9 |
SrCl2·4AlCl3·1,5Et2O |
– |
– |
– |
401,8(0,5) |
57,0(0,75) ПМ |
290,4 (72,0) |
| 10 |
BaCl2·4AlCl3·2,5Et2O |
463,5 (0,5) |
106,25 (1,25) |
330,8 (80) |
463,5 (0,5) |
60,0(1,25) MM |
322,0 (74,7) |
| 11 |
BaCl2·4AlCl3·2,5Et2O |
– |
– |
– |
463,5 (0,5) |
77,5 (1,25) ЭМ |
313,9(70,0) |
| 12 |
BaCl2·4AlCl3·2,5Et2O |
– |
– |
– |
463,5 (0,5) |
95 (1,25) ПМ |
319,2(68,5) |
| Примечание: |
| MM – метилмеркаптан |
| ЭМ – этилмеркаптан |
| ПМ – пропилмеркаптан |
Таблица 4
Условия получения амилбензола с участием эфиратов полихлоралюминатов щелочноземельных металлов |
 опыта опыта |
Условия проведения опыта |
Получено С6Н5·С5Н11, г (%) |
| Формула соединения |
Взято, г (моль) |
MCl2·4AlCl3·nEt2O |
| С6Н6 |
С5Н10 |
г (моль) |
% (по бензолу) |
| 1 |
CaCl2·4AlCl3·4,5Et2O |
78(1) |
70(1) |
7,8 (0,008) |
10 |
125,8 (85) |
| 2 |
CaCl2·4AlCl3·4,5Et2O |
39 (0,5) |
35 (0,5) |
5,85 (0,006) |
15 |
62,9 (85) |
| 3 |
CaCl2·4AlCl3·4,5Et2O |
19,5 (0,25) |
17,5 (0,25) |
0,975 (0,001) |
5 |
25,9 (70) |
| 4 |
SrCl2·4AlCl3·1,5Et2O |
78(1) |
70(1) |
7,8 (0,001) |
10 |
130,2 (88) |
| 5 |
SrCl2·4AlCl3·1,5Et2O |
39 (0,5) |
35 (0,5) |
5,85 (0,007) |
15 |
65,1 (88) |
| 6 |
SrCl2·4AlCl3·1,5Et2O |
19,5 (0,25) |
17,5 (0,25) |
0,975 (0,001) |
5 |
27,7 (75) |
| 7 |
BaCl2·4AlCl3·2,5Et2O |
78(1) |
70(1) |
7,8 (0,008) |
10 |
118,4(80) |
| 8 |
BaCl2·4AlCl3·2,5Et2O |
39 (0,5) |
35 (0,5) |
5,85 (0,006) |
15 |
56 (80) |
| 9 |
BaCl2·4AlCl3·2,5Et2O |
19,5 (0,25) |
17,5 (0,25) |
0,975 (0,001) |
5 |
24,1 (65) |
Таблица 5
Условия получения хлористого бензила с участием эфиратов полихлоралюминатов щелочноземельных металлов |
 опыта опыта |
Условия проведения опыта |
Получено C6H5CH2Cl, г (%) |
| Формула соединения |
Взято, г (моль) |
MCl2·4AlCl3·nEt2O |
| С6Н6 |
НСl |
СН2O |
г (моль) |
% (по бензолу) |
| 1 |
CaCl2·4AlCl3·4,5Et2O |
78(1) |
36,5 (1) |
38(1) |
7,8 (0,008) |
10 |
103,7(82) |
| 2 |
CaCl2·4AlCl3·4,5Et2O |
39 (0,5) |
18,25(0,5) |
19(0,5) |
5,85 (0,006) |
15 |
51,9(82) |
| 3 |
CaCl2·4AlCl3·4,5Et2O |
19,5 (0,25) |
9,2 (0,25) |
9,5 (0,25) |
0,975 (0,001) |
5 |
22,1 (70) |
| 4 |
SrCl2·4AlCl3·1,5Et2O |
78(1) |
36,5(1) |
38(1) |
7,8 (0,001) |
10 |
110,1(87) |
| 5 |
SrCl2·4AlCl3·1,5Et2O |
39 (0,5) |
18,25(0,5) |
19 (0,5) |
5,85 (0,007) |
15 |
55,0 (87) |
| 6 |
SrCl2·4AlCl3·1,5Et2O |
19,5 (0,25) |
9,2 (0,25) |
9,5 (0,25) |
0,975 (0,001) |
5 |
23,7 (75) |
| 7 |
BaCl2·4AlCl3·2,5Et2O |
78(1) |
36,5(1) |
38(1) |
7,8 (0,008) |
10 |
101,2 (80) |
| 8 |
BaCl2·4AlCl3·2,5Et2O |
39 (0,5) |
18,25 (0,5) |
19(0,5) |
5,85 (0,006) |
15 |
50,6 (80) |
| 9 |
BaCl2·4AlCl3·2,5Et2O |
19,5 (0,25) |
9,2 (0,25) |
9,5 (0,25) |
0,975 (0,001) |
5 |
22,1 (70) |
Таблица 6
Условия получения гидридов металлов с участием полихлоралюминатов щелочноземельных металлов в среде диэтилового эфира, Et2O=(C2H5)2O |
 опыта опыта |
Условия проведения опыта |
Получено АlН3, г (%) |
| Наименование соединения |
Взято, г (моль) |
| MCl2·4AlCl3·nEt2O |
LiAlH4 |
| 1 |
CaCl2·4AlCl3·4,5Et2O |
978 (1) |
476 (14) |
384 (80) |
| 2 |
CaCl2·4AlCl3·4,5Et2O |
489 (0,5) |
238 (7) |
192 (80) |
| 3 |
CaCl2·4AlCl3·4,5Et2O |
244,5 (0,25) |
119(3,5) |
96 (80) |
| 4 |
SrCl2·4AlCl3·1,5Et2O |
803,6 (1) |
476 (14) |
408 (85) |
| 5 |
SrCl2·4AlCl3·1,5Et2O |
401,8 (0,5) |
238 (7) |
204 (85) |
| 6 |
SrCl2·4AlCl3·1,5Et2O |
200,9 (0,25) |
119(3,5) |
102 (85) |
| 7 |
BaCl2·4AlCl3·2,5Et2O |
927 (1) |
476 (14) |
374,4 (78) |
| 8 |
BaCl2·4AlCl3·2,5Et2O |
463,5 (0,5) |
238 (7) |
115,2(78) |
| 9 |
BaCl2·4AlCl3·2,5Et2O |
231,75 (0,25) |
119(3,5) |
93,6 (78) |
Формула изобретения
Полихлоралюминаты щелочноземельных металлов в среде диэтилового эфира общей формулы
МСl2·4АlСl3·nЕt2O, в которой
при М=Са n=4,5; при М=Sr n=1, 1,5; при М=Ва n=2,5,
полученные взаимодействием хлоридов щелочноземельных металлов с хлоридом алюминия в среде диэтилового эфира, в качестве реагентов для очистки нефтепродуктов и природного газа от сероводорода, катализаторов в процессах хлорметилирования и алкилирования ароматических углеводородов, исходных веществ при получении гидридов металлов.
|
|